Zuurbase titraties Acidimetrie Marco Houtekamer 18 november 2017

Zuur-base titraties Acidimetrie Marco Houtekamer; 18 november 2017

Voorwoord 2 Deze ZIL (zelfinstruerende leereenheid) gaat over het onderwerp zuur-base titraties (acidimetrie) en is gemaakt voor studenten van de opleiding Laboratoriumtechniek van Scalda. Je gaat als student de ZIL zelfstandig doornemen. Hiervoor dien je een planning te maken, dit wordt uitgelegd in hoofdstuk één. De hoofdstukken twee tot en met vijf bevatten uitleg over de onderwerpen reacties, p. H en eindpuntbepaling van een titratie (visueel en berekend). Ieder hoofdstuk wordt afgesloten met een oefeningen of opdrachten. De opdrachten dien je te maken en op te sturen aan je docent voor een tussenbeoordeling. In hoofdstuk zes pas je de eindpuntberekening toe met het programma Excel. Hoofdstuk zeven is een samenvatting. De ZIL wordt in hoofdstuk acht afgesloten met een eindtoets, die beoordeeld wordt door je docent. Je kan door de ZIL navigeren met de pijltjes toetsen op het toetsenbord, of door op de iconen te drukken onderaan de pagina. Als je op het “huisje” klikt, kom je bij de inhoudsopgave en van daaruit kan je ieder hoofdstuk aanklikken. Klik ook op de links die in de tekst staan voor meer uitleg! Veel plezier met het doorlopen van deze ZIL

Inhoudsopgave H 1: H 2: H 3: H 4: H 5: H 6: H 7: H 8: Bestudering van deze ZIL en maken van een planning Titraties en reacties Het begrip p. H Theorie acidimetrie en eindpuntbepaling visueel Eindpuntbepaling - methode van 2 e afgeleide Methode van 2 e afgeleide m. b. v. EXCEL Samenvatting Eindtoets 3 1 2 3 2 KU KU KU 1 KU

Doelen Hoofddoel: De theorie van acidimetrische (zuur-base) titraties kunnen reproduceren en berekeningen aan deze titraties kunnen toepassen. De totale tijdsduur is ongeveer 12 SBU of KU verspreid over 4 weken. Subdoelen: Na het doornemen van deze ZIL kan je tevens 1. De reactievergelijking opstellen van een zuur-base titratie; 2. Het begrip p. H uitleggen en berekeningen met de p. H toepassen; 3. Een geschikte indicator selecteren voor een visuele eindpuntbepaling bij een acidimetrische titratie; 4. Het eindpunt van een acidimetrische titratie bepalen m. b. v. de methode van de 2 e afgeleide; 5. Berekeningen uitvoeren aan acidimetrische titraties m. b. v. EXCEL. 4

H 1: Planning • Dit is een zelfstudie, dus het is voor jou een vereiste om een planning te maken; • Neem het eerste lesuur de tijd om deze ZIL in zijn geheel door te nemen; • Ieder hoofdstuk wordt afgesloten met oefeningen, te herkennen aan de blauwe tegel; • Soms staat er ook een opdracht, te herkennen aan de bruine afbeelding. Het antwoord dien je te mailen aan je docent voor tussenbeoordeling; • Een schatting van de tijdsduur per onderdeel is gegeven bij de inhoudsopgave; • Stel nu een balkenplanning op m. b. v. Excel; • In de 4 e week dien je les 8 (de eindopdracht) gemaakt te hebben en deze in te leveren via de mail bij je docent. 5

H 2: Titraties - algemeen 6 Wat zijn titraties? Bij titraties wordt m. b. v. een buret nauwkeurig oplossing (=de titrant) toegevoegd aan het te bepalen analiet. Het analiet is een exacte hoeveelheid materiaal wat is afgewogen met een analytische balans of gepipetteerd met een volumepipet. Waarom titraties? Titreren is een kwantitatieve techniek ook wel titrimetrie of volumetrie genoemd. De analysefout is gemiddeld < 1 %. Een beperking van de techniek: een mengsel kan worden geanalyseerd op een totaal parameter (bijv. zuur), echter vaak niet op zijn individuele componenten (bijv. fosforzuur en azijnzuur). (NC State University Chemistry Department, 2017)

H 2: Soorten titraties (I) Er 1. 2. 3. 4. zijn diverse soorten titraties: Zuur-base titratie (Acidimetrie) Neerslag titratie (Argentometrie) Redox titratie (Potentiometrie) Complexvormende titratie (Complexometrie) Voor ALLE titraties geldt: Wat gebeurt er in het bekerglas? ! Deze kleurverandering is het gevolg van een reactie! 7
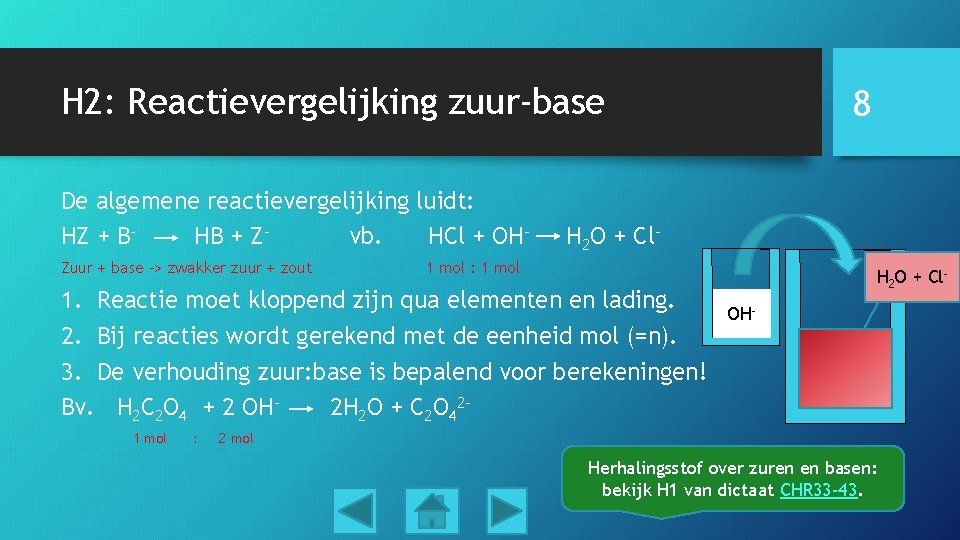
H 2: Reactievergelijking zuur-base De algemene reactievergelijking luidt: HZ + BHB + Zvb. HCl + OHZuur + base -> zwakker zuur + zout H 2 O + Cl- 1 mol : 1 mol 1. Reactie moet kloppend zijn qua elementen en lading. 2. Bij reacties wordt gerekend met de eenheid mol (=n). 3. De verhouding zuur: base is bepalend voor berekeningen! Bv. H 2 C 2 O 4 + 2 OH 2 H 2 O + C 2 O 421 mol : 8 H 2 O + Cl. OHHCl 2 mol Herhalingsstof over zuren en basen: bekijk H 1 van dictaat CHR 33 -43.

H 2: Rekenen met reacties 9 • Maak gebruik van het rekenschema!

H 2: Reacties - Oertiterstoffen Bij een titratie begint men altijd eerst met het bepalen van de concentratie van de titrant (= titerstelling). Dit doet men m. b. v. oertiterstoffen, ook wel primaire standaarden genoemd. Een oertiterstof is een chemische verbinding die: - Zeer zuiver te verkrijgen is (zuiverheid > 99, 99 %) - Zeer stabiel is; dus niet hygroscopisch (water opnemen) of verweren (water afstaan) - Hoog molair gewicht heeft (i. v. m. de inweeg) - Een aflopende reactie (alles wordt omgezet) 10

H 2: Reacties - Oertiterstoffen voor het stellen van een zuur: a. Natriumcarbonaat (Na 2 CO 3) b. Natriumtetraboraat ook borax genoemd (Na 2 B 4 O 7. 10 H 2 O) Oertiterstoffen voor het stellen van een base: a. Kaliumwaterstofftalaat (KH 5 C 8 O 4) b. Benzoëzuur (H 6 C 7 O 2) c. Oxaalzuur ook ethaandizuur genoemd (H 2 C 2 O 4. 2 H 2 O) d. Kaliumwaterstofjodaat (KH(IO 3)2) 11
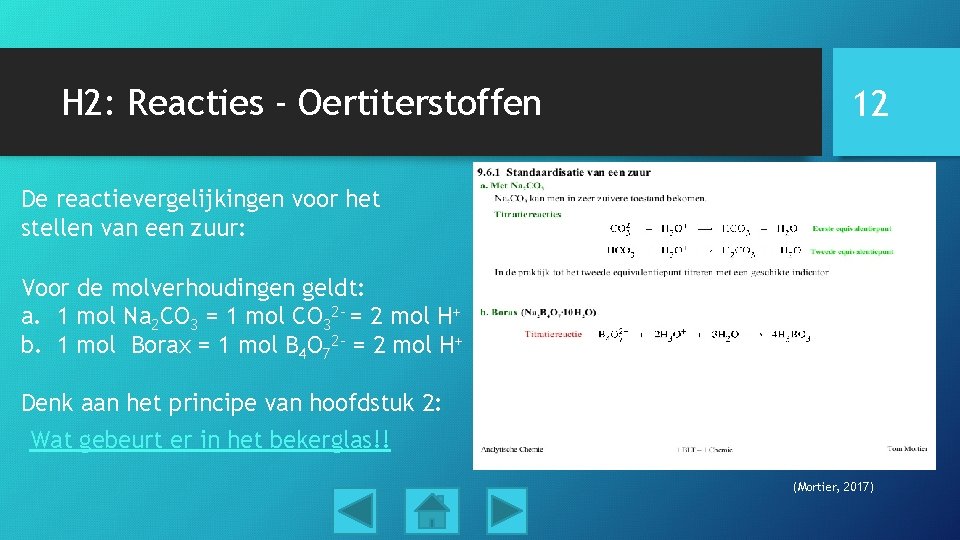
H 2: Reacties - Oertiterstoffen 12 De reactievergelijkingen voor het stellen van een zuur: Voor de molverhoudingen geldt: a. 1 mol Na 2 CO 3 = 1 mol CO 32 - = 2 mol H+ b. 1 mol Borax = 1 mol B 4 O 72 - = 2 mol H+ Denk aan het principe van hoofdstuk 2: Wat gebeurt er in het bekerglas!! (Mortier, 2017)
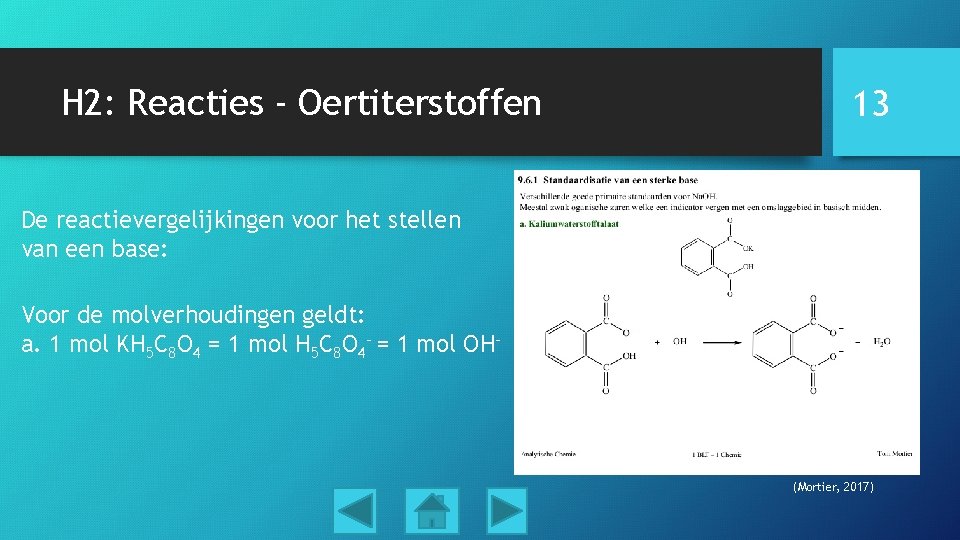
H 2: Reacties - Oertiterstoffen 13 De reactievergelijkingen voor het stellen van een base: Voor de molverhoudingen geldt: a. 1 mol KH 5 C 8 O 4 = 1 mol H 5 C 8 O 4 - = 1 mol OH- (Mortier, 2017)
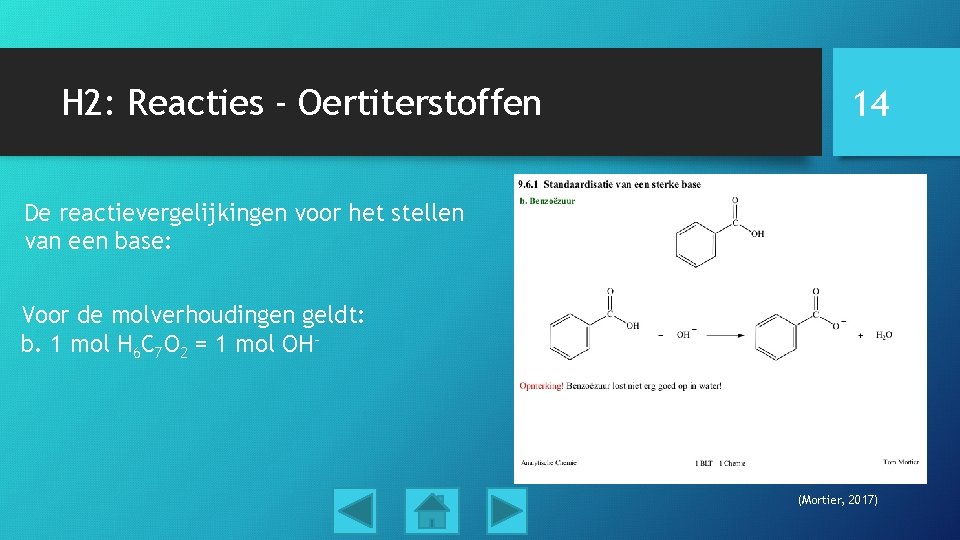
H 2: Reacties - Oertiterstoffen 14 De reactievergelijkingen voor het stellen van een base: Voor de molverhoudingen geldt: b. 1 mol H 6 C 7 O 2 = 1 mol OH- (Mortier, 2017)
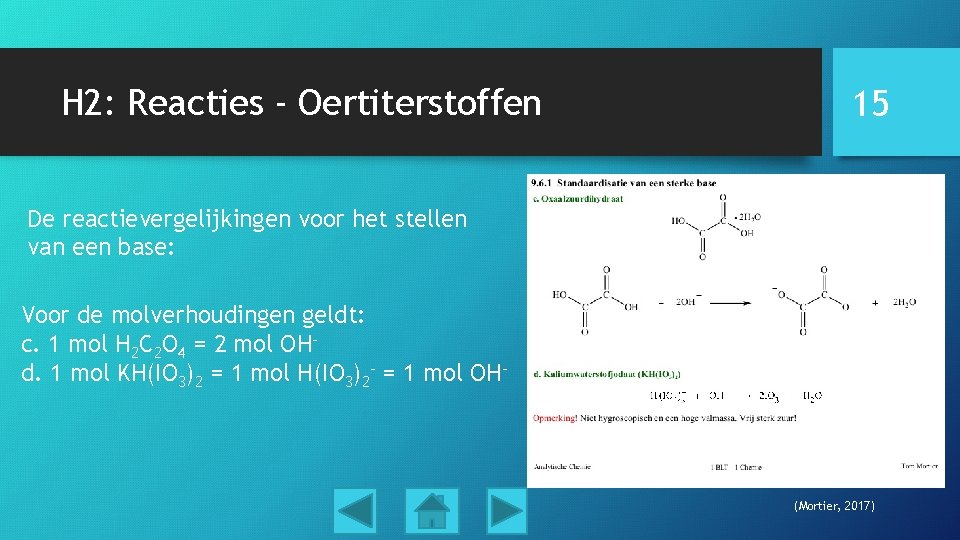
H 2: Reacties - Oertiterstoffen 15 De reactievergelijkingen voor het stellen van een base: Voor de molverhoudingen geldt: c. 1 mol H 2 C 2 O 4 = 2 mol OHd. 1 mol KH(IO 3)2 = 1 mol H(IO 3)2 - = 1 mol OH- (Mortier, 2017)

H 2: Soorten titraties (II) 16 De soort titratie kan ook ingedeeld worden op de techniek die gebruikt wordt voor de eindpuntbepaling: 1. Visueel (klassiek, met indicator en oogwaarneming) 2. Instrumenteel (met apparatuur): a. p. H-meter; Potentiometrie b. geleidbaarheidsmeter; Conductometrie c. fotometer; Fotometrie d. ion-selectieve electrode p. H Geleidbaarheid e. redox electrode Redox (Metrohm , 2017)

H 2: Titraties – evolutie technieken handmatig Semi-automatisch Automatische buret 17 Automatisch met p. H (Metrohm , 2017) Volledig automatische titreerstraat Automatisch met p. H en sampler

H 2: Titraties - Oefeningen Een aantal oefeningen m. b. t. titraties: 1. Maak de volgende kruiswoordpuzzel over titraties 2. Beantwoord tevens deze meerkeuzevragen De antwoorden van de puzzel en de vragen staan hier 18

H 3: Het begrip p. H 19 p. H is een maat voor de zuurgraad van een waterige oplossing. p. H komt overeen met de concentratie van H+ ionen in een oplossing Als c[H+] >> dan wordt de p. H << De p. H schaal is logaritmisch en loopt van 0 tot 14. Er geldt: p. H = - log [H+] en dus ook [H+] = 10 -p. H (Sanibel Seaschool, 2017)

H 3: Het begrip p. H (en p. OH) Naast de p. H bestaat ook de gerelateerde term p. OH is eveneens een logaritmische maat, maar dan voor de basegraad (OH- concentratie) van een waterige oplossing Er geldt: p. OH = - log [OH-] en dus ook [OH-] = 10 -p. OH Er geldt: p. H + p. OH = 14 Dus als c[OH-] >> dan wordt de p. OH << en de p. H >> 20

H 3: De p. H meting 21 Een p. H meting wordt gedaan met een p. H-combi electrode en een m. V meter, zie bijgaande afbeelding. De m. V wordt door een kalibratie omgezet naar de p. H schaal. De p. H-combi-electrode bestaat uit: - Referentie electrode (Ag/Ag. Cl) - Glaselectrode (H+ gevoelig) - Eventueel een temperatuursensor (Delta Ohm Benelux B. V. , 2017)

H 3: De p. H meting • Een p. H meting bestaat in principe uit de volgende onderdelen: - p. H elektrode: geeft een spanning af die afhankelijk is van de p. H waarde van de vloeistof - Referentie elektrode: geeft een stabiele (referentie) spanning af - Temperatuurvoeler: meet de temperatuur van de vloeistof - Elektronica: zet het gemeten signaal om naar een p. H waarde - Formule: p. H = (E meting - E 0)/59, 16 (@ 25°C) 22

H 3: De p. H meting 23 - meetgedeelte van de p. H elektrode bestaat uit p. H gevoelig glas. - hier ontstaat onder invloed van vocht een 'H+ gevoelige' laag. Een spanning wordt opgewekt. - Als referentiepunt geldt: de spanning van de referentie elektrode. - de vloeistof tussen deze elektrodes zorgt er voor dat de 'stroomkring' wordt gesloten. Dit geeft meteen aan waarom de vloeistof elektrisch geleidend moet zijn voor een p. H meting. (Delta Ohm Benelux B. V. , 2017) Bekijk deze film voor meer uitleg over de p. H electrode (Endress + Hauser, 2017)

H 3: De p. H meting - kalibratie 24 In bijgaande grafiek is de kalibratie van een p. H meter weergegeven. Het signaal van de voltmeter (m. V) wordt uitgezet tegen de p. H. Wat valt hier op? Het is een lineair verband met een ideale richtingscoefficiënt van 59. 16 m. V/p. H (bij 25⁰C). Bij p. H 7 is het voltage ~ 0 m. V (Delta Ohm Benelux B. V. , 2017)

H 3: De p. H meting - kalibratie 25 • Buffer p. H m. V 1 7, 00 0, 15 2 4, 01 170, 50

H 3: De p. H meting – praktische zaken Diafragma moet open zijn, anders is de stroomkring doorbroken en wordt het signaal gelijk aan 0 m. V De wand van glasbol mag niet vervuild zijn, anders geeft de hechting van H+ ionen problemen. Voorkomen van bovenstaande: - Voorzichtig omgaan met p. H elektrodes; ze zijn kwetsbaar! - p. H elektrode niet laten uitdrogen (i. v. m. glas bol) - p. H elektrode NIET bewaren in demiwater, maar in KCl-oplossing - p. H elektrode niet in zeer vervuilde oplossingen toepassen - p. H elektrode mag niet lang (max. 1 minuut) in een schoonmaakvloeistof (bevat HF!) - p. H meting niet doen in de buurt van elektronische stoorbronnen 26

H 3: Rekenen met p. H – voorbeeld 1. Een analist bepaalt de p. H van een oplossing met een gekalibreerde p. H meter op 5, 40. a. Bereken de concentratie [H+] in de oplossing in mol/L b. Bereken de p. OH van de oplossing c. Bereken de concentratie [OH-] in mol/L. Uitleg antwoorden: druk op de pijltjes van je toetsenbord a. Er geldt c[H+] = 10 -p. H , dus p. H = 10 -5, 40 = 3. 98*10 -6 mol/L b. Er geldt: p. H + p. OH = 14, dus p. OH = 14 – p. H = 14 – 5, 40 = 8, 60 c. Er geldt c[OH-] = 10 -p. OH, dus c[OH-] = 10 -8, 60 = 2. 51*10 -9 mol/L 27

H 3: p. H - Oefeningen 28 Vraag 1: In bijgaande afbeelding staat een p. H electrode. Combineer de onderstaande onderdelen met de nummers op de afbeelding. - Interne oplossing van de referentie electrode Interne oplossing van de glaselectrode Vulopening Diafragma Ag/Ag. Cl referentie electrode Ag. Cl glaselectrode met zilverdraad 1 2 3 4 5 6

H 3: p. H - Oefeningen 29 Vraag 1: In bijgaande afbeelding staat een p. H electrode afgebeeld. Combineer de onderstaande onderdelen met de nummers op de afbeelding. - Interne oplossing van de referentie electrode; 3 - Interne oplossing van de glaselectrode; 6 - Vulopening; 1 - Diafragma; 4 - Ag/Ag. Cl referentie electrode; 2 - Ag. Cl meetelectrode met zilverdraad; 5 1 2 3 4 5 6 (Nikita, 2017)

H 3: Oefeningen Vraag 2: Welke van de onderstaande stellingen over het omgaan met een p. H electrode is waar? I – Een p. H electrode mag niet uitdrogen en bewaar je het best in demiwater II – Een p. H electrode mag je tijdens de p. H-meting gebruiken om te roeren a. Alleen bewering I is juist b. Alleen bewering II is juist c. Geen van deze beweringen is juist 30

H 3: Oefeningen Vraag 2: Welke van de onderstaande stellingen over het omgaan met een p. H electrode is waar? I – Een p. H electrode mag niet uitdrogen en bewaar je het best in demiwater II – Een p. H electrode mag je tijdens de p. H-meting gebruiken om te roeren a. Alleen bewering I is juist b. Alleen bewering II is juist c. Geen van deze beweringen is juist 31
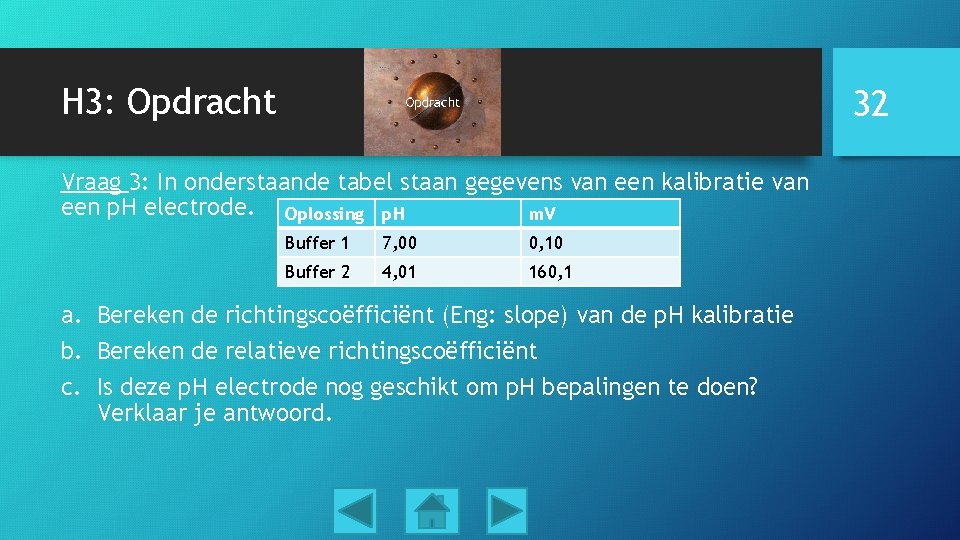
H 3: Opdracht 32 Vraag 3: In onderstaande tabel staan gegevens van een kalibratie van een p. H electrode. Oplossing p. H m. V Buffer 1 7, 00 0, 10 Buffer 2 4, 01 160, 1 a. Bereken de richtingscoëfficiënt (Eng: slope) van de p. H kalibratie b. Bereken de relatieve richtingscoëfficiënt c. Is deze p. H electrode nog geschikt om p. H bepalingen te doen? Verklaar je antwoord.
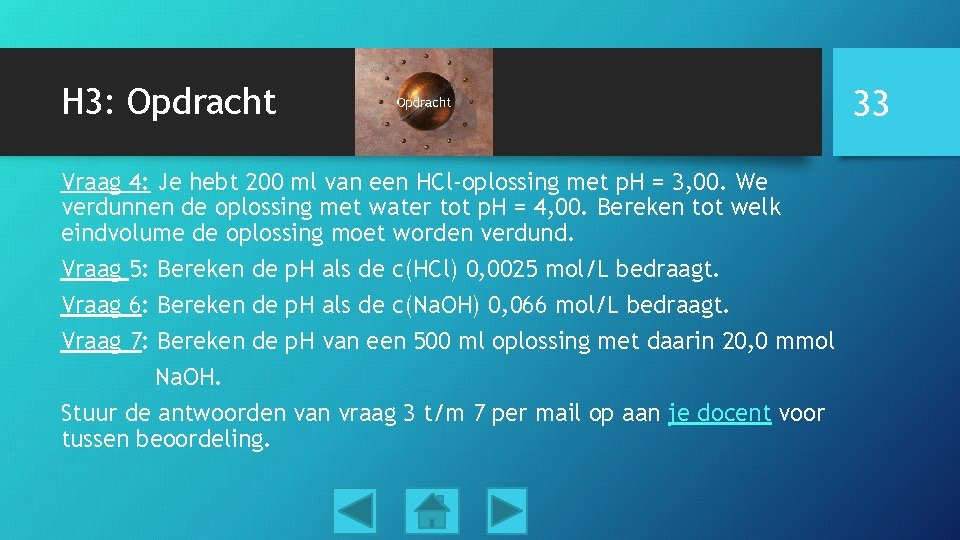
H 3: Opdracht Vraag 4: Je hebt 200 ml van een HCl-oplossing met p. H = 3, 00. We verdunnen de oplossing met water tot p. H = 4, 00. Bereken tot welk eindvolume de oplossing moet worden verdund. Vraag 5: Bereken de p. H als de c(HCl) 0, 0025 mol/L bedraagt. Vraag 6: Bereken de p. H als de c(Na. OH) 0, 066 mol/L bedraagt. Vraag 7: Bereken de p. H van een 500 ml oplossing met daarin 20, 0 mmol Na. OH. Stuur de antwoorden van vraag 3 t/m 7 per mail op aan je docent voor tussen beoordeling. 33

H 4: Theorie acidimetrie Potentiometrische titraties zijn titraties waarbij het equivalentiepunt wordt vastgesteld m. b. v. electrode potentialen. Deze potentiaal is afhankelijk van één van de reagerende deeltjes in de oplossing. De meest bekende potentiometrische titratie is m. b. v. een p. H elektrode. Het reagerende deeltje is hierbij het H+-ion. Met noemt dit acidimetrie. Het Latijnse 'acidus' betekent 'zuur‘. 34

H 4: Acidimetrie - titratiecurve Als men een zuur met een base titreert, verkrijgt men een titratiecurve zoals de afbeelding hiernaast. Klik op deze link en bekijk de diverse curves die mogelijk zijn. (Sint-Martinusscholen Herk-de-Stad, 2017) Klik rechtsonder op het blauwe pijltje om de cursor (van volume) te bewegen en de bijbehorende p. H af te lezen. Verander ook eens de indicator! Vragen die jezelf kan stellen: Wat gebeurt er met de p. H in de curves? En waarom? En waar is het equivalentiepunt of eindpunt van de titratie? En wat is een geschikte indicator? 35 (Syntax Media, 2017)

H 4: Acidimetrie - eindpuntbepaling 36 Bepaling van het eindpunt of equivalentiepunt kan op vijf manieren: 1. Circle-fit methode; grafische methode, zie dictaat CHT 47 -Hoofdstuk 10 2. Raaklijn methode; grafische methode, zie dictaat CHT 47 - Hoofdstuk 10 3. Methode van de 2 e afgeleide; rekenkundige methode 4. Methode van Gran; rekenkundige methode 5. Visueel; met indicatoren Methode 3, 4 en 5 worden over het algemeen toegepast binnen laboratoria. De methoden 3 en 5 worden behandeld in LTO 42 en LTO 43.

H 4: Acidimetrie – Visueel (met indicator) 37 Bepaling van het eindpunt met indicator is de authentieke manier van eindpuntbepaling. In een bepaald p. H gebied verandert de indicator van kleur; het equivalentiepunt dient uiteraard in dat gebied te vallen! Dus als het eq-punt bij p. H 4, 0 ligt, dan is methyloranje veel geschikter dan lakmoes of fenolftaleïne. Bij een omslagpunt van p. H 9 of 10 is fenolftaleïne veel geschikter dan methylrood of methyloranje. (Syntax Media, 2017) Meer indicatoren inclusief structuurformules staan hier (Engineeringtoolbox, 2017)

H 4: Acidimetrie – Visueel (met indicator) Daarnaast zijn er ook mengsel van indicatoren mogelijk: mengindicator. Deze hebben een zeer klein p. H-gebied en dus een scherpe kleuromslag. Voorbeelden: - methylrood/broomkresolgroen; p. H omslag is 5, 1 - Thymolblauw/Fenolftaleïne; p. H omslag is 9, 0 De 1. 2. 3. 4. algemene eisen voor een indicator zijn: Verschil in kleur tussen de “zure” en “basische” vorm Hoge kleurintensiteit (inweeg is laag; bijv. 100 mg/100 ml = 0, 1 %) Het kleurevenwicht is snel instelbaar De indicator verbruikt geen titrant 38

H 4: Acidimetrie - indicatoren Het gebruik van indicatoren kan ook problemen geven! Onderstaand een aantal mogelijke foutenbronnen: 1. indicatorfout; het omslagpunt ≠ het equivalentiepunt 2. Verbruik van titreervloeistof door de indicator (eis < 0, 1 %) 3. Ondoorzichtige oplossingen 4. Titratiesnelheid is te hoog (je schiet voorbij equivalentiepunt) 5. Ongevoeligheid van het oog voor de kleuromslag 6. Temperatuurverschil; evenwichten zijn temperatuurafhankelijk 39

H 4: Oefening Indicatoren 40 Bekijk de volgende titratiecurves en bepaal welke indicatoren (van bijgaande afbeelding) geschikt zijn voor de titraties. Het equivalentiepunt is met een stippellijn aangegeven. Per titratie zijn meerdere indicatoren te gebruiken! A. Titratie van een sterk zuur (Syntax Media, 2017)

H 4: Oefening Indicatoren 41 Bekijk de volgende titratiecurves en bepaal welke indicatoren (van bijgaande afbeelding) geschikt zijn voor de titraties. Het equivalentiepunt is met een stippellijn aangegeven. Per titratie zijn meerdere indicatoren te gebruiken! B. Titratie van een zwak zuur (Syntax Media, 2017)

H 4: Oefening Indicatoren 42 Bekijk de volgende titratiecurves en bepaal welke indicatoren (van bijgaande afbeelding) geschikt zijn voor de titraties. Het equivalentiepunt is met een stippellijn aangegeven. Per titratie zijn meerdere indicatoren te gebruiken! C. Titratie van een tweewaardig zwak zuur (Syntax Media, 2017)

H 4: Oefening Indicatoren 43 Bekijk de volgende titratiecurves en bepaal welke indicatoren (van bijgaande afbeelding) geschikt zijn voor de titraties. Het equivalentiepunt is met een stippellijn aangegeven. Per titratie zijn meerdere indicatoren te gebruiken! D. Titratie van een sterke base (Syntax Media, 2017)

H 4: Oefening Indicatoren 44 Bekijk de volgende titratiecurves en bepaal welke indicatoren (van bijgaande afbeelding) geschikt zijn voor de titraties. Het equivalentiepunt is met een stippellijn aangegeven. Per titratie zijn meerdere indicatoren te gebruiken! E. Titratie van een zwakke base (Syntax Media, 2017)

H 4: Oefening Indicatoren 45 Bekijk de volgende titratiecurves en bepaal welke indicatoren (van bijgaande afbeelding) geschikt zijn voor de titraties. Het equivalentiepunt is met een stippellijn aangegeven. Per titratie zijn meerdere indicatoren te gebruiken! F. Titratie van een tweewaardig zwakke base (Syntax Media, 2017)
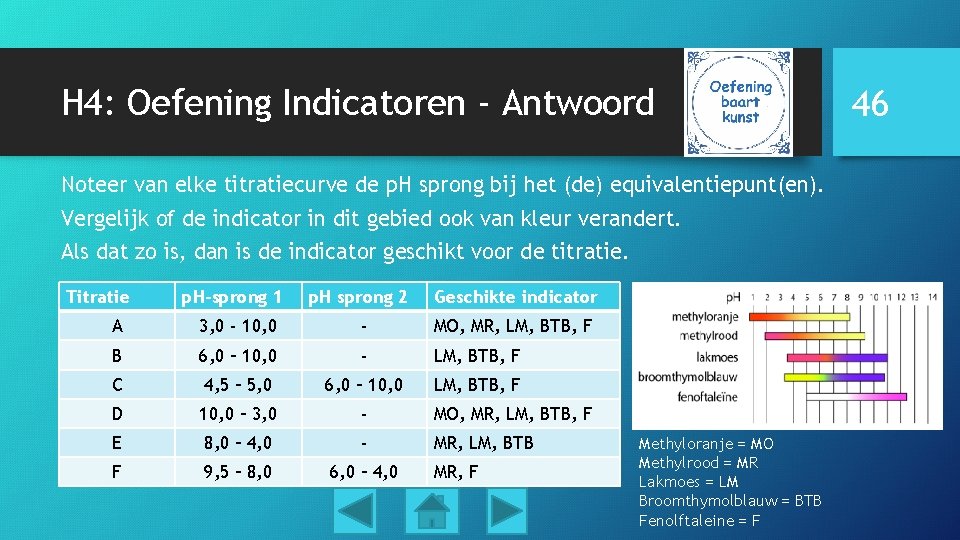
H 4: Oefening Indicatoren - Antwoord Noteer van elke titratiecurve de p. H sprong bij het (de) equivalentiepunt(en). Vergelijk of de indicator in dit gebied ook van kleur verandert. Als dat zo is, dan is de indicator geschikt voor de titratie. Titratie p. H-sprong 1 p. H sprong 2 Geschikte indicator A 3, 0 - 10, 0 - MO, MR, LM, BTB, F B 6, 0 – 10, 0 - LM, BTB, F C 4, 5 – 5, 0 6, 0 – 10, 0 LM, BTB, F D 10, 0 – 3, 0 - MO, MR, LM, BTB, F E 8, 0 – 4, 0 - MR, LM, BTB F 9, 5 – 8, 0 6, 0 – 4, 0 MR, F Methyloranje = MO Methylrood = MR Lakmoes = LM Broomthymolblauw = BTB Fenolftaleine = F 46

H 4: Opdracht 1 – indicatoren 1) Lees onderstaande tekst door en geef aan wat hier fout is en waarom. a. Een analiste gaat een titratie uitvoeren van oxaalzuur met 0, 1 M Na. OH. Volgens literatuur ligt het equivalentiepunt van de titratie rond p. H 8, 0. Ze weegt 150 mg oxaalzuur af met een analytische balans en spoelt deze kwantitatief over in een bekerglas van 250 ml voor titratie. Ze voegt 6 druppels van de indicator methyloranje toe en gaat titreren met een buret die is voorgespoeld met 0, 1 M Na. OH. b. Een technisch onderwijs assistent wil een nieuwe indicator-oplossing aanmaken van fenolftaleïne. Hij weegt hiervoor 1, 00 g fenolftaleïne af met een bovenweger en spoelt deze kwantitatief over in een maatkolf van 100 ml. De oplossing wordt aangevuld met 50% ethanol. 47

H 4: Opdracht 2 - Indicatoren 48 Opdracht 2) Bijgaand een titratiecurve van een tweewaardig zuur met loog. Zoek in deze lijst een geschikte indicator voor de titratie. Let op: Meerdere antwoorden zijn mogelijk! Verklaar je keuze(s). Mail je antwoorden van opdracht 1 en 2 aan je docent. (Syntax Media, 2017)

H 5: Eindpuntbepaling - Methode van 2 e afgeleide 49 Grotere nauwkeurigheid en vooral automatisering heeft geleid tot het gebruik van een p. H meter in combinatie met eerder genoemde rekenmethodes. C Hoe werkt de methode van de 2 e afgeleide? We kijken eerst naar een curve. A. In het begin van de curve loopt de p. H langzaam op. B. Rondom het eq-punt is de curve het steilst. C. Na het eq-punt vlakt de curve weer af. B A (Syntax Media, 2017)

H 5: Methode van 2 e afgeleide Uitvoeren van een titratie: A. Begin; je kunt in grote stappen (bijv. 1 ml) titrant toevoegen (=titreren) B. Rondom het eq-punt; in kleine stapjes titreren (bijv. 0, 05 of 0, 1 ml) C. Na het eq-punt; in grotere stappen titreren (bijv. 1 ml titrant) Op deze manier verkrijgt men een dataset waarin staat: ml titrant en de bijbehorende p. H. De meest interessante data is bij punt B (rondom equivalentiepunt). 50

H 5: Methode van 2 e afgeleide Men titreert zuur met loog. Door eerst een snel titratie uit te voeren bleek, dat het omslag punt tussen de 10 en 11 ml ligt. Vervolgens is de titratie opnieuw uitgevoerd, maar nu met kleine gelijke stapjes van 0, 1 m. L rond het verwachte equivalentiepunt. Men verkrijgt de data in de tabel. 1. Bepaal bij elke stap het verschil tussen de p. H-waarden. Dit noemt men Δp. H (“delta –p. H”) of 1 e afgeleide. 2. Bepaal daarna bij elke stap het verschil tussen de Δp. H Dit noemt men ΔΔp. H of 2 e afgeleide. 3. Zoek bij ΔΔp. H de twee punten op, waarbij deze van + naar – gaat of omgekeerd. Noteer bijbehorende data. 4. In dit geval: 10, 50 ml; +1, 60 en 10, 60; -1, 20 51 V(Na. OH) [ml] p. H 10, 00 10, 10 10, 20 10, 30 10, 40 10, 50 10, 60 10, 70 10, 80 10, 90 11, 00 4, 30 4, 33 4, 40 4, 60 5, 00 5, 70 8, 00 9, 10 9, 50 9, 70 9, 81 Δ(p. H) ΔΔ(p. H) 2 e 1 e afgeleide 0, 03 0, 04 0, 07 0, 13 0, 20 0, 40 0, 30 0, 70 1, 60 2, 30 -1, 20 1, 10 -0, 70 0, 40 -0, 20 -0, 09 0, 11
![H 5: Methode van 2 e afgeleide • 52 V(Na. OH) [ml] p. H H 5: Methode van 2 e afgeleide • 52 V(Na. OH) [ml] p. H](http://slidetodoc.com/presentation_image/44e9498f0416e2dc284b41b092b1b52c/image-52.jpg)
H 5: Methode van 2 e afgeleide • 52 V(Na. OH) [ml] p. H 10, 00 10, 10 10, 20 10, 30 10, 40 10, 50 10, 60 10, 70 10, 80 10, 90 11, 00 4, 30 4, 33 4, 40 4, 60 5, 00 5, 70 8, 00 9, 10 9, 50 9, 70 9, 81 Δ(p. H) ΔΔ(p. H) 1 e 2 e afgeleide 0, 03 0, 07 0, 20 0, 40 0, 70 2, 30 1, 10 0, 40 0, 20 0, 11 0, 04 0, 13 0, 20 0, 30 1, 60 -1, 20 -0, 70 -0, 20 -0, 09
H 5: Methode van 2 e afgeleide 53 • Maak gebruik van het rekenschema!

H 5: Methode van 2 e afgeleide Nog een voorbeeld om te oefenen. . Een analist wil het zuur gehalte in azijnzuur oplossing bepalen m. b. v. een titratie met natronloog. De natronloog oplossing wordt eerst gesteld met 113, 9 mg oxaalzuur (H 2 C 2 O 4. 2 H 2 O; Molmassa = 126, 07 g/mol). Men verkrijgt de volgende titratiegegevens. a. Bereken het equivalentiepunt m. b. v. de 2 e afgeleide van de titerstelling natronloog (in m. L). b. Bereken de c(Na. OH) in mol/L aan de hand van het verkregen antwoord bij vraag a. 54 V(Na. OH) [ml] 11, 00 11, 05 11, 10 11, 15 11, 20 11, 25 11, 30 11, 35 11, 40 11, 45 11, 50 11, 55 11, 60 p. H 3, 60 3, 63 3, 80 3, 89 4, 50 5, 97 8, 76 9, 25 9, 55 9, 75 9, 90 9, 95 9, 99
![H 5: Methode van 2 e afgeleide • 55 V(Na. OH) [ml] 11, 00 H 5: Methode van 2 e afgeleide • 55 V(Na. OH) [ml] 11, 00](http://slidetodoc.com/presentation_image/44e9498f0416e2dc284b41b092b1b52c/image-55.jpg)
H 5: Methode van 2 e afgeleide • 55 V(Na. OH) [ml] 11, 00 11, 05 11, 10 11, 15 11, 20 11, 25 11, 30 11, 35 11, 40 11, 45 11, 50 11, 55 11, 60 p. H 3, 60 3, 63 3, 80 3, 89 4, 50 5, 97 8, 76 9, 25 9, 55 9, 75 9, 90 9, 95 9, 99 Δ(p. H) 0, 03 0, 17 0, 09 0, 61 1, 47 2, 79 0, 49 0, 30 0, 2 0, 15 0, 04 ΔΔ(p. H) 0, 14 -0, 08 0, 52 0, 86 1, 32 -2, 3 -0, 19 -0, 1 -0, 05 -0, 1 -0, 01

H 5: Methode van 2 e afgeleide • 56
H 5: Methode van 2 e afgeleide - Oefeningen van rekensommen met de 2 e afgeleide en vervolg berekeningen. Klik op deze link voor de vragen. Klik op deze link voor de uitwerkingen. 57

H 6: Methode van 2 e afgeleide m. b. v. EXCEL. De berekening van de 2 e afgeleide kan ook uitgevoerd worden m. b. v. het programma EXCEL. Bekijk bijgaande video met uitleg hoe dat gedaan kan worden. 58

H 6: Methode van 2 e afgeleide via EXCEL. Klik op onderstaande dataset van een zuur-base titratie en bepaal het eindpunt van de titratie m. b. v. de 2 e afgeleide. De formule voor de berekening dient in EXCEL te worden gemaakt. - Dataset 1 Volg de instructies in het Excel blad en stuur een uitgewerkte dataset met je antwoord op de vragen per mail aan je docent voor een tussenbeoordeling. 59

H 7: Samenvatting Even alles op een rijtje: In H 2 werd de zuur-base reactie behandeld en bijbehorende berekeningen met de mol en molaire of massaconcentratie. In H 3 staan p. H berekeningen, maar ook de p. H electrode en de p. H kalibratie werd uitgelegd. In H 4 leer je de juiste indicator te kiezen bij een zuur-base titratie. In H 5 wordt uitgelegd hoe het eindpunt wordt berekend met de methode van de 2 e afgeleide. In H 6 gebruik je deze methode, maar dan programmeer je deze in EXCEL en bereken je vervolgens de concentratie van een titrant. 60
H 8: Eindtoets - Acidimetrie Alle onderdelen zijn behandeld, dus het is nu mogelijk om jullie kennis te toetsen. Vraag eerst per mail toestemming aan je docent! Klik op vervolgens op bijgaande link om de eindtoets te openen. Volg de instructies op het 1 e blad van de toets. Veel succes! 61
Einde 62 Dank voor jullie aandacht!
Literatuur Delta Ohm Benelux B. V. (2017, 11 3). p. H meetprincipe en FAQ. Opgehaald van www. deltaohm. nl: https: //www. deltaohm. nl/home/ph-meetprincipe-en-faq Endress + Hauser. (2017, 11 3). p. H sensors and transmitters. Opgehaald van www. nl. endress. com: https: //www. nl. endress. com/nl/Field-instruments-overview/liquid-analysis-product-overview/p. Hsensors-transmitters? highlight=potentiometric%20 measurement Engineeringtoolbox. (2017, 10 19). Acid base p. H indicators. Opgehaald van www. engineeringtoolbox. com: https: //www. engineeringtoolbox. com/p. H-color-change-acid-basep. Ka-structure-indicator-d_1951. html Metrohm. (2017, 10 28). Elektrode zoeken. Opgehaald van www. metrohm. com: https: //www. metrohm. com/nl-nl/producten/accessoires/elektrode-zoeken/# Mortier, T. (2017, 10 18). zuurbase-titraties deel I. Opgehaald van www. slideshare. net: https: //www. slideshare. net/tomor/zuurbase-titraties-deel-i 63
Literatuur NC State University Chemistry Department. (2017, 10 28). Lab 9 - Titrations. Opgehaald van www. webassign. net: http: //www. webassign. net/question_assets/ncsugenchem 102 labv 1/lab_9/manual. html Nikita. (2017, 11 4). Cheap DIY Electronic PH Meter. Opgehaald van www. instructables. com: http: //www. instructables. com/id/cheap-DIY-electronic-p. H-meter/ Sanibel Seaschool. (2017, 11 15). p. H. Opgehaald van classroom. sanibelseaschool. org: http: //classroom. sanibelseaschool. org/ph Sint-Martinusscholen Herk-de-Stad. (2017, 10 18). wiskundehoekje-titraties. Opgehaald van users. telenet. be: http: //users. telenet. be/wiskundehoekje/chemoef/titratie. htm Syntax Media. (2017, 10 29). 3 Acidimetrie. Opgehaald van www. mlochemie. nl: http: //www. mlochemie. nl/index. php/3 -acidimetrie 64
- Slides: 64