ZRAAT FAKLTES TARIMSAL BYOTEKNOLOJ BLM ZMT 302 MOLEKLER

ZİRAAT FAKÜLTESİ TARIMSAL BİYOTEKNOLOJİ BÖLÜMÜ ZMT 302 -MOLEKÜLER GENETİK DOÇ. DR. LEVENT MERCAN

DNA Onarımı ZMT 302 -MOLEKÜLER GENETİK Hafta-4

DNA Onarımı • DNA, herhangi bir molekül gibi çeşitli biyokimyasal tepkimelere uğrayabilir. • Hücre genomunun tek kopyası olması nedeniyle DNA’nın yapısındaki değişiklikler hücrenin RNA’lar ve proteinler gibi diğer bileşenlerindeki değişimlerinden çok daha önemli sonuçlar doğurabilir.
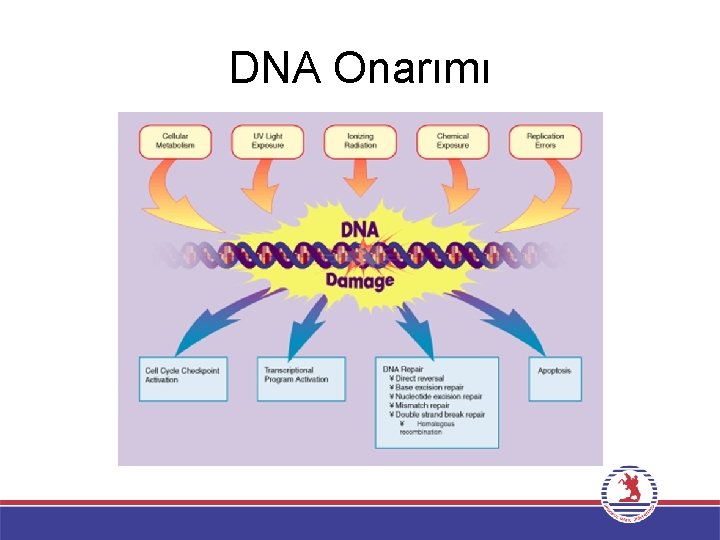
DNA Onarımı
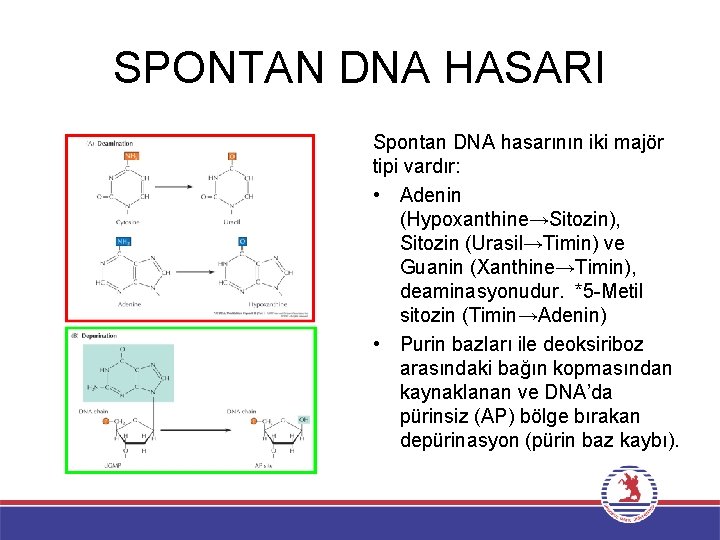
SPONTAN DNA HASARI Spontan DNA hasarının iki majör tipi vardır: • Adenin (Hypoxanthine→Sitozin), Sitozin (Urasil→Timin) ve Guanin (Xanthine→Timin), deaminasyonudur. *5 -Metil sitozin (Timin→Adenin) • Purin bazları ile deoksiriboz arasındaki bağın kopmasından kaynaklanan ve DNA’da pürinsiz (AP) bölge bırakan depürinasyon (pürin baz kaybı).
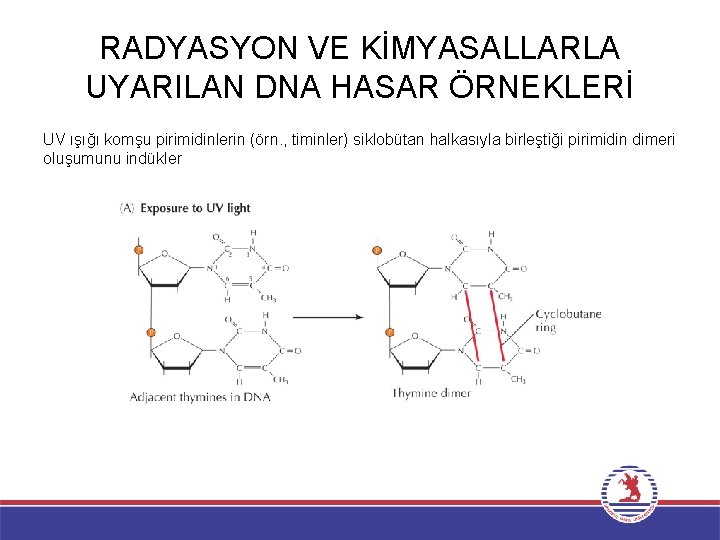
RADYASYON VE KİMYASALLARLA UYARILAN DNA HASAR ÖRNEKLERİ UV ışığı komşu pirimidinlerin (örn. , timinler) siklobütan halkasıyla birleştiği pirimidin dimeri oluşumunu indükler
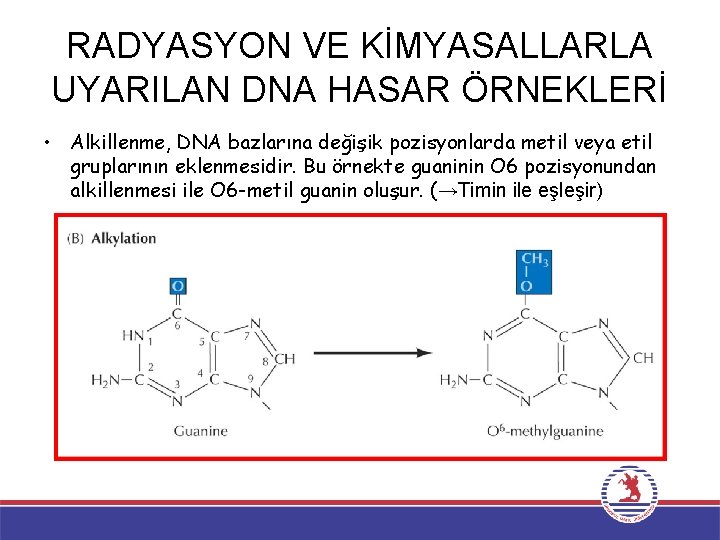
RADYASYON VE KİMYASALLARLA UYARILAN DNA HASAR ÖRNEKLERİ • Alkillenme, DNA bazlarına değişik pozisyonlarda metil veya etil gruplarının eklenmesidir. Bu örnekte guaninin O 6 pozisyonundan alkillenmesi ile O 6 -metil guanin oluşur. (→Timin ile eşleşir)
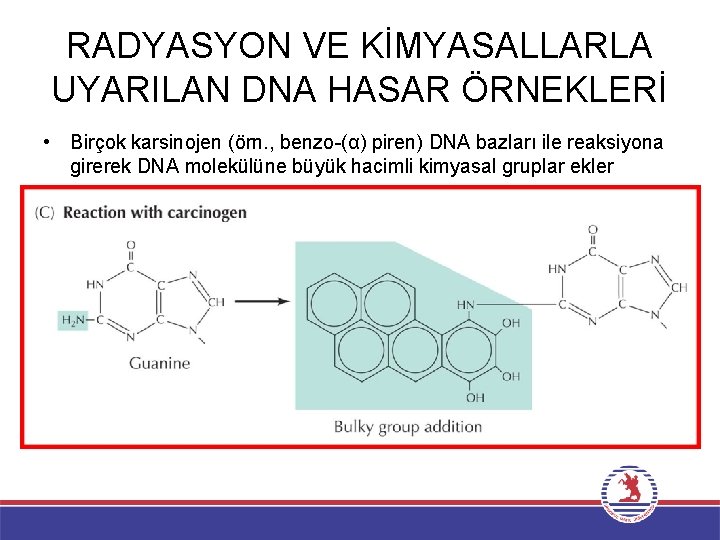
RADYASYON VE KİMYASALLARLA UYARILAN DNA HASAR ÖRNEKLERİ • Birçok karsinojen (örn. , benzo-(α) piren) DNA bazları ile reaksiyona girerek DNA molekülüne büyük hacimli kimyasal gruplar ekler

DNA Onarımı • Hücreler genomlarının bütünlüğünü korumak için hasarlı DNA’yı onaran mekanizmalar geliştirmişlerdir. • DNA onarım mekanizmaları iki ana gruba ayrılır. 1. DNA hasarını oluşturan kimyasal reaksiyonun doğrudan tersine çevrilmesi 2. Hasarlı bazların yeni sentezlenen DNA ile değiştirilmesi • DNA onarımının çalışmadığı noktalarda ise, hücrelerin hasarla başa çıkabilmesi için ek mekanizmalar gelişmiştir.

DNA hasarının doğrudan geri döndürülmesi • DNA’da oluşan birçok hasar, hasarlı bazların uzaklaştırılmasının ardından çıkarılan bölgenin yeniden sentezlenmesi ile onarılır. • DNA’da bazı hatalar doğrudan hasarın geri döndürülmesi ile onarılabilir. • Özellikle morötesi (UV) ışığa maruz kalınmasıyla oluşan pirimidin dimerleri ve purin halkasına O 6 pozisyonundan metil ve etil gruplarının eklenmesiyle değişime uğramış alkillenmiş guaninler bu yolla onarılır.

DNA hasarının doğrudan geri döndürülmesi • UV ışını ile uyarılan en yaygın DNA hasarı aynı DNA ipliği üzerindeki komşu iki pirimidinin 5 ve 6. karbonları arasındaki çift bağın doyurulması sonucunda iki pirimidinin siklobütan halkasıyla birleşmesi ile oluşan pirimidin dimerleridir. • Bu dimerlerin oluşumu DNA zincirinin yapısında biçim bozukluklarına neden olur ve hasarlı bölgeyi geçerken replikasyon ve transkripsiyonu durdurur. • Onarılmaları hücrenin UV ışığına karşı dayanıklılığı ile yakından ilişkilidir. • Siklobütan halka yapısının kırılması için gerekli olan enerji görünür ışıktan sağlandığı için bu süren fotoreaktivasyon olarak adlandırılır.

Fotoreaktivasyon • • Normal yapılarına döndürülmüş olan orijinal pirimidin bazları DNA’da kalır. Güneş’ten gelen UV ışınının farklı hücrelerde başlıca DNA hasar olmasının sonucu olarak pirimidin dimerlerinin fotoreaktivasyon ile uzaklaştırılması <e. coli, maya ve bazı bitki ve hayvan türlerinde ortaktır. Bununla birlikte fotoreaktivasyon genellenemez Birçok tür (insan dahil) bu DNA onarım mekanizmasına dahil değildir.
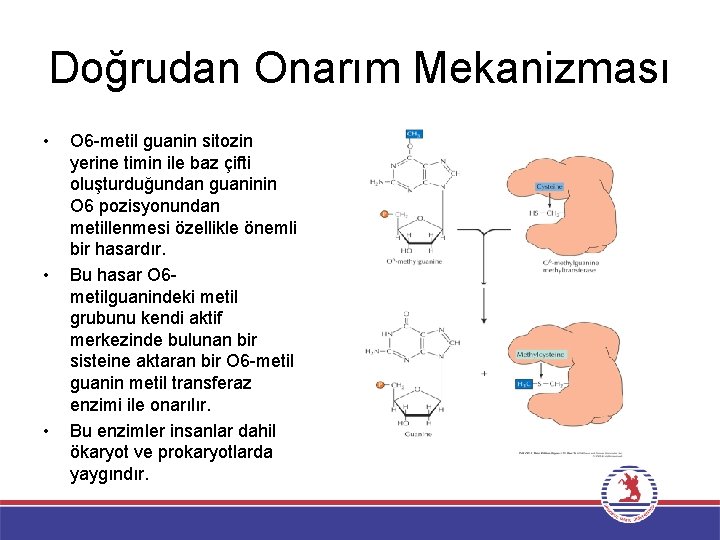
Doğrudan Onarım Mekanizması • • • O 6 -metil guanin sitozin yerine timin ile baz çifti oluşturduğundan guaninin O 6 pozisyonundan metillenmesi özellikle önemli bir hasardır. Bu hasar O 6 metilguanindeki metil grubunu kendi aktif merkezinde bulunan bir sisteine aktaran bir O 6 -metil guanin metil transferaz enzimi ile onarılır. Bu enzimler insanlar dahil ökaryot ve prokaryotlarda yaygındır.

Kesip Çıkararak Onarım • Doğrudan onarım DNA hasarlarının tamirinde etkin olmakla beraber kimyasal değişimin onarımı için kesip çıkararak hatanın düzeltilmesi daha genel bir mekanizmadır. • Kesip çıkararak onarımın değişik tipleri prokaryot ve ökaryot hücrelerin herikisi için de en önemli DNA onarım mekanizmasıdır.

Kesip Çıkararak Onarım 1. Hasarlı DNA tanınır. 2. Serbest baz ya da nukleotidler halinde çıkarılır. 3. Oluşan boşluk hasarsız tamamlayıcı iplik kalıp olarak kullanılarak sentezlenen yeni bir DNA ipliği ile doldurulur.

Kesip Çıkararak Onarım Hücrelerin değişik tipteki DNA hasarlarının onarımı için üç çeşit kesip çıkararak onarım tipi bulunmaktadır. 1. Baz çıkarma 2. Nükleotid çıkarma 3. Hatalı eşleşme onarımı

Baz Çıkarma Onarımı Urasil içeren DNA’nın onarımı hasarlı tek bazların tanınarak DNA molekülünden uzaklaştırıldığı baz çıkarma onarımı için iyi bir örnektir.

Baz Çıkarma Onarımı • DNA’da urasil iki mekanizma ile ortaya çıkar 1. Urasil (d. UTP[deoksiüridin trifosfat] DNA sentezi sırasında nadiren timinin yerine katılır. 2. Urasil sitozinin deaminasyonu ile oluşabilir • İkinci mekanizma tamamlayıcı baz eşleşme düzenini değiştirmesi ve mutajenik bir etki göstermesi nedeniyle biyolojik anlamda büyük önem taşır. • DNA’daki urasil DNA omurgasındaki deoksiriboz ile baz (urasil) arasındaki bağı koparan DNA glikozilaz tarafından çıkarılır.
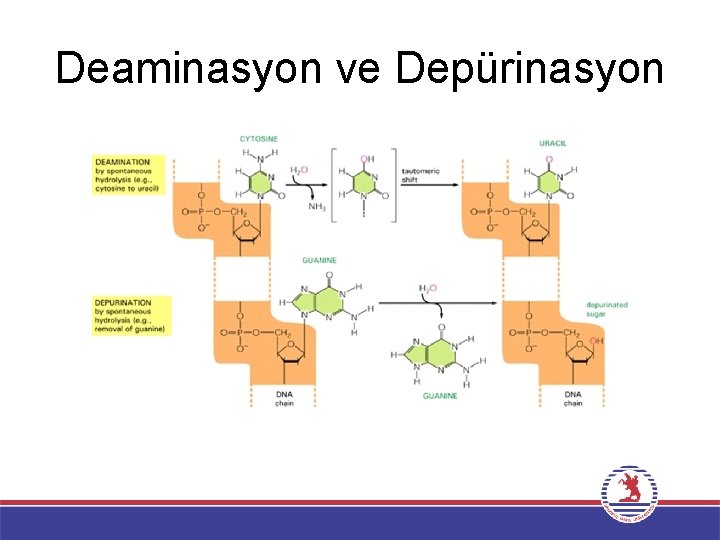
Deaminasyon ve Depürinasyon

DNA nükleotidlerinin deaminasyonu Ave G’nin spontan deaminasyonu doğal olmadığı için tanınır ve onarılır. C, U ve T deaminasyon için amino grubuna sahip değildir. C nukleotidleri gen anlatımını kontrol etmek için metillenir. 5 -metil C nukleotidleri deaminasyona uğradığında T nukleotidi oluşur. T zıt iplikteki G ile eşleşir ve yanlış eşleşme oluşur.
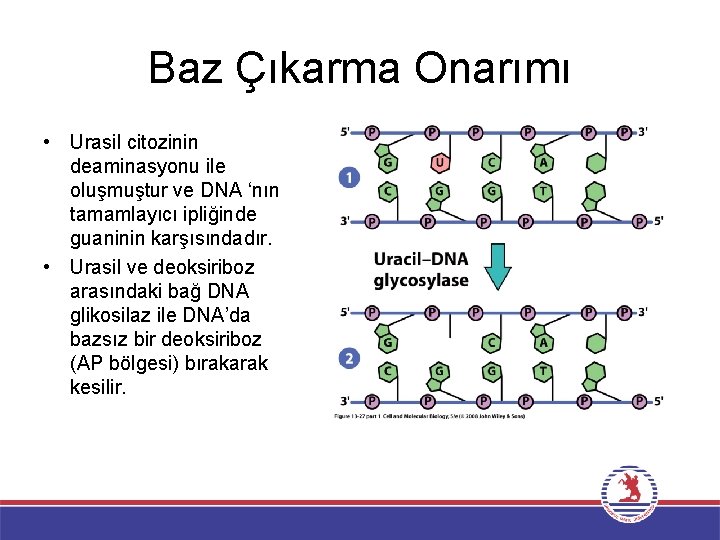
Baz Çıkarma Onarımı • Urasil citozinin deaminasyonu ile oluşmuştur ve DNA ‘nın tamamlayıcı ipliğinde guaninin karşısındadır. • Urasil ve deoksiriboz arasındaki bağ DNA glikosilaz ile DNA’da bazsız bir deoksiriboz (AP bölgesi) bırakarak kesilir.

Baz Çıkarma Onarımı DNA glikozilaz ayrıca adeninin deaminasyonu ile oluşan hipoksantin , pirimidin dimerleri , O 6 metil guanin dışındaki alkillenmiş pürinleri ve oksidasyon veya iyonize radyasyon ile hasarlanan bazlar gibi normal olmayan bazları da tanır ve uzaklaştırır.
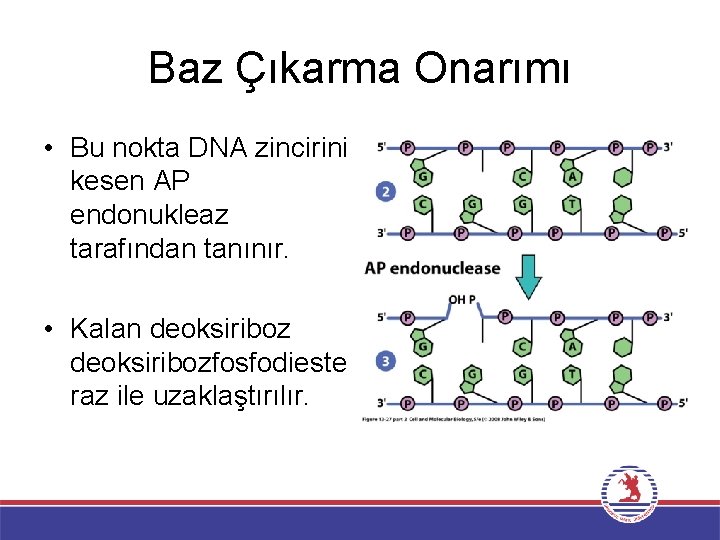
Baz Çıkarma Onarımı • Bu nokta DNA zincirini kesen AP endonukleaz tarafından tanınır. • Kalan deoksiribozfosfodieste raz ile uzaklaştırılır.
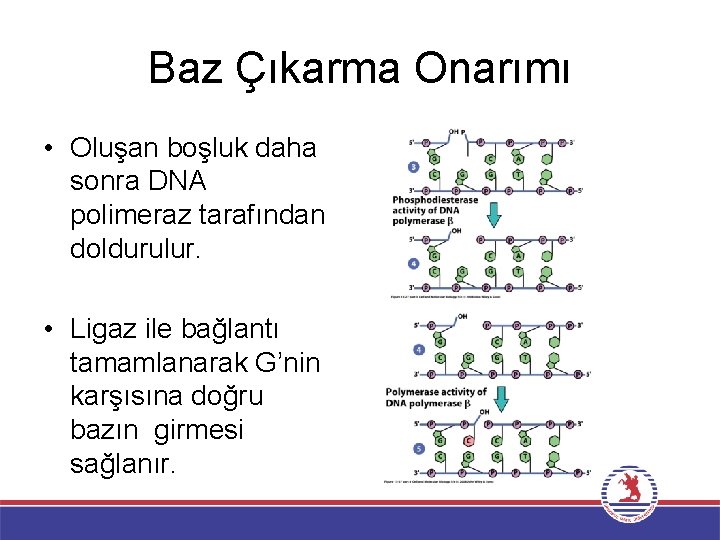
Baz Çıkarma Onarımı • Oluşan boşluk daha sonra DNA polimeraz tarafından doldurulur. • Ligaz ile bağlantı tamamlanarak G’nin karşısına doğru bazın girmesi sağlanır.

Polimerizasyon ve Ligaz ile Bağlanma
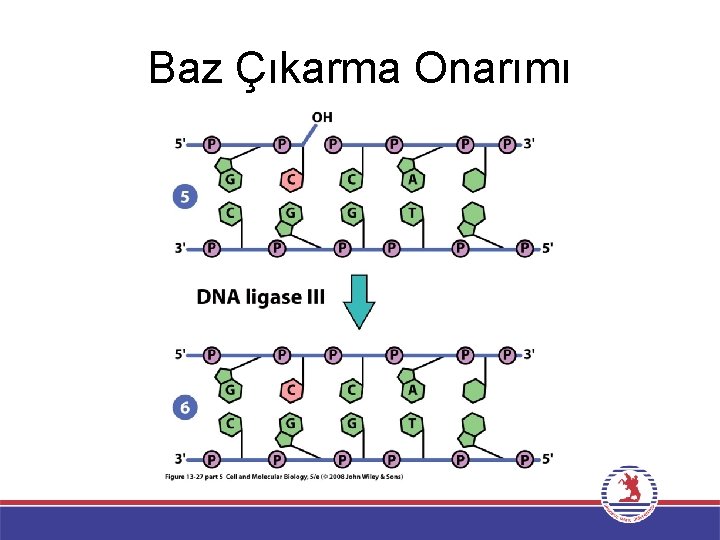
Baz Çıkarma Onarımı
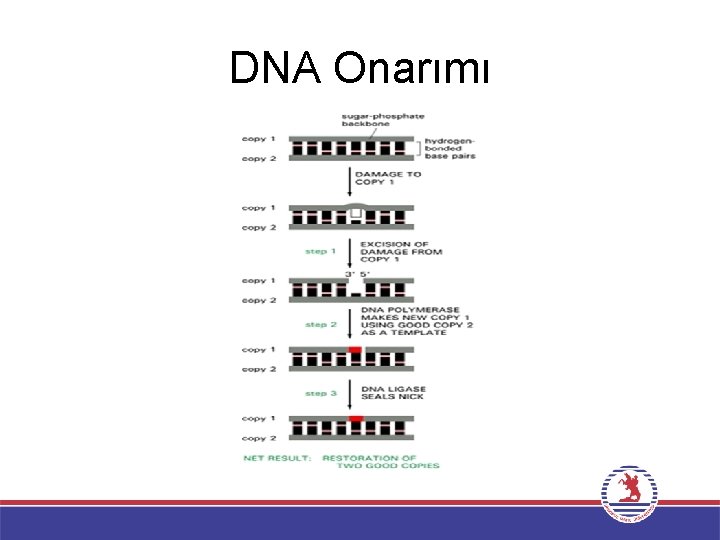
DNA Onarımı

Nukleotid Çıkarma Onarımı • DNA glikozilazlar sadece spesifik hasarlı baz tiplerini tanıdığı halde diğer kesip-çıkararak onarım sistemleri DNA molekülünü çarpıtan UV ile indüklenmiş pirimidin dimerleri gibi çeşitli hatalı bazları ve DNA ile bir çok karsinojenin etkileşimi sonucu DNA’ya eklenen büyük kitleler gibi geniş çeşitlilikte hasarları tanırlar. • Hasarlı bazların lezyonu içeren oligonukleotidle birlikte uzaklaştırılması sebebiyle bu yaygın DNA onarım formu nukleotid – çıkarma onarımı olarak adlandırılır.

Timin Dimerlerinin Nükleotid Çıkarma Onarımı • E. colide nukleotid çıkarma onarımı üç genin (uvr. A, B ve C) ürünleri tarafından katalizlenir. • Uvr. A proteini hasarlı DNA’yı tanırve Uvr. B ile Uvr. C’yi bu bozuk bölgeye sürükler. • Daha sonra Uvr. B ve Uvr. Chasarlı bölgeyi sırasıyla 3’ ve 5’ taraflarından keserek 12 ila 13 bazlık bir oligonukleotid çıkarırlar. • Uvr. ABC kompleksi eksonukleaz olarak adlandırılır. • Hasar içeren oligonukleotidin çift iplikli DNA molekülünden uzaklaştırılması için helikaz aktivitesi gerekir. • Oluşan boşluk DNA polimeraz I ile doldurulur ve ligaz ile uçlar bağlanır

Timin Dimerlerinin Nükleotid Çıkarma Onarımı Hasarlı DNA tanınır ve timin dimerinin heriki yanından, 3’ ve 5’ nukleazlar tarafından kesilir.

Timin Dimerlerinin Nükleotid Çıkarma Onarımı • Helikaz ile bölgenin açılması hasarlı bazı içeren oligonukleotidin uzaklaştırılmasıyla sonuçlanır. • Oluşan boşluk DNA polimeraz ile doldurulur ve ligaz tarafından bağlantı tamamlanır.

Nükleotid Çıkarma Onarımı • NÇO sistemi maya kemirgen ve insanları da kapsayan ökaryotlarda kapsamlı bir şekilde çalışılmıştır. • Mayalarda E. coli ’de olduğu gibi DNA onarımıyla ilişkili birkaç gen (radyasyon) duyarlılığı nedeniyle RAD genleri olarak adlandırılır) UV ışığına aşırı duyarlı mutantların izolasyonu ile tanımlanmıştır. • İnsanda DNA onarım genleri DNA onarımı kusurlu kalıtsal hastalıkları barındıran bireylerde yapılan çalışmalarda tanımlanmıştır.

Nükleotid Çıkarma Onarımı • Bu hastalıklardan en fazla çalışılanı 250. 000 kişiden birini etkileyen nadir bir genetik hastalık olan xeroderma pigmentosum (XP)’dur. • Bu hastalığı taşıyan bireyler UV ışığına aşırı duyarlıdır ve güneş gören vücut bölgelerinde yaygın deri kanserleri geliştirirler

Nükleotid Çıkarma Onarımı • 1968 yılında James Cleaver XP hastalarının nükleotid-çıkarma onarım sisteminin kusurlu olduğunu göstererek kanser ve DNA onarımı arasındaki bağı gösterdi. • Bu bulgu sadece XP hastalında değil ayrıca DNA onarım kusurunda kaynaklanan iki farklı insan hastalığı (*Cockayne sendromu ve ^trichothiodystrophy) ve bir kemirgen hücre hattının UV duyarlı mutantlarından elde edilen verilerle de kanıtlanmıştır. *Cockayne sendromu gerçekten nadir rastlanan ancak hemen, hemen istisnasız olarak hastayı çok erken yaşta ölüme götüren ağır bir genetik hastalıktır. Hastalığın temel bulguları güneş ışığına hassasiyet, cücelik ve erken yaşlanma belirtileri ile karakterize git gide ağırlaşan bir seyir göstermesidir. ^Otozomal resesif kalıtılan, sülfür içeriği çok düşük olan anormal, kısa ve kırılgan saçlarla karakterize hastalık grubudur.

Nükleotid Çıkarma Onarımı • Moleküler klonlama ile XP’da mutasyona uğrayan 7 farklı onarın geni (FPA-XPG) tanımlanmıştır. • Memeli DNA onarım genleri tarafından kodlanan proteinlerin maya RAD genleri tarafından kodlanan proteinlere yakın benzerlik göstermesi, nukleotid çıkarma onarımının ökaryotlarda korunmuş olduğunu gösterir. • Klonlanmış memeli ve maya onarım genlerinin kodladıkları proteinleri saflaştırılması ve onarım sistemindeki rollerini araştırmak üzere in vitro sistemler geliştirilmiştir.

Nükleotid Çıkarma Onarımı • • Memeli hücrelerindeki kesip çıkararak onarımın ilk basamağı, hatalı baz eşleşmesinin XPC ile maya Rad 23 proteinin homologu olan ve h. HR 23 B adlı bir proteinden oluşan kompleks tarafından tanınmasıdır. Bunu çok altbirimli bir transkripsiyon faktörü (TFIIH)’nün bileşenleri olan XPB ve XPD proteinleri (helikaz aktivitesi) ile XPG (endonukleaz aktivitesi) proteinlerinin toplanması izler.

Nükleotid Çıkarma Onarımı • • • XPA protein hasarını onaylar. XPF proteinini ERCC 1 (UV duyarlı kemirgen hücrelerinde tanımlanmış onarım prteini) ile heterodimer yapmış olarak onarım kompleksine ekler. XPF/ERCC 1 ve XPG, DNA’yı hasarlı bölgenin sırasıyla 5’ ve 3’ yanlarından kesen endonukleazlardır. Bu kesim ~ 30 bç. ’lik oligonukleotidi çıkarır. Ortaya çıkan boşluk DNA polimeraz δ ve ε ile doldurulur. Ligaz tarafından uçlar birleştirilir.

Nükleotid Çıkarma Onarımı • XPC/h. HR 23 B kompleksi genom boyunca hasarlı DNA’yı tanırken nukleotid – çıkarma onarımının transkripsiyon eşlikli onarım olarak adlandırılan alternatif formu özgün olarak aktif transkribsiyona uğrayan gen içerisindeki hasarların onarımını gerçekleştirir. • Onarım ve transkripsiyon arasındaki bağlantı ilk kez memeli hücrelerinde ve E. coli’de transkripsiyon olan ipliklerin olmayanlardan daha hızlı onarıldığını gösteren deneyler ile ortaya atılmıştır. • DNA hasarı onarımı baskıladığından transkripsiyon-onarım eşleşmesinin aktif olarak anlatım yapan genlerin hasarının öncelikli olarak onarılmasını sağladığı için avantajlı olduğu düşünülmektedir.

Transkripsiyon Eşlikli Onarım E. coli’de kopyalanan DNA ipliğinde bir hasara takılmış olan RNA polimerazın tanınmasını gerektirir. • Duran RNA polimeraz transkripsiyon onarım eşleşme faktörü adı verilen ve RNA polimerazı hasarlı bölgeden ayırıp Uvr. ABC eksonukleazı göreve çağıran bir protein tarafından tanınır. Memeli hücrelerinde ise transkripsiyon – eşlikli onarım duran RNA polimerazın CSA ve CSB proteinleri tarafından tanınmasını gerektirir. Bu proteinler de Cockayne sendromunda etkili olan genler tarafından kodlanmaktadır. XP hastalarının aksine Cockayne sendromu hastalarında transkripsiyon eşilikli onarım bakımından kusurludurlar. CSA ve CSB, XPC/h. HR 23 B kompleksine benzer hareket ederler.
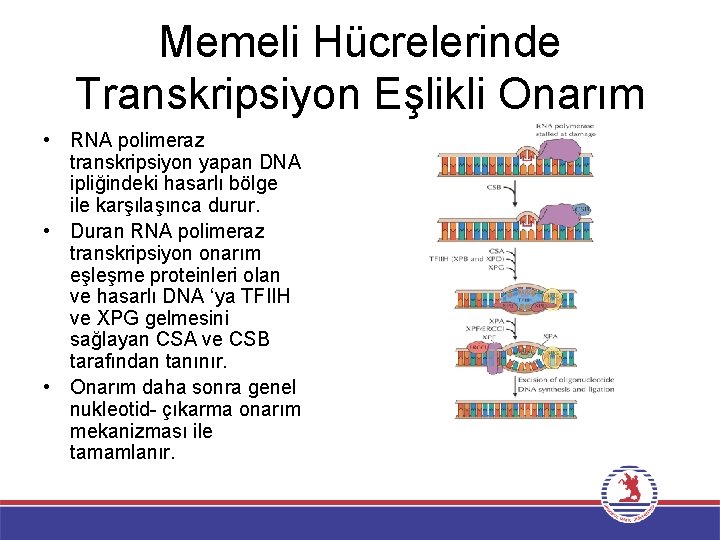
Memeli Hücrelerinde Transkripsiyon Eşlikli Onarım • RNA polimeraz transkripsiyon yapan DNA ipliğindeki hasarlı bölge ile karşılaşınca durur. • Duran RNA polimeraz transkripsiyon onarım eşleşme proteinleri olan ve hasarlı DNA ‘ya TFIIH ve XPG gelmesini sağlayan CSA ve CSB tarafından tanınır. • Onarım daha sonra genel nukleotid- çıkarma onarım mekanizması ile tamamlanır.
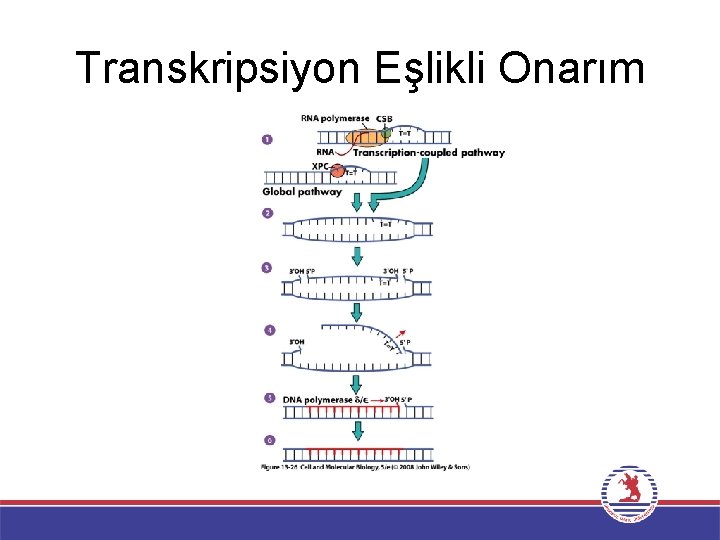
Transkripsiyon Eşlikli Onarım
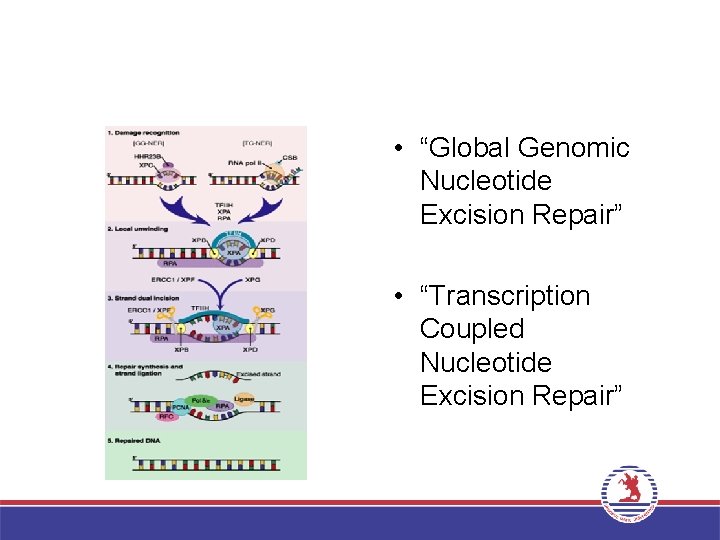
• “Global Genomic Nucleotide Excision Repair” • “Transcription Coupled Nucleotide Excision Repair”

Yanlış Eşleşme Onarım Sistemi • Üçüncü onarım sistemi DNA replikasyon sürecinde yanlış eşleşmiş bazları tanıyarak düzeltir. • Birçok yanlış eşleşmiş baz yeni sentezlenmiş DNA’yı tarayan DNA polimerazın kendi yanlışını düzeltme aktivitesi ile düzeltilir. • Gözden kaçan hatalar yanlış eşleşme onarım sistemi tarafından onarılarak orijinal dizinin korunması sağlanır.

Yanlış Eşleşme Onarım Sistemi E. coli • Atasal DNA ipiliği ile yeni sentezlenen DNA ipliğini birbirinden ayırt edebilmesi bu bakterinin DNA’sının GATC dizisinde yer alan adeninin 6 metiladenin şeklinde değiştirilmesi esasına dayanır. • Metillenme replikasyondan sonra oluştuğu için yeni sentezlenen DNA iplikleri metillenmez böylelikle yanlış eşleşme onarım enzimleri tarafından özgün şekilde tanınır.
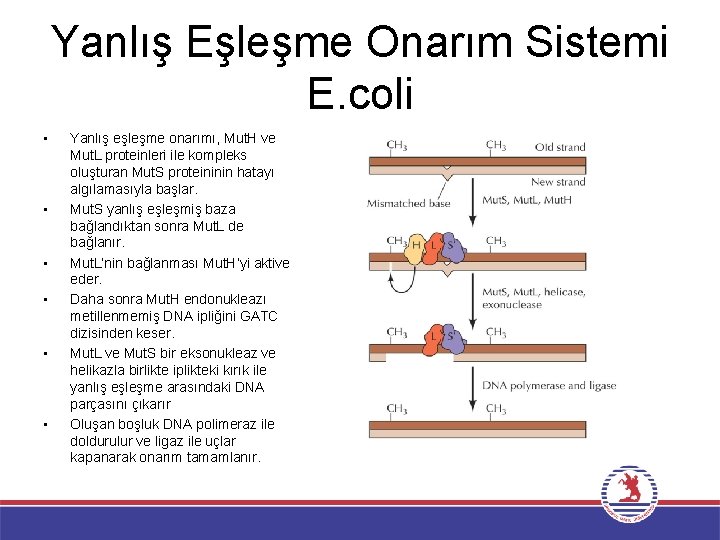
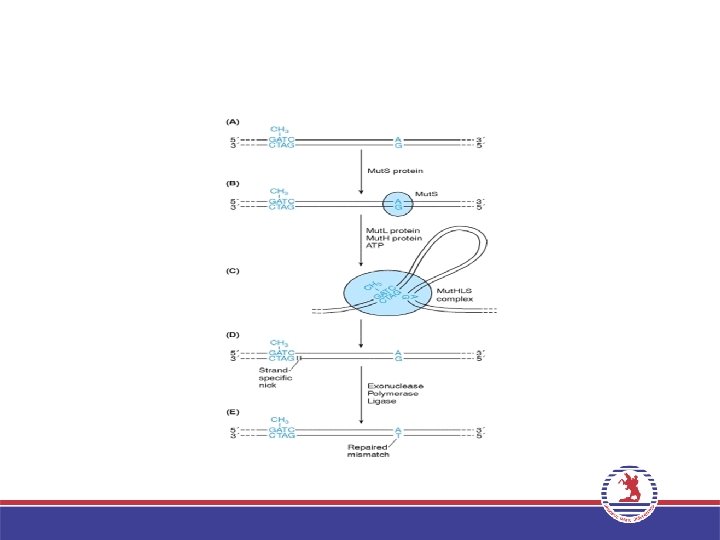
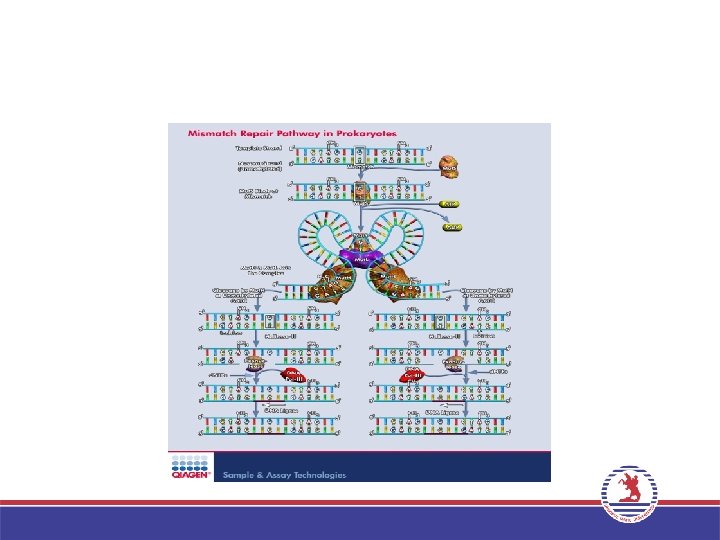
Yanlış Eşleşme Onarım Sistemi E. coli • • • Yanlış eşleşme onarımı, Mut. H ve Mut. L proteinleri ile kompleks oluşturan Mut. S proteininin hatayı algılamasıyla başlar. Mut. S yanlış eşleşmiş baza bağlandıktan sonra Mut. L de bağlanır. Mut. L’nin bağlanması Mut. H’yi aktive eder. Daha sonra Mut. H endonukleazı metillenmemiş DNA ipliğini GATC dizisinden keser. Mut. L ve Mut. S bir eksonukleaz ve helikazla birlikte iplikteki kırık ile yanlış eşleşme arasındaki DNA parçasını çıkarır Oluşan boşluk DNA polimeraz ile doldurulur ve ligaz ile uçlar kapanarak onarım tamamlanır.

Yanlış Eşleşme Onarım Sistemi Memeli • Temelde E. coli ile benzer sisteme sahiptir. • Yanlış baz eşleşmesi onarımında iplik özgünlüğü DNA metilasyonu ile tanımlanmamaktadır. • Yeni sentezlenmiş iplikteki tek iplik kıvrımlarının varlığı veya Mut. Sve Mut. L’nin ökaryot homologlarının replikasyon sistemi ile biraraya gelmesi onarılacak ipliği belirliyor olabileceği ileri sürülmektedir. • Mut. S ve Mut. L homologları yanlış eşleşmiş baza bağlanırlar ve E. coli’de olduğu gibi hatalı eşleşmenin olduğu bölgeyi çıkarırlar. • Muts ve Mut. L ‘nin insandaki eşdeğerlerinde mutasyonların yaygın bir kalıtsal kolon kanseri tipinin oluşumundan sorumlu olması bu onarım sisteminin önemini göstermektedir.

Yanlış Eşleşme Onarım Sistemi Memeli • HNPCC “Hereditary nonpolyposis colorectal cancer” en yaygın kalıtsal hastalıklardan biridir. ABD’de kolorektal kanserlerin %15’in oluşum nedenidir. Her 200 kişiden 1’inde görülür. • Yanlış eşleşme onarımındaki aksaklık ile HNPCC arasındaki ilişki 1993 de iki araştırma grubunun Mut. S’nin insan homologunu klonlamaları ve bu gendeki mutasyonların bütün HNPCC vakalarının yarısından sorumlu olduğunu bulmaları ile keşfedilmiştir. • Daha sonraki çalışmalar da geri kala HNPCC olgularının çoğunun Mut. L’nin eşdeğeri olan üç insan geninden birindeki mutasyonlardan kaynaklandığını göstermiştir. • Bu genlerdeki bozukluğun hücrenin diğer genlerinde mutasyon sıklığını artırdığı ve bu mutasyonlardan bazılarının sonuçta kansere neden olma olasılığının da bununla uyumlu olacak şekilde artacağı öngörülmektedir.
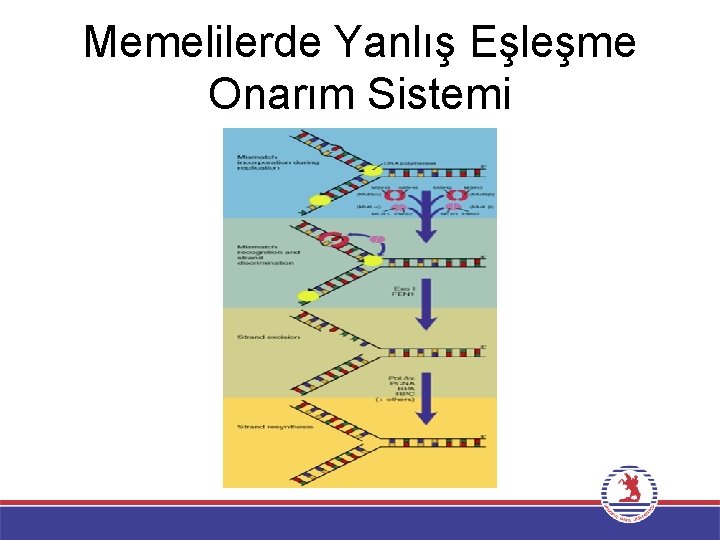
Memelilerde Yanlış Eşleşme Onarım Sistemi

Hata Eğilimli Onarım • Doğrudan uzaklaştırma ve kesip çıkararak onarım sistemleri DNA hasarını replikasyondan önce onarırlar. • Bu sistemler başarısız olursa hücrenin , replikasyon çatalında hasarlı DNA’yı onarabileceği alternatif mekanizmaları bulunmaktadır. • Pirimidin dimerleri ve diğer birçok hasarlı bölge DNA polimerazın normal işleviyle kopyalanamaz. • Replikasyon bu hasarlı bölgeye geldiğinde durur. • Hücreler DNA’nın hasarlı bölgesinde replikasyonu devam ettirebilen sıra dışı özelleşmiş DNA polimeraza da sahiptir. • Bu şekilde replikasyon ile doğru olmayan bazların eklenme olasılığı artabilir, bu nedenle DNA hasarının bu şekilde düzeltilmesine hata eğilimli onarım adı verilir.

Hata Eğilimli Onarım Prokaryotik • İlk hata eğilimli DNA polimeraz 1999 yılında E. coli’de bulunmuştur. Bu enzim DNA polimeraz V olarak adlandırılır ve aşırı UV radyasyonuna yanıt olarak indüklenmekte ve timin dimerleri üzerinden yeni DNA ipliğinin sentezini gerçekleştirebilmektedir. • Diğer iki E. coli DNA polimerazı Polimeraz II ve IV de benzer şekilde DNA hasarı ile indüklenirler ve hata eğilimli onarımda görev alırlar.
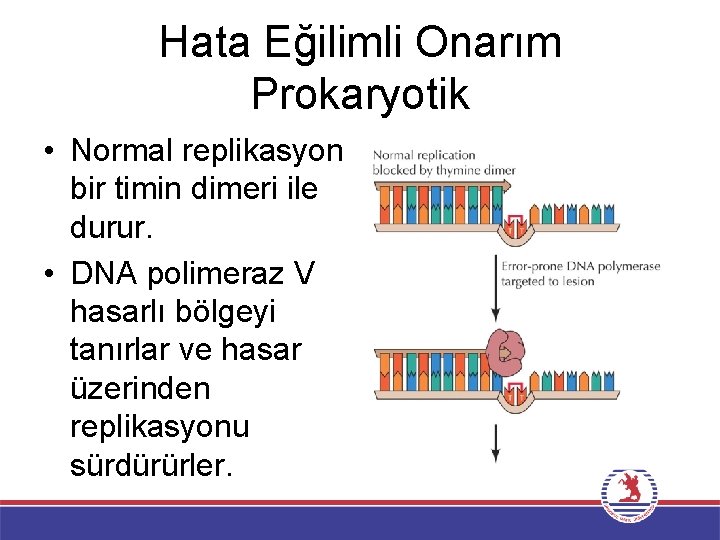
Hata Eğilimli Onarım Prokaryotik • Normal replikasyon bir timin dimeri ile durur. • DNA polimeraz V hasarlı bölgeyi tanırlar ve hasar üzerinden replikasyonu sürdürürler.
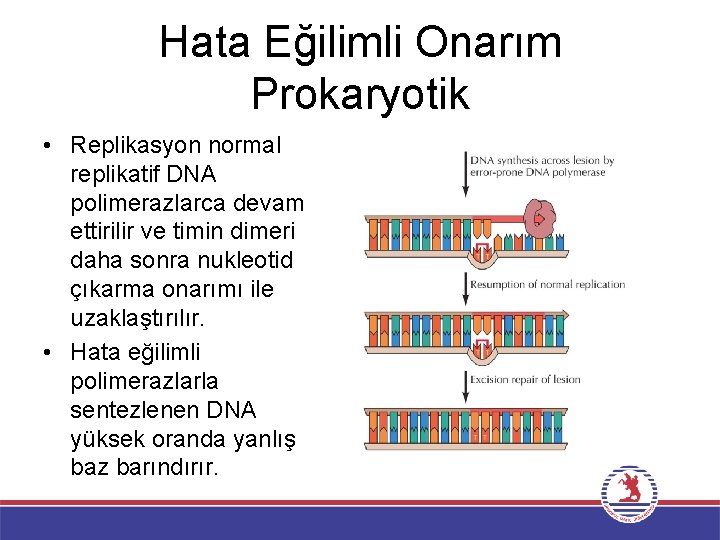
Hata Eğilimli Onarım Prokaryotik • Replikasyon normal replikatif DNA polimerazlarca devam ettirilir ve timin dimeri daha sonra nukleotid çıkarma onarımı ile uzaklaştırılır. • Hata eğilimli polimerazlarla sentezlenen DNA yüksek oranda yanlış baz barındırır.

Hata Eğilimli Onarım Ökaryotik • Ökaryot hücreler de çok sayıda hata eğilimli onarım DNA polimerazları içerirler • Bugüne kadar insanda 9 adet polimeraz saptanmıştır. • Bütün bu DNA polimerazlar hasarlı olmayan DNA’yı kopyaladıklarında düşük doğrulukta çalışırlar. • Normal replikatif DNA polimerazlara (örn, E. coli’de polimeraz III ve ökaryotlarda δ ve ε) kıyasla hata oranları 100 -10. 000 kez daha yüksektir. • Ek olarak hata eğilimli polimerazlar normal replikatif polimerazlar gibi 3’ den 5’ne yanlış düzeltme aktivitesine sahip değildir.

Hata Eğilimli Onarım • Hata eğilimli polimerazların hasarlı DNA’daki spesifik hasarlı bölge karşısına doğru bazları yerleştirmek üzere özelleşmiş olmaları ve hasarlı DNA’yı kalıp olarak kullanarak doğru bir yeni iplik sentezlemeleri önemlidir. • E. coli polimeraz V spesifik olarak timinleri tanır ve doğru biçimde karşı ipliğe AA ekler. • Diğer taraftan polimeraz V başka tipte hasarları olan bir ipliğin karşısına yeni bir DNA ipliğini sentezlediğinde yüksek oranda hata yapar.
- Slides: 56