znme durumuna gre Tam znme Bir elementin dieri
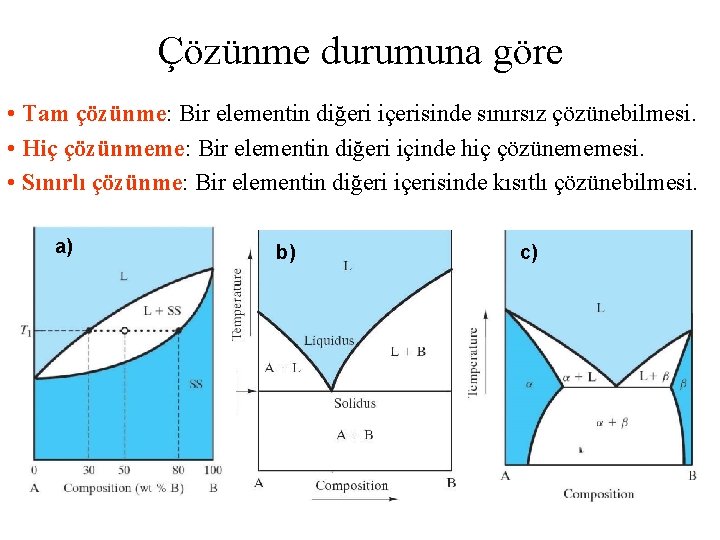
Çözünme durumuna göre • Tam çözünme: Bir elementin diğeri içerisinde sınırsız çözünebilmesi. • Hiç çözünmeme: Bir elementin diğeri içinde hiç çözünememesi. • Sınırlı çözünme: Bir elementin diğeri içerisinde kısıtlı çözünebilmesi. a) b) c)

Gibbs Faz kuralı • Bir sistemde bileşen ve faz sayısının belirli olması durumunda serbest değişken olup olmadığını belirlemede kullanılan bir kuraldır. Basıncın değişken bir parametre olması durumu F=C–P+2 Basıncın sabit olması durumu (en çok kullanılan bağıntı) F=C–P+1 Serbest değişken sayısı Faz sayısı Bileşen sayısı

Erime noktasında Gibbs kuralı • Diyagramda saf element için erime noktasındaki (TA) durum: • P = 2 (sıvı ve olarak 2 faz) • C = 1 (Tek bileşen A) F=1 -2+1=0 T TA • Basınç sabit, kimyasal Sıvının soğuması bileşimde değişmediği için tek değişken olan sıcaklıktır. Katılaşma aralığı Ancak buda erime/katılaşma boyunca sıcaklık sabittirserbest değişken bulunmaz t nın soğuması

b noktasında: • P=2 (2 Faz: sıvı ve ) • C=2 (Bileşenler: A ve B) • F=2– 2+1=1 • Tek değişken: Sıcaklık a noktasında: • P=2 (2 Faz: sıvı ve ) • C=2 (Bileşenler: A ve B) • F=2– 2+1=1 • Tek değişken: Sıcaklık c noktasında: • P=1 (1 Faz: sıvı) • C=2 (Bileşenler: A ve B) • F = 2 -1 + 1 = 2 • Değişkenler: Sıcaklık ve bileşim.
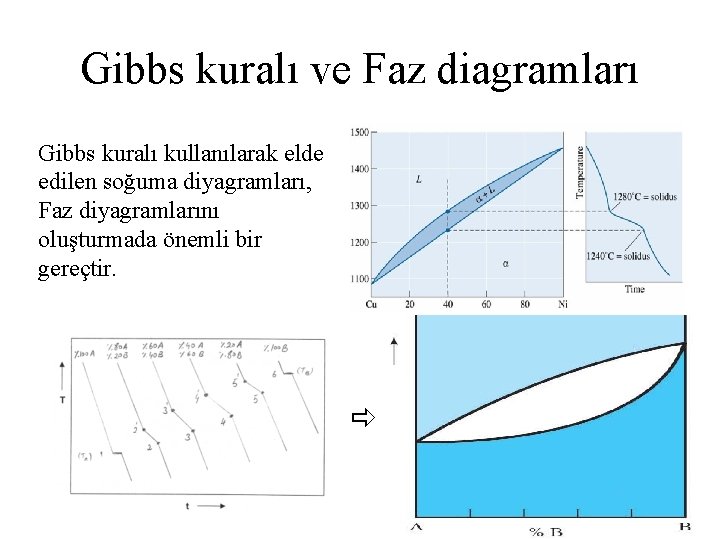
Gibbs kuralı ve Faz diagramları Gibbs kuralı kullanılarak elde edilen soğuma diyagramları, Faz diyagramlarını oluşturmada önemli bir gereçtir.

Örnek Cu-40% Ni alaşımı için aşağıdaki sıcaklıklarda serbestlik derecelerini bulunuz (a) 1300 o. C, (b) 1250 o. C, and (c) 1200 o. C. Cu - Ni faz diyagramlarında Basınç sabit olduğu için eşitlik: (1 + C = F + P) olur. (a) 1300 o. C, (a) P=1 (Sadece sıvı faz), (b) C=2 (Cu ve Ni) Böylece; 1+C=F+P 1+2=F+1 F=2
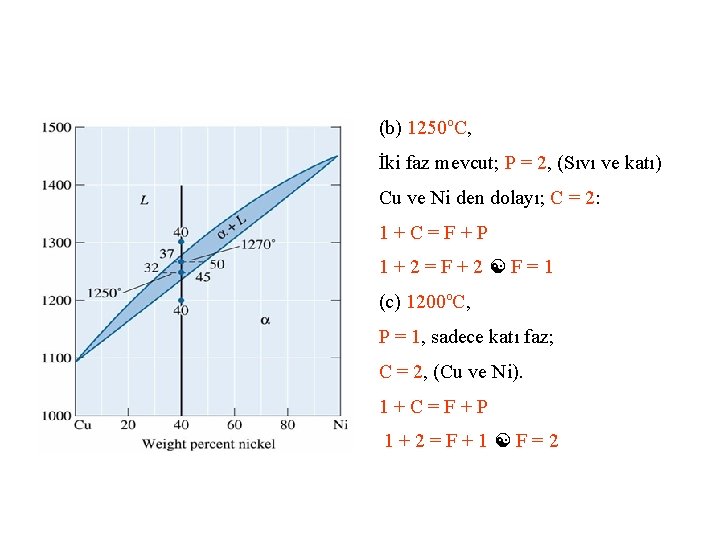
(b) 1250 o. C, İki faz mevcut; P = 2, (Sıvı ve katı) Cu ve Ni den dolayı; C = 2: 1+C=F+P 1+2=F+2 F=1 (c) 1200 o. C, P = 1, sadece katı faz; C = 2, (Cu ve Ni). 1+C=F+P 1+2=F+1 F=2

Terazi kuralı Faz diyagramları: • Hangi sıcaklık ve bileşimde hangi fazlar var? • Bu fazların bileşimi nedir? Faz diyagramında, fazların oranlarını ve bileşimlerini bulmak için terazi kuralı (lever rule) kullanılır.
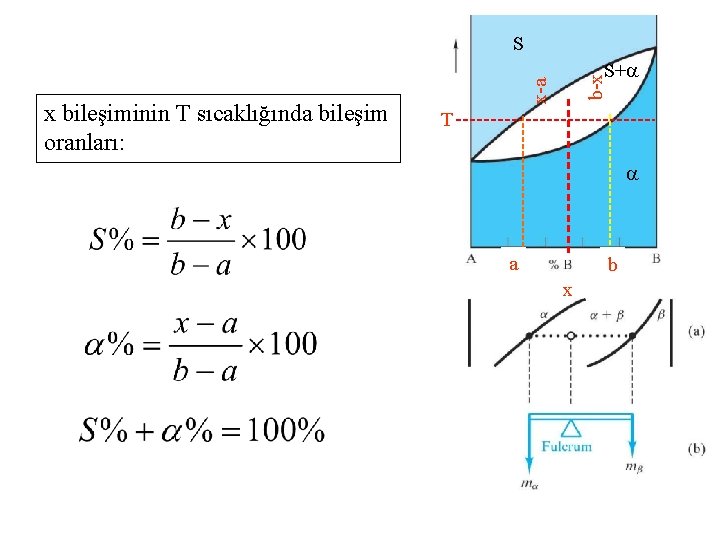
S b-x x-a x bileşiminin T sıcaklığında bileşim oranları: S+ T a b x
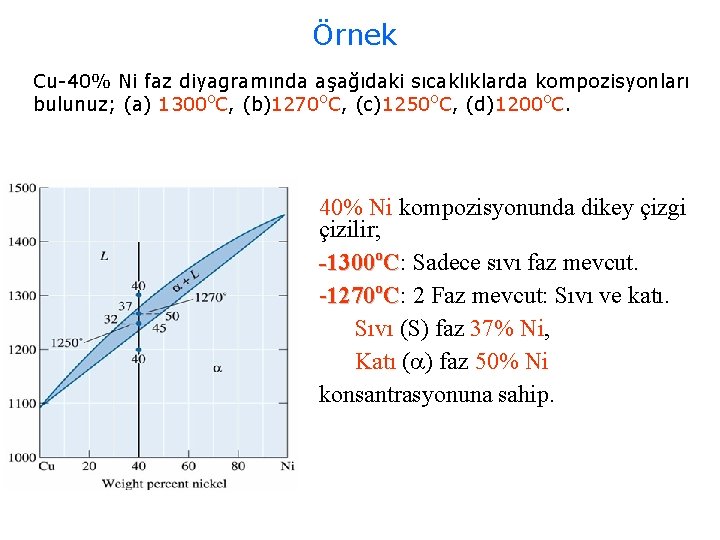
Örnek Cu-40% Ni faz diyagramında aşağıdaki sıcaklıklarda kompozisyonları bulunuz; (a) 1300 o. C, (b)1270 o. C, (c)1250 o. C, (d)1200 o. C. 40% Ni kompozisyonunda dikey çizgi çizilir; -1300 o. C: Sadece sıvı faz mevcut. -1270 o. C: 2 Faz mevcut: Sıvı ve katı. Sıvı (S) faz 37% Ni, Katı ( ) faz 50% Ni konsantrasyonuna sahip.
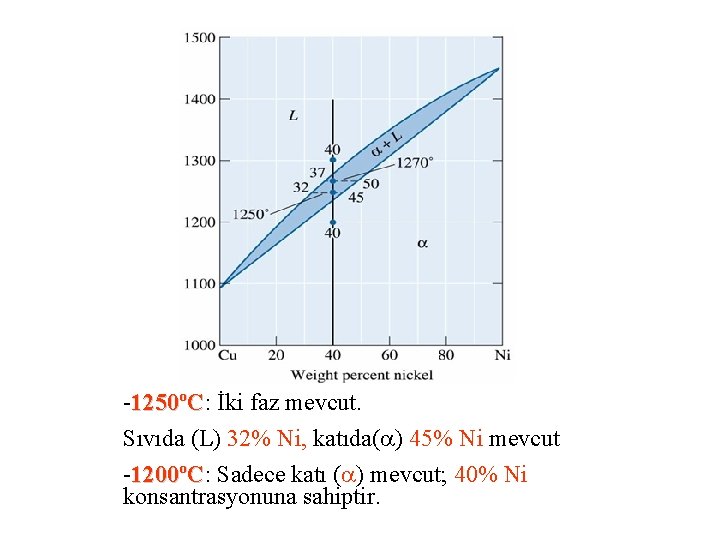
-1250 o. C: İki faz mevcut. Sıvıda (L) 32% Ni, katıda( ) 45% Ni mevcut -1200 o. C: Sadece katı ( ) mevcut; 40% Ni konsantrasyonuna sahiptir.
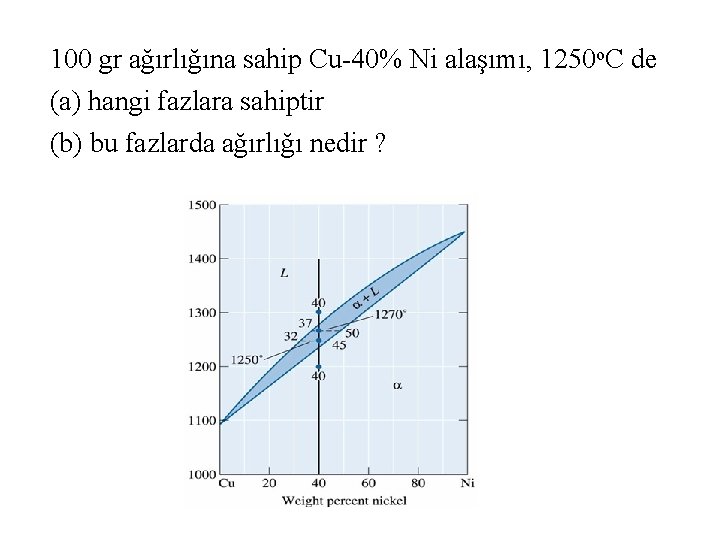
100 gr ağırlığına sahip Cu-40% Ni alaşımı, 1250 o. C de (a) hangi fazlara sahiptir (b) bu fazlarda ağırlığı nedir ?
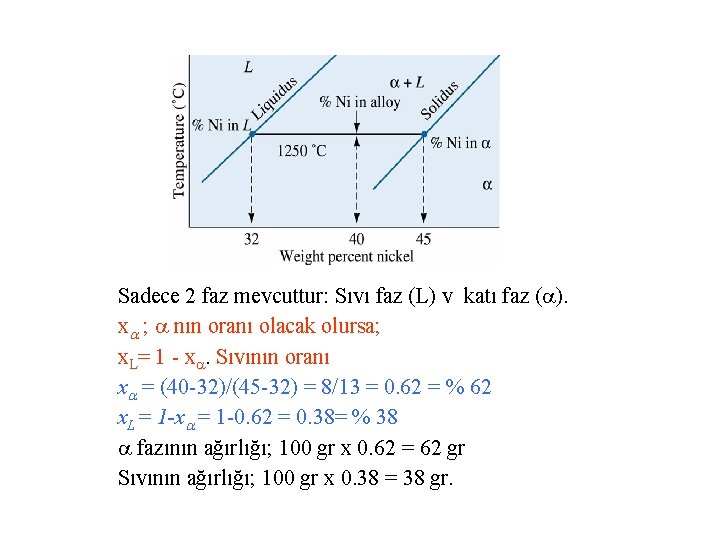
Sadece 2 faz mevcuttur: Sıvı faz (L) v katı faz ( ). x ; nın oranı olacak olursa; x. L= 1 - x. Sıvının oranı x = (40 -32)/(45 -32) = 8/13 = 0. 62 = % 62 x. L = 1 -x = 1 -0. 62 = 0. 38= % 38 fazının ağırlığı; 100 gr x 0. 62 = 62 gr Sıvının ağırlığı; 100 gr x 0. 38 = 38 gr.
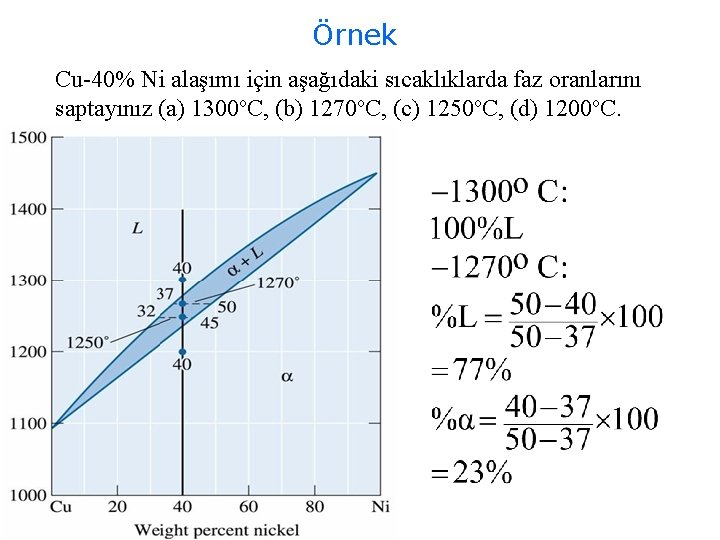
Örnek Cu-40% Ni alaşımı için aşağıdaki sıcaklıklarda faz oranlarını saptayınız (a) 1300 o. C, (b) 1270 o. C, (c) 1250 o. C, (d) 1200 o. C.

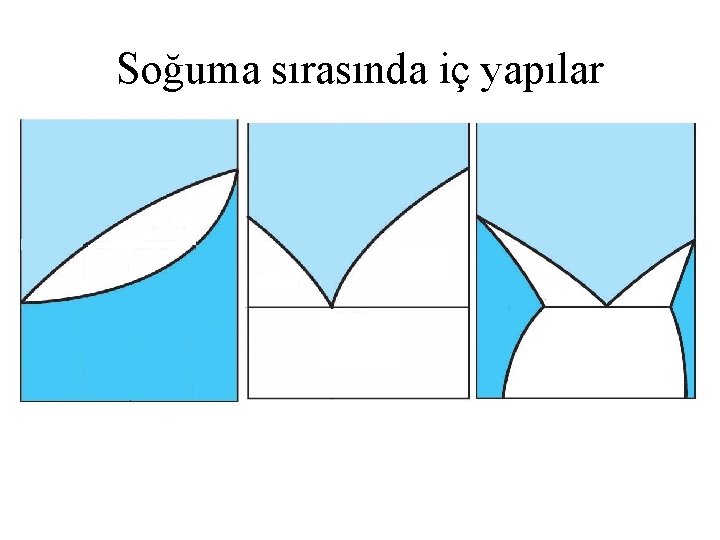
Soğuma sırasında iç yapılar
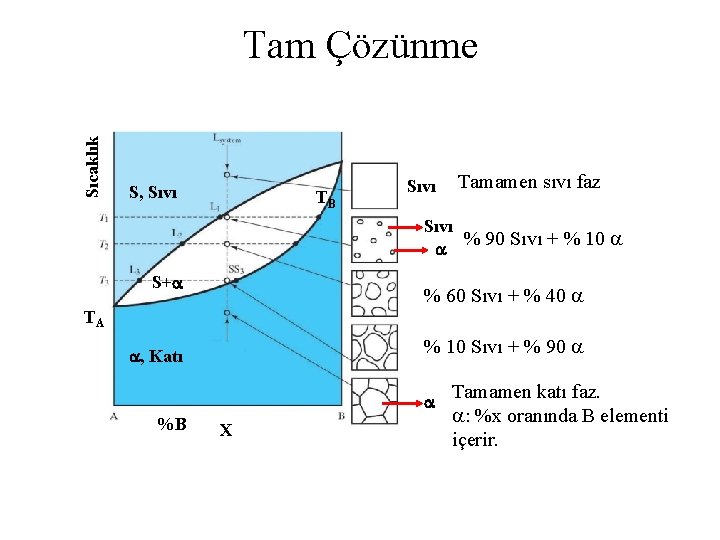
Sıcaklık Tam Çözünme S, Sıvı TB Sıvı Tamamen sıvı faz Sıvı % 90 Sıvı + % 10 S+ % 60 Sıvı + % 40 TA % 10 Sıvı + % 90 , Katı %B X Tamamen katı faz. : %x oranında B elementi içerir.

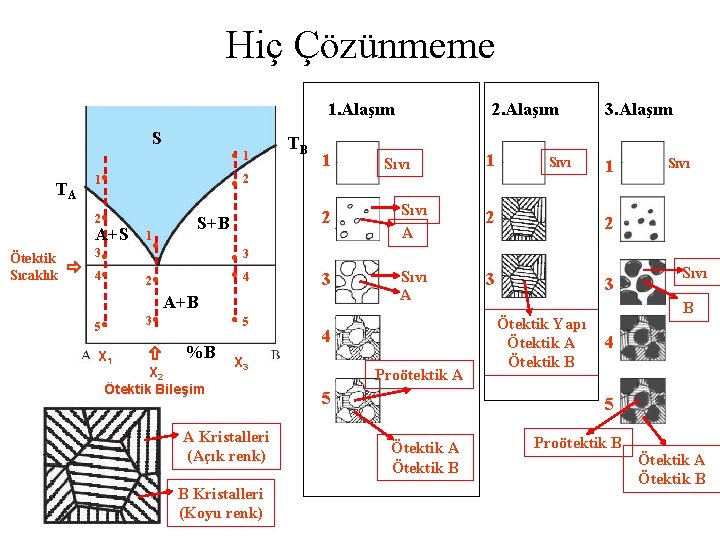
Hiç Çözünmeme 2. Alaşım 1. Alaşım S TA 1 • A+S 3 • 4 • TB 1 Sıvı • 2 2 • Ötektik Sıcaklık • 1 1 S+B • • 3 • 4 2 • 5 • 3 • X 1 A+B %B X 2 Ötektik Bileşim • 5 B Kristalleri (Koyu renk) 1 2 Sıvı A 2 2 3 Sıvı A 3 3 4 X 3 A Kristalleri (Açık renk) 3. Alaşım Proötektik A 5 Ötektik Yapı Ötektik A Ötektik B Sıvı B 4 5 Ötektik A Ötektik B Proötektik B Ötektik A Ötektik B
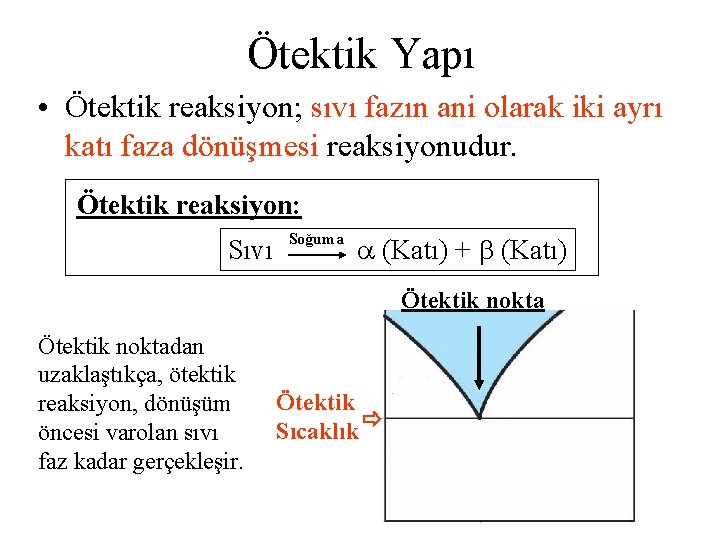
Ötektik Yapı • Ötektik reaksiyon; sıvı fazın ani olarak iki ayrı katı faza dönüşmesi reaksiyonudur. Ötektik reaksiyon: Sıvı Soğuma (Katı) + (Katı) Ötektik noktadan uzaklaştıkça, ötektik reaksiyon, dönüşüm öncesi varolan sıvı faz kadar gerçekleşir. Ötektik Sıcaklık
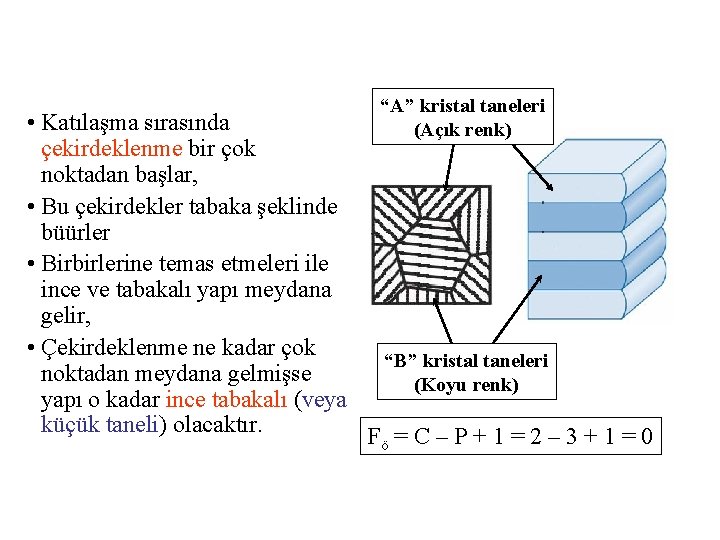
“A” kristal taneleri (Açık renk) • Katılaşma sırasında çekirdeklenme bir çok noktadan başlar, • Bu çekirdekler tabaka şeklinde büürler • Birbirlerine temas etmeleri ile ince ve tabakalı yapı meydana gelir, • Çekirdeklenme ne kadar çok “B” kristal taneleri noktadan meydana gelmişse (Koyu renk) yapı o kadar ince tabakalı (veya küçük taneli) olacaktır. Fö = C – P + 1 = 2 – 3 + 1 = 0
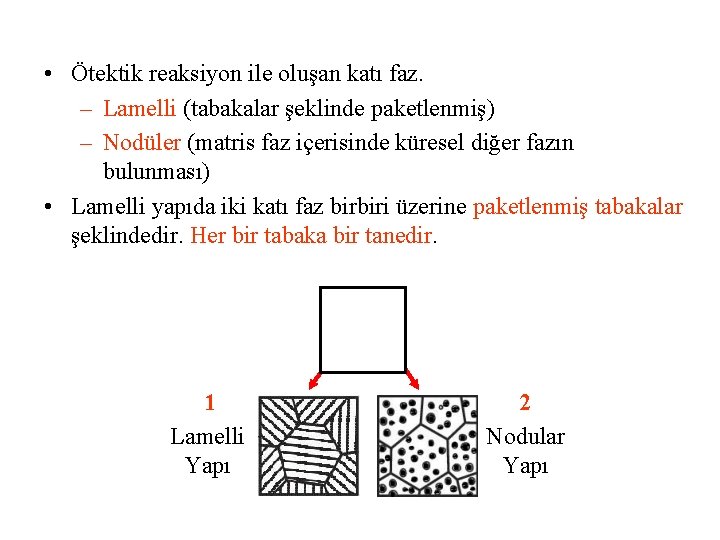
• Ötektik reaksiyon ile oluşan katı faz. – Lamelli (tabakalar şeklinde paketlenmiş) – Nodüler (matris faz içerisinde küresel diğer fazın bulunması) • Lamelli yapıda iki katı faz birbiri üzerine paketlenmiş tabakalar şeklindedir. Her bir tabaka bir tanedir. 1 Lamelli Yapı 2 Nodular Yapı

Sınırlı Çözünme
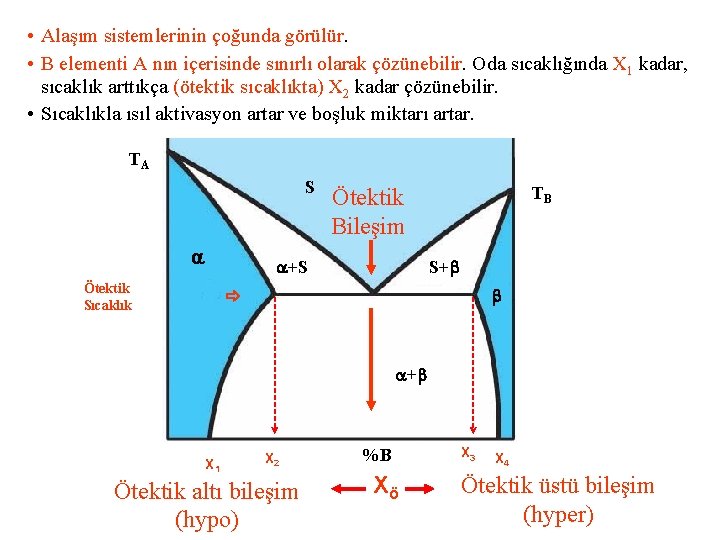
• Alaşım sistemlerinin çoğunda görülür. • B elementi A nın içerisinde sınırlı olarak çözünebilir. Oda sıcaklığında X 1 kadar, sıcaklık arttıkça (ötektik sıcaklıkta) X 2 kadar çözünebilir. • Sıcaklıkla ısıl aktivasyon artar ve boşluk miktarı artar. TA S +S Ötektik Sıcaklık TB Ötektik Bileşim S+ + X 1 X 2 Ötektik altı bileşim (hypo) %B Xö X 3 X 4 Ötektik üstü bileşim (hyper)
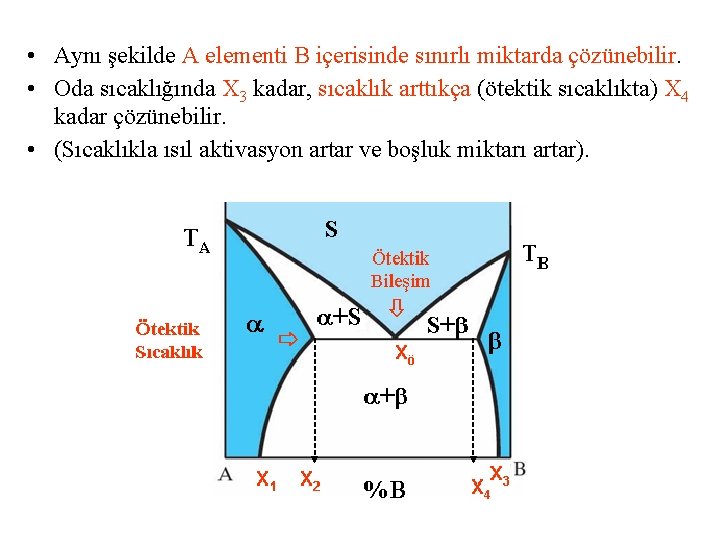
• Aynı şekilde A elementi B içerisinde sınırlı miktarda çözünebilir. • Oda sıcaklığında X 3 kadar, sıcaklık arttıkça (ötektik sıcaklıkta) X 4 kadar çözünebilir. • (Sıcaklıkla ısıl aktivasyon artar ve boşluk miktarı artar).
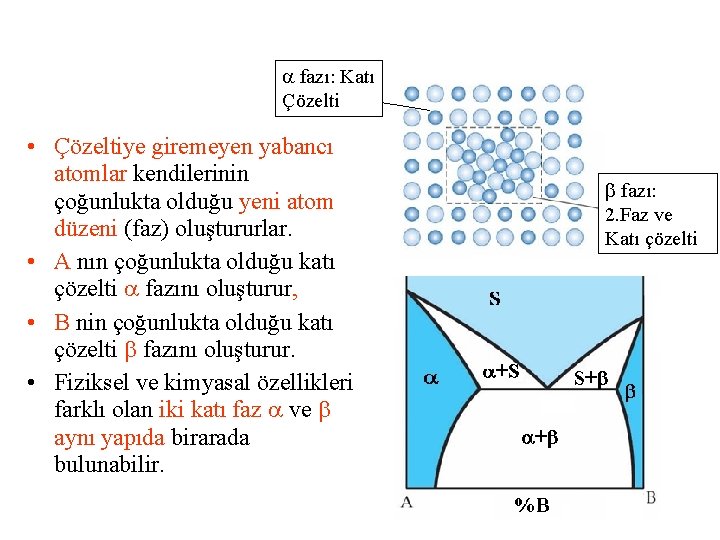
fazı: Katı Çözelti • Çözeltiye giremeyen yabancı atomlar kendilerinin çoğunlukta olduğu yeni atom düzeni (faz) oluştururlar. • A nın çoğunlukta olduğu katı çözelti fazını oluşturur, • B nin çoğunlukta olduğu katı çözelti fazını oluşturur. • Fiziksel ve kimyasal özellikleri farklı olan iki katı faz ve aynı yapıda birarada bulunabilir. fazı: 2. Faz ve Katı çözelti

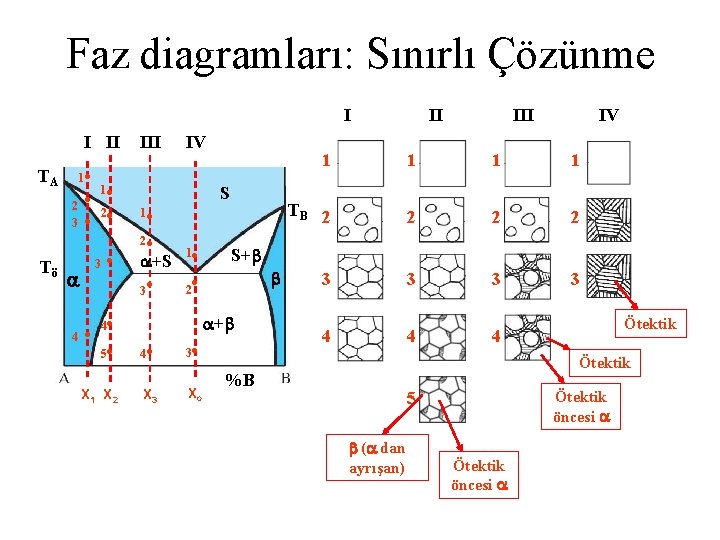
Faz diagramları: Sınırlı Çözünme I I II TA Tö III IV 1 • • 2 2 • 3 4 • • S 1 • 2 • +S 3 • 1 • 5 • X 1 X 2 III IV 1 1 TB 2 2 3 3 4 4 4 S+ 2 • + 4 • II 4 • 3 • X 3 Xö Ötektik %B 5 ( dan ayrışan) Ötektik öncesi
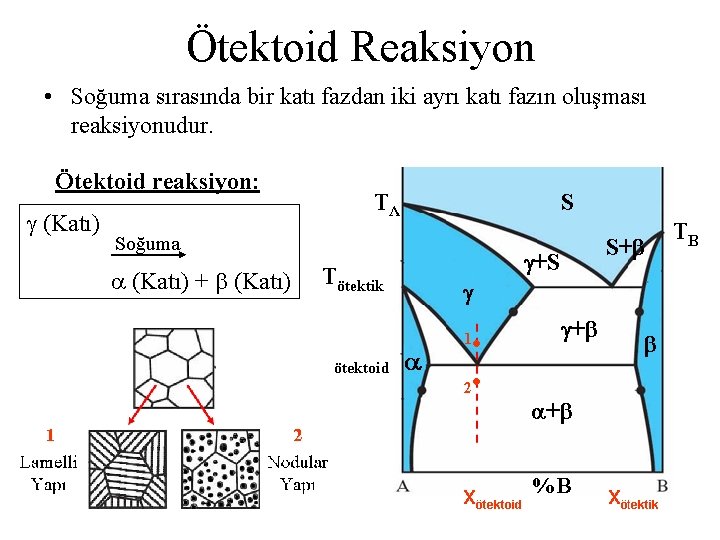
Ötektoid Reaksiyon • Soğuma sırasında bir katı fazdan iki ayrı katı fazın oluşması reaksiyonudur. Ötektoid reaksiyon: (Katı) Soğuma (Katı) + (Katı)
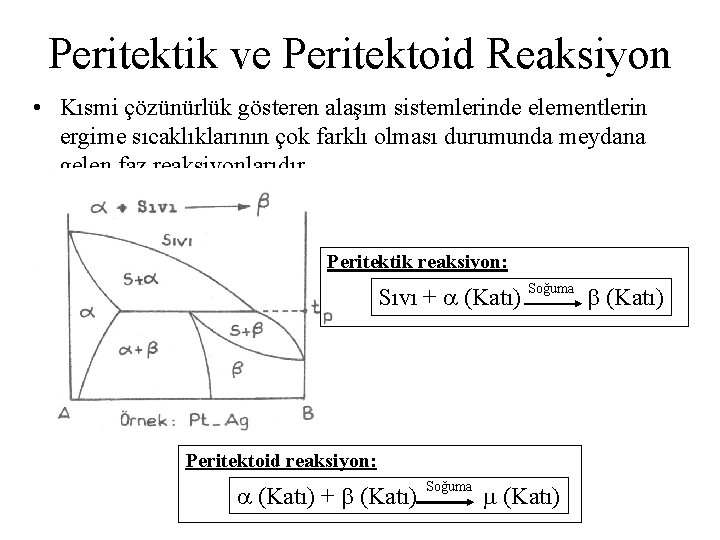
Peritektik ve Peritektoid Reaksiyon • Kısmi çözünürlük gösteren alaşım sistemlerinde elementlerin ergime sıcaklıklarının çok farklı olması durumunda meydana gelen faz reaksiyonlarıdır. Peritektik reaksiyon: Sıvı + (Katı) Soğuma Peritektoid reaksiyon: (Katı) + (Katı) Soğuma (Katı)
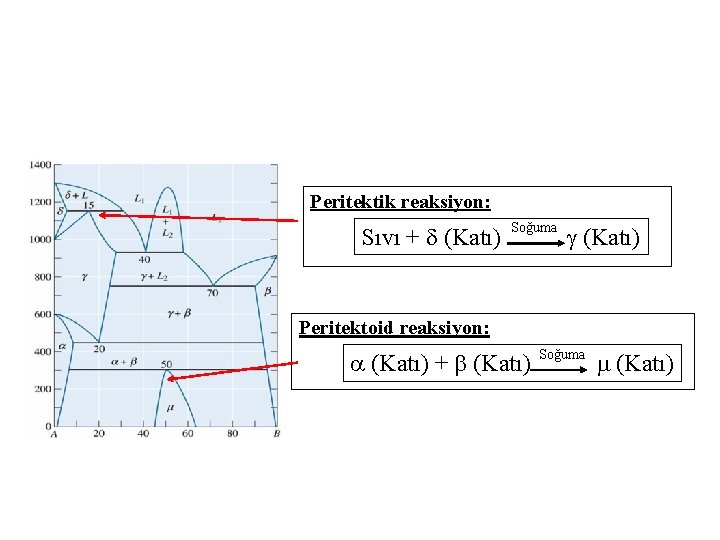
Peritektik reaksiyon: Sıvı + (Katı) Soğuma (Katı) Peritektoid reaksiyon: (Katı) + (Katı) Soğuma (Katı)
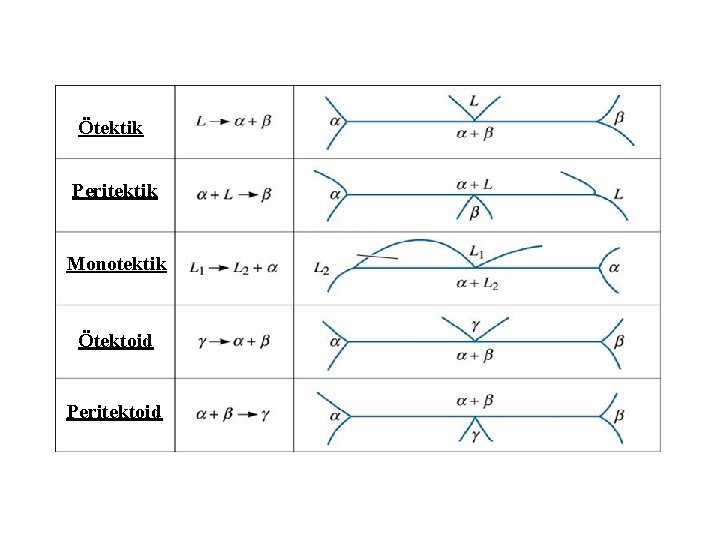
Ötektik Peritektik Monotektik Ötektoid Peritektoid
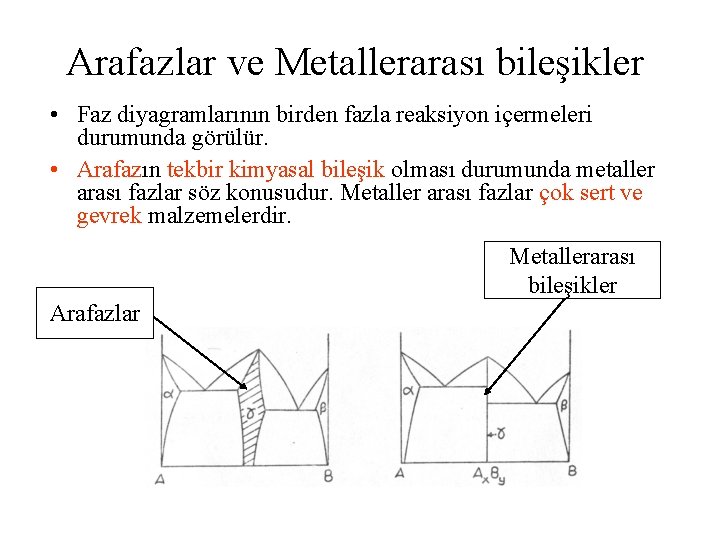
Arafazlar ve Metallerarası bileşikler • Faz diyagramlarının birden fazla reaksiyon içermeleri durumunda görülür. • Arafazın tekbir kimyasal bileşik olması durumunda metaller arası fazlar söz konusudur. Metaller arası fazlar çok sert ve gevrek malzemelerdir. Metallerarası bileşikler Arafazlar
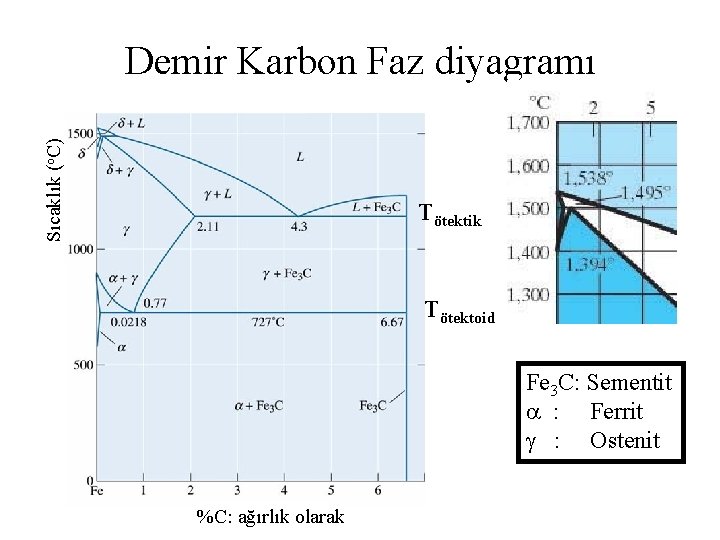
Sıcaklık (o. C) Demir Karbon Faz diyagramı Tötektik Tötektoid Fe 3 C: Sementit : Ferrit : Ostenit %C: ağırlık olarak
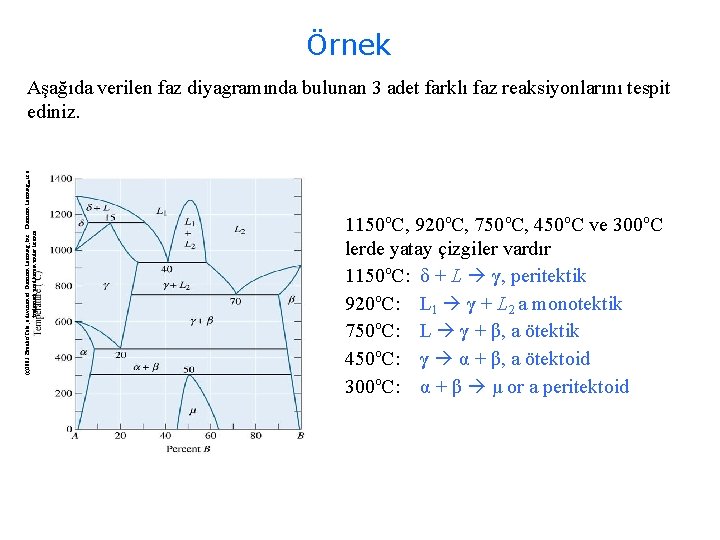
Örnek (c)2003 Brooks/Cole, a division of Thomson Learning, Inc. Thomson Learning™ is a trademark used herein under license. Aşağıda verilen faz diyagramında bulunan 3 adet farklı faz reaksiyonlarını tespit ediniz. 1150 o. C, 920 o. C, 750 o. C, 450 o. C ve 300 o. C lerde yatay çizgiler vardır 1150 o. C: δ + L γ, peritektik 920 o. C: L 1 γ + L 2 a monotektik 750 o. C: L γ + β, a ötektik 450 o. C: γ α + β, a ötektoid 300 o. C: α + β μ or a peritektoid
- Slides: 35