ZKLADY ELEKTROTECHNIKY Prprava na vyuovaciu hodinu v systme





































- Slides: 45

ZÁKLADY ELEKTROTECHNIKY

Príprava na vyučovaciu hodinu v systéme výučby s uzavretým cyklom Škola: SOŠT Volgogradská 1 PREŠOV Ročník: prvý Predmet: Základy elektrotechniky Tematický celok: Aktívne súčiastky Téma vyučovacej hodiny: Batérie a akumulátory Ing. Ľubomír GREŠ

Prečo žiadna batéria, neposkytne nekonečný elektrický prúd, keď ju prepojíme nakrátko? Ako možno vysvetliť rôznu energetickú bilanciu troch rovnakých elektrických článkov v rôznom zapojení?

Batérie, akumulátory

nakresliť schému skutočného zdroja elektrickej energie a jednotlivé prvky. uviesť spôsoby spájania zdrojov elektrickej energie.

uviesť použitie batérií a akumulátorov. uviesť princípy prevádzky a nabíjania akumulátorov.

Vymenujte zložky vnútorného odporu reálneho zdroja Vymenujte prevádzkové vlastnosti chemických zdrojov

Popíšte základné faktory ovplyvňujúce životnosť chemických elektrických zdrojov

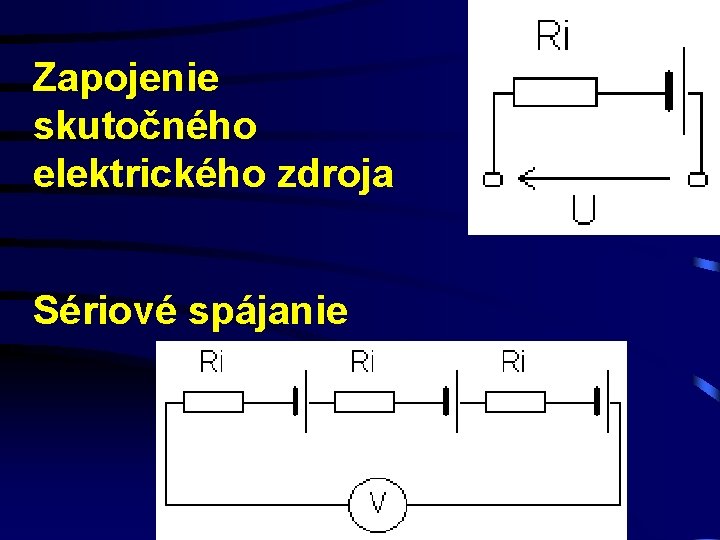
Zapojenie skutočného elektrického zdroja Sériové spájanie

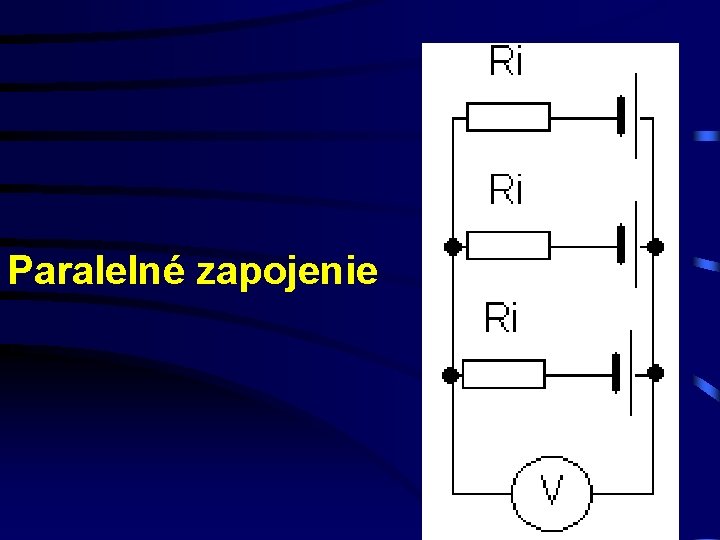
Paralelné zapojenie

Starnutie chemických zdrojov: Príčiny: 1. nedokonalosť chemických zlúčenín 2. nevratnosť chemickej reakcie 3. zlá prevádzka 4. chyba výroby

Nabíjanie akumulátorov Zásady: 1. každý výrobca predpisuje iný postup nabíjania 2. obsluha len s predpísanými bezpečnostnými opatreniami 3. zrýchlenie nabíjania pri prekročení nabíjacieho prúdu o 20 -30%

Výmena akumulátorov Zásady: 1. výmena len pri odpojenom stave 2. skladovať na predpísanom mieste – obsahujú škodlivé látky 3. nové články je potrebné naformátovať

• Technológia oznamovacích zariadení musí byť v prevádzke nepretržite t. j. 24 hodín, preto pre napájanie elektrických obvodov sa prevažne používajú akumulátory, ktoré sú v normálnej prevádzke dobíjané zo siete v prípade výpadku elektrickej energie podľa daného typu musia byť schopné napájať zariadenie 6 – 24 hodín. V praxi sa používajú: olovené (kyslé), niklokadmiové (alkalické) a striebrozinkové akumulátory.

• Doposiaľ najpoužívanejším akumulátorom je olovený akumulátor, vynájdený roku 1859 Francúzom Gastonom Planté. Jeho základom sú dosky zhotovené z inertného nosiča, ktorý je upravený do tvaru mriežky, aby mal čo najväčší povrch. Na mriežku sa nanáša pasta tvorená síranom olovnatým Pb. SO 4 a kyselinou sírovou H 2 SO 4, ktorá sa používa ako elektrolyt (20% roztok). Dosky sú oddelené tzv. separátorom, ktorý je zhotovený zo sklenenej vaty a obsahuje ďalšie prímesi. Ak ku elektródam pripojíme zdroj jednosmerného elektrického prúdu, na katóde (-) sa bude vylučovať tmavošedé olovo Pb a na anóde (+) sa bude vytvárať vrstva červenohnedého oxidu olovičitého PBO 2. Týmto spôsobom vznikne sústava, ktorú môžeme po odpojení zdroja využiť ako galvanický článok. Jeho napätie je približne 2 V. Kapacita pri malých prevedeniach je 1 -100 Ah u veľkých je cez 10 000 Ah.

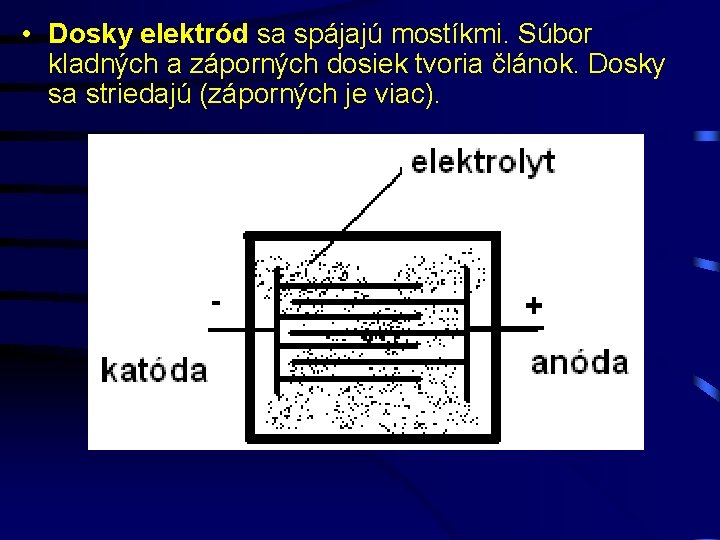
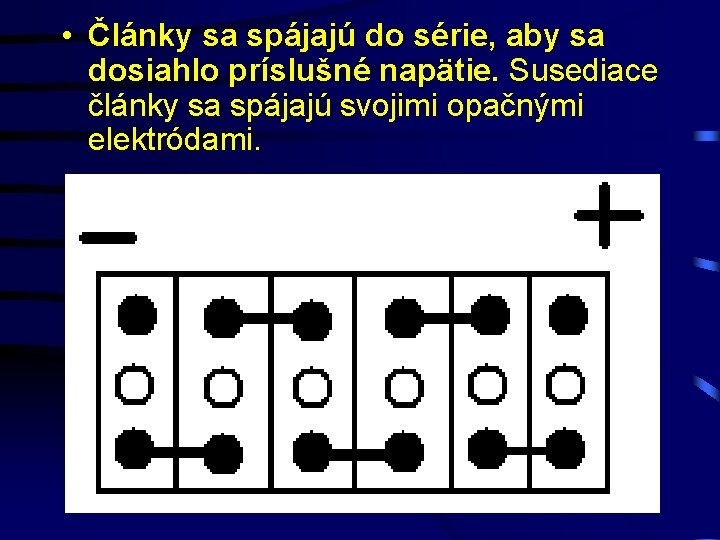
• Dosky elektród sa spájajú mostíkmi. Súbor kladných a záporných dosiek tvoria článok. Dosky sa striedajú (záporných je viac).

• Články sa spájajú do série, aby sa dosiahlo príslušné napätie. Susediace články sa spájajú svojimi opačnými elektródami.

• Články sa dajú spájať aj paralelne alebo sériovo-paralelne. • Akumulovanie elektrickej energie v akumulátore umožňujú elektrochemické procesy, ktoré prebiehajú vnútri jednotlivých článkov. Tieto procesy sú vratné, čiže po jednom cykle – nabitie – vybitie – sú pomery v článku rovnaké.

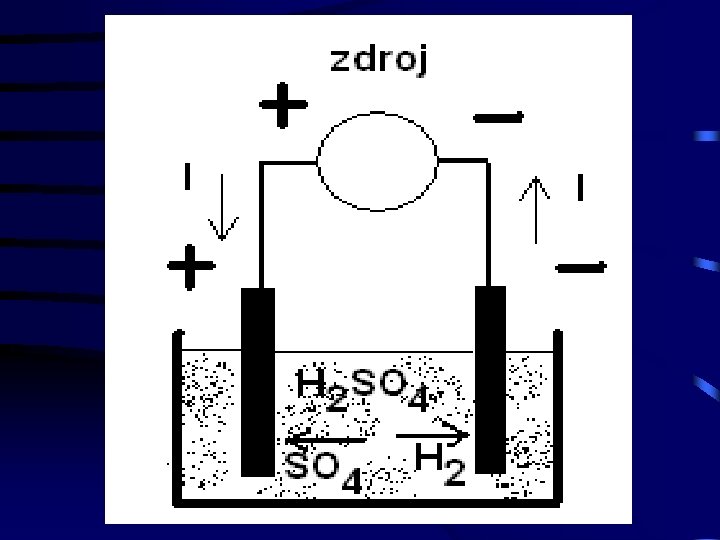
• Článok sa nabíja jednosmerným prúdom. Kladný pól zdroja sa spojí s kladným pólom akumulátora a záporný so záporným pólom akumulátora. Prúd prechádza z kladného pólu zdroja cez kladnú elektródu článku, elektrolyt, zápornú elektródu k mínus pólu zdroja.


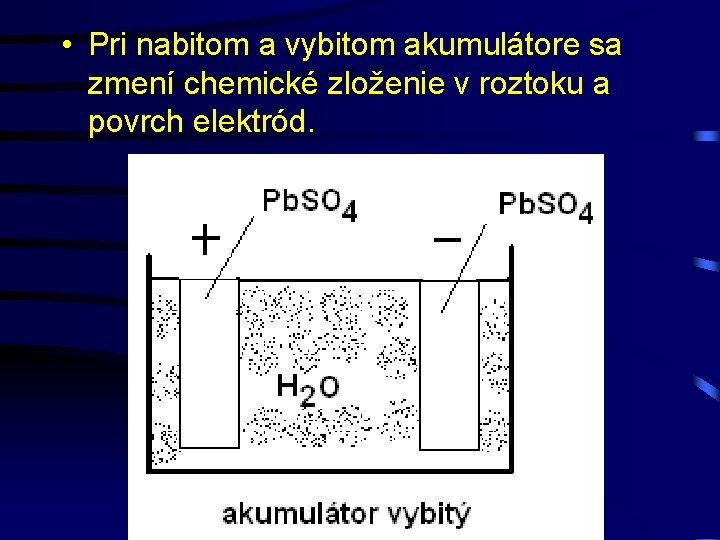
• Pri nabitom a vybitom akumulátore sa zmení chemické zloženie v roztoku a povrch elektród.

• Keď pri nabíjaní bol na zápornej doske nahradený všetok síran olovnatý - Pb. SO 4 olovom - Pb a na kladnej doske kysličníkom olovičitým - Pb. O 2 , začne sa elektrolytický rozklad vody. Pri tomto rozklade sa pri kladných elektródach vytvára kyslík a pri záporných vodík.

• Elektrolytický rozklad vody je hlavnou príčinou poklesu hladiny elektrolytu v akumulátore. • Aby vznikajúce plyny mali možnosť z nádoby unikať, sú v zátkach otvory. Pri nabíjaní akumulátora v nabíjacej stanici sa zátky z článkov vyberajú. • Pri nabíjaní sa z článkov akumulátora odparuje voda, preto sa musí kontrolovať hladina elektrolytu, tak aby elektródy neostali suché a úbytok sa doplňuje destilovanou vodou. • Hustota elektrolytu v akumulátore sa mení najmä následkom chemických reakcií, ktoré prebiehajú pri vybíjaní a nabíjaní akumulátora. Pri nabíjaní hustota stúpa, pri vybíjaní klesá. Hustota je jedným z ukazovateľov okamžitého stavu akumulátora.

• Dôležitou hodnotou akumulátora je jeho vnútorný odpor Rv. Má byť čo najmenší, aby sa nadmerne nezohrieval pri prechode elektrického prúdu. Vnútorný odpor je súčtom odporu elektrolytu, činnej hmoty, vývodov a mostíkov. Odpor závisí od stavu nabitia. S pokračujúcim vybíjaním rastie odpor činných hmôt, pretože v nich pribúda síran olovnatý, ktorý je nevodič. • Výkonnosť akumulátora ovplyvňuje najmä teplota, lebo pri vybíjaní spomaľuje chemické reakcie.

• Aktuálny stav akumulátora môžeme odmerať hustomerom, ktorý odmeria hustotu elektrolytu a je ciachovaný v ampérhodinách, čiže priamo zistíme akú ma kapacitu daný článok akumulátora. Spoľahlivejšie sa stav článkov zisťuje skúšačkou akumulátorov (so zaťažovacím rezistorom). Nedá sa však použiť na plastové prevedenia. • Najdôležitejšie veličiny, ktoré charakterizujú každý akumulátor sú napätie a kapacita. Tieto údaje sa uvádzajú aj v typovom označení akumulátorov. Napr. pri označení 3 ST 66 alebo 6 N 50 prvé číslo znamená počet článkov. Napätie jedného článku je približne 2 V. V prvom prípade ide o 6 V akumulátor, v druhom o 12 V akumulátor. Písmená označujú typ, číslo za typom sa udáva kapacita v ampérhodináh. Prvý má teda kapacitu 66 Ah druhý 50 Ah.

• Kapacita C udávaná v ampérhodinách Ah je veličina charakterizujúca schopnosť akumulátora udržať – akumulovať elektrickú energiu. Akumuluje sa prostredníctvom chemických reakcií medzi činnou hmotou a elektrolytom. Kapacita klesá s teplotou elektrolytu. • C = I. t (Ah) kde I je prúd a t je čas • Príklad: Akumulátor s kapacitou 100 Ah je schopný dodávať prúd 5 A počas 20 hodín až do úplného vybitia. Napätie článku nemá poklesnúť pod 1, 75 V!

• Olovený akumulátor sa používa najčastejšie v automobiloch. Stredné napätie jedného článku oloveného akumulátora býva asi 2 V. V zapojení za sebou sa využívajú olovené články v motocykloch s napätím 6 V , v osobných automobiloch 12 V a v nákladných automobiloch 24 V. Používajú sa na rozbehnutie motora, zapaľovanie paliva.

• Akumulátory, vrátane oloveného sú najvýznamnejšou skupinou, ktorá sa podieľa na ohrození životného prostredia. Skoro všetky obsahujú zvlášť nebezpečné látky – ťažké kovy – ortuť – kadmium a olovo. Je dokázané, že zaťaženie životného prostredia ťažkými kovmi je pre živé organizmy v porovnaní s ostatnými odpadmi 10 000 krát vyššie.

• Nevýhodou je veľká hmotnosť, obmedzená životnosť, tepelná závislosť, nebezpečné a neekologické chemické materiály. • Prednosťou je stálosť napätia, malý vnútorný odpor, obnoviteľný zdroj elektrickej energie a dobré kapacitné vlastnosti. • Niklokadmiové akumulátory • Patria do skupiny alkalických akumulátorov. Ich charakteristickým znakom je použitie elektrolytu z roztoku hydroxidu draselného KOH (luh draselný).

• Menovité napätie jedného článku je 1, 2 V. Elektródy sú vyrobené z oceľového poniklovaného plechu. Elektródy sú perforované s vreckami, v ktorých je lisovaná aktívna látka. Na kladných elektródach je oxid nikličný a oxid niklitý, na záporných elektródach kadmium s prímesou železa. Nádoba a veká sú z oceľového poniklovaného plechu. Vývody pólov sú riešené ako hrubé skrutkové svorky. • Články sa spájajú do batérie po 5 kusoch na napätie 6 V a ukladajú sa do drevených rámov, ktoré umožňujú ich prenos a zapojenie do celkov 12 – 24 V.

• Elektrolyt sa mení približne raz za rok. V prevádzke sa do nich nalieva iba destilovaná voda. Články môžu pracovať v rozsahu +40 až -40 stupňov. Neškodí im občasné hlboké vybitie, alebo prebíjanie. Neškodia im otrasy. Majú 5 krát dlhšiu životnosť ako olovené akumulátory. Pri rovnakej kapacite a napätí sú rozmernejšie, ťažšie a asi 4 krát drahšie. • Akumulátor sa môže skladovať so striebrozinkovým akumulátorom, ale nesmie sa skladovať spolu s oloveným akumulátorom. Pretože sa aktívne látky navzájom neutralizujú.

Striebrozinkové akumulátory • Elektródy sú vyrobené zo striebra a zinku. Elektrolyt je hydroxid draselný KOH. Článok má kapacitu v porovnaní s predchádzajúcimi akumulátormi podstatne väčšiu, ale má menšie rozmery. Používa sa na napájanie zariadení, kde je požiadavka na zdroje malých rozmerov, malej váhy, kde nie je rozhodujúca cena zariadenia – letecká technika, vojenské zariadenia, napájanie mobilných zariadení. • Všeobecne pri všetkých druhoch akumulátorov musíme dodržiavať bezpečné opatrenia z dôvodov výbušných plynov, leptajúcich účinkov tekutín, neekologických materiálov. Všetky akumulátory musia mať evidenčné listy so zameraním na výrobné číslo, účtovný celok, dátum: uvedenia do prevádzky, dobíjania, kapacitnej skúšky, opravy a vyradenia z prevádzky.

Skratový prúd chemického zdroja meriame: 1. čo najkratšie. 2. čo najdlhšie 3. so sériovvo zaradeným kondenzátorom 4. s paralelne zapojenou cievkou

Náhradná schéma batérie má zapojenie ideálneho zdroja: 5. napäťového s paralelným odporom . 6. napäťového so sériovým odporom 7. prúdového so sériovým odporom 8. prúdového so sériovým kondenzátorom

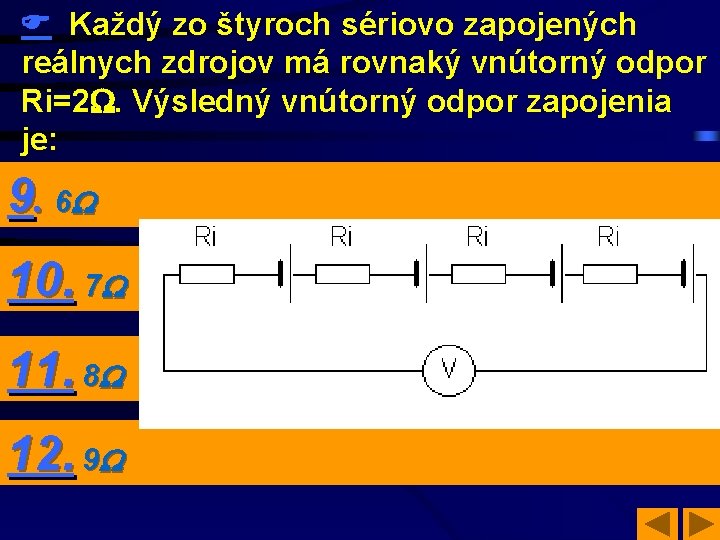
Každý zo štyroch sériovo zapojených reálnych zdrojov má rovnaký vnútorný odpor Ri=2. Výsledný vnútorný odpor zapojenia je: 9. 6 . 10. 7 11. 8 12. 9

Nový akumulátor má pri plnom nabití vnútorný odpor: 13. nulový. 14. nekonečný 15. malý, ktorý sa v čase vybíjania zväčšuje 16. malý, ktorý sa v čase vybíjania zmenšuje

Vymenujte chemické zdroje, ktoré majú najmenší vnútorný odpor z energetického hľadiska. Popíšte rozdiely medzi reálnym zdrojom prúdu a napätia.

Uveďte dôvod, prečo niektoré chemické zdroje majú na svorkách pripojený veľkokapacitný kondenzátor. Vysvetlite, akým spôsobom sa dobíja a reguluje dobíjanie autoakumulátora.

Výsledky úloh: Priebežný test: 1, 6, 11, 15 Pre záujemcov:

Najmenší vnútorný odpor majú chemické zdroje s najväčším výkonom a sú to akumulátory v elektrárňach v ponorkách a záložné batérie pre veľké prevádzky.

Napäťový zdroj sa skladá zo sériovej náhrady ideálneho napäťového zdroja a malého odporu a prúdový zdroj je paralelná kombinácia ideálneho prúdového zdroja a veľkého odporu.

Niektoré zdroje majú na svojich svorkách zapojený veľkokapacitný kondenzátor, kvôli nečakanému špičkovému odberu. Používajú sa tam, kde trvalo nie je zdroj preťažovaný, ale náhly pokles napätia by mohol spôsobiť poruchu v obvode. Kondenzátor má naakumulovanú energiu, ktorú v prípade zvýšených prúdových nárokoch môže poskytnúť namiesto zdroja.

Motor poháňa alternátor, ktorý od veľkosti budiaceho napätia vyrába striedavé napätie. To sa v usmerňovači usmerní a dobíja akumulátor a zásobuje automobil elektrickou energiu. Vyššie harmonické a napäťové špičky sa v akumulátore vysktratujú. Usmerňovač sníma hladinu napätia akumulátora pri chode motora a podľa potreby ju zvýši a tým sa automaticky akumulátor dobíja. Ak je hladina napätia vysoká, alternátor vyrába menej energie a tým je batéria stále maximálne nabitá.

Zdroje: www. baterie. batteries. pl www. avacom. cz www. bateriedomobilu. cz www. smodel. cz www. solarexpert. com Maťátko, J. : Elektronika. Alfa Bratislava: 1993

Ing. Ľubomír GREŠ