Zkladn poznatky molekulovej fyziky Molekulov fyzika Zkladom MF












- Slides: 17

Základné poznatky molekulovej fyziky

Molekulová fyzika Základom MF je kinetická teória látok. 1. Látky sa skladajú z častíc 2. Častice konajú chaotické neusporiadané pohyby 3. Častice na seba pôsobia príťažlivými a odpudivými silami

1. Látky sa skladajú z častíc Čo potvrdil vynález elektrónového mikroskopu molekuly vody bez tlaku a pod tlakom Molekuly vodíka na povrchu zlata

2. Častice konajú chaotické pohyby • Difúzia – samovoľné prenikanie častíc jednej látky medzi častice druhej látky • Brownov pohyb • Tlak plynu

3. Častice na seba pôsobia príťažlivými a odpudivými silami Príťažlivé a odpudivé sily závisia od vzdialenosti medzi časticami. Najväčšie príťažlivé sily pôsobia medzi časticami pevnej látky, najmenšie medzi časticami plynov. Sily, ktoré viažu atómy v molekule látky nazývame väzbové sily.

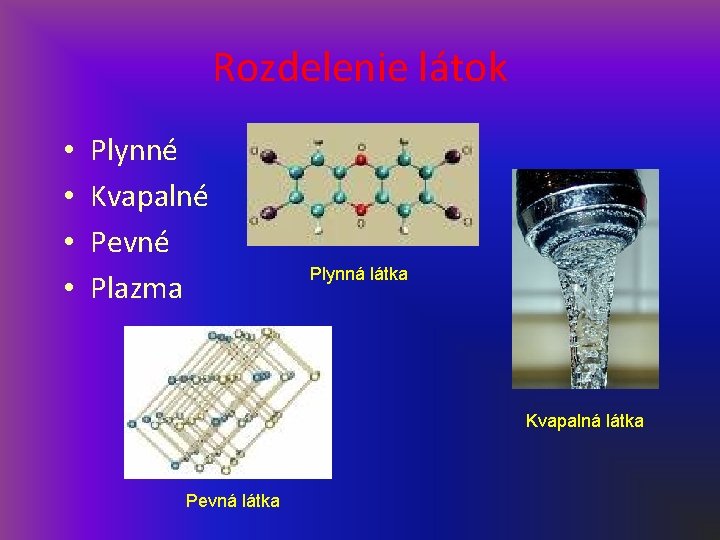
Rozdelenie látok • • Plynné Kvapalné Pevné Plazma Plynná látka Kvapalná látka Pevná látka

Molekuly plynných látok • • Skladajú sa z jedného alebo viacerých atómov Majú veľkú kinetickú energiu Ek Plyny sú rozpínavé a stlačiteľné Môžu zaujať akýkoľvek priestor Stredná vzdialenosť molekúl je rádovo 3 nm Ek>Ep Pohybujú sa vo všetkých smeroch Zmena smeru a veľkosti nastáva v dôsledku zrážky molekúl

Molekuly pevných látok Príťažlivé sily sú veľmi veľké Častice kmitajú okolo rovnovážnych polôh Ep>Ek Stredná vzdialenosť je rádovo 0, 2 nm Sú zložené z častíc s pravidelným usporiadaním • Tvoria kryštalickú štruktúru, niektoré ju však nemajú, napr: sklo, vosk ( pevné látky = kryštalické + amorfné ) • • •

Molekuly kvapalných látok • Príťažlivé sily sú veľmi veľké • Konajú kmitavý pohyb okolo rovnovážnych polôh, ale vplyvom vonkajších síl a zvyšovaním teploty je možné usmerniť ich pohyb • Ep = Ek • Stredná vzdialenosť je rádovo 0, 2 nm • Častice sa vyznačujú istou usporiadanosťou na krátku vzdialenosť

Plazma • Látka skladajúca sa z rôznych častíc s nábojom • Je navonok neutrálna • Pri vysokých teplotách môže byť zložená len z voľných jadier a elektrónov • Podoby: oheň, blesk, polárna žiara

Rovnovážny stav termodynamickej sústavy • Teleso alebo skupina telies, ktorých stav skúmame je termodynamická sústava • Veličiny, ktoré určujú jej stav sú stavové veličiny (objem V, teplota T, tlak p, . . . )

Izolovaná sústava • Je sústava, v ktorej neprebieha výmena energie s okolím a jej chemické zloženie a hmotnosť zostávajú konštantné • Kalorimeter c. m. (t -t) = c. m. (t -t) 1 1 1 2 2 2 Popis fyzikálnych veličín v kalorimetrickej rovnici : c 1, 2 - merné tepelné kapacity látok 1, 2 m 1, 2 - hmotnosti látok 1, 2 t 1, 2 – pôvodná teplota látok 1, 2 t - výsledná teplota rovnovážneho stavu

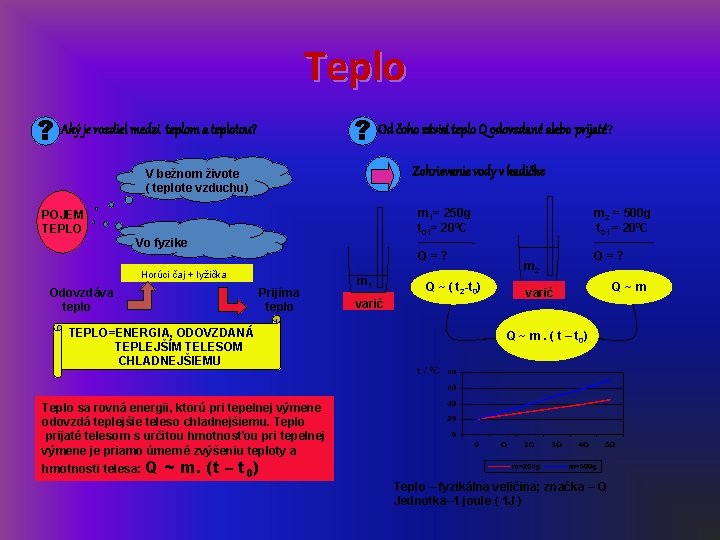
Teplo ? Aký je rozdiel medzi teplom a teplotou? ? Od čoho závisí teplo Q odovzdané alebo prijaté? Zohrievanie vody v kadičke V bežnom živote ( teplote vzduchu) m 1= 250 g t 01= 200 C ––––Q=? POJEM TEPLO Vo fyzike Horúci čaj + lyžička Odovzdáva teplo Prijíma teplo TEPLO=ENERGIA, ODOVZDANÁ TEPLEJŠÍM TELESOM CHLADNEJŠIEMU m 1 Q ~ ( t 2 -t 0) varič m 2 = 500 g t 01 = 200 C ––––– Q=? varič Q ~ m. ( t – t 0) t / 0 C Teplo sa rovná energii, ktorú pri tepelnej výmene odovzdá teplejšie teleso chladnejšiemu. Teplo prijaté telesom s určitou hmotnosťou pri tepelnej výmene je priamo úmerné zvýšeniu teploty a hmotnosti telesa: Q ~ m. (t – t 0) Teplo – fyzikálna veličina; značka – Q Jednotka– 1 joule ( 1 J ) Q~m

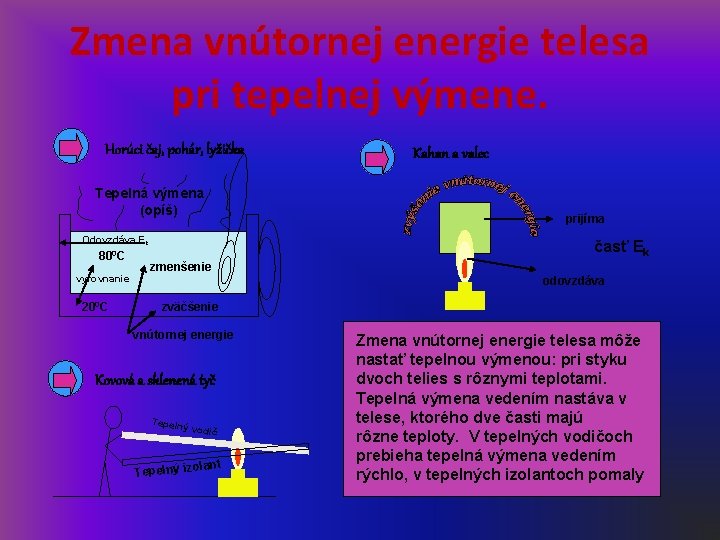
Zmena vnútornej energie telesa pri tepelnej výmene. Horúci čaj, pohár, lyžička Tepelná výmena (opíš) prijíma Odovzdáva Ek 800 C vyrovnanie 200 C Kahan a valec časť Ek zmenšenie odovzdáva zväčšenie vnútornej energie Kovová a sklenená tyč Tepeln ý vodič nt ola Tepelný iz Zmena vnútornej energie telesa môže nastať tepelnou výmenou: pri styku dvoch telies s rôznymi teplotami. Tepelná výmena vedením nastáva v telese, ktorého dve časti majú rôzne teploty. V tepelných vodičoch prebieha tepelná výmena vedením rýchlo, v tepelných izolantoch pomaly

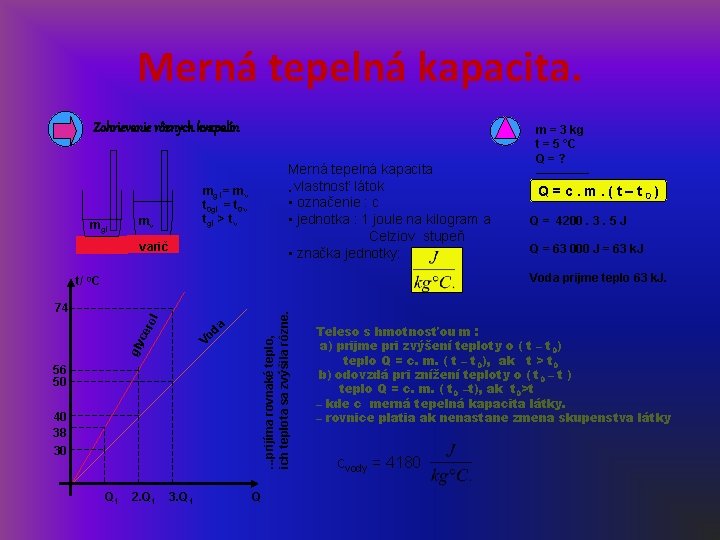
Merná tepelná kapacita. Zohrievanie rôznych kvapalín mgl Merná tepelná kapacita • vlastnosť látok • označenie : c • jednotka : 1 joule na kilogram a Celziov stupeň • značka jednotky: mg l= mv t 0 gl = t 0 v tgl > tv mv varič m = 3 kg t = 5 °C Q=? –––– Q = c. m. ( t – t 0) Q = 4200. 3. 5 J Q = 63 000 J = 63 k. J Voda prijme teplo 63 k. J. t/ 0 C gly Vo da ce ro l . . . prijíma rovnaké teplo, ich teplota sa zvýšila rôzne. 74 56 50 40 38 30 Q 1 2. Q 1 3. Q 1 Q Teleso s hmotnosťou m : a) prijme pri zvýšení teploty o ( t – t 0) teplo Q = c. m. ( t – t 0), ak t > t 0 b) odovzdá pri znížení teploty o ( t 0 – t ) teplo Q = c. m. ( t 0 –t), ak t 0>t – kde c merná tepelná kapacita látky. – rovnice platia ak nenastane zmena skupenstva látky cvody = 4180

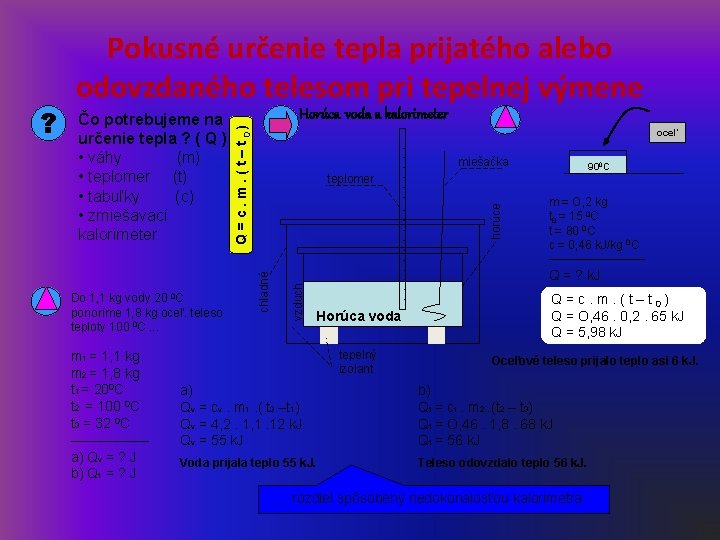
m 1 = 1, 1 kg m 2 = 1, 8 kg t 1 = 200 C t 2 = 100 0 C t 3 = 32 0 C ––––– a) Qv = ? J b) Qt = ? J oceľ miešačka 900 C horúce teplomer m = O, 2 kg t 0 = 15 0 C t = 80 0 C c = 0, 46 k. J/kg 0 C –––––––- Q = ? k. J vzduch Do 1, 1 kg vody 20 0 C ponoríme 1, 8 kg oceľ. teleso teploty 100 0 C. . . Horúca voda a kalorimeter chladné Čo potrebujeme na určenie tepla ? ( Q ) • váhy (m) • teplomer (t) • tabuľky (c) • zmiešavací kalorimeter Q = c. m. ( t – t 0) ? Pokusné určenie tepla prijatého alebo odovzdaného telesom pri tepelnej výmene Horúca voda tepelný izolant Q = c. m. ( t – t 0) Q = O, 46. 0, 2. 65 k. J Q = 5, 98 k. J Oceľové teleso prijalo teplo asi 6 k. J. a) Qv = cv. m 1. ( t 3 –t 1) Qv = 4, 2. 1, 1. 12 k. J Qv = 55 k. J b) Qt = ct. m 2. (t 2 – t 3) Qt = O, 46. 1, 8. 68 k. J Qt = 56 k. J Voda prijala teplo 55 k. J. Teleso odovzdalo teplo 56 k. J. . . rozdiel spôsobený nedokonalosťou kalorimetra

Druhy teplotných stupníc Celziova t stupnica °C – stupeň Celzia Bod varu vody - 100°C Bod topenia ľadu - 0°C • Thomsonova termodynamická teplotná stupnica K - Kelvin Trójny bod vody - sústava: ľad – voda – nasýtená para Tr = 273, 16 K
 Katedra fyziky chemie a odborného vzdělávání
Katedra fyziky chemie a odborného vzdělávání Obory fyziky
Obory fyziky Historie fyziky
Historie fyziky Didaktika fyziky
Didaktika fyziky Vlastnosti oka
Vlastnosti oka Zrážkomer fyzika
Zrážkomer fyzika Fyzika 7 rocnik teplota
Fyzika 7 rocnik teplota Výsledek
Výsledek Druhy teploměrů fyzika
Druhy teploměrů fyzika Energia v prirode fyzika
Energia v prirode fyzika Ek fyzika
Ek fyzika Kedy je teleso v pohybe
Kedy je teleso v pohybe Protdy
Protdy Zvuk fyzika 8 třída
Zvuk fyzika 8 třída Metrolgia
Metrolgia Plynový teploměr princip
Plynový teploměr princip Slnečná energia fyzika
Slnečná energia fyzika Archimedova skrutka
Archimedova skrutka