ZKLADN KOLA ST NAD LABEM ANEKY ESK 70217

ZÁKLADNÍ ŠKOLA ÚSTÍ NAD LABEM, ANEŽKY ČESKÉ 702/17, PŘÍSPĚVKOVÁ ORGANIZACE ČÍSLO PROJEKTU: CZ. 1. 07/1. 4. 00/21. 2887 NÁZEV PROJEKTU: „UČÍME LÉPE A MODERNĚJI“ OP VK 1. 4 VÝUKOVÝ MATERIÁL Název DUMu: VY_52_INOVACE_05_3_NÁZVOSLOVÍ KYSELIN Číslo skupiny: 2 Autor: Ing. Stanislava Kolářová Vzdělávací oblast/Předmět/Téma: ČLOVĚK A PŘÍRODA / CHEMIE / KYSELINY Druh učebního materiálu: PREZENTACE Metodický list: NE Anotace: Vysvětlení principů názvosloví kyslíkatých kyselin včetně procvičování tvorby názvů i vzorců. Prezentace zároveň slouží jako podklad procvičení a zápis nové látky do sešitu. Ověřeno ve třídě: 9. A Datum ověření: 30. 9. 2011 Prohlášení: Prohlašuji, že při tvorbě výukového materiálu jsem respektoval(a) všeobecně užívané právní a morální zvyklosti, autorská a jiná práva třetích osob, zejména práva duševního vlastnictví (např. práva k obchodní firmě, autorská práva k software, k filmovým, hudebníma fotografickým dílům nebo práva k ochranným známkám)dle zákona 121/2000 Sb. (autorský zákon). Nesu veškerou právní odpovědnost za obsah a původ svého díla. Prohlašuji dále, že výše uvedený materiál jsem ověřil(a) ve výuce a provedl(a) o tom zápis do TK. Dávám souhlas, aby moje dílo bylo dáno k dispozici veřejnosti k účelům volného užití (§ 30 odst. 1 zákona 121/2000 Sb. ), tj. že k uvedeným účelům může být kýmkoliv zveřejňováno, používáno, upravováno a uchováváno. Datum: 30. 9. 2011 Podpis:

NÁZVOSLOVÍ KYSLÍKATÝCH KYSELIN

zápis do sešitu Jak vytvořit vzorec kyslíkaté kyseliny z názvu? . . nejprve si napíšeme prvky tvořící kyselinu ve tvaru HXO, kde X představuje kyselinotvorný prvek …. z koncovky názvu kyseliny odvodíme oxidační číslo kyselinotvorného prvku. . protože sloučenina je navenek elektroneutrální, je součet součinů oxidačních čísel a počtu atomů roven nule. . dopočítáme počet vodíků a kyslíků

Úkol: napsat vzorec pro kyselinu dusičnou. … nejprve si napíšeme základní poznatek, že jde o sloučeninu složenou z vodíku, dusíku a kyslíku HNO … přidáme oxidační čísla. Víme, že kyslík má vždy -II, vodík I a z názvu plyne, že dusík má oxidační číslo V (koncovka -ičná): HINVO -II

… součet kladných oxidačních čísel je 6. Proto stačí ke kyslíku připsat už pouze malou 3: HINVO 3 -II … a tím bude součet součinů oxidačního čísla daného prvku a počtu atomů daného prvku roven nule: HINVO 3 -II 1*I+1*V+3*(-II) = 0 Kyselina dusičná má tedy vzorec HNO 3.

Úkol: napsat vzorec pro kyselinu sírovou. … nejprve si napíšeme, že jde o sloučeninu složenou z vodíku, síry a kyslíku HSO … přidáme oxidační čísla. Víme, že kyslík má vždy -II, vodík I a z názvu plyne, že síra má oxidační číslo VI (koncovka–ová) I VI -II HS O

… součet kladných oxidačních čísel u vodíku a síry je: I + VI = 7. Sedm je liché číslo, aby byla molekula kyseliny elektroneutrální, museli bychom ke kyslíku připsat 3, 5. To nelze, protože v molekule jsou jen celé atomy. Proto připíšeme k vodíku malou 2 2*I + 1*VI = 8 Nyní vypadá součet součinů oxidačních čísel u vodíku a síry takto: aby výsledný náboj molekuly byl nula, stačí připsat ke kyslíku malou 4 2*I + 1*VI + 4*(-II) = 0 H 2 ISVIO 4 - Kyselina sírová má tedy vzorec H 2 SO 4. II

ÚKOL: UTVOŘ VZORCE KYSELIN � Kyselina manganistá � Kyselina chromová � Kyselina zlatitá Ř

zápis do sešitu: Jak pojmenovat anorganickou kyslíkatou kyselinu. . nejprve si napíšeme oxidační číslo ke kyslíku a vodíku. . . protože sloučenina je navenek elektroneutrální, je součet součinů oxidačních čísel a počtu atomů roven nule, proto připíšeme k třetímu prvku patřičné oxidační číslo. …. z oxidačního čísla a názvu kyselinotvorného prvku odvodíme název celé kyseliny.

Úkol: pojmenovat HNO 2. . nejprve si napíšeme oxidační číslo ke kyslíku a vodíku. I -II H NO 2 . . protože sloučenina je navenek elektroneutrální, je součet součinů oxidačních čísel a počtu atomů roven nule, proto připíšeme k třetímu prvku patřičné oxidační číslo. I III -II HN O 2 …. z oxidačního čísla (a jemu příslušné koncovky) už můžeme odvodit název celé kyseliny. kyselina dusit

Úkol: pojmenovat H 2 CO 3. . nejprve si napíšeme oxidační číslo ke kyslíku a vodíku. H ICOII 2 3 . . protože sloučenina je navenek elektroneutrální, měl by součet součinů oxidačních čísel a počtu atomů být roven nule, proto připíšeme k třetímu prvku patřičné oxidační číslo. H ICIVO-II 2 3 …. z oxidačního čísla (a jemu příslušné koncovky) už můžeme odvodit název celé kyseliny kyselina uhličitá
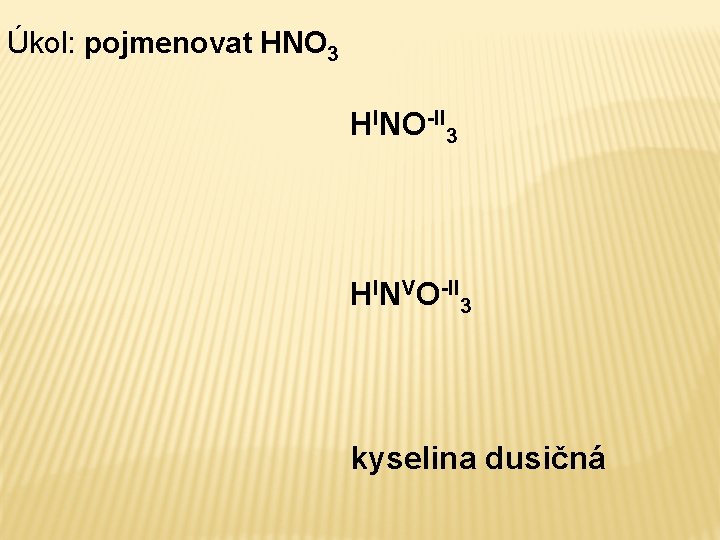
Úkol: pojmenovat HNO 3 HINO-II 3 HINVO-II 3 kyselina dusičná

ÚKOL: POJMENUJ NÁSLEDUJÍCÍ KYSELINY: H 2 SO 3 HCl. O 3 H 2 SO 4 Ř

ŘEŠENÍ ÚKOLŮ: H 2 SO 3 kyselina siřičitá HCl. O 3 kyselina chlorečná H 2 SO 4 kyselina sírová ZPĚT

ŘEŠENÍ ÚKOLŮ: Kyselina manganistá HMn. O 4 Kyselina chromová H 2 Cr. O 4 Kyselina zlatitá HAl. O 2 ZPĚT

CITACE Autorem materiálu a všech jeho částí, není-li uvedeno jinak, je Ing. Stanislava Kolářová.
- Slides: 16