Zellschdigung und Adaptation Internetversion Vorlesung Pathologie I 4
























- Slides: 29

Zellschädigung und Adaptation Internetversion Vorlesung Pathologie I (4)

Basis aller Krankheiten ist die Schädigung der kleinsten lebenden Einheit der Körpers, der Zelle Rudolf Virchow (1821 -1902)

Was kann alles eine Zelle schädigen?

Die Schädigung von Zellen kann als „Stress“, der auf die Zellen wirkt, verstanden werden. • Traumen • Hypoxie und Ischämie • endogene und exogene chemische Stoffe, wie - Harnsäure - Alkohol • physikalische Noxen, wie - Hitze, Kälte - ionisierende Strahlen • belebte Ursachen, wie - Bakterien - Viren • immunologische Prozesse

Was passiert mit einer geschädigten Zelle?

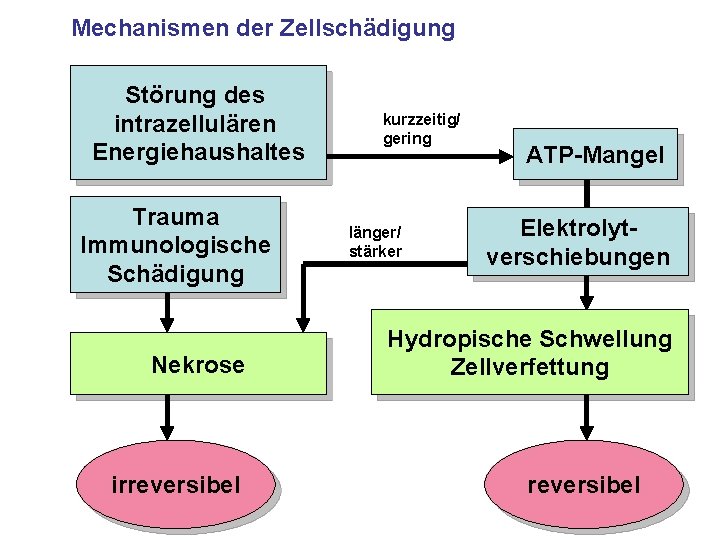
Mechanismen der Zellschädigung Störung des intrazellulären Energiehaushaltes Trauma Immunologische Schädigung Nekrose irreversibel kurzzeitig/ gering länger/ stärker ATP-Mangel Elektrolytverschiebungen Hydropische Schwellung Zellverfettung reversibel

Was kann die betroffene Zelle/Gewebe/ Organismus zu ihrem Schutz tun?

Die Zellen besitzen ein limitiertes Repertoire von Antworten auf Stress • Funktionelle Anpassung an Stress - Hitzeschockproteine - Proteine der „Phase der akuten Antwort“ • Zytologische Adaptation - Hydropische Schwellung - Sub- und intrazelluläre Ablagerungen - Atrophie - Hyperplasie • Histologische Adaptation - Metaplasie - Dysplasie

Funktionelle Anpassung an Stress 1. Hitzeschockproteine (HSP 70, Ubiquitin) • Werden permanent von allen Zellen synthetisiert, aber normalerweise nicht sezerniert • Verstärkte Synthese bei erhöhter Temperatur (Fieber), Ischämie, akuter Entzündung und durch Alkohol • Die Wirkung von HSPs soll das Überleben einzelner Zellen gewährleisten

Funktionelle Anpassung an Stress 2. Proteine der „Phase der akuten Antwort“ • PPAA werden permanent von Hepatozyten sezerniert • Relativ langsamer Anstieg, aber längere Reaktion bei Infekten, Traumen, Verbrennungen, körperliche Anstrengungen, Geburt (!) • PPAAs sollen das Überleben des Gesamtorganismus durch Verteidigung oder Adaptation sichern

Proteine der „Phase der akuten Antwort“ • C-reaktives Protein (CRP) - chronische Entzündungen - Tumoren • Serumamyloid A (SAA) - Bindung an HDL • Haptoglobin • Hämopexin • a 1 -Proteaseinhibitor (a 1 -Antitrypsin) • a 1 -Antichymotrypsin • Fibrinogen • Transthyretin • Interleukin-4 (IL-4)

Zytologische Adaptation 1. Die mildeste Form der Zellschädigung wird als hydropische Schwellung (akutes Zellödem) bezeichnet und ist reversibel • Das Zellvolumen wird durch einen energieabhängigen Austausch von K+- und Na+-Ionen sowie durch Enzyme der Zellmembran konstant gehalten • Die normal höhere intrazelluläre K+-Konzentration wird durch Ionen-Pumpen gewährleistet • Ionen-Pumpen benötigen ATP • Bei ATP-Mangel kommt es zum Wassereinstrom in das Zytoplama und die Mitochondrien

Zytologische Adaptation 2. Sub- und intrazelluläre Ablagerungen • „Stress“ kann zu abnormen Ablagerungen in der Zelle führen - Lipide, Proteoglykane, Sphingolipide, Glykogen - Pigmente • Ablagerungen können aber auch Ausdruck eines direkten subzellulären Defekts sein - lysosomale Speicherkrankheiten - alpha-1 -Antitrypsinmangel • Bei funktioneller Überlastung - z. B. Hämochromatose

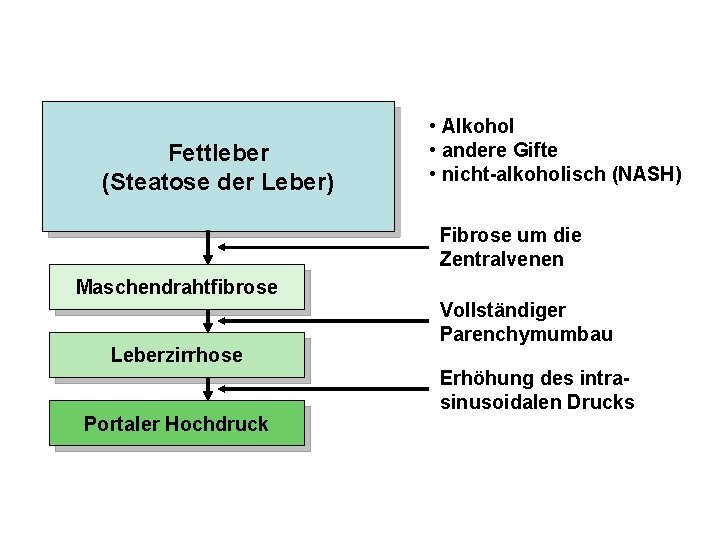
Fettleber (Steatose der Leber) • Alkohol • andere Gifte • nicht-alkoholisch (NASH) Fibrose um die Zentralvenen Maschendrahtfibrose Leberzirrhose Portaler Hochdruck Vollständiger Parenchymumbau Erhöhung des intrasinusoidalen Drucks

Hämosiderin • Lokal, z. B. als „blaues Auge“ • Hämolytische Anämien • Exogene Eisenzufuhr Medikamente, Transfusion • Zerstörung der intestinalen Eisenschranke • Primäre Hämochromatose („Bronzediabetes“) Autosomal-rezessives Erbleiden mit ungehemmter Eisenaufnahme in fast alle Organe Leberfibrose Zirrhose Pankreasfibrose Inselzerstörung mit Diabetes m. Herzmuskel

Zytologische Adaptation 3. Atrophie • Eine Atrophie eines Organes kann durch Verlust und/oder Verkleinerung einzelner Zellen zustande kommen • Eine Zellschrumpfung geschieht bei Beschleunigung der normalen katabolen Prozesse der Zelle • Die Atrophie kann physiologisch, funktionsangepasst oder pathologisch sein Beispiel Skelettmuskulatur bei - physiologischem Alterungsprozess - Gipsverband - Mangelernährung

Zytologische Adapation 4. Hypertrophie • Der Begriff der zellulären Hypertrophie beschreibt eine volumenmäßige Vergrößerung von Zellen • Zellen, die sich vergrößern, synthetisieren vermehrt Proteine. Dies erkennt man im Mikroskop durch - ein basophiles Zytoplasma (mehr Ribosomen) - vergrößerte Nukleolen (mehr m. RNA) - vergrößerte Zellkerne und aufgelockertes Chromatin (vermehrte Transkription der DNS; Polyploidisierung)

Zytologische Adaptation 5. Hyperplasie • Zahlenmäßige Vermehrung von Zellen aus verschiedenen Gründen • Durch vermehrte mitotische Zellteilung entwickelt sich eine Organvergrößerung • Daher können auch nur in Geweben mit teilungsfähigen Zellen eine Hyperplasie entstehen • Von besonderer klinischer Wichtigkeit sind folgende Hyperplasieformen - Struma (Kropf) - (adenomyomatöse) Prostatahyperplasie

Histologische Adaptation 1. Metaplasie • Umwandlung eines differenzierten Gewebes in ein anderes differenziertes Gewebe • Sinn der Metaplasie ist die Anpassung eines Gewebes an eine chronische Schädigung • Die Metaplasie birgt aber auch Gefahren - reduzierte/fehlende Funktion des metaplastischen Gewebes - Gangobstruktionen - Übergang in ein dysplastisches Epithel

Metaplasie-Beispiele Bronchus Pankreas Cervix uteri Ösophagus Harnblase Magen Arterien Knochen nach Fraktur Herzklappen Zylinderepithel mit Zilien Kubisches Epithel der Ausführungsgänge Nicht-verhornendes Plattenepithel Urothel Sekretorisches Epithel Bindegewebe Plattenepithel parakeratotisch verhorntes Plattenepithel Drüsenepithel (Barrett-Epithel) Drüsenepithel Dünndarm. Epithel Knochengewebe Knorpelgewebe myxoides Bindegewebe

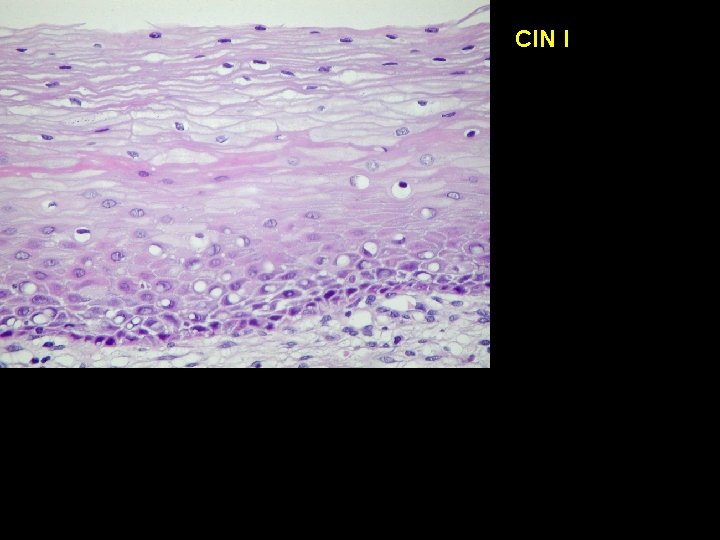
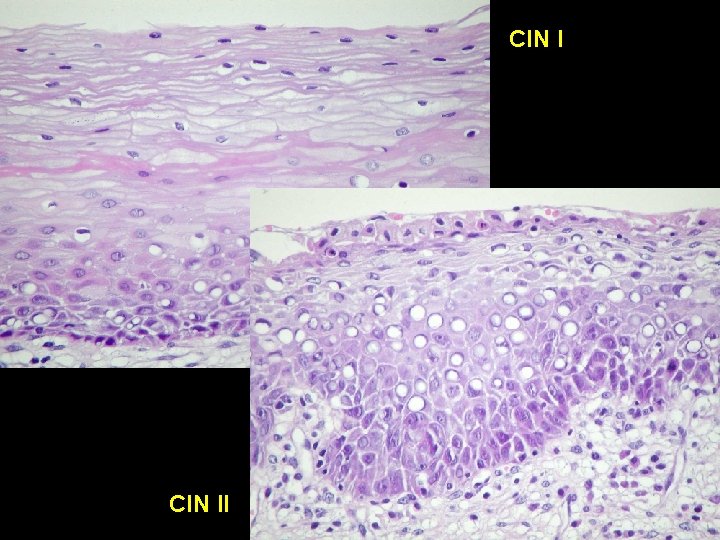
Histologische Adapation 2. Dysplasie von Zellen • Dysplastische Zellen sind transformierte epitheliale oder mesenchymale Zellen mit - abnormer Wachstumstendenz - Potenz zur malignen Entartung • Folgende zytologische Veränderungen sind für dysplastische Zellen charakteristisch - Vergrößerung der Zellkerne - eine Dyskaryose - Deformierung/Polymorphie der Zellkerne - Zunahme der Kern/Plasma-Relation

Histologische Kriterien der Dysplasie • Die Kerne dysplastischer Zellen liegen näher als bei normalen Zellen • Mitosen kommen auch oberhalb der Basalzellschicht vor • Die Polarisation des Epithels ist gestört oder aufgehoben • In der Regel ist dysplastisches Epithel auch hyperplastisch

CIN I

CIN II

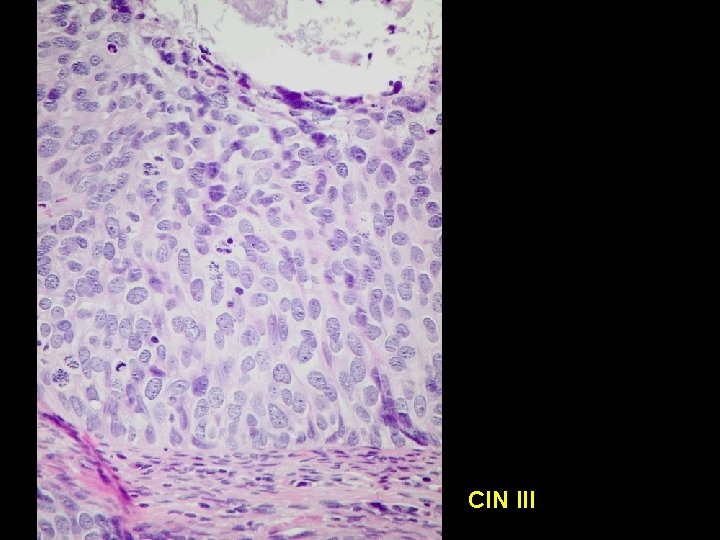
CIN III

Zytologie der Cervix Einteilung nach Papanicolaou Pap II W oder K Pap III D Pap IVA Pap IV B Pap V Normale Epithelien Normale Endozervixzellen Normale Epithelien Entzündungszellen Normale Endozervixzellen Kontrolle erforderlich Reaktiv-abnorme Zellen Entzündungszellen Zellen mit geringen/mittelgradiger Dysplasie Virusveränderungen Zellen mit schwergradiger Dysplasie Virusveränderungen Verdacht auf invasives Karzinom Zellen eines invasiven Karzinoms

Zytologie der Cervix Einteilung nach Papanicolaou Pap II W oder K Pap III D Pap IVA Pap IV B Pap V Normale Epithelien Normale Endozervixzellen Normale Epithelien Entzündungszellen Normale Endozervixzellen Kontrolle erforderlich Reaktiv-abnorme Zellen Entzündungszellen 3 Mon. Zellen mit geringen/mittelgradiger Dysplasie Virusveränderungen 6 Mon. Zellen mit schwergradiger Dysplasie Virusveränderungen Verdacht auf invasives Karzinom Konisation Zellen eines invasiven Karzinoms

Take-Home-Message I • Eine Schädigung von Zellen kann als „Stress“ aufgefasst werden • Die wichtigsten „Stressfaktoren“ sind Sauerstoffmangel, Strahlen, chemische Stoffe, Viren, Bakterien und immunologische Prozesse • Die Zellschädigung geschieht über freie Radikale, die Zellmembranen schädigen

Take-Home-Message II • Die erste Reaktion der geschädigten Zellen ist eine Reduktion ihrer physiologische Proteine und eine vermehrte Synthese selektiver Proteine („Stressproteine“) • Bei anhaltendem Stress erfolgt eine strukturelle Anpassung (Adaptation), wie hydropische Schwellung, Atrophie, Hypertrophie und Hyperplasie • Diese Adaptation geht vielfach auch mit abnormen intrazellulären Ablagerungen einher • Phenotypische Veränderungen bei „Stress“ sind Metaplasie und Dysplasie