Zakad Chemii Fizycznej Wydzia Chemii UAM Pozna Sposb

Zakład Chemii Fizycznej Wydział Chemii UAM, Poznań Sposób na porządek Samoorganizacja kontra entropia Waldemar Nowicki gwnow@amu. edu. pl

Dlaczego porządkowanie (konstrukcja uporządkowanych struktur) stwarza problemy?

Dlaczego porządkowanie (konstrukcja uporządkowanych struktur) stwarza problemy?

Proces samorzutny E < 0 E=Emin
Proces samorzutny E < 0 E=Emin G < 0 G=Gmin
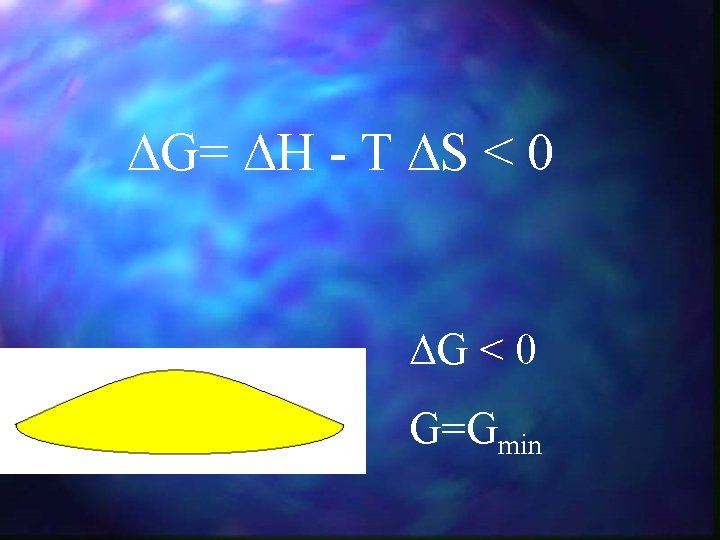
G= H - T S < 0 G < 0 G=Gmin

G= H - T S < 0 H < 0 Maleje energia układu - T S < 0 Rośnie bałagan
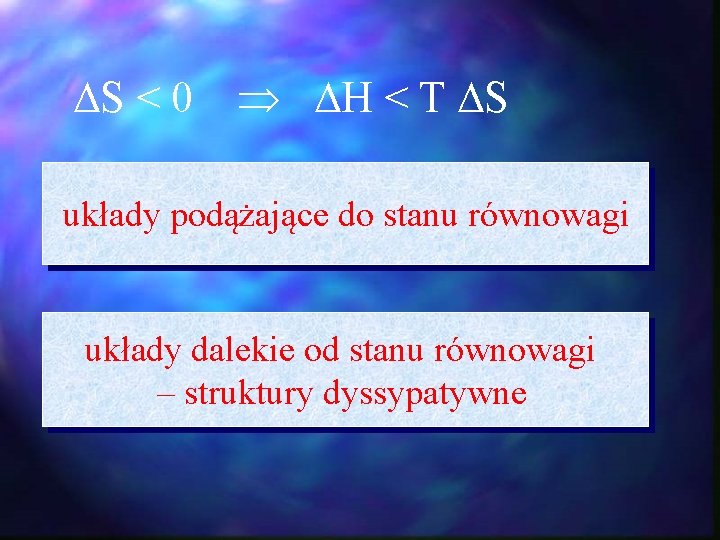
S < 0 H < T S układy podążające do stanu równowagi układy dalekie od stanu równowagi – struktury dyssypatywne

układy podążające do stanu równowagi S < 0 H < T S

Siły grawitacji Siły elektrostatyczne Siły magnetyczne Siły oddziaływań międzycząsteczkowych Siły napięcia powierzchniowego, kohezji i adhezji



Oddziaływania międzycząsteczkowe – siły elektrostatyczne oraz siły van der Waalsa
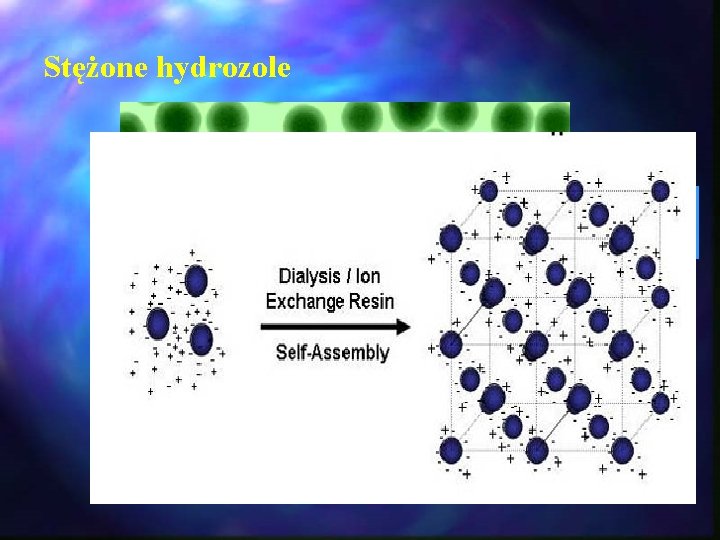
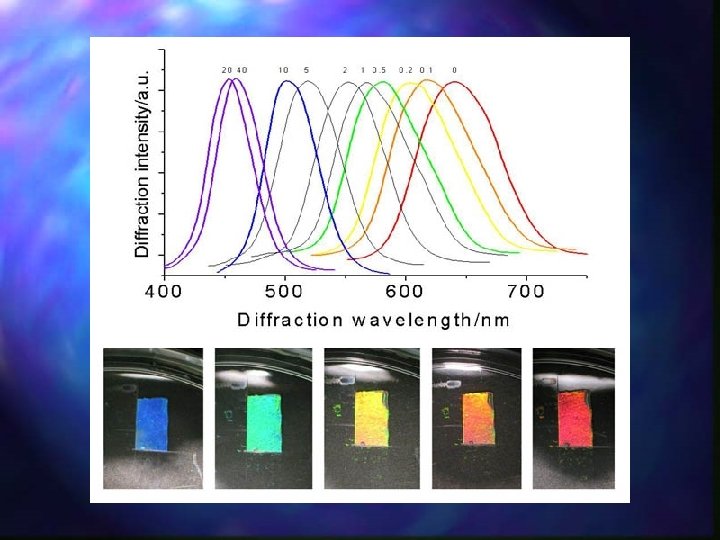
Stężone hydrozole
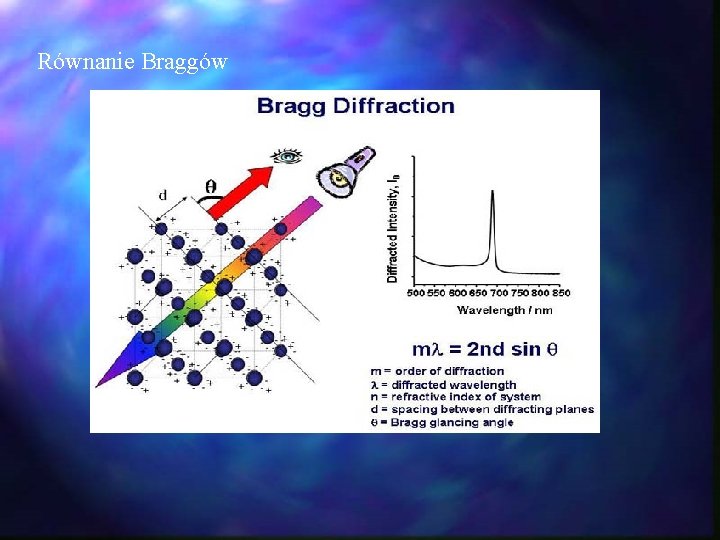
Równanie Braggów
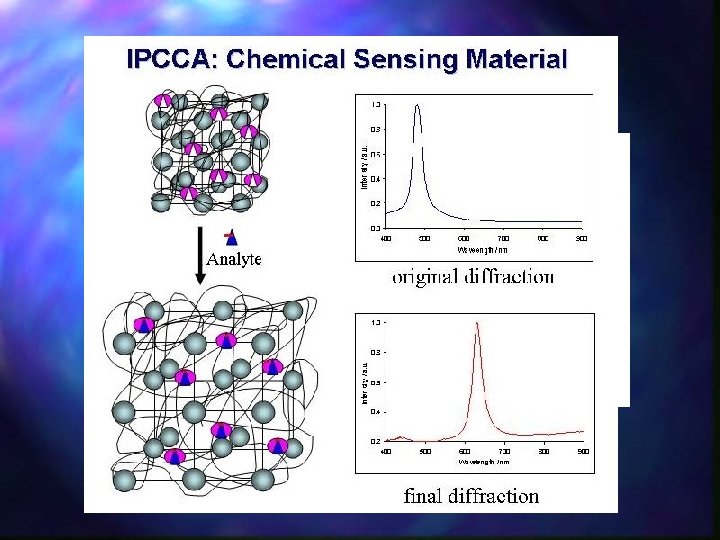
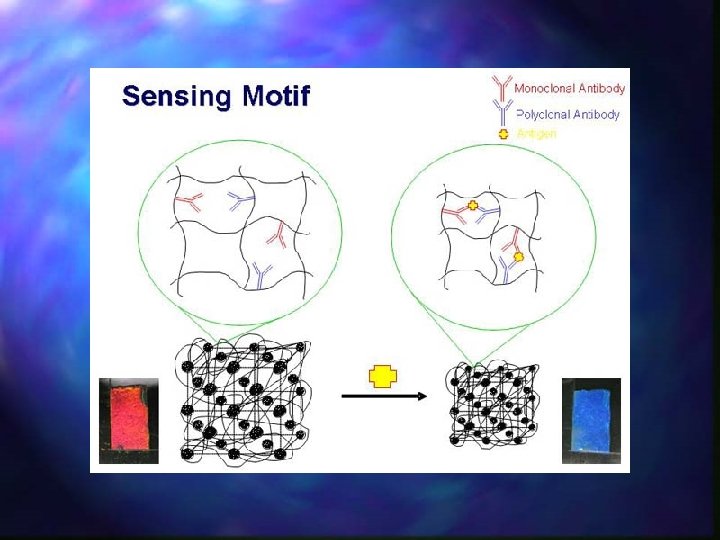

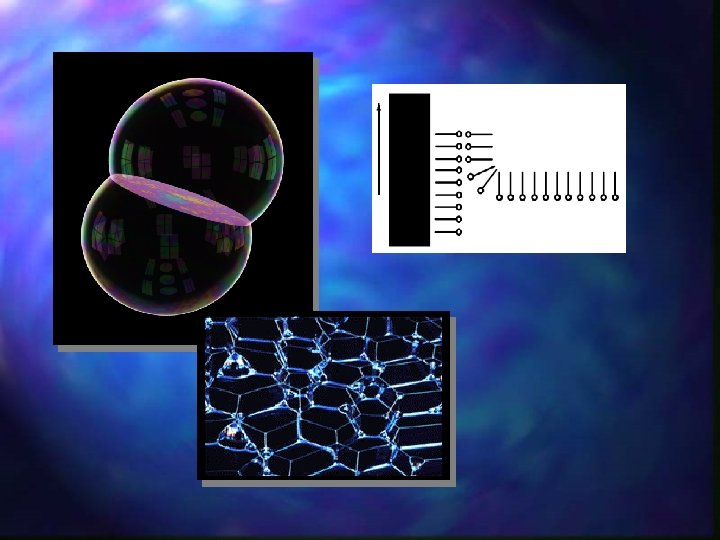
Napięcie powierzchniowe
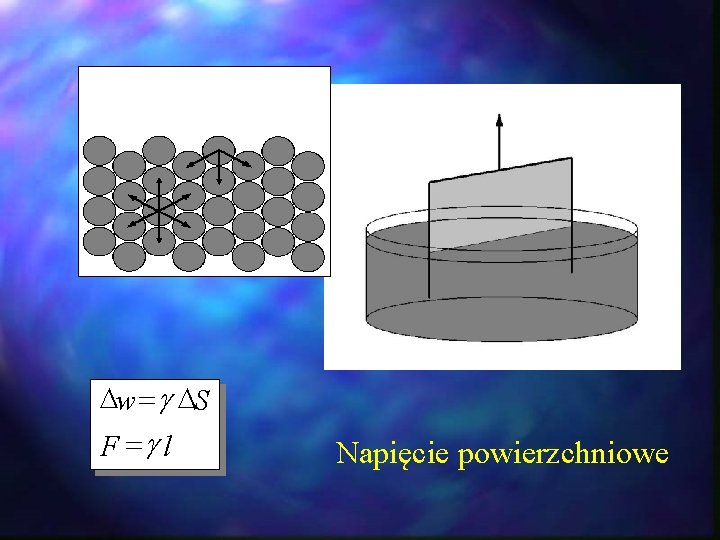
w = g S F =g l Napięcie powierzchniowe

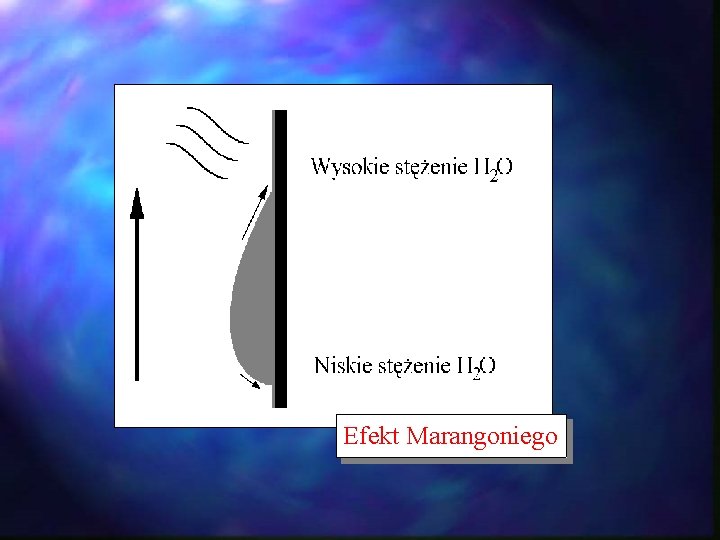
Efekt Marangoniego
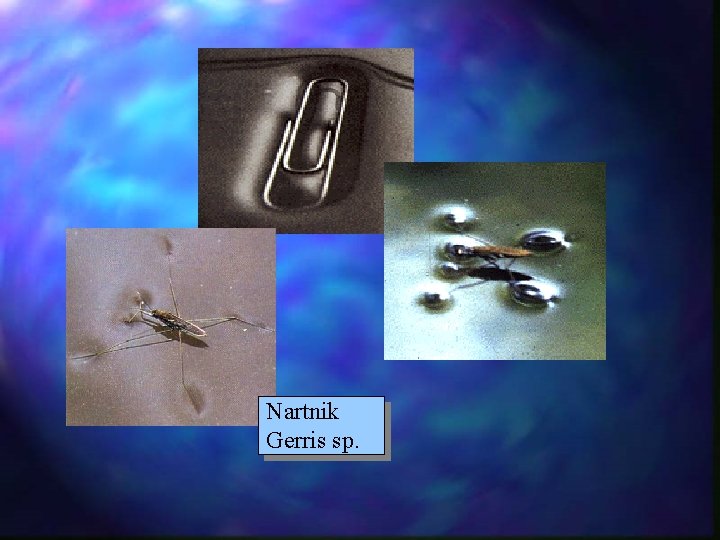
Nartnik Gerris sp.
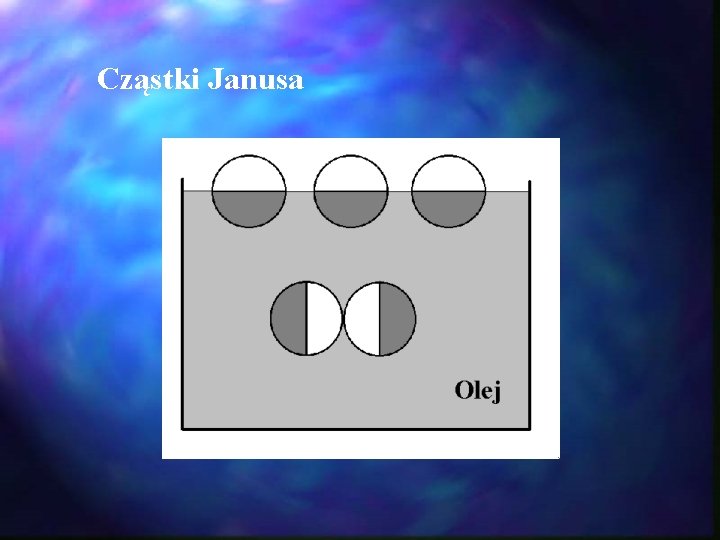
Cząstki Janusa

2 D

Piany i stężone emulsje Ciecze komórkowe

Prawa Plateau: • Krawędzie Plateau są tworzone przez trzy ciekłe filmy pomiędzy którymi występują kąty dwuścienne równe 2/3 (120°) • Wierzchołki powstają w wyniku złożenia czterech krawędzi pod kątami tetraedrycznymi, tzn. arccos(1/3)=109. 5° Prawo Laplace’a Różnica ciśnień występująca po obu stronach filmu jest odwrotnie proporcjonalna do jego krzywizny

Piany monodyspersyjne Arystoteles – czworościan należy do wielościanów foremnych wypełniających przetrzeń Kelvin – bryłą wypełniającą przestrzeń bez reszty i posiadającą najmniejszą możliwą powierzchnię jest czternastościan Thomson W. (Lord Kelvin), On the division of space with minimum partitional area, Phil. Mag. , 24, 503 (1887) Weaire-Phelan – mniejszy stosunek powierzchni do objętości (o 0. 3 %) ma sieć Kelvin złożona z komórek elementarnych zawierających dwa dwunastościany. Arystoteles i sześć czternastościanów ( z dwunastoma ścianami w kształcie pięciokatów) Weaire-Phelan Weaire D. , Phelan R. , A counterexample to Kelvin’s conjecture on minimal surfaces, Phil. Mag. Lett. , 69, 107 (1994) Eksperyment – Tomografia w świetle widzialnym Thomas P. D. , Darton R. C. , Whalley P. B. , Liquid foam structure analysis by visible light tomography, Chem. Eng. J. , 187 (1995) 187 -192 Garcia-Gonzales R. , Monnreau C. , Thovert J. -F. , Adler P. M. , Vignes-Adler W. , Conductivity of real foams, Colloid Surf. A, 151 (1999) 497 -503
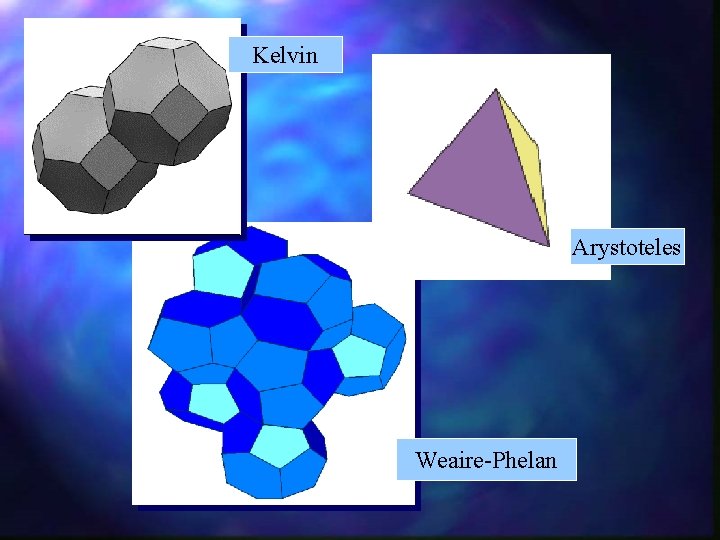
Kelvin Arystoteles Weaire-Phelan
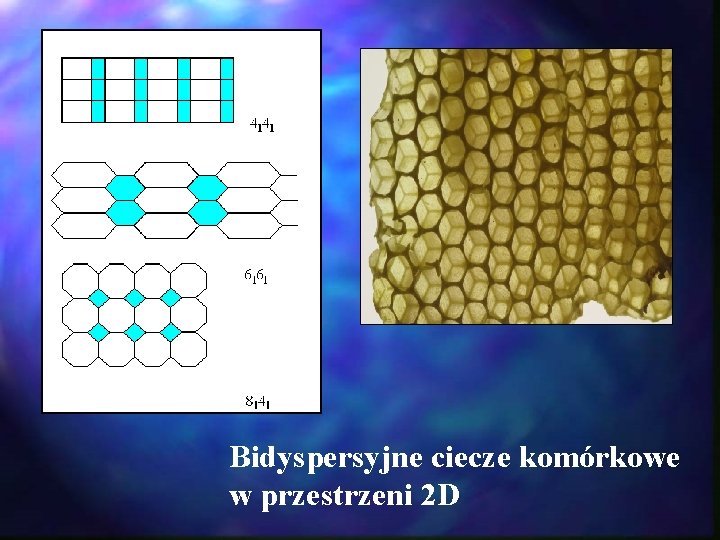
Bidyspersyjne ciecze komórkowe w przestrzeni 2 D
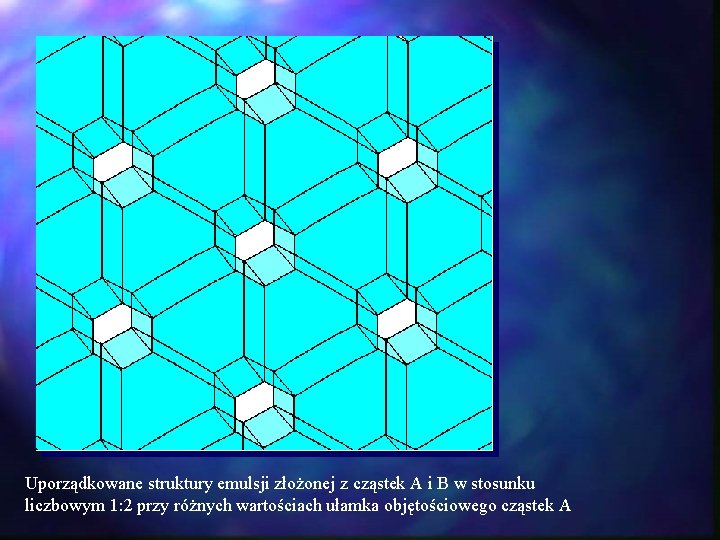
Uporządkowane struktury emulsji złożonej z cząstek A i B w stosunku liczbowym 1: 2 przy różnych wartościach ułamka objętościowego cząstek A
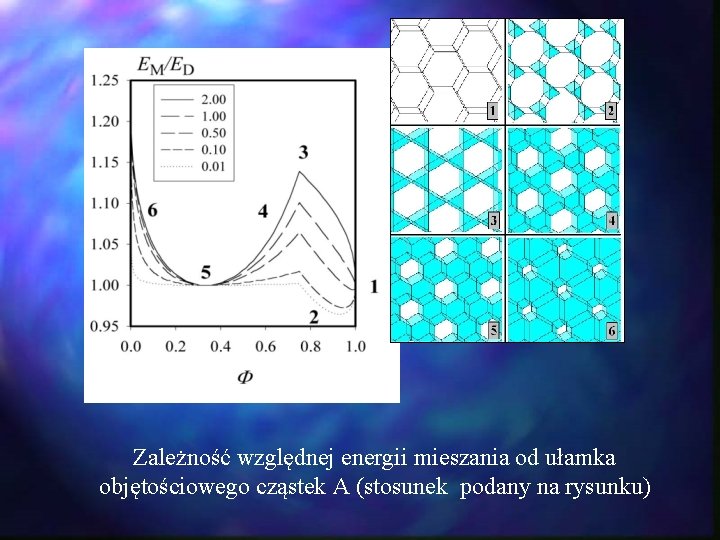
Zależność względnej energii mieszania od ułamka objętościowego cząstek A (stosunek podany na rysunku)
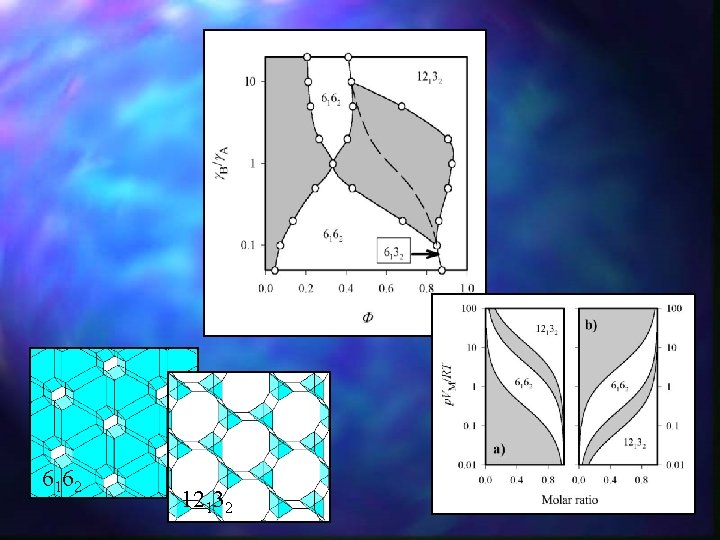
6162 12132

Porządkowanie kosztem wzrostu entropii? Paradoksy entropii!!! Układy micelarne (oddziaływania hydrofobowe) Adsorpcja polimeru Depletion flocculation
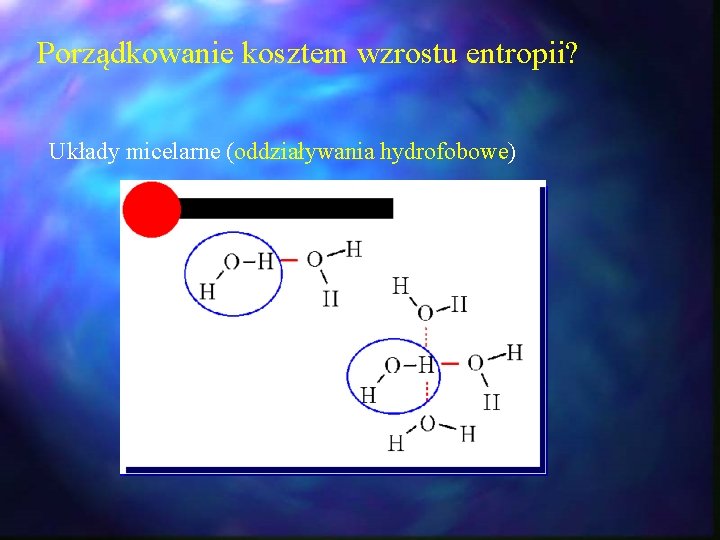
Porządkowanie kosztem wzrostu entropii? Układy micelarne (oddziaływania hydrofobowe)
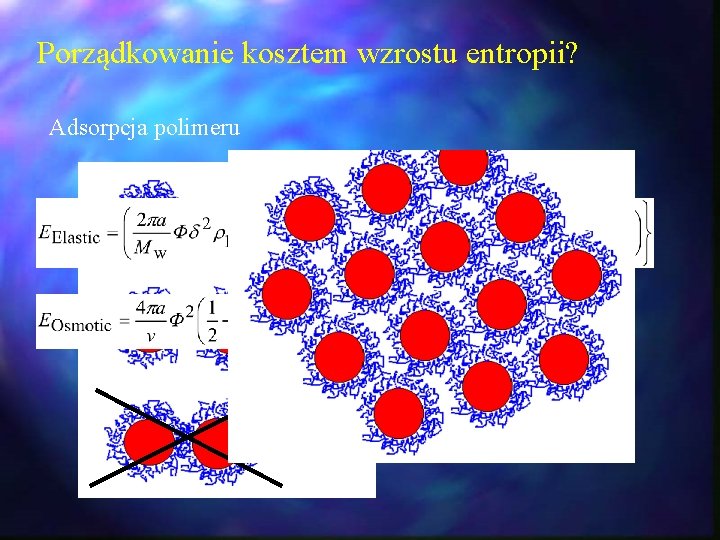
Porządkowanie kosztem wzrostu entropii? Adsorpcja polimeru
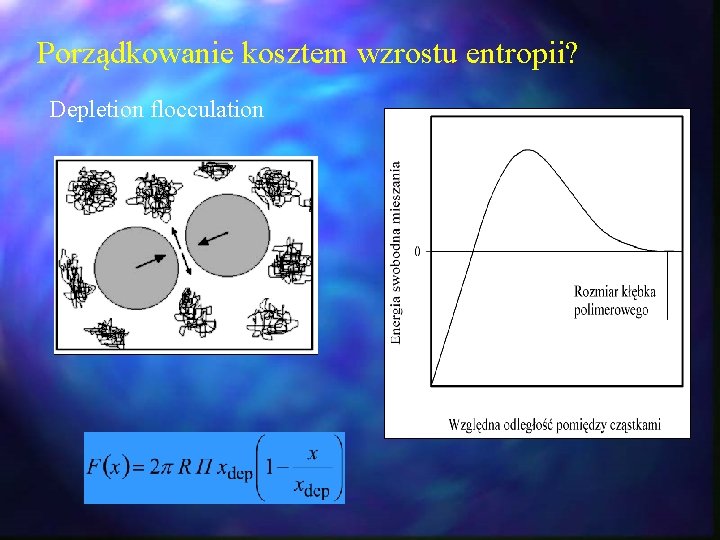
Porządkowanie kosztem wzrostu entropii? Depletion flocculation
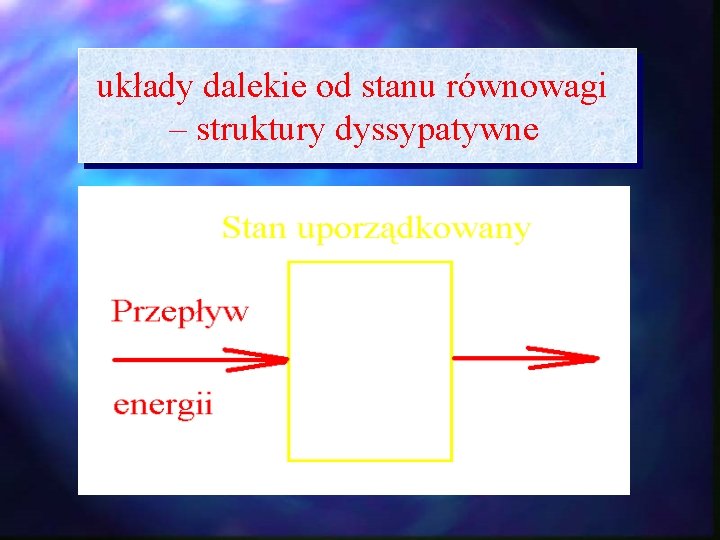
układy dalekie od stanu równowagi – struktury dyssypatywne
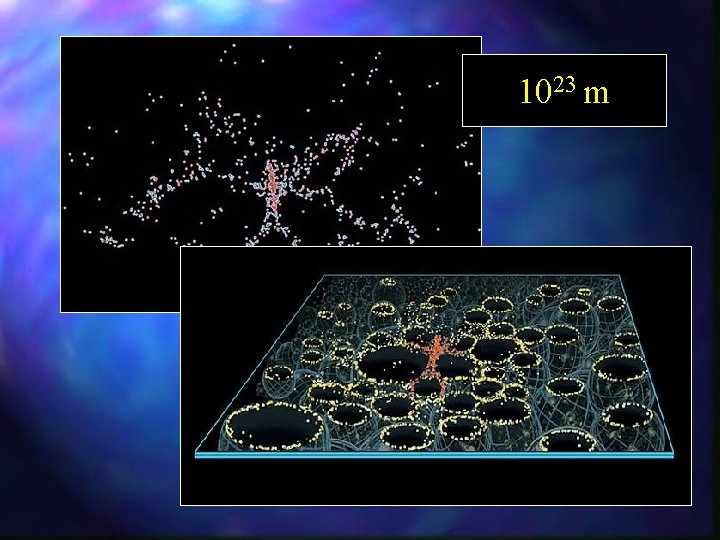
1023 m

106 m

Komórki konwekcyjne Rayleigha-Benarda 10 -2 m Konwekcja? ? ?

Misja Apollo 17 Efekt Marangoniego!!!

Struktura minerałów Porfiroblasty

Coś dla chemika! Pierścienie Lieseganga Reakcje oscylacyjne

Pierścienie Lieseganga 4 Ag+ + Cr 2 O 7 -2 + H 2 O 2 Ag 2 Cr. O 4 + 2 H+
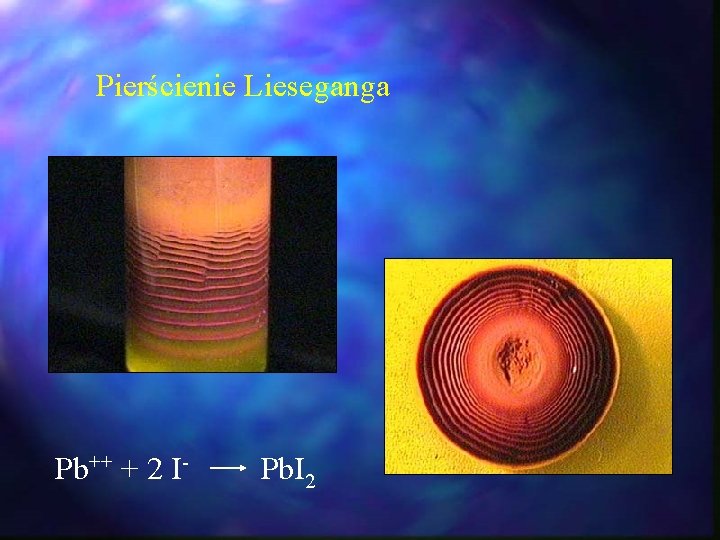
Pierścienie Lieseganga Pb++ + 2 I- Pb. I 2

Reakcja Biełousowa-Żabotyńskiego
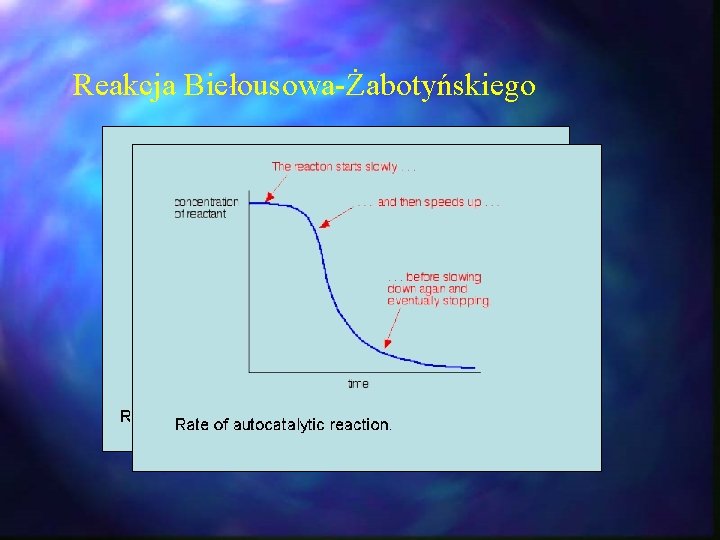
Reakcja Biełousowa-Żabotyńskiego

Reakcja Biełousowa-Żabotyńskiego Br– + Br. O 3– + 2 H+ HBr. O 2 + HOBr Br– + HBr. O 2 + H+ 2 HOBr Br. O 3– + HBr. O 2 + H+ 2 Br. O 2 + 2 H 2 O Ce 3+ + Br. O 2 + H+ Ce 4+ + HBr. O 2 2 HBr. O 2 HOBr + Br. O 3– + H+ 2 Ce 4+ + HOBr +2 Br. O 3– + 2 CH 2(COOH)2 2 Ce 3+ + 3 H+ + 3 Br– + 6 CO 2 + 4 H 2 O OREGONATOR 3 Br. O 3–+5 CH 2(COOH)2+3 H+ 3 Br. CH(COOH)2+2 HCOOH+4 CO 2+5 H 2 O

Reakcja Biełousowa-Żabotyńskiego Br– + Br. O 3– + 2 H+ HBr. O 2 + HOBr Br– + HBr. O 2 + H+ 2 HOBr Br. O 3– + HBr. O 2 + H+ 2 Br. O 2 + 2 H 2 O Ce 3+ + Br. O 2 + H+ Ce 4+ + HBr. O 2 2 HBr. O 2 HOBr + Br. O 3– + H+ 2 Ce 4+ + HOBr +2 Br. O 3– + 2 CH 2(COOH)2 2 Ce 3+ + 3 H+ + 3 Br– + 6 CO 2 + 4 H 2 O 3 Br. O 3–+5 CH 2(COOH)2+3 H+ 3 Br. CH(COOH)2+2 HCOOH+4 CO 2+5 H 2 O

Reakcja Biełousowa-Żabotyńskiego Br– + Br. O 3– + 2 H+ HBr. O 2 + HOBr Br– + HBr. O 2 + H+ 2 HOBr Br. O 3– + HBr. O 2 + H+ 2 Br. O 2 + 2 H 2 O Ce 3+ + Br. O 2 + H+ Ce 4+ + HBr. O 2 2 HBr. O 2 HOBr + Br. O 3– + H+ 2 Ce 4+ + HOBr +2 Br. O 3– + 2 CH 2(COOH)2 2 Ce 3+ + 3 H+ + 3 Br– + 6 CO 2 + 4 H 2 O 3 Br. O 3–+5 CH 2(COOH)2+3 H+ 3 Br. CH(COOH)2+2 HCOOH+4 CO 2+5 H 2 O

Reakcja Biełousowa-Żabotyńskiego Stan I Br– + Br. O 3– + 2 H+ HBr. O 2 + HOBr Br– + HBr. O 2 + H+ 2 HOBr Br. O 3– + HBr. O 2 + H+ 2 Br. O 2 + 2 H 2 O Ce 3+ + Br. O 2 + H+ Ce 4+ + HBr. O 2 2 HBr. O 2 HOBr + Br. O 3– + H+ 2 Ce 4+ + HOBr +2 Br. O 3– + 2 CH 2(COOH)2 2 Ce 3+ + 3 H+ + 3 Br– + 6 CO 2 + 4 H 2 O 3 Br. O 3–+5 CH 2(COOH)2+3 H+ 3 Br. CH(COOH)2+2 HCOOH+4 CO 2+5 H 2 O

Reakcja Biełousowa-Żabotyńskiego Stan I Br– + Br. O 3– + 2 H+ HBr. O 2 + HOBr Br– + HBr. O 2 + H+ 2 HOBr Br. O 3– + HBr. O 2 + H+ 2 Br. O 2 + 2 H 2 O Ce 3+ + Br. O 2 + H+ Ce 4+ + HBr. O 2 2 HBr. O 2 HOBr + Br. O 3– + H+ 2 Ce 4+ + HOBr +2 Br. O 3– + 2 CH 2(COOH)2 2 Ce 3+ + 3 H+ + 3 Br– + 6 CO 2 + 4 H 2 O Stan II 3 Br. O 3–+5 CH 2(COOH)2+3 H+ 3 Br. CH(COOH)2+2 HCOOH+4 CO 2+5 H 2 O
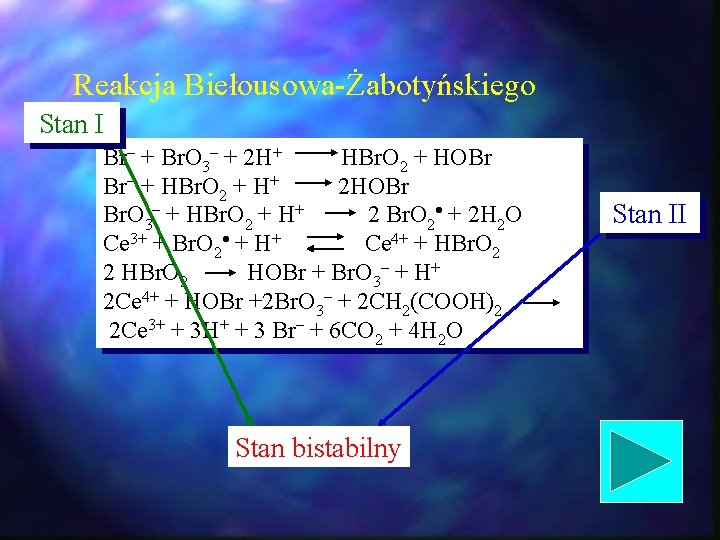
Reakcja Biełousowa-Żabotyńskiego Stan I Br– + Br. O 3– + 2 H+ HBr. O 2 + HOBr Br– + HBr. O 2 + H+ 2 HOBr Br. O 3– + HBr. O 2 + H+ 2 Br. O 2 + 2 H 2 O Ce 3+ + Br. O 2 + H+ Ce 4+ + HBr. O 2 2 HBr. O 2 HOBr + Br. O 3– + H+ 2 Ce 4+ + HOBr +2 Br. O 3– + 2 CH 2(COOH)2 2 Ce 3+ + 3 H+ + 3 Br– + 6 CO 2 + 4 H 2 O Stan bistabilny Stan II


- Slides: 59