Z ATOMSKI BROJ ili redni broj Z NpNe


Z – ATOMSKI BROJ ili redni broj (Z= N(p)=N(e)) A – MASENI BROJ ( A= N(p) + N(n) = Z + N(n)) Izotopi – atomi istog elementa koji imaju isti broj protona, a različit broj neutrona (npr. O – 16, O -17, O -18 ili H-1 vodonik, H-2 deuterijum, H– 3 tricijum)
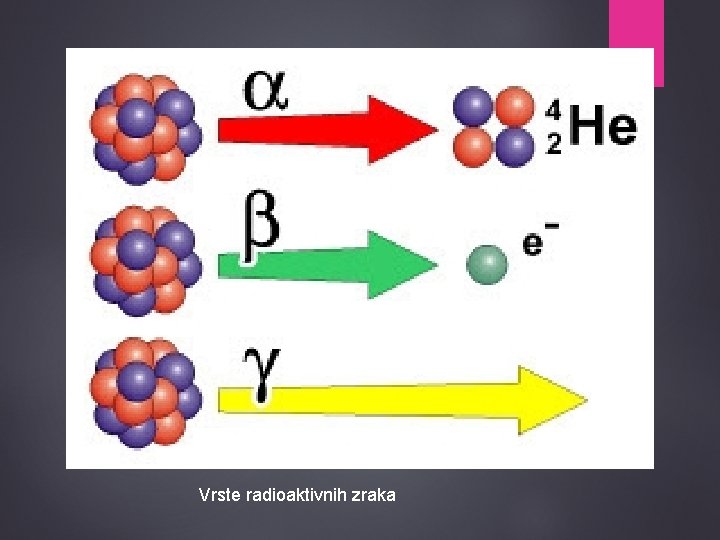
Vrste radioaktivnih zraka


Ø Proučavajući produkte raspadanja naučnici Raderford i Sodi otkrili su da atomi nastali radioaktivnim raspadanjem i sami mogu biti radioaktivni i prelaziti u atome novih elemenata. Raspadanje se nastavlja u nizu, po određenim zakonitostima, dok ne nastane stabilan, neradioaktivan atom. Ø U prirodi postoje 3 radioaktivna niza: uranov, torijumov i aktinijumov. Ø Svi nizovi završavaju stabilnim olovom. Ø Najpoznatiji od njih je proces raspada U-238.
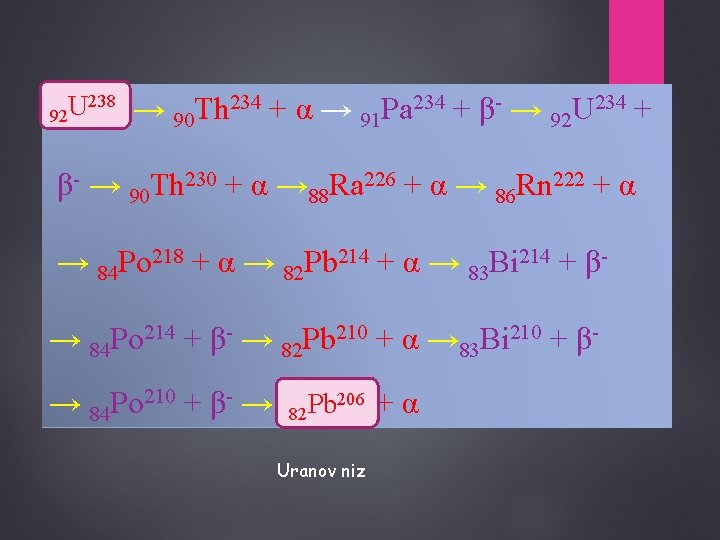
238 → Th 234 + α → Pa 234 + β- → U 234 + U U 92 92 90 91 92 β- → 90 Th 230 + α → 88 Ra 226 + α → 86 Rn 222 + α → 84 Po 218 + α → 82 Pb 214 + α → 83 Bi 214 + β→ 84 Po 214 + β- → 82 Pb 210 + α → 83 Bi 210 + β 206 + α → 84 Po 210 + β- → 8282 Pb Pb 206 Uranov niz

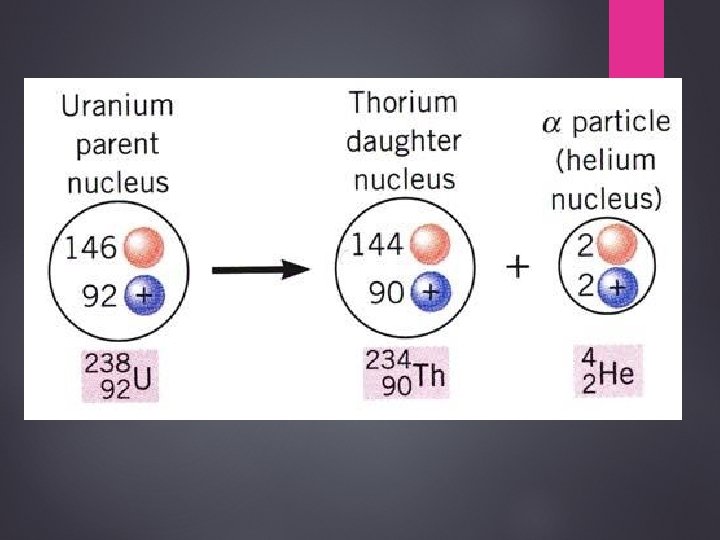
Fajans - Sodijevo pravilo: Ø Ako neki element emituje α- česticu, njegov maseni broj se smanjuje za 4, a redni za 2 Ø Ako emituje β –česticu maseni broj ostaje isti, a redni broj se povećava za 1 Ø Emisijom γ –zraka ne mijenja se ni maseni ni redni broj
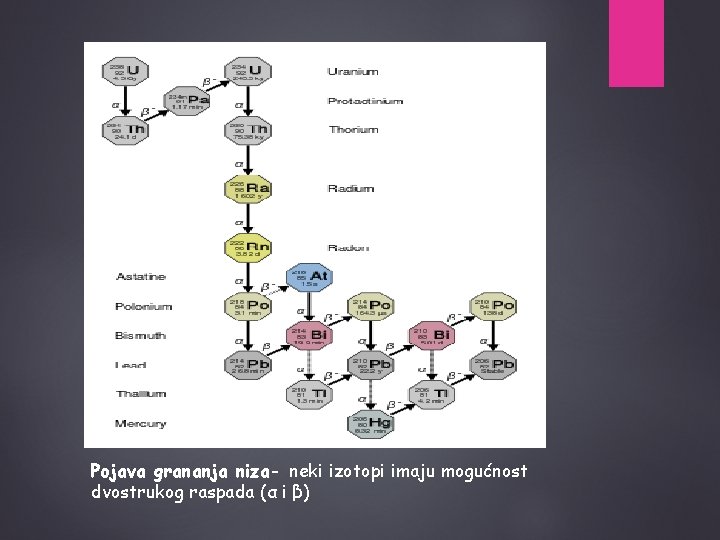
Pojava grananja niza- neki izotopi imaju mogućnost dvostrukog raspada (α i β)
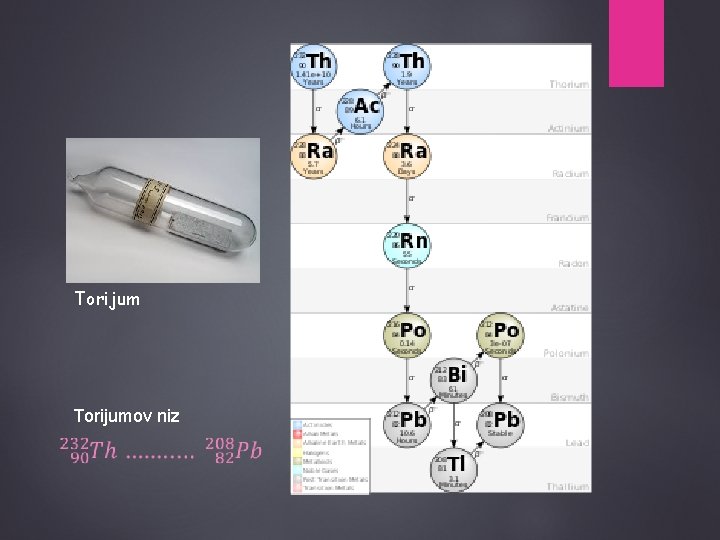
Torijumov niz
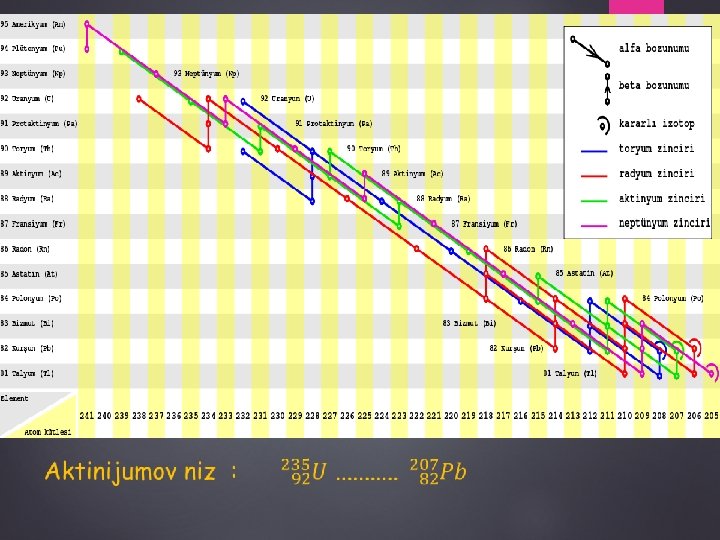


Vrijeme poluraspada izotopa uranovog niza
- Slides: 13