Ya Asitlerinin Farkl Oksidasyonlar 22 26 karbonlu doymu

Yağ Asitlerinin Farklı Oksidasyonları

22 -26 karbonlu, doymuş ve dallanmamış uzun yağ asitlerinin önemli bir bölümü perosizomlarda yıkılır. Bu yağ asitlerinin açil Co. A türevleri, karnitine ihtiyaç göstermeksizin, peroksizom içine girer. H 2 O 2 ve asetil Co. A ürünleri oluşturan flavinli (FAD veya FMN‘li) dehidrogenazlar marifetiyle zincir oktanoil Co. A'ya kadar kısaltılır.

Asetil ve oktanoil Co. A' 1 ar, daha sonra, mitokondriye aktarılarak metabolize olurlar. Zellweger sendromu gibi peroksizomların gelişmediği durumlarda, yukarıda özellikleri verilen yağ asitlerinin karaciğer ve sinir hücrelerinde birikerek ölüme yol açtığı ortaya konulmuştur.

Beyin ve diğer doku mikrozomlarında, fitik asit(klorofil yapısındaki fıtol zincirinden oluşur) gibi dallanmış yağ asitleri α-oksidasyona maruz kalmaktadır. Çünkü, bu zincirler izopren türevi olduklarından, β karbonlarında bulunan -CH 3 yıkılamazlar. grubu α yüzünden -oksidasyonu kişilerde Refsum hastalığı görülür. β -oksidasyonla gerçekleştiremeyen

Karaciğer mikrozomlarında karşılan bir başka yağ asidi oksidasyonu çeşidi de ω-oksidasyonu ile karboksil karbonuna en uzaktaki karbonun yükseltgenmesidir. Burada dikarboksilatlar meydana gelir ve TCA bileşiklerine çevrilerek metabolize olurlar. devri ara

Hem α-, hem de ω-oksidasyonlarının ilk basamaklarında NADPH, O 2, sitokrom P 450 veya monooksigenazlarla hidroksilasyon vardır. başka

Keton Cisimleri

Yağ asitleri oksidasyonunda oluşan asetil Co. A‘lar, eğer yağ ve karbonhidrat yıkımları dengeli ise, sitrik asit devrine girerler. Metabolizmada sözü edilen "yağlar karbonhidratların aleviyle yanar" deyişinin moleküler temeli bugün çok daha iyi bilinmektedir.

Asetil Co. A'nın TCA'ya girişi, sitrat oluşumu için ortamda okzalasetatın varhğına bağlıdır. Eğer yağ yıkımı fazla ise, asetil Co. A farklı bir yola gider.

Açlık ve şeker hastalığı durumunda okzalasetat glukoneogenez yolunda kullanılacağından asetil Co. A ile birleşebilecek seviyenin altına düşer.

Bu şartlar altında asetil Co. A, asetoasetat ve D-3 hidroksibütirata dönüştürülür. işte bu mekanizma ile oluşan aseton, asetoasetat ve D-3 -hidroksibütirat, keton cisimleri adını alır.

Asetoasetat asetil Co. A'dan üç basamakta oluşur: Önce iki asetil Co. A β-ketotiyolaz (1) enzimi katalizörlüğünde birleşerek asetoasetil Co. A oluşturur. Bu reaksiyon yağ asitleri oksidasyonunun tiyolitik basamağının dönüşümünden ibarettir. parçalanma

Daha sonra asetoasetil Co. A, asetil Co. A ile hidroksimetilglutaril Co. A (HMGCo. A) sentetaz (2) enzimi katalizörlüğünde 3 -hidroksi 3 -metil glutaril Co. A'yı meydana getirir.

Bu da daha sonra hidroksimetilglutaril Co. A parçalayıcı enzim (3) vasıtasıyla asetil Co. A ve asetoasetata ayrılır. D-3 Hidroksibütirat, D-3 -hidroksibütirat dehidrogenaz (4) katalizörlüğünde asetoasetatın indirgenmesi sonucu oluşur. mitokondri matriksinde

Hidroksibütirat / asetoasetat oram mitokondri içinde NADH/NAD+ oranına bağlıdır. Asetoasetat yavaş ve kendiliğinden bir dekarboksilasyonla asetona çevrilir. Kanında yüksek asetoasetat seviyesi olan şahısların nefesleri aseton kokar.

Asetoasetat ve D-3 -hidroksibütiratın üretildiği başlıca organ karaciğerdir. Daha sonra karaciğer mitokondrilerinden difuze olarak periferal dokulara kan dolaşımıyla taşınırlar. Önceleri keton cisimlerinin patolojik bir ürün olduğu düşünülmekteydi. Bu bileşiklerin fizyolojik önemi sonradan aydınlatılmıştır.

George Cahill ve diğer bazı araştırmacılar bu bileşiklerin enerji metabolizmasında önemli rolleri olduğunu göstermişlerdir. Asetoasetat ve D-3 -hidroksibütirat bazı dokuların normal yakıt maddeleri şeklinde enerji kaynağı olarak önemli miktarda kullanılmaktadır. Gerçekten kalp kası ve böbrek korteksi asetoasetatı glukoza tercih eder.

Beyin dokusu ise, başlıca yakıt kaynağı olarak, dengeli beslenme durumunda glukoz kullanılır. Bununla birlikte açlık ve şeker hastalığında asetoasetattan faydalanacak şekle adapte olur. Uzun açlık döneminde beynin yakıt ihtiyacının % 75'i asetoasetat tarafından sağlanır.

Kanda D-3 -hidroksi bütirat olarak taşman ve girdiği periferal doku hücrelerinde tekrar asetoasetata yükseltgenen keton cisimleri, spesifik bir Co. A transferaz enzimi tarafından katalizlenen bir reaksiyonla, süksinil Co. A'dan Co. A transferi sonucu aktifîeştirilir. Asetoasetil Co. A daha sonra iki molekül asetil Co. A vermek üzere parçalanır.

Asetil Co. A'lar daha sonra sitrik asit devrine girerler. Karaciğerde spesifik Co. A transferaz enzimi bulunmadığı ve eritrositlerde de mitokondri olmadığı için keton cisimlerini yakıt olarak kullanamazlar.

Asetoasetat, asetil Co. A'nm suda çözünebilir ve taşınabilir bir şekli olarak değerlendirilebilir. Yağ asitleri adipoz doku tarafından salıverilir, karaciğer tarafından asetoasetata çevrilerek diğer dokulara gönderilir.

Asetoasetatın düzenleyici bir rolü de vardır. Kandaki yüksek asetoasetat seviyesi asetil birimlerinin bolluğuna işarettir ve adipoz dokuda lipolizin azalmasına yol açar.

YAĞ ASİTLERİNİN SENTEZİ

Yağ asitlerinin sentezi aynen glikojen ve glukozda olduğu gibi, yıkımdan farklı reaksiyonlarla gerçekleşir. Bu reaksiyon serisinin başlıca özellikleri şunlardır:

l. Yağ asitlerinin yıkımı mitokondri matriksinde cereyan ederken, biyosentezi sitozolde gerçekleşir. 2. Yağ asidi sentezinin ara bileşikleri bir taşıyıcı proteinin (ACP) sülfhidril gruplarına kovalent bağlıdır. Yıkımda ise Co. A'ya takılıdır.

3. Yağ asidi biyosentezi enzimlerinin çoğu yağ asidi sentetaz kompleksi adı verilen bir multienzim sistemi şeklinde organize olmuşlardır. Yıkım enzimlerinde ise böyle bir durum söz konusu değildir.

4. Yağ asidine karbon atomları ikili birimler halinde asetil Co. A'dan sağlanır. Zincir uzaması basamağında iki karbon birimini veren aktifleşmiş bileşik malonil Co. A'dır. C 02'nin uzaklaştırılması ile uzama reaksiyonu ilerler.

5. Yağ asidi sentezinde indirgeyici olarak NADPH kullanılır. 6. Yağ asidi sentetaz kompleksinin uzatma reaksiyonu 16 karbonlu palmitat oluşumuna kadar devam eder ve durur. Bundan sonraki uzamalar ve çift bağların oluşumu başka enzim sistemleri tarafından katalizlenir.

Doymuş Yağ Asitlerinin Sentezi

Yağ asitlerinin biyosentezinin aydınlatılması, Salih Wakil'in bikarbonatın kullanılma mekanizmasını ortaya koymasından sonra mümkün olmuştur. Gerçekten, yağ asitlerinin biyosentezi asetil Co. A'nın malonil Co. A'ya karboksilasyonu ile başlar. Prostetik grup olarak biyotin ihtiva eden asetil Co. A karboksilaz enzimi tarafından katalizlenen bu: reaksiyon dönüşümsüzdür.

Biyotinin karboksil grubu, aynen piruvat karboksilaz enziminde olduğu gibi, lisin rezidüsünün ε-amino grubuna kovalent bağlıdır. İki enzim arasındaki bir başka benzerlik de, asetil karboksillenmesidir. Co. A'nın Önce, bir iki basamakta ATP harcanarak karboksibiyotin oluşmakta, sonra da C 02 malonil Co. A teşkil etmek üzere asetil Co. A'ya aktarılmaktadır.

CO 2~Biyotin-enzim+Asetil Co. A Malonil Co. A+Biyotin-enzim

Substratların bu enzime bağlanmaları ve ürünlerin salıverilmeleri spesifik bir sıra takip etmektedir. Burada, asetii Co. A karboksilaz enzimi, bütün substratlar bağlanmadan önce bir veya daha fazla ürünün salıverildiği ping-pong reaksiyon mekanizmasına iyi bir örnek olmaktadır. Sitrat bu enzimin bir allosterik aktivatörü iken, son ürün palmitoil Co. A da yağ asit sentezinin bu ilk dönüşümsüz reaksiyonunu inhibe etmektedir.

P. Roy Vagelos yağ asidi sentezi ara bileşiklerinin bir açil taşıyıcı proteine (ACP) bağlı olduğunu ortaya koymuştur. Bu protein de aynen Co. A gibi bir fosfopantetein grubu ihtiva etmekte ve ara bileşikler bu grubun sülfidril grubuna bağlanmaktadır. ACP'de adı geçen grup bir serin rezidüsüne kovalent takılmıştır. 77 amino asitten ibaret olan açil taşıyıcı protein bir makro Co. A' yı andırmaktadır.

Doymuş uzun zincirli yağ asitlerini asetil Co. A, malonil Co. A ve NADPH'dan sentezleyen enzim sistemi yağ asidi sentetaz enzim kompleksidir. Bakteri yağ asidi sentetazları hücre parçalandığı zaman ayrışmaktadır.

Bu ayrışan enzimlerin tek izole edilmesi, yağ asidi sentezi basamaklarının aydınlatılmasında çok faydalı olmuştur. Gerçekten yüksek organizmalarda yağ asidi sentezine yol açan reaksiyonlar bakterilerinkiyle çok büyük benzerlik arz etmektedir.

Bakterilerin aksine ökaryotik yağ asidi sentetazlan enzimleri birbirine kovalet bağlı multienzim kompleksi halindedir. Mesela maya enzim kompleksi 2300 kdal molekül ağırlığında, elektron mikroskobunda 250 A° boyunda ve 210 A° eninde elips şekline sahip yapılar halinde görülen ve her biri tek gen tarafından şifrelenen iki çeşit polipeptid zincirinden ibarettir.

Memeli yağ asidi sentetazı ise, tıpkı maya hücreleri gibi, her biri 260 kdal molekül ağırlığında olan iki alt biriminden ibarettir. Her zincir birbirine peptid zinciriyle bağlı 3 'domain'den ibarettir.

I. domain, substratın giriş ve kondansasyon (birleşme) birimidir ve asetiltransferaz (AT), maloniltransferaz (MT) ve 3 -ketoacilsentaz (CE) (birleştirici-condensing enzim) enzimlerinden, II. domain, indirgenmenin birimi olup, 3 ketoaçil redüktaz (KR), dehidrataz (DH) ve enoil redüktaz (ER) enzimlerinden ve III. domain ise, sentezlenen palmitatın salıverildiği birim olup tiyoesteraz enziminden gelmiştir. meydana

Yani, bir polipeptid zinciri üzerinde 7 farklı katalitik bölge yer almaktadır. Gerçekten bir çok ökaryotik multienzim kompleksleri, farklı, enzimlerin tek bir polipeptid zincirinde kovalent bağlanmış çok fonksiyonlu proteinlerdir. Bu tarz düzenleme ile, farklı enzimlerin sentez fonksiyonlarının koordineli olarak yerine getirilmesi sağlanmaktadır.

Substratlar difüzyonla zaman kaybetmemekte ve son ürün oluşuncaya kadar ara bileşikler kompleksten ayrılmamaktadır. Açil taşıyıcı protein (ACP) II. domainde yer alırken, malonil Co. A'yı sentezleyen asetil Co. A karboksiiaz enzimi yağ asidi sentetaz kompleksinden ayrı bir yapıdır.

Yağ asitleri sentezinin uzama safhası asetil ve malonil gruplarının ACP'ye bağlanmasıyla başlar. Yağ asidi sentetaz iki esensiyal -SH grubuna sahiptir. Bunlardan birisi ACP'deki 4'-fosfopantetein prostetik grubuna (Pn) ait olup, diğeri spesifik domain I'deki 3 -ketoaçil sentaz enziminin sistein (Cys) kalıntısıdır. Her ikisi de yağ asidi sentezine katılır. Birinci -SH grubu malonil grubunun, ikinci -SH grubu da asetil grubunun giriş yeridir.
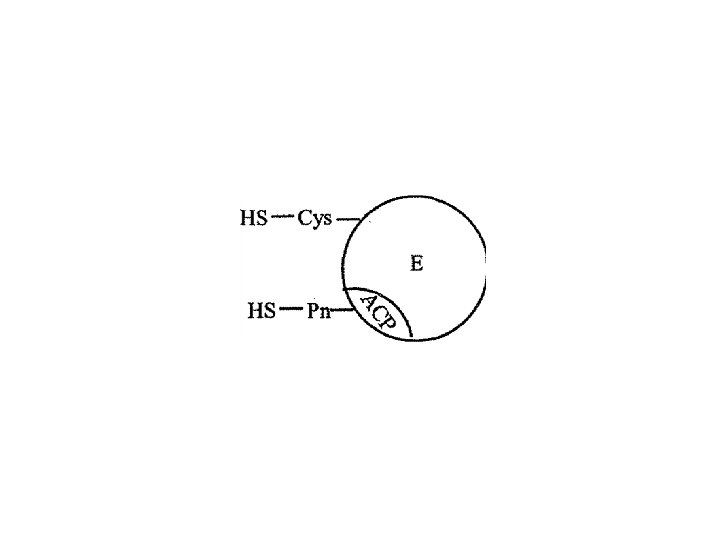

Asetil ve malonil gruplarının ACP'ye bağlanması iki enzimatik reaksiyonla gerçekleşir. Birinci reaksiyonda, asetil transferaz vasıtasıyla asetil Co. A'nın asetil grubu (tek karbon sayılı yağ asitlerinde propiyonil Co. A'nın propiyonil grubu) yağ asidi sentetazın sistein -SH grubuna transfer edilir:


İkinci reaksiyonda, malonil transferaz vasıtasıyla, malonil Co. A'nın malonil grubu ACP'nin fosfopantetein sülfhidril grubuna transfer edilir. Malonil grubu sadece panteteinin -SH grubuna bağlanabilir.

Böylece iki açil grubu yağ asidi sentetaz üzerinde birbirine çok yaklaşmıştır ve zincir uzama prosesi için hazırdırlar.

Daha sonra yağ asidi sentetazın -SH gruplarına kovalent bağlanan asetil ve malonil grupları, fosfopanteteinin -SH grubuna asetoasetil grubu oluşturacak şekilde kondanse olurlar. Bu reaksiyon 3 ketoaçil sentaz tarafından katalizlenir:

Bu kondansasyon reaksiyonunun sonucu olarak iki ve üçer karbonlu birimlerden dört karbonlu birim oluşmaktadır. Acaba niçin bu sentez iki tane iki karbon birimlerinden meydana gelmemektedir?

Bunun cevabı asetoasetil-ACP'nin iki asetil grubu bağlanmış E-ACP'den oluşumunun termodinamik yönden mümkün olmamasının altında yatmaktadır. Ancak, asetil ve malonil gruplarının kondansasyonu sırasında dekarboksilasyon sonucu serbest enerjide bir azalma olmaktadır. Aslında, bu reaksiyon doğrudan doğruya olmasa da, dolaylı olarak ATP hidrolizi ile yürümektedir.

Çünkü asetil Co. A'nın enerjice zengin maloniî Co. A'ya karboksilasyonunda ATP kullanılmakta ve bu serbest enerji dekarboksilasyonla açığa çıkmaktadır.

Yağ asidi sentezinde bundan sonraki üç basamakla C -3'teki keto grubu metilen grubuna indirgenir. Sentezin ilk devrindeki asetoasetil ACP oluşumundan itibaren olan reaksiyonlar Şekil 12. 5'de verilmiştir.

Önce asetoasetil ACP, 3 -ketoaçil redüktaz katalizörlüğünde D-3 -hidroksibütiril ACP'ye indirgenir. Bu reaksiyonun yıkım safhasındaki oksidasyonun dönüşümü olayından iki farkı vardır.

Birincisi, L-yerine D-izomeri oluşmaktadır; ve ikinci olarak da oksidasyonda NAD+ kullanılırken indirgeme NADPH tarafından gerçekleştirilmektedir.

Böylece biyosentez olaylarında NADPH‘ın indirgeyici gücünden faydalanılırken, enerji sağlayan reaksiyonlar sonucunda da NADH'ın oluştuğu genel prensibinin bir örneği burada görülmektedir.

İkinci reaksiyonda dehidrataz beraberliğinde D-3 - hidroksibutiril ACP'den bir H 20 çıkartılarak trans-Δ 2 bütenoil-ACP oluşmaktadır. Bu dehidrasyon olayı sonucu oluşan ara bileşik bir trans- Δ 2 -enoil-ACP'dir.

Devir sonunda, trans-Δ 2 -bütenoil-ACP redüktaz katalizörlüğünde ve bir NADPH harcanması ile bütiril. ACP'ye indirgenmektedir. Oluşan butiril grubu Cys-SH grubuna transfer edilir.

Yağ asidi sentezinin ikinci devrinde bütiril grubu (C 4), yukarıdaki gibi malonil grubuyla kondanse olarak bir C 6 -βketoaçil-ACP oluşturarak yeni bir devri başlatırlar. Bu uzama safhası C 16 -açil-ACP oluşuncaya kadar devam eder. Daha sonra tiyoesteraz tarafından palmitat ve ACP-E vermek üzere hidrolizlenir.

Şeki! 11. 5. Yağ asidi sentezinin iki redüktaz, dehidrataz ve translokasyon basamakaları. Son reaksiyondan sonra butiril grubu Cysr. SH grubuna transfer edilir. Şimdi Pn-SH grubu malonil Co. A'dan malonÜ grubunu aîmaya hazırdır.

Tablo 11. 3. Yağ asidi sentezinin temel reaksiyonları.

Asetil Co. A+7 Malonil Co. A+14 NADPH+7 H+ Palmitat+7 CO 2+14 NADP++8 Co. A+6 H 2 O Bu reaksiyonda kullanılan malonil Co. A’nın oluşum olayını 7 Asetil Co. A+ 7 CO 2+7 ATP 7 Malonil+7 ADP+7 Pi+ 7 H+

İlave ettiğimiz zaman palmitat sentezinin net denklemi 8 Asetil Co. A+7 ATP+14 NADPH palmitat+14 NADP++8 Co. A+6 H 2 O+7 ADP+7 Pi

Buradan görüldüğü gibi, bir palmitat molekülünün sentezlenmesi için 8 molekül asetil Co. A, 14 NADPH ve 7 ATP gereklidir, Yağ asitleri sentezinin sitozolde, piruvattan asetil Co. A oluşumunun mitokondride cereyan ettiği göz önüne alındığında, asetil Co. A'ların mitokondriden sitoplazmaya transferi gerekmektedir. Bu transfer olayı sitrat tarafından gerçekleştirilir.

Önce, mitokondri matriksinde asetil Co. A ve okzalasetatm kondansasyonu ile sitrat teşekkül eder ve sitoplazmaya trikarboksilat taşıyıcı proteini tarafından çıkarılır. Burada sitrat liyaz enzimi katalizörlüğünde Sitrat+ATP+Co. A reaksiyonuyla parçalanır. Asetil Co. A +ADP+Ps+Okzalasetat

Böylece, asetil Co. A ve okzalasetat mitokondriden sitoplazmaya bir ATP harcanmasıyla transfer edilir. Asetil Co. A transferi amacıyla sitoplazmaya gecen okzalasetatın mitokondriye geri dönmesi gerekmektedir. İç mitokondri membranı okzalasetata geçirgen değildir. Geçiş için bir seri reaksiyon gerekir.

Önce okzalasetat NADH ile malata indirgenir. Sitoplazmik malat dehidrogenaz tarafından sentezlenen bu reaksiyon şöyledir: Okzalasetat + NADH + H+ Malat + NAD+

Daha sonra önceden karşılaşmadığımız bir reaksiyon ve bir NADP+-bağlı malat enzimi(malik enzim de denir) vasıtasıyla malat, oksidatif dekarboksilasyonla piruvata dönüştürülür: Malat + NADP+ Piruvat+CO 2+ NADPH+H+

Burada oluşan piruvat mitokondriye geçer ve piruvat karboksilaz enzimi katalizörlüğünde tekrar okzalasetata çevrilir. Piruvat + C 02 + ATP + H 20 Okzalasetat + ADP + Pi + 2 H

Böylece mitokondriden sitoplazmaya geçen her bir asetil Co. A başına bir NADPH üretilmektedir. Palmitat sentezinde 8 Asetil Co. A kullanıldığına göre, 14 NADPH'ın 8'i bu mekanizma ile oluşturulmaktadır. Geride kalan 6 NADPH ise pentoz-fosfat yolundan sağlanmaktadır.

Şekil 11. 6. Asetil Co. A’ın mitokondriden sitoplazmaya taşınması.
- Slides: 70