XIII TYPY CHEMICKCH REAKC 1 Acidobazick reakce 2

XIII. TYPY CHEMICKÝCH REAKCÍ 1) Acidobazické reakce 2) Redox reakce vč. hoření (viz kap. XII) 3) Srážecí reakce 4) Tepelný rozklad (jen FBI) 5) Reakce oxidů 6) Tvorba plynu (pro jedničkáře a dvojkaře) Pozn. : V rovnicích dále nejsou uvedeny stechiometrické koeficienty.

1) ACIDOBAZICKÉ reakce – přenáší se H+ A) Neutralizace: kys. + zás. → sůl + H 2 O Př. : HCl + Na. OH → Na. Cl + H 2 O B) Hydrolýza solí je reakce soli s vodou za vzniku kyselého či zásaditého roztoku. Zjednodušeně: hydrolýza je opak neutralizace (neplatí pro sůl ze silné kyseliny a silné zásady) Př. : Na. Cl (vznikla z HCl a Na. OH, tj. z silné kyseliny a silné zásady) – proto nehydrolyzuje; podobně: K 2 SO 4 (vznikla z KOH a H 2 SO 4) – nehydrolyzuje Na. NO 3 (vznikla z HNO 3 a Na. OH) - nehydrolyzuje

Ale: K 2 CO 3, Fe. Cl 3, Al 2(SO 4)3, NH 4 Cl, Zn(NO 3)2 hydrolyzují Proč? H 2 CO 3 je slabá kyselina; Fe(OH)3, Al(OH)3, NH 4 OH, Zn(OH)2 = slabé zásady Př. : hydrolýza K 2 CO 3 : K 2 CO 3 vznikl z slabé kyseliny H 2 CO 3, tzn. hydrolyzuje K 2 CO 3 + H 2 O → KOH + H 2 CO 3 roztok bude zásaditý zjednodušeně: KOH je silná zásada, H 2 CO 3 je slabá kyselina; vliv KOH převáží vliv H 2 CO 3 a proto bude roztok zásaditý

Př. : hydrolýza Fe. Cl 3 sůl Fe. Cl 3 vznikla ze slabé zásady Fe(OH)3, tzn. hydrolyzuje Fe. Cl 3 + H 2 O → HCl + Fe(OH)3 roztok bude kyselý zjednodušeně: HCl je silná kyselina, Fe(OH)3 je slabá zásada; vliv HCl převáží vliv Fe(OH)3 a roztok bude kyselý C) Vytěsňování: a) slabé kyseliny z její soli silnější kyselinou Př. Fe. S(s) + H 2 SO 4 = H 2 S + Fe. SO 4 b) slabé zásady z její soli silnější zásadou Př. NH 4 Cl + Na. OH = NH 4 OH + Na. Cl

2) REDOX reakce – přenáší se elektrony Pozn. : Reakce na tomto listu jsou uvedeny v kap. XII, list 8 až 10. a) Reakce kovů s kyselinami : Tj. : kov obecný (příp. ušlechtilý) s kyselinou neoxidující příp. oxidující) b) HGF i FBI: Reakce obecného kovu s H 2 O (studenou) Jen FBI: Reakce obecného kovu s H 2 O (za horka) c) Jen HGF : Vytěsňování ušlechtilejšího kovu kovem méně ušlechtilým Zn + Cu. SO 4 → Cu + Zn. SO 4
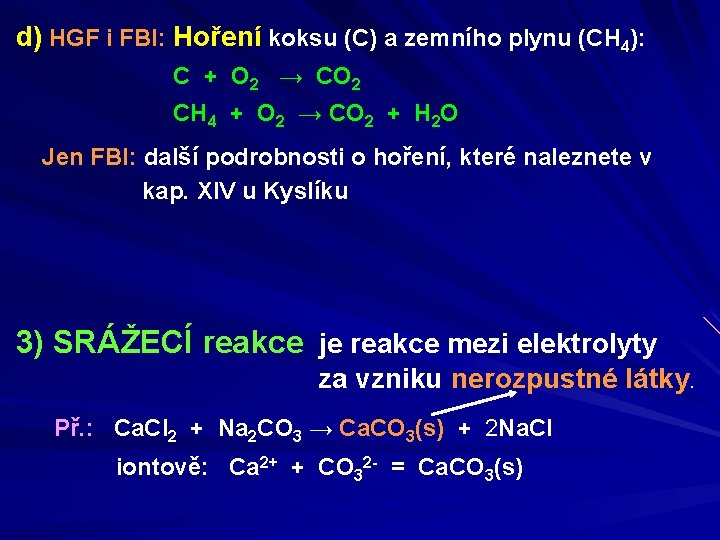
d) HGF i FBI: Hoření koksu (C) a zemního plynu (CH 4): C + O 2 → CO 2 CH 4 + O 2 → CO 2 + H 2 O Jen FBI: další podrobnosti o hoření, které naleznete v kap. XIV u Kyslíku 3) SRÁŽECÍ reakce je reakce mezi elektrolyty za vzniku nerozpustné látky. Př. : Ca. Cl 2 + Na 2 CO 3 → Ca. CO 3(s) + 2 Na. Cl iontově: Ca 2+ + CO 32 - = Ca. CO 3(s)

4) Jen FBI: TEPELNÝ rozklad (např. při požáru) Pozn. : co vzniká závisí též na T a) uhličitany se rozkládají za vzniku CO 2, např. : Ca. CO 3 → Ca. O + CO 2 T>900 o. C (NH 4)2 CO 3 → NH 3 + CO 2 + H 2 O Na. HCO 3 T >60 o. C → Na 2 CO 3 + CO 2 + H 2 O b) mnohé soli oxokyselin se rozloží za vzniku O 2, nebezpečné, zásobují požár kyslíkem Na. NO 3 → Na. NO 2 + O 2(g) NH 4 NO 3 → N 2 O(g) NH 4 NO 3 Na. NO 2 zahřát + H 2 O(g) T<250 o. C → N 2(g) + O 2(g) + H 2 O(g) T>250 o. C → Na 2 O + O 2(g) + NO(g) vysoké T

Ca(Cl. O)2 → KCl. O 3 → Na. Cl. O 4 → NH 4 Cl. O 4 → Ca. Cl 2 + O 2(g) KCl + O 2(g) Na. Cl + O 2(g) T>480 o. C Cl 2(g) + N 2(g) + O 2(g) + H 2 O(g) KMn. O 4 → K 2 Mn. O 4 + O 2(g) + Mn. O 2 K 2 Cr 2 O 7 → Cr 2 O 3 + O 2(g) + K 2 O c) peroxidy se rozloží také za vzniku O 2: H 2 O 2 Na 2 O 2 → H 2 O(g) + O 2(g) → Na 2 O + O 2(g) T>200 o. C

5) Reakce OXIDŮ: A) Zásadotvorné oxidy – jsou tvořeny s-prvky a d-prvky o nízkém oxid. čísle např. K 2 O, Ca. O, Mn. O Jejich reakcí: a) s vodou - vznikne hydroxid Ca. O + H 2 O → Ca(OH)2 b) s kyselinou – vznikne sůl a voda Mg. O + HNO 3 → Mg(NO 3)2 + H 2 O c) se zásadou - nereagují

B) Kyselinotvorné oxidy – jsou tvořeny nekovy a d-prvky o vysokém oxid. čísle např. CO 2, P 2 O 5, Mn 2 O 7 Jejich reakcí: a) s vodou – vznikne kyselina SO 2 + H 2 O → H 2 SO 3 b) se zásadou – vznikne sůl a voda CO 2 + Na. OH → Na 2 CO 3 + H 2 O c) s kyselinou - nereagují

C) Pozn. : pro jedničkáře a dvojkaře : Amfoterní oxidy – např. Sn. O 2, Sn. O, Al 2 O 3, Zn. O, Cr 2 O 3 a) s vodou nereagují (jsou nerozpustné) b) s kyselinami i zásadami dávají sůl D) Pozn. : pro jedničkáře a dvojkaře : Netečné oxidy – N 2 O, CO. Netvoří ani kyseliny ani zásady. E) Vzájemná reakce oxidů: kyselinotvorný oxid + zásadotvorný oxid = sůl SO 3 + Ca. O = Ca. SO 4

6) TVORBA PLYNU : Pozn. : pro jedničkáře a dvojkaře. Př. : Na. Cl(s) + H 2 SO 4(l) → HCl(g) + Na 2 SO 4(s) Ca. C 2(s) + H 2 O → C 2 H 2(g) + Ca(OH)2 Ca 3 P 2(s) + H 2 O → PH 3(g) + Ca(OH)2 Ca 3 P 2(s) + HCl → PH 3(g) + Ca. Cl 2
- Slides: 12