WYKAD 6 12 01 2019 BIAKA Biaka POLIPEPTYD

WYKŁAD 6 12. 01. 2019

BIAŁKA

Białka • POLIPEPTYD • Aminokwasy połączone wiązaniami amidowymi (peptydowymi) i disiarczkowymi • POLIPEPTYD + fragment niebiałkowy • • • Glikoproteiny Metaloproteiny Fosfoproteiny Lipoproteiny Nukleoproteiny
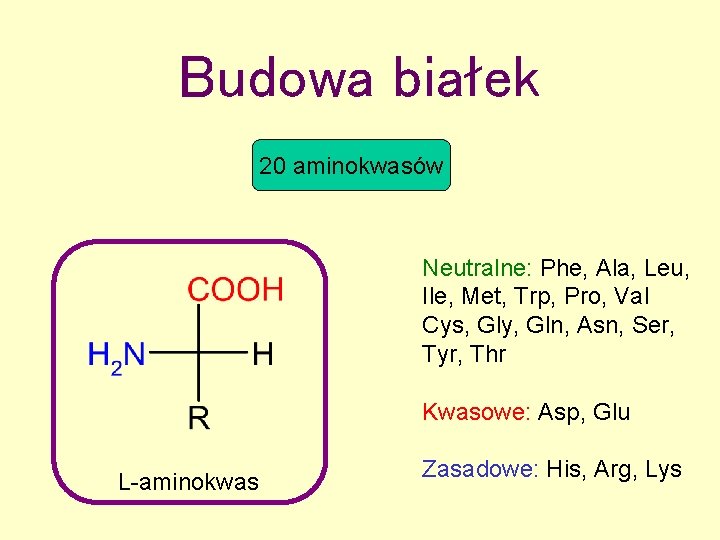
Budowa białek 20 aminokwasów Neutralne: Phe, Ala, Leu, Ile, Met, Trp, Pro, Val Cys, Gly, Gln, Asn, Ser, Tyr, Thr Kwasowe: Asp, Glu L-aminokwas Zasadowe: His, Arg, Lys
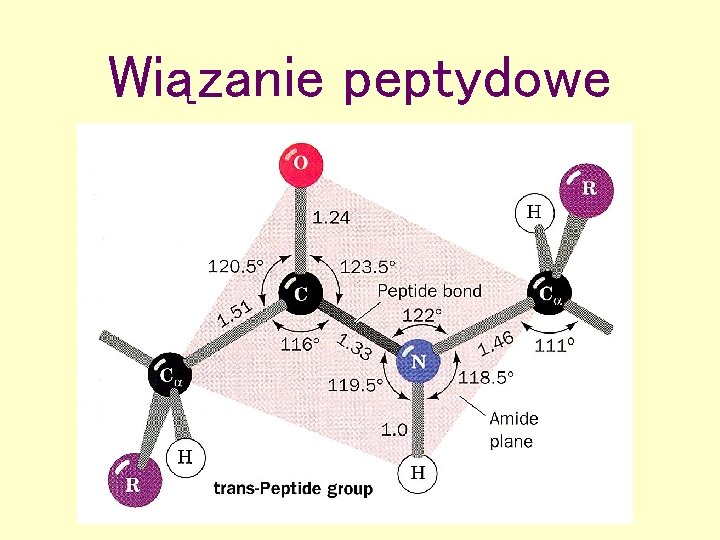
Wiązanie peptydowe
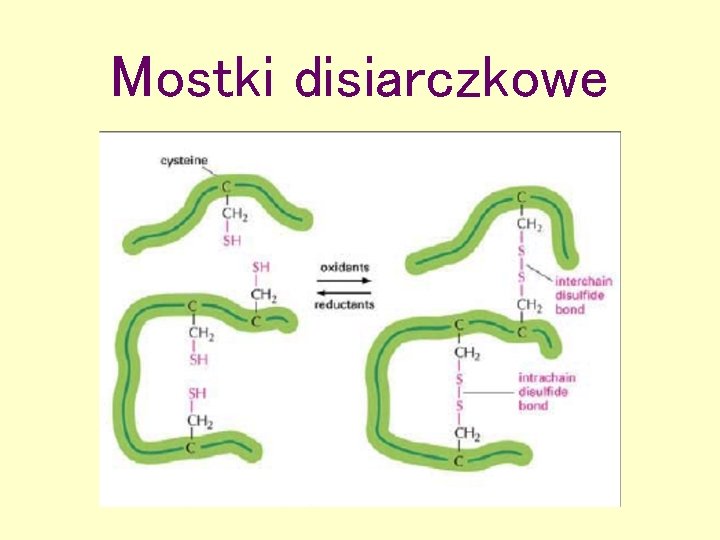
Mostki disiarczkowe
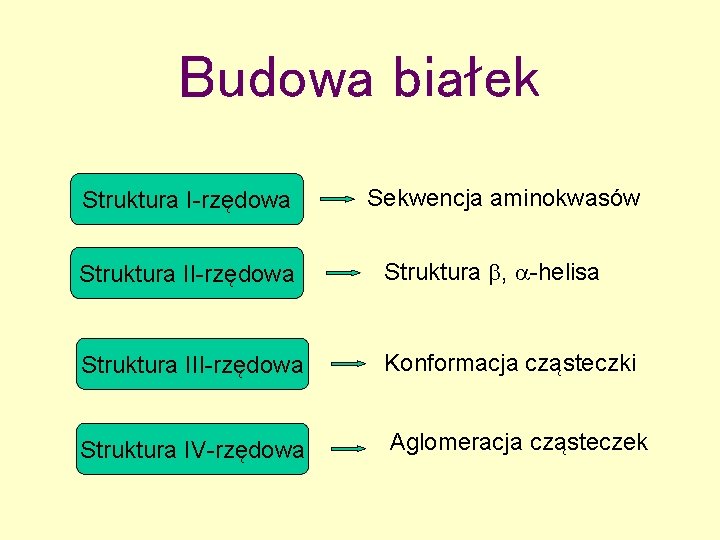
Budowa białek Struktura I-rzędowa Sekwencja aminokwasów Struktura II-rzędowa Struktura , -helisa Struktura III-rzędowa Konformacja cząsteczki Struktura IV-rzędowa Aglomeracja cząsteczek
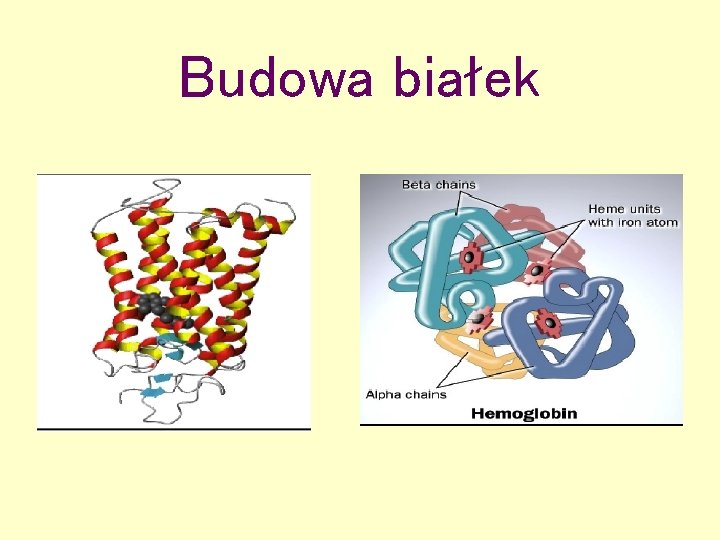
Budowa białek

Biologiczne funkcje białek • Enzymy • Białka transportujące • Hormony • Białka ochronne • Białka zapasowe • Białka kurczliwe • Białka budulcowe • Toksyny

Właściwości białek • GLOBULARNE (rozpuszczalne w H 2 O) • FIBRYLARNE (nierozpuszczalne w H 2 O) • Lizozym • Insulina • Mioglobina • Kolagen • Elastyna • Keratyna

Struktura białek Aminokwasy hydrofobowe – wewnątrz cząsteczki osłonięte przed kontaktem z wodą Aminokwasy hydrofilowe – na zewnątrz cząsteczki oraz w centrach katalitycznych enzymów Imidazol histydyny – donor lub akceptor protonu przy fizjologicznym p. H (centra katalityczne enzymów) Grupy – CH 2 OH i CH 2 SH (seryna, cysteina) działają jako nukleofile podczas katalizy enzymatycznej

Denaturacja białek Rozpad wiązań stabilizujących strukturę II i III-rzędową Czynniki powodujące denaturację: • Podwyższona temperatura (60 -70 C) • Niskie i wysokie p. H • Promieniowanie • Ultradźwięki • Detergenty • Rozpuszczalniki organiczne • Obecność jonów nieorganicznych

Skład aminokwasowy białek żywności Niezbędne Zawartość Wzorzec FAO Pozostałe Zawartość Ile 4 -5% 4% Arg 4 -6% Leu Lys Met 7 -9% 6 -9% 1 -3% 7% 5. 5% His Ala Asp+Asn 2 -3% 3 -6% 9 -12% Cys Phe Tyr 1 -2% 4 -5% 3 -4% Glu+Gln Gly Pro 17 -33% 2 -5% 4 -10% Thr Trp Val 4 -5% 1 -2% 4 -7% Ser 4 -8% } } 3. 5% 6. 0% 4% 1% 5%

Reakcje białek podczas przetwarzania i przechowywania żywności • Działanie podwyższonej temperatury • Ekstremalne p. H • Obecność utleniaczy • Obecność węglowodanów, lipidów

Obróbka termiczna i przemysłowe przetwarzanie powodują: Skutki korzystne: • Ograniczenie psucia się • Przedłużenie czasu przechowywania Efekty niekorzystne: • Obniżenie wartości odżywczej • Utrata właściwości funkcjonalnych • Powstawanie produktów toksycznych • Niekorzystne zmiany zapachu i smaku

Obróbka termiczna do 100 C: • Zmniejszenie rozpuszczalności białek globularnych • Struktura pierwszorzędowa nienaruszona • Inaktywacja enzymów • Destrukcja toksyn i czynników przeciwżywieniowych • Poprawa przyswajalności

Obróbka termiczna > 115 C: • Degradacja cysteiny i cystyny (powstaje H 2 S, (CH 3)2 S, kwas cysteinowy • Reakcje deamidacji Asn i Gln (powstaje NH 3, zmiana p. I, kowalencyjne sieciowanie) • W obecności tlenu – degradacja tryptofanu

Obróbka termiczna > 200 C oraz zasadowe środowisko: • Izomeryzacja (obniżenie przyswajalności i wartości odżywczej) • Powstawanie cyklicznych pochodnych o działaniu mutagennym • Degradacja w środowisku zasadowym (Arg, Cys, Ser, Thr, Lys)

Obróbka termiczna 200 -300 C • Sieciowanie – grupy aminowe Lys i Arg reagują z karboksylowymi Glu i Asp (obniżenie przyswajalności, zmiany wł. funkcjonalnych) • Powstawanie cyklicznych pochodnych o działaniu mutagennym, kancerogennym
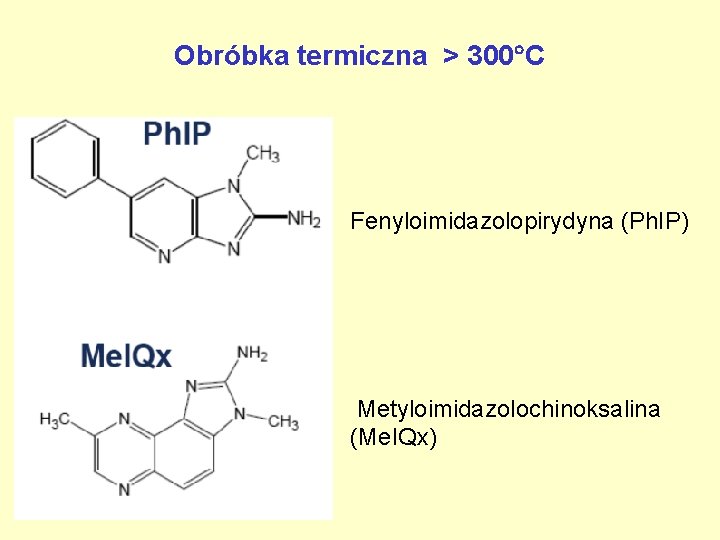
Obróbka termiczna > 300 C Fenyloimidazolopirydyna (Ph. IP) Metyloimidazolochinoksalina (Me. IQx)

Niebiałkowe związki azotowe

Małe cząsteczki zawierające azot • W surowcach Uczestniczą w reakcjach metabolicznych w komórkach. Po zbiorze ulegają przemianom katabolicznym, mikrobiologicznym • W produktach Powstają wskutek procesów technologicznych oraz podczas przechowywania
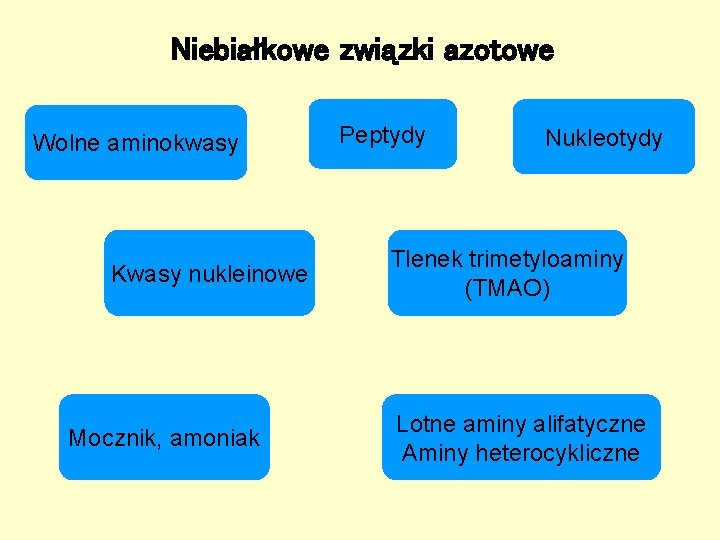
Niebiałkowe związki azotowe Wolne aminokwasy Kwasy nukleinowe Mocznik, amoniak Peptydy Nukleotydy Tlenek trimetyloaminy (TMAO) Lotne aminy alifatyczne Aminy heterocykliczne

Żywność bogata w niebiałkowe związki azotu • Mięso • Ryby i bezkręgowce morskie (15 -55% azotu w związkach niebiałkowych) • Warzywa (20 -65% azotu w związkach niebiałkowych)
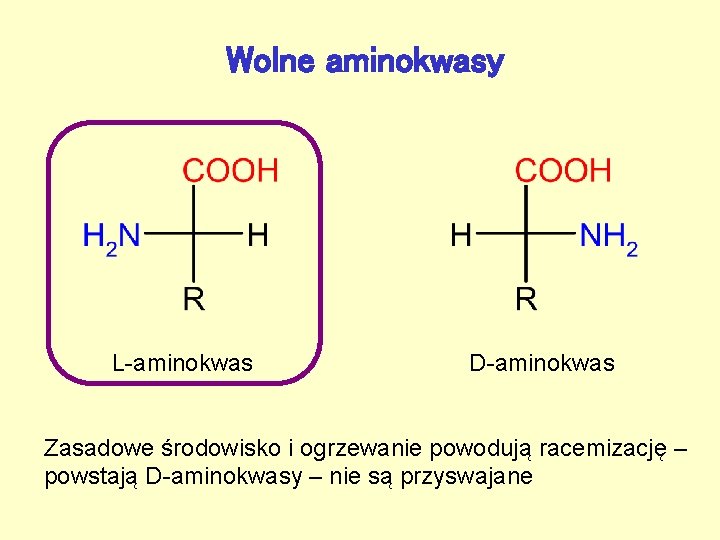
Wolne aminokwasy L-aminokwas D-aminokwas Zasadowe środowisko i ogrzewanie powodują racemizację – powstają D-aminokwasy – nie są przyswajane

Enancjomery aminokwasów mają różny smak: L (stęż. progowe mmol/L) Ala Asn His Gly Ile Leu Phe Ser Thr Trp Tyr słodki obojętny gorzki 12 -18 słodki 45 -50 słodki gorzki słodki gorzki D (stęż. progowe mmol/L) 10 -12 11 -13 5 -7 25 -35 35 -45 4 -6 kofeina sacharoza (roztwory wodne, p. H 6 -7) 25 -35 słodki słodki gorzka słodka 12 -18 3 -6 2 -4 1 -1. 2 mmol/L 10 -12 mmol/L 8 -12 2 -5 1 -3 30 -40 40 -50 0. 2 -0. 4 1 -3
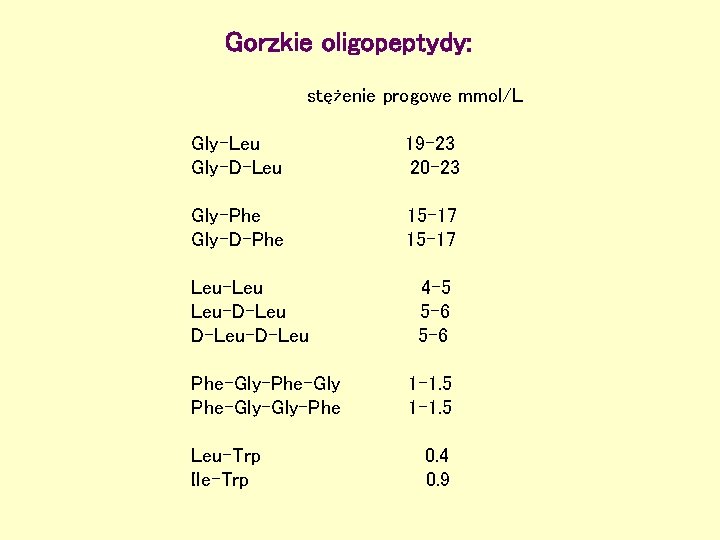
Gorzkie oligopeptydy: stężenie progowe mmol/L Gly-Leu Gly-D-Leu 19 -23 20 -23 Gly-Phe Gly-D-Phe 15 -17 Leu-Leu Leu-D-Leu-D-Leu Phe-Gly-Phe-Gly-Phe Leu-Trp Ile-Trp 4 -5 5 -6 1 -1. 5 0. 4 0. 9
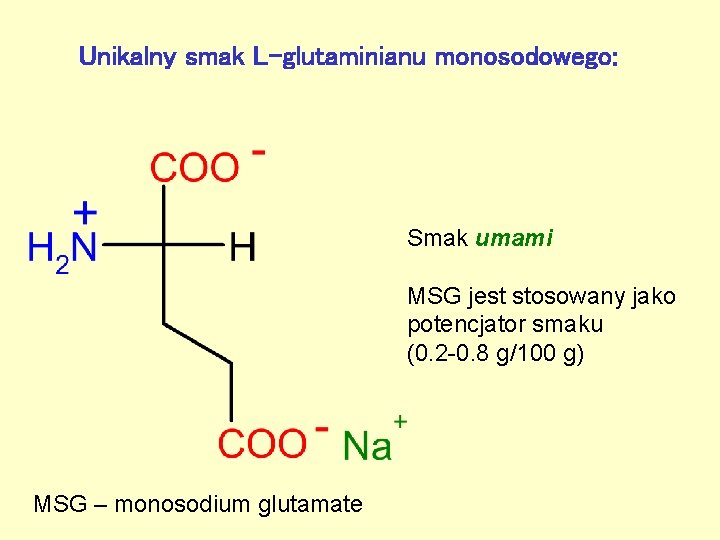
Unikalny smak L-glutaminianu monosodowego: Smak umami MSG jest stosowany jako potencjator smaku (0. 2 -0. 8 g/100 g) MSG – monosodium glutamate

Wolne aminokwasy białkowe w żywności: Sery, pomidory – monoglutaminian sodu Mięso, ryby – histydyna, glicyna, alanina, lizyna Skorupiaki – glicyna, arginina, prolina, alanina, seryna Ziemniaki – kwas asparaginowy, glutaminowy, walina Miód - prolina
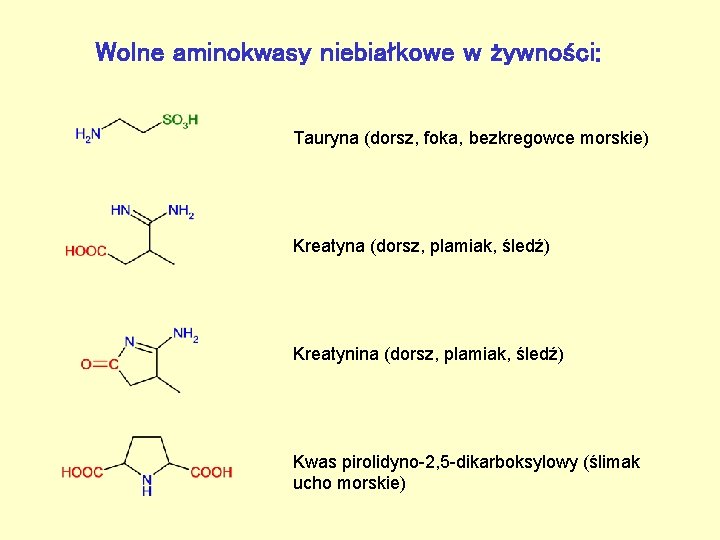
Wolne aminokwasy niebiałkowe w żywności: Tauryna (dorsz, foka, bezkregowce morskie) Kreatyna (dorsz, plamiak, śledź) Kreatynina (dorsz, plamiak, śledź) Kwas pirolidyno-2, 5 -dikarboksylowy (ślimak ucho morskie)
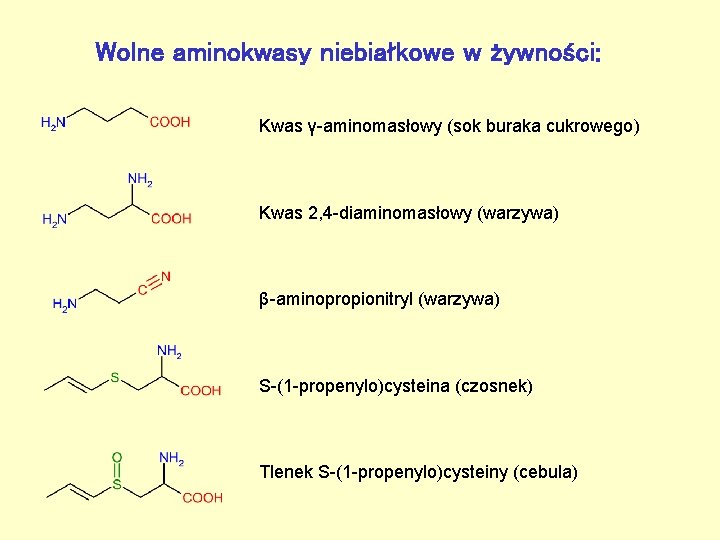
Wolne aminokwasy niebiałkowe w żywności: Kwas γ-aminomasłowy (sok buraka cukrowego) Kwas 2, 4 -diaminomasłowy (warzywa) β-aminopropionitryl (warzywa) S-(1 -propenylo)cysteina (czosnek) Tlenek S-(1 -propenylo)cysteiny (cebula)
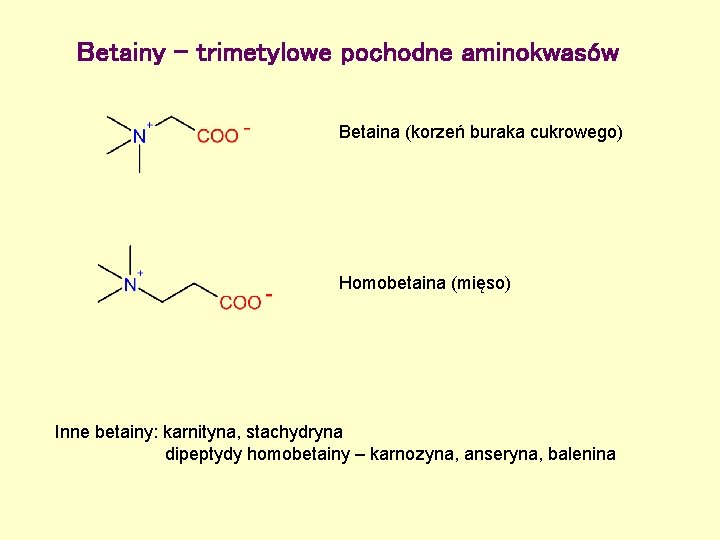
Betainy – trimetylowe pochodne aminokwasów Betaina (korzeń buraka cukrowego) Homobetaina (mięso) Inne betainy: karnityna, stachydryna dipeptydy homobetainy – karnozyna, anseryna, balenina
Produkty degradacji aminokwasów Siarkowodór Ketokwasy Amoniak Aminy alifatyczne Aminy aromatyczne Tiole Kwasy karboksylowe Aldehydy Zw. heterocykliczne
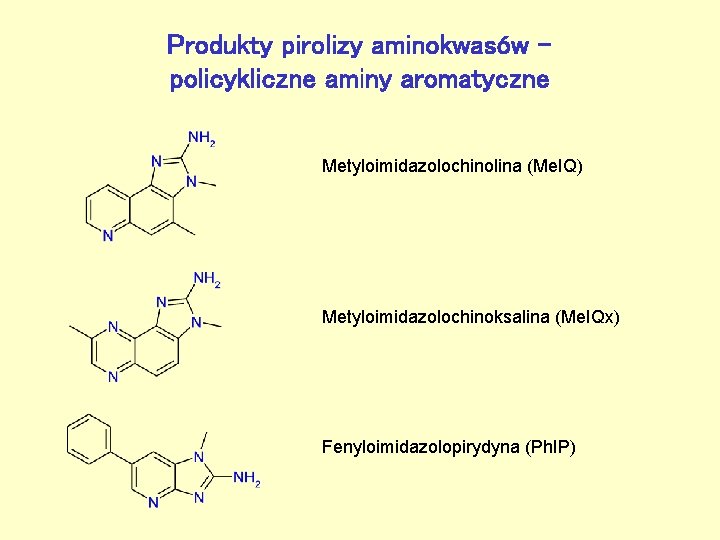
Produkty pirolizy aminokwasów – policykliczne aminy aromatyczne Metyloimidazolochinolina (Me. IQ) Metyloimidazolochinoksalina (Me. IQx) Fenyloimidazolopirydyna (Ph. IP)
- Slides: 34