Wykad 3 Empiryczne pola siowe czyli co robi

Wykład 3 Empiryczne pola siłowe, czyli co robić gdy chemia kwantowa jest za droga
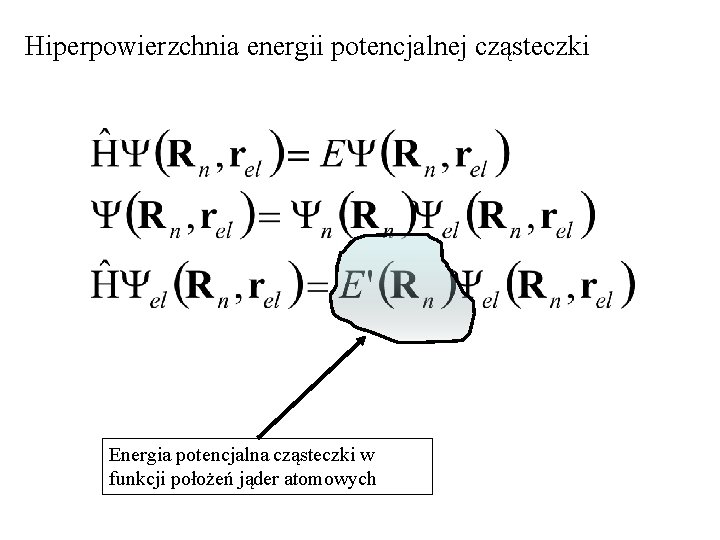
Hiperpowierzchnia energii potencjalnej cząsteczki Energia potencjalna cząsteczki w funkcji położeń jąder atomowych

Charakterystyka metod chemii kwantowej Zalety: Ø Możliwość badania zarówno reakcji chemicznych jak i przemian konformacyjnych Ø Uniwersalność Ø Wysoka wiarygodność wyników Wady: Ø Energia jest niejawną funkcją współrzędnych Ø Wysoki lub bardzo wysoki koszt obliczeń

Empiryczne pola siłowe: przybliżone analityczne wyrażenia na energię potencjalną cząsteczki (cząsteczek) poprzez wielkości geometryczne wraz z odpowiednimi parametrami. Cząsteczka jest traktowana jako układ kulek połączonych sprężynkami.

Charakterystyka empirycznych pól siłowych Zalety: Ø Energia jest jawną funkcją współrzędnych Ø Niski koszt obliczania energii Wady: Ø Umożliwiają badanie jedynie przemian konformacyjnych Ø Mogą być stosowane tylko w klasie związków na które je sparametryzowano (nieprzenaszalność) Ø Niska wiarygodność obliczonych energii

Zastosowania empirycznych pól siłowych: Ø Mechanika molekularna (znajdowanie stabilnych konformacji) Ø Dynamika molekularna (badanie ewolucji czasowej cząsteczki lub układu cząsteczek)

Wybór zmiennych Ø Współrzędne kartezjańskie • pola MM Allingera (węglowodory, alkohole, estry) • AMBER (biomolekuły) • CHARMM (biomolekuły) • CFF (biomolekuły) • XPLOR (udokładnianie struktur krystalograficznych) Ø Kąty dwuścienne • ECEPP (peptydy i białka)

Wyrażenie na energię konformacyjną w empirycznych polach siłowych
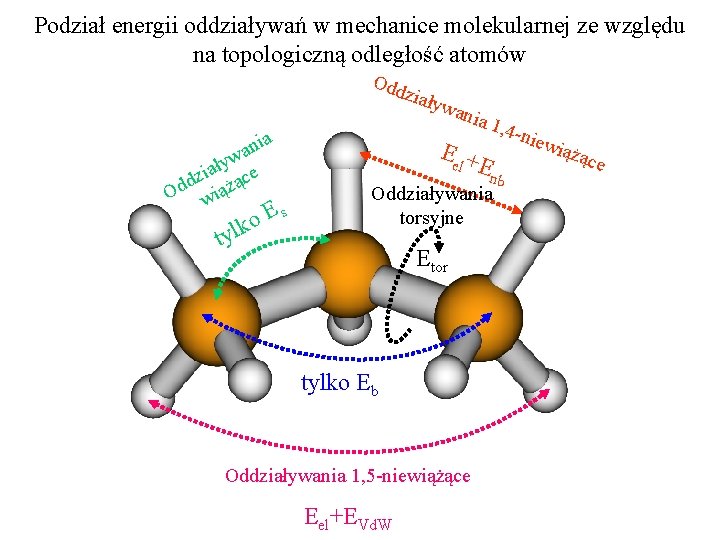
Podział energii oddziaływań w mechanice molekularnej ze względu na topologiczną odległość atomów Odd ziały a ni a ływ e a i dz ążąc d O wi Es o lk ty wan ia Ee + l 1, 4 niew En Oddziaływania torsyjne Etor tylko Eb Oddziaływania 1, 5 -niewiążące Eel+EVd. W iążą b ce
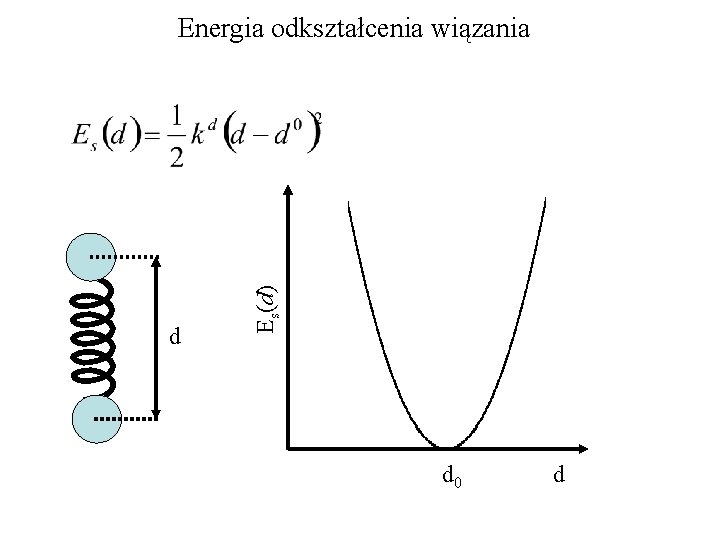
d Es(d) Energia odkształcenia wiązania d 0 d
![Typowe wartości stałych d 0 i kd Wiązanie d 0 [A] kd [kcal/(mol A Typowe wartości stałych d 0 i kd Wiązanie d 0 [A] kd [kcal/(mol A](http://slidetodoc.com/presentation_image_h2/875e67b4ac73159b4c82284ae4243f94/image-11.jpg)
Typowe wartości stałych d 0 i kd Wiązanie d 0 [A] kd [kcal/(mol A 2)] Csp 3 -Csp 3 1. 523 317 Csp 3 -Csp 2 1. 497 317 Csp 2=Csp 2 1. 337 690 Csp 2=O 1. 208 777 Csp 2 -Nsp 3 1. 438 367 C-N (amid) 1. 345 719
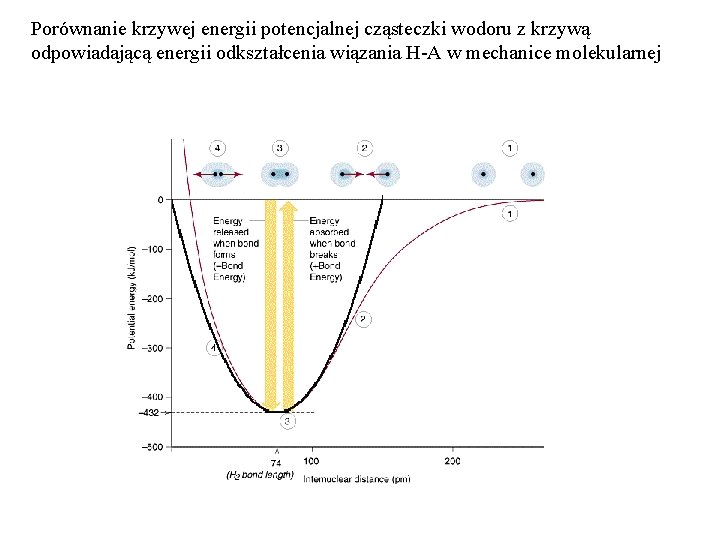
Porównanie krzywej energii potencjalnej cząsteczki wodoru z krzywą odpowiadającą energii odkształcenia wiązania H-A w mechanice molekularnej
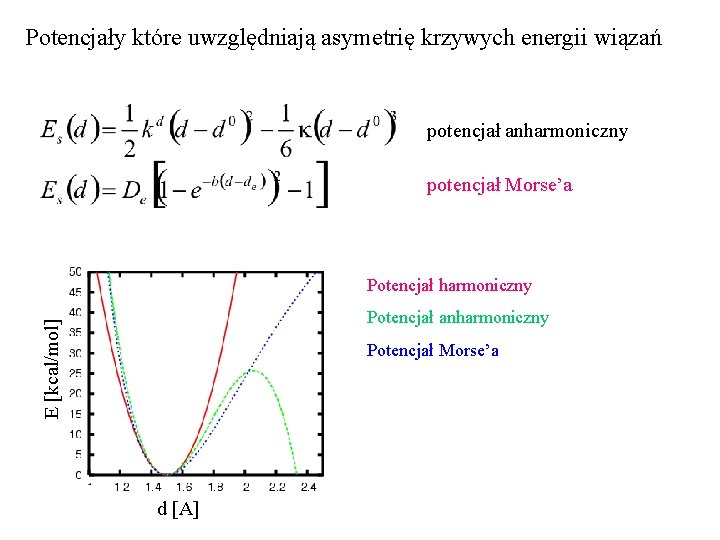
Potencjały które uwzględniają asymetrię krzywych energii wiązań potencjał anharmoniczny potencjał Morse’a Potencjał harmoniczny E [kcal/mol] Potencjał anharmoniczny Potencjał Morse’a d [A]
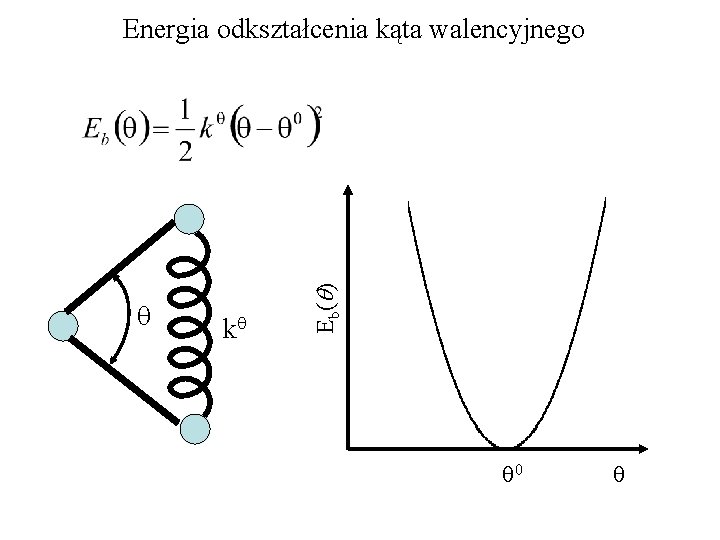
q kq E b( q ) Energia odkształcenia kąta walencyjnego q 0 q
![Typowe wartości stałych q 0 i kq q 0 [stopnie] Csp 3 -Csp 3 Typowe wartości stałych q 0 i kq q 0 [stopnie] Csp 3 -Csp 3](http://slidetodoc.com/presentation_image_h2/875e67b4ac73159b4c82284ae4243f94/image-15.jpg)
Typowe wartości stałych q 0 i kq q 0 [stopnie] Csp 3 -Csp 3 109. 47 kq [kcal/(mol stopień2)] 0. 0099 Csp 3 -H 109. 47 0. 0079 H-Csp 3 -H 109. 47 0. 0070 Kąt Csp 3 -Csp 2 -Csp 3 117. 2 0. 0099 Csp 3 -Csp 2=Csp 2 121. 4 0. 0121 Csp 3 -Csp 2=O 0. 0101 122. 5
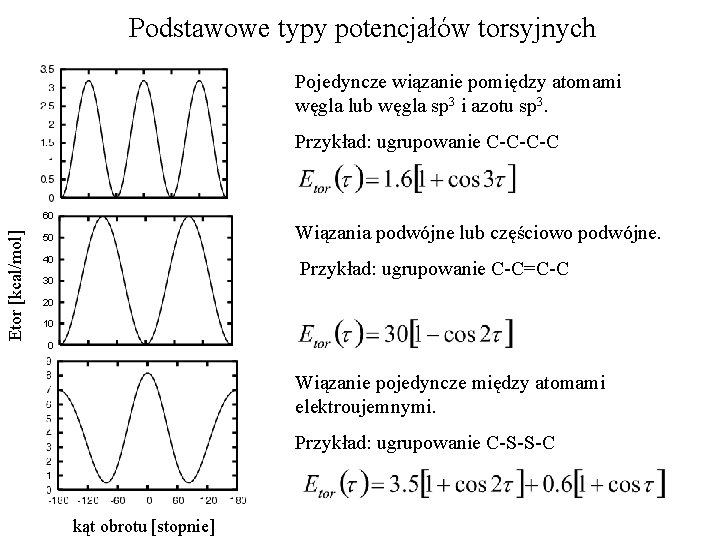
Podstawowe typy potencjałów torsyjnych Pojedyncze wiązanie pomiędzy atomami węgla lub węgla sp 3 i azotu sp 3. Przykład: ugrupowanie C-C-C-C Etor [kcal/mol] 60 Wiązania podwójne lub częściowo podwójne. 50 40 Przykład: ugrupowanie C-C=C-C 30 20 10 0 Wiązanie pojedyncze między atomami elektroujemnymi. Przykład: ugrupowanie C-S-S-C kąt obrotu [stopnie]
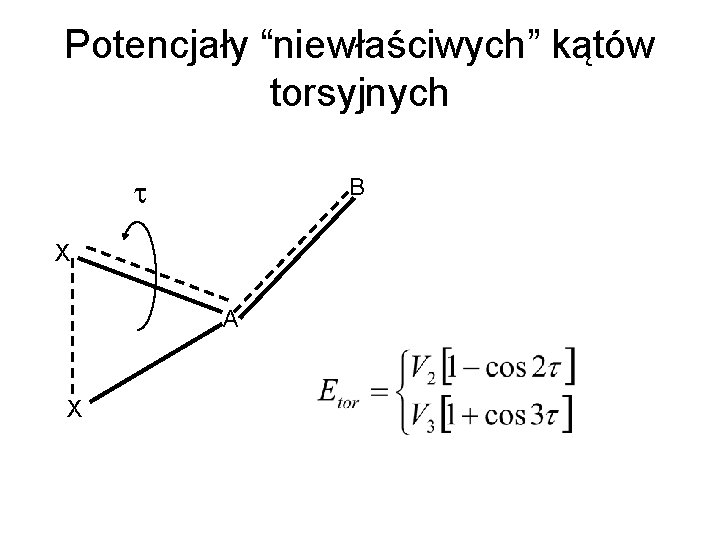
Potencjały “niewłaściwych” kątów torsyjnych t B X A X
![Enb [kcal/mol] Potencjał niewiążący Lennarda-Jonesa (6 -12) -e s r 0 r [A] Enb [kcal/mol] Potencjał niewiążący Lennarda-Jonesa (6 -12) -e s r 0 r [A]](http://slidetodoc.com/presentation_image_h2/875e67b4ac73159b4c82284ae4243f94/image-18.jpg)
Enb [kcal/mol] Potencjał niewiążący Lennarda-Jonesa (6 -12) -e s r 0 r [A]
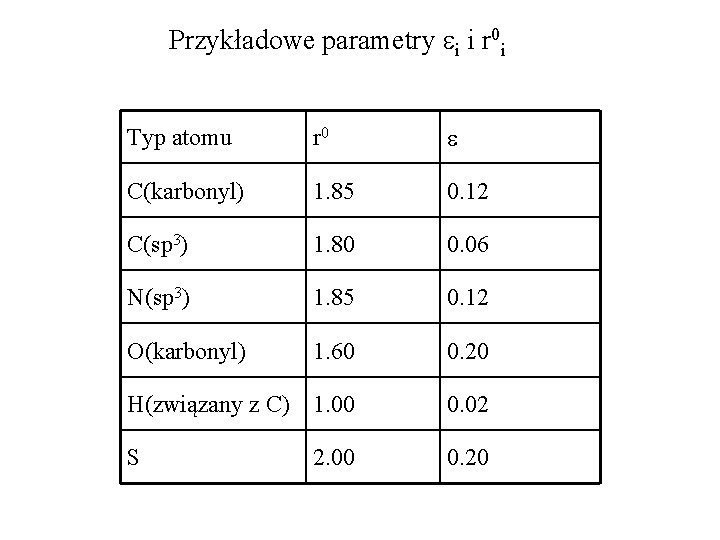
Przykładowe parametry ei i r 0 i Typ atomu r 0 e C(karbonyl) 1. 85 0. 12 C(sp 3) 1. 80 0. 06 N(sp 3) 1. 85 0. 12 O(karbonyl) 1. 60 0. 20 H(związany z C) 1. 00 0. 02 S 0. 20 2. 00

Inne potencjały niewiążące Potencjał Buckinghama Potencjał 10 -12 używany w niektórych polach siłowych do opisu wiązań wodorowych
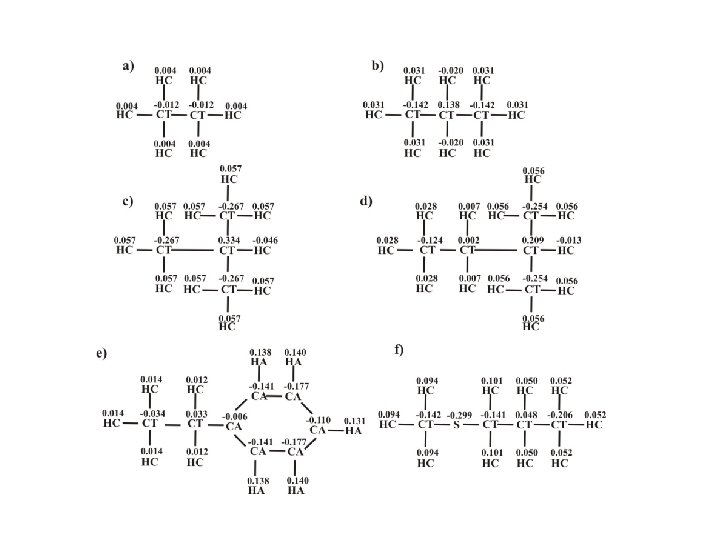
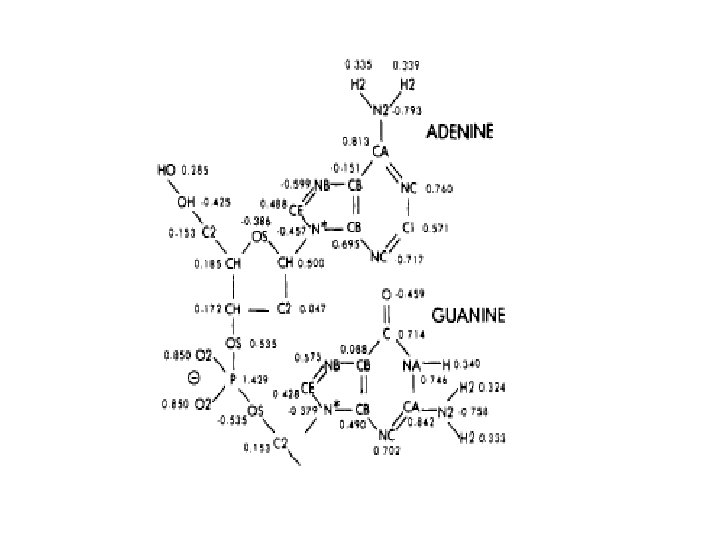
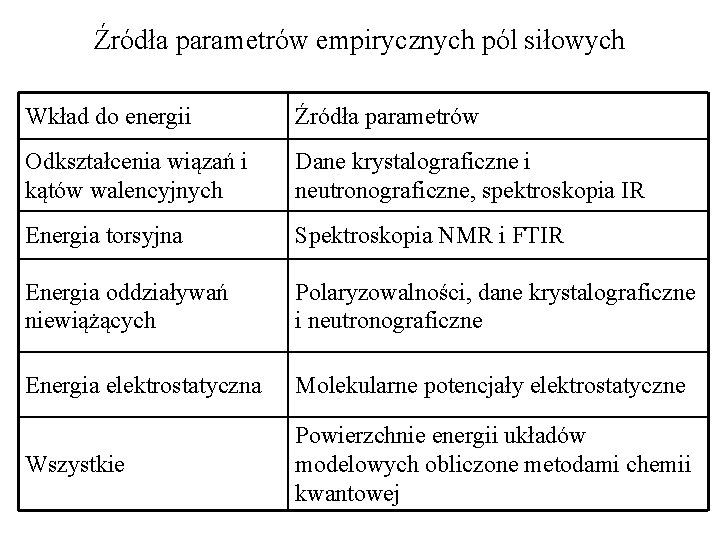
Źródła parametrów empirycznych pól siłowych Wkład do energii Źródła parametrów Odkształcenia wiązań i kątów walencyjnych Dane krystalograficzne i neutronograficzne, spektroskopia IR Energia torsyjna Spektroskopia NMR i FTIR Energia oddziaływań niewiążących Polaryzowalności, dane krystalograficzne i neutronograficzne Energia elektrostatyczna Molekularne potencjały elektrostatyczne Wszystkie Powierzchnie energii układów modelowych obliczone metodami chemii kwantowej
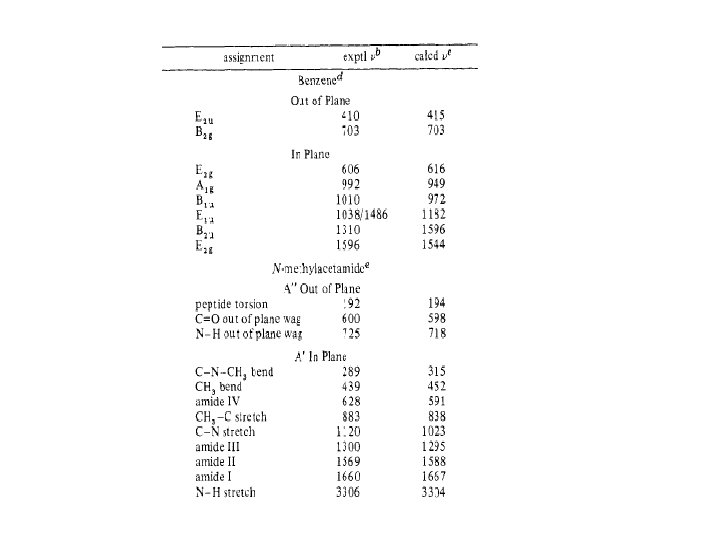

Uwzględnienie rozpuszczalnika Ø Modele dyskretne wody • TIP 3 P • TIP 4 P • TIP 5 P • SPC Ø Modele ciągłe wody • modele powierzchni dostępnej dla rozpuszczalnika • modele powierzchni molekularnej • uogólniony model Borna • model PCM).
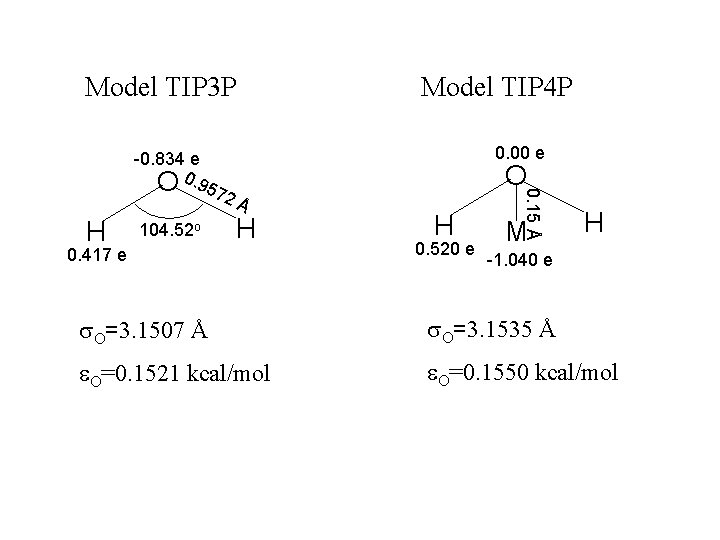
Model TIP 3 P Model TIP 4 P 0. 00 e O 57 H 104. 52 o 2Å H 0. 417 e H 0. 520 e 0. 15 Å -0. 834 e O 0. 9 M H -1. 040 e s. O=3. 1507 Å s. O=3. 1535 Å e. O=0. 1521 kcal/mol e. O=0. 1550 kcal/mol
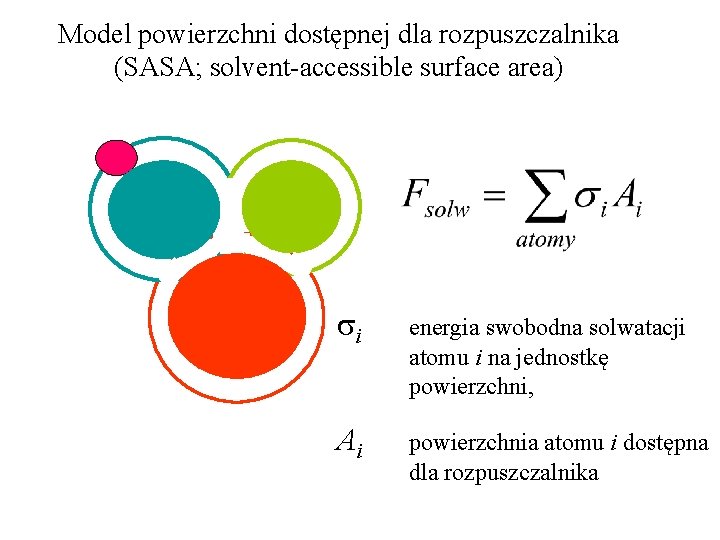
Model powierzchni dostępnej dla rozpuszczalnika (SASA; solvent-accessible surface area) si energia swobodna solwatacji atomu i na jednostkę powierzchni, Ai powierzchnia atomu i dostępna dla rozpuszczalnika
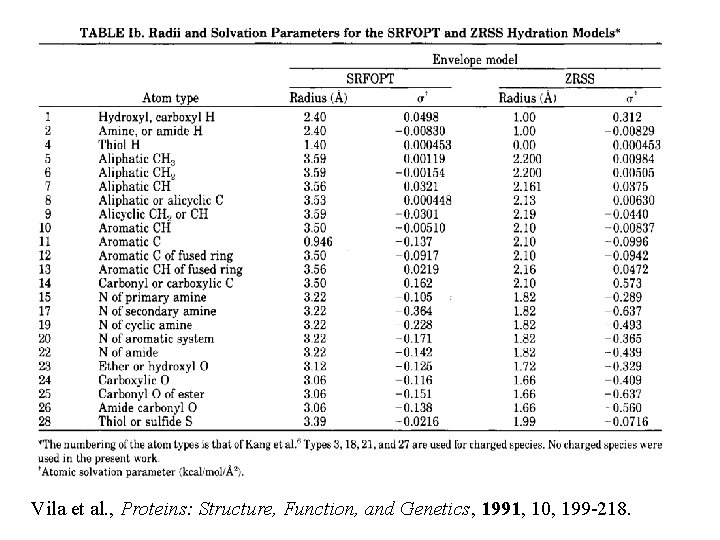
Vila et al. , Proteins: Structure, Function, and Genetics, 1991, 10, 199 -218.
![Porównanie konformacji [Met 5]enkefaliny uzyskanej przy pomocy pola siłowego ECEPP/3 w próżni i w Porównanie konformacji [Met 5]enkefaliny uzyskanej przy pomocy pola siłowego ECEPP/3 w próżni i w](http://slidetodoc.com/presentation_image_h2/875e67b4ac73159b4c82284ae4243f94/image-29.jpg)
Porównanie konformacji [Met 5]enkefaliny uzyskanej przy pomocy pola siłowego ECEPP/3 w próżni i w wodzie Próżnia Woda (model SRFOPT)
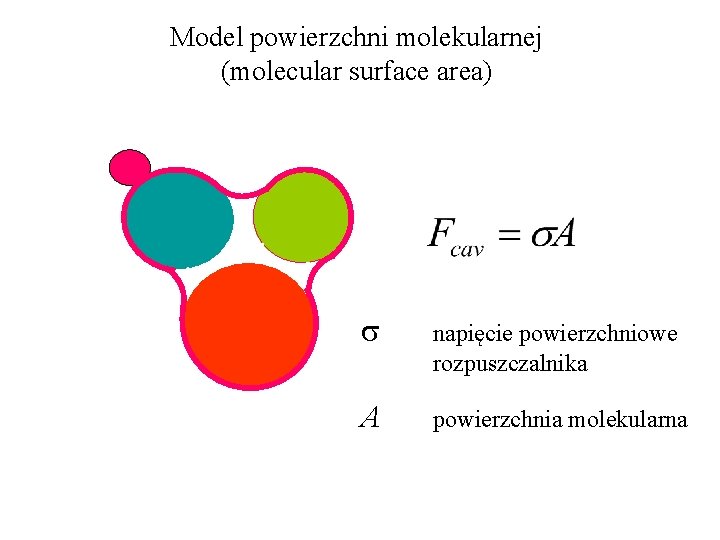
Model powierzchni molekularnej (molecular surface area) s napięcie powierzchniowe rozpuszczalnika A powierzchnia molekularna

Uogólniony model Borna i powierzchni molekularnej (GBSA; Generalized Born Surface Area model)
- Slides: 31