Wykad 15 9 8 Najprostsze obwody elektryczne A

Wykład 15 9. 8 Najprostsze obwody elektryczne A. Dzielnik napięcia. B. Mostek Wheatstone’a C. Kompensacyjna metoda pomiaru siły elektromotorycznej D. Prosty układ RC 10. Prąd elektryczny w cieczach 10. 1 Dysocjacja elektrolityczna 10. 2 Prawa elektrolizy Faraday’a 10. 3 Teoria przewodnictwa elektrolitycznego Reinhard Kulessa 1
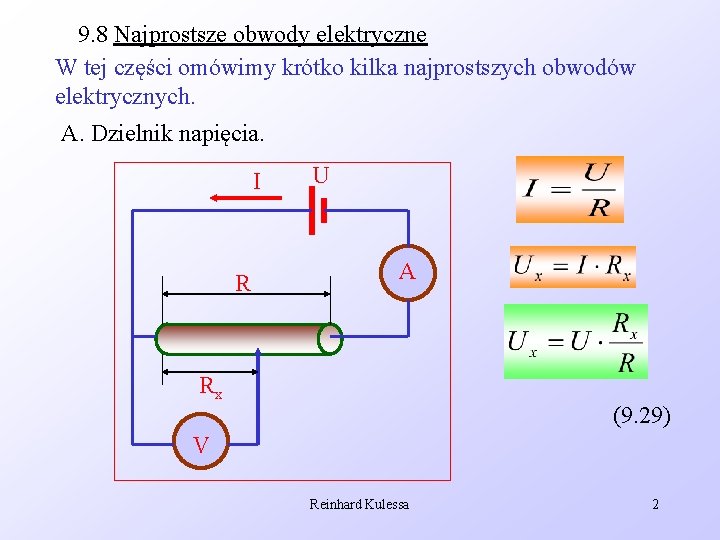
9. 8 Najprostsze obwody elektryczne W tej części omówimy krótko kilka najprostszych obwodów elektrycznych. A. Dzielnik napięcia. I R U A Rx (9. 29) V Reinhard Kulessa 2
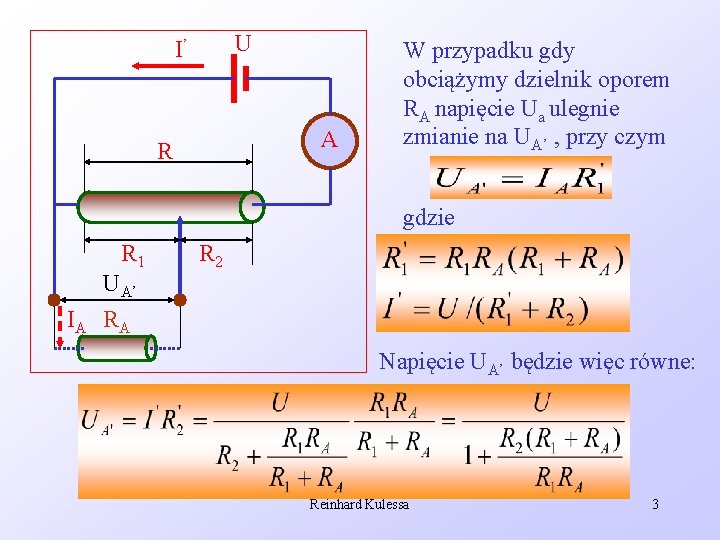
U I’ A R W przypadku gdy obciążymy dzielnik oporem RA napięcie Ua ulegnie zmianie na UA’ , przy czym gdzie R 1 IA UA’ RA R 2 Napięcie UA’ będzie więc równe: Reinhard Kulessa 3
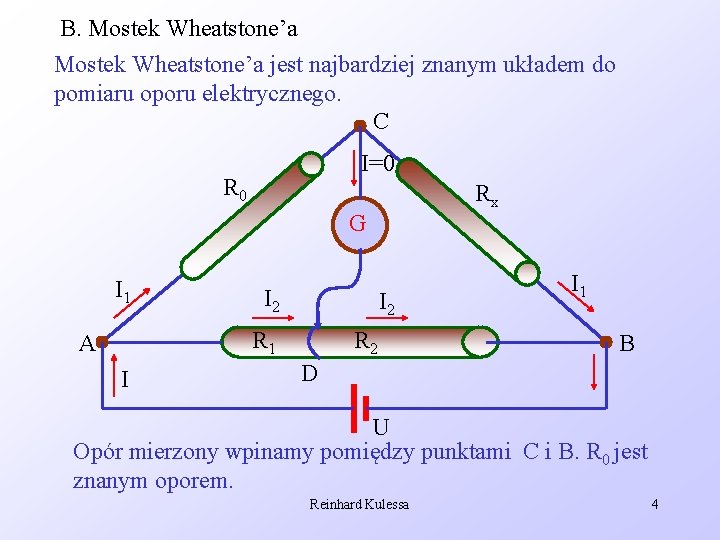
B. Mostek Wheatstone’a jest najbardziej znanym układem do pomiaru oporu elektrycznego. C I=0 R 0 Rx G I 1 I 2 R 1 A I R 2 I 1 B D U Opór mierzony wpinamy pomiędzy punktami C i B. R 0 jest znanym oporem. Reinhard Kulessa 4

Suwak na oporze AB przesuwamy tak długo, aż w gałęzi CD nie popłynie prąd. Oznacza to równość potencjałów w punktach C i D. Rozważając oczko ACD otrzymujemy; . Z kolei rozważając oczko CBD otrzymujemy; . Dzieląc drugą linijkę tych równań przez siebie, otrzymujemy; (9. 29) Reinhard Kulessa 5
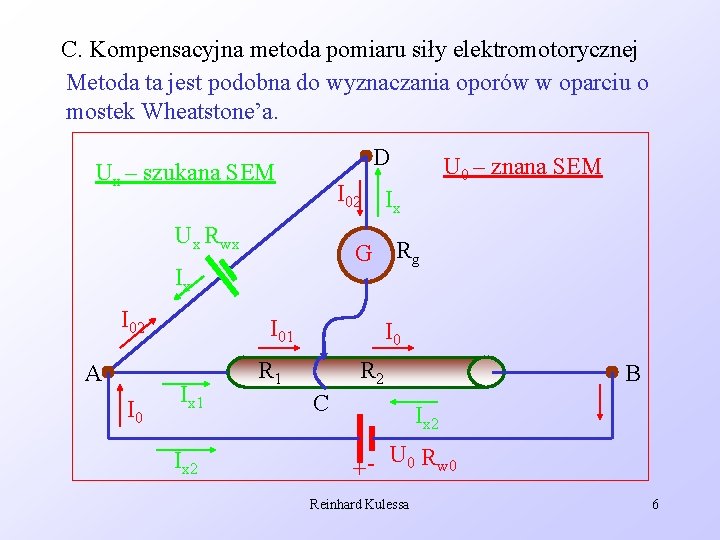
C. Kompensacyjna metoda pomiaru siły elektromotorycznej Metoda ta jest podobna do wyznaczania oporów w oparciu o mostek Wheatstone’a. D Ux – szukana SEM I 02 Ux Rwx A I 01 Ix 2 Ix G Rg Ix I 02 U 0 – znana SEM I 0 R 1 R 2 C B Ix 2 U 0 Rw 0 + Reinhard Kulessa 6

Zmieniamy ustawienie suwaka na oporze AB tak długo, aż w galwanometrze przestanie płynąć prąd. Wtedy wiemy, że; Prąd w każdej gałęzi jest algebraiczną sumą prądów pochodzących od każdej siły elektromotorycznej oddzielnie, przy czym muszą zostać uwzględnione opory wewnętrzne wszystkich ogniw. Musimy również uwzględnić opór galwanometru. Dla prądów związanych z szukaną siłą elektromotoryczną otrzymamy w oparciu o Prawa Kirchoffa; . Reinhard Kulessa 7

Dla prądów wywołanych przez siłę elektromotoryczną U 0 otrzymamy; . Z układu podanych równań można znaleźć Ix 1 i Ix 2 w funkcji oporów i Ux , oraz I 01 i I 02 w funkcji tych samych oporów i U 0. Z warunku znikania prądu w galwanometrze otrzymujemy, . (9. 30) Gdy Rw 0 << R=R 1+R 2, metoda ta jest dokładna. Reinhard Kulessa 8
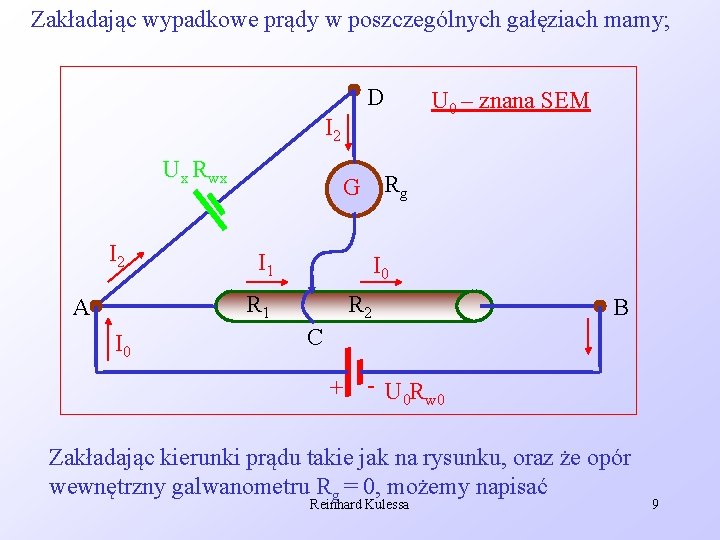
Zakładając wypadkowe prądy w poszczególnych gałęziach mamy; D I 2 Ux Rwx I 2 G Rg I 1 I 0 R 1 A I 0 U 0 – znana SEM R 2 B C + - U 0 Rw 0 Zakładając kierunki prądu takie jak na rysunku, oraz że opór wewnętrzny galwanometru Rg = 0, możemy napisać Reinhard Kulessa 9

Ustawiając suwak w punkcie D tak, aby przez galwanometr nie płynął prąd, czyli I 2 = 0, mamy Reinhard Kulessa 10
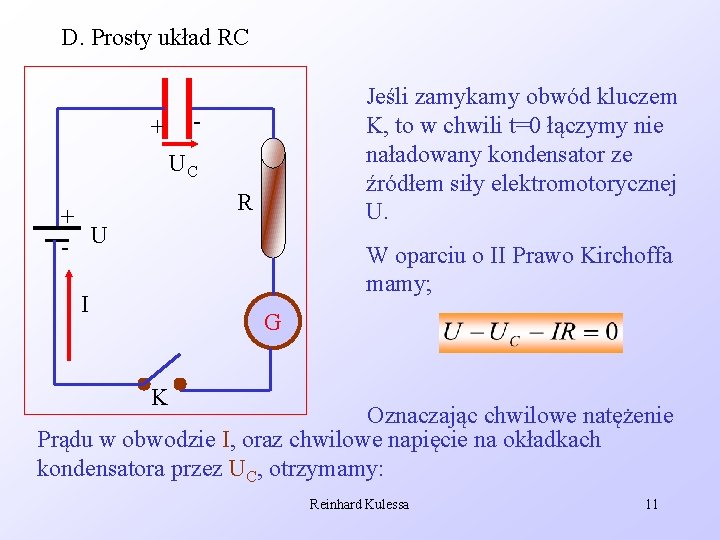
D. Prosty układ RC + Jeśli zamykamy obwód kluczem K, to w chwili t=0 łączymy nie naładowany kondensator ze źródłem siły elektromotorycznej U. UC R + - U W oparciu o II Prawo Kirchoffa mamy; I G K Oznaczając chwilowe natężenie Prądu w obwodzie I, oraz chwilowe napięcie na okładkach kondensatora przez UC, otrzymamy: Reinhard Kulessa 11

Po podstawieniu do poprzedniego równania otrzymamy: Po przekształceniu i podzieleniu przez R otrzymamy: Rozwiązanie tego równania ma postać: Reinhard Kulessa 12

Ponieważ : , napięcie na kondensatorze, będzie się więc zmieniało zgodnie z równaniem: . (9. 31) Iloczyn RC ma wymiar czasu i jest nazwany czasem relaksacji. Wstawiając wyrażenie na czasową zależność napięcia na kondensatorze do naszego wyjściowego równania, otrzymamy wzór na czasową zależność natężenia prądu ładującego kondensator. Reinhard Kulessa 13
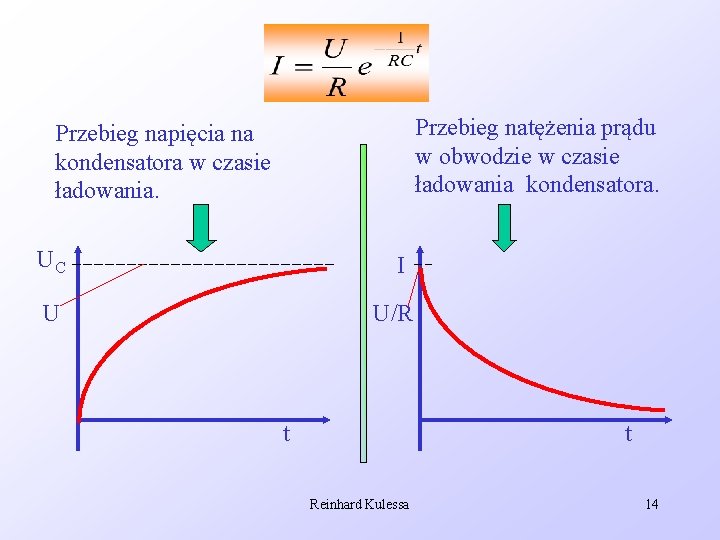
Przebieg natężenia prądu w obwodzie w czasie ładowania kondensatora. Przebieg napięcia na kondensatora w czasie ładowania. UC I U U/R t t Reinhard Kulessa 14

10. Prąd elektryczny w cieczach 10. 1 Dysocjacja elektrolityczna Powszechnie znany jest fakt, że wiele czystych cieczy źle przewodzi prąd elektryczny. Do wody destylowanej np. . wystarczy dodać roztworu Na. Cl czy H 2 SO 4 , aby stała się ona dobrym przewodnikiem. Jeśli w takim roztworze umieścimy elektrody, to będą się na nich wydzielały składniki roztworów. Takie przewodniki nazywamy elektrolitami. Przepływ prądu w elektrolicie polega na poruszaniu się jonów pod wpływem przyłożonego pola elektrycznego. Rozpad związków chemicznych na cząsteczki składowe pod wpływem rozpuszczalnika nazywamy dysocjacją elektrolityczną. Reinhard Kulessa 15

Najbardziej znane są elektrolity następujących soli: Ilościowo rozpad cząsteczek na jony określa współczynnik dysocjacji elektrolitycznej . Należy pamiętać, że w roztworze cząsteczki nie tylko ulegają dysocjacji, lecz również rekombinacji, tak, że zwykle dochodzi do stanu równowagi. Jeżeli w jednostce objętości roztworu znajduje się n 0 cząsteczek, a n 1 z nich jest zdysocjowanych na jony, to (10. 1) gdzie jest współczynnikiem dysocjacji. Reinhard Kulessa 16
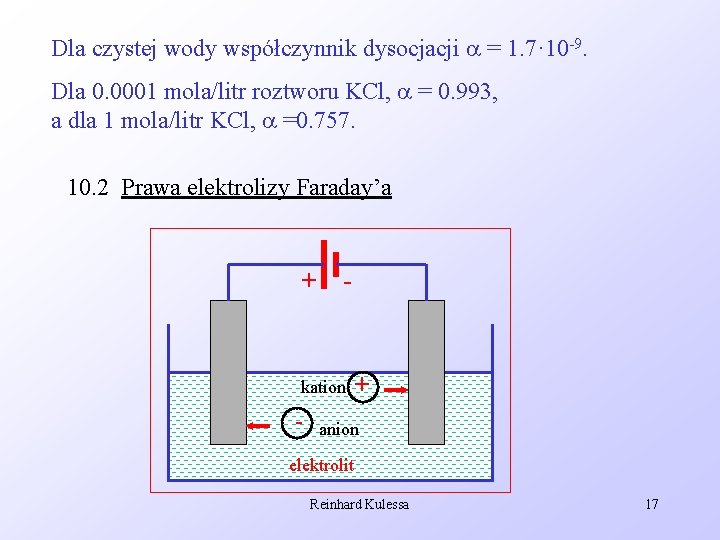
Dla czystej wody współczynnik dysocjacji = 1. 7· 10 -9. Dla 0. 0001 mola/litr roztworu KCl, = 0. 993, a dla 1 mola/litr KCl, =0. 757. 10. 2 Prawa elektrolizy Faraday’a + - kation - + anion elektrolit Reinhard Kulessa 17

I Prawo Faraday’a mówi, że masa wydzielającej się substancji m jest proporcjonalna do przepływającego przez elektrolit ładunku Q. (10. 2) Stała k jest równoważnikiem elektrochemicznym, równym liczbowo masie wydzielonej przy przepływie przez elektrolit ładunku 1 kulomba w czasie 1 sek. Stała ta ma wymiar [kg/As]. II Prawo Faraday’a mówi, że równoważniki elektrochemiczne k pierwiastków są proporcjonalne do ich równoważników chemicznych(obecnie jest to wielkość nielegalna). (10. 3) Reinhard Kulessa 18

W poprzednim wzorze M jest masą jonu, Wi jest wartościowością jonu, a F jest stałą Faraday’a (F=96485 C/mol), czyli ładunkiem mola elektronów. Łącząc I i II prawo Faraday’a otrzymujemy: 10. 3 Teoria przewodnictwa elektrolitycznego W elektrolicie jony poruszają się pod wpływem dwóch przyczynków. Pierwszy pochodzi od ukierunkowanego ruchu związanego z przyłożonym polem elektrycznym, a drugi od ruchów termicznych. Reinhard Kulessa 19

Ze względu na to, że jony są znacznie większe od elektronów, nie możemy zaniedbać oporu ośrodka. Równanie ruchu jonu dodatniego będzie następujące: gdzie m oznacza masę jonu, a – przyśpieszenie jonu, v – prędkość jonu, k – współczynnik tarcia, E – natężenie pola elektrycznego. Dla pewnej prędkości v, q. E – k+v+ = 0, więc prędkość jony przyjmuje stałą wartość. (10. 4) Reinhard Kulessa 20

v+ ma kierunek wektora natężenia pola elektrycznego. Analogicznie określamy prędkość jonów ujemnych. Prąd w elektrolicie jest sumą prądów jonów dodatnich i ujemnych. Liczba jonów każdego znaku w jednostce objętości jest równa: Całkowita gęstość prądu j jest sumą Wyrażenie to możemy również napisać następująco: . Reinhard Kulessa (10. 5) 21

W równaniu (10. 5) F jest stałą Faraday’a, a jest tzw. stężeniem równoważnym , równym ilości gramorównoważników rozpuszczonej substancji przypadającej na jednostkę objętości roztworu. Jeśli przez N’ oznaczymy liczbę cząsteczek w gramorównoważniku substancji, to stała Faraday’a F=q. N’, a = n 0/N’. Wtedy qn 0 = F. Podstawiając do wzoru (10. 5) wyrażenie na prędkość jonów (wzór (10. 4)), otrzymamy: Reinhard Kulessa 22

Możemy jeszcze wprowadzić do ostatniego równania wyrażenie na ruchliwość jonów, ± = q/k± , otrzymujemy: (10. 6) W oparciu o ostatnie wyrażenie otrzymujemy na wspólczynnik przewodnictwa elektrolitu wyrażenie: (10. 7) Odwrotność przewodnictwa właściwego daje nam wyrażenie na opór właściwy. Reinhard Kulessa 23
- Slides: 23