WYKAD 10 25 05 18 BIAKA Metabolizm ywnoci

WYKŁAD 10 25. 05. 18

BIAŁKA
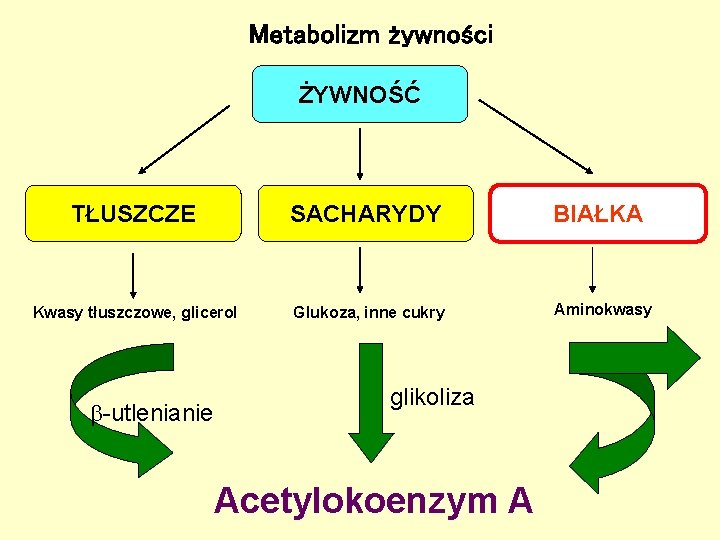
Metabolizm żywności ŻYWNOŚĆ TŁUSZCZE SACHARYDY BIAŁKA Kwasy tłuszczowe, glicerol Glukoza, inne cukry Aminokwasy -utlenianie glikoliza Acetylokoenzym A

Białka • POLIPEPTYD • Aminokwasy połączone wiązaniami amidowymi (peptydowymi) i disiarczkowymi • POLIPEPTYD + fragment niebiałkowy • • • Glikoproteiny Metaloproteiny Fosfoproteiny Lipoproteiny Nukleoproteiny
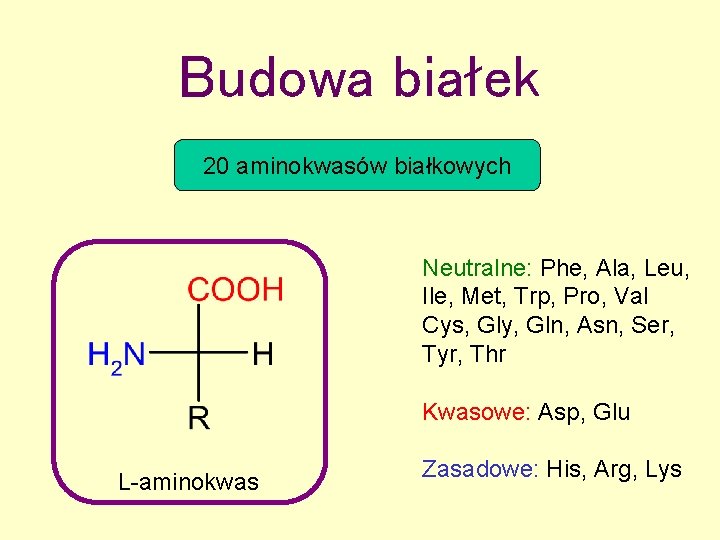
Budowa białek 20 aminokwasów białkowych Neutralne: Phe, Ala, Leu, Ile, Met, Trp, Pro, Val Cys, Gly, Gln, Asn, Ser, Tyr, Thr Kwasowe: Asp, Glu L-aminokwas Zasadowe: His, Arg, Lys
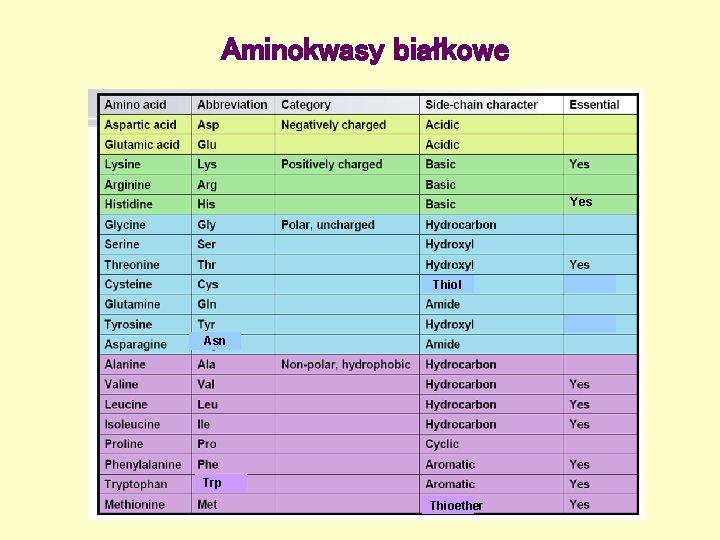
Aminokwasy białkowe Yes Thiol Asn Trp Thioether
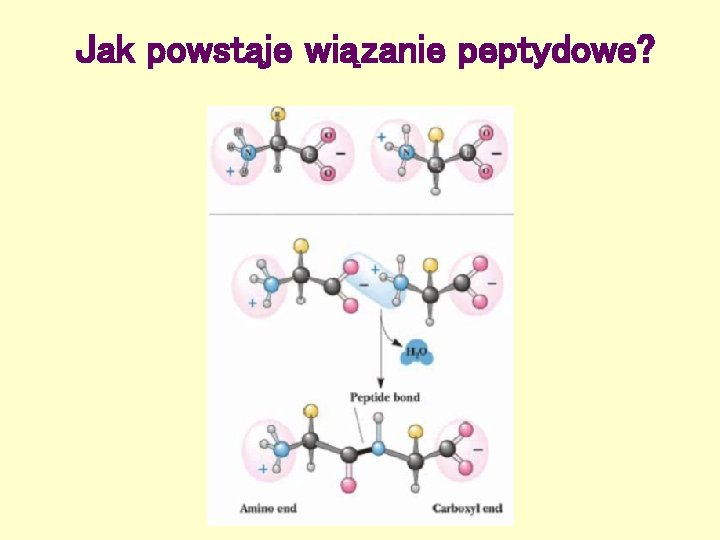
Jak powstaje wiązanie peptydowe?
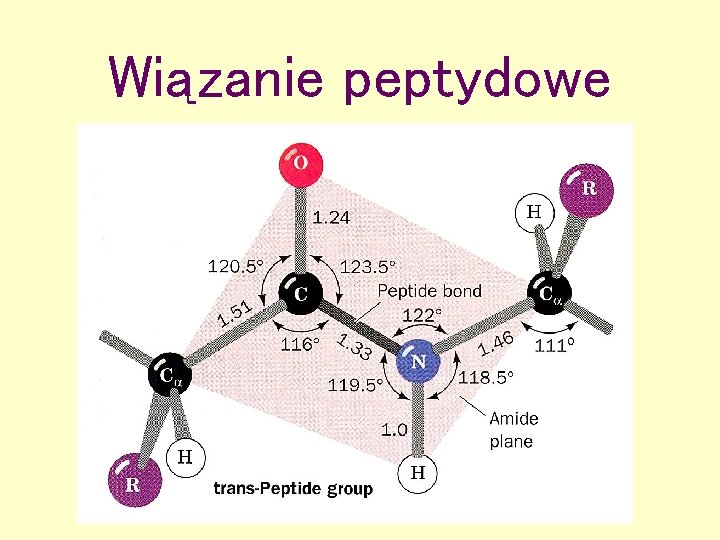
Wiązanie peptydowe
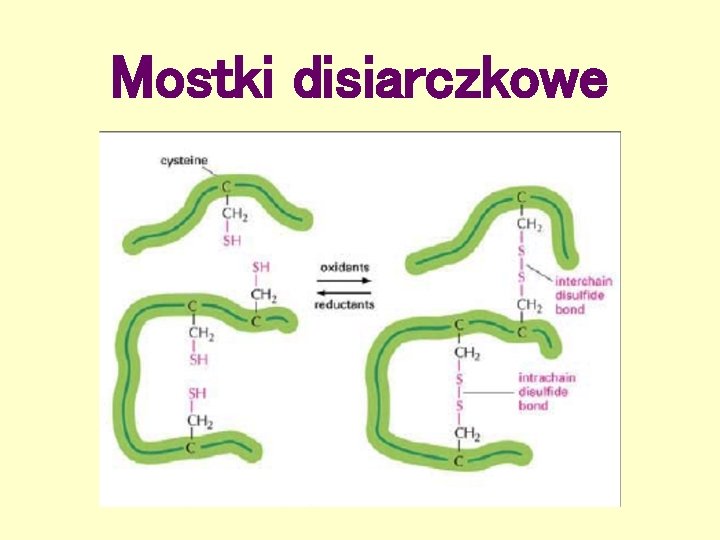
Mostki disiarczkowe
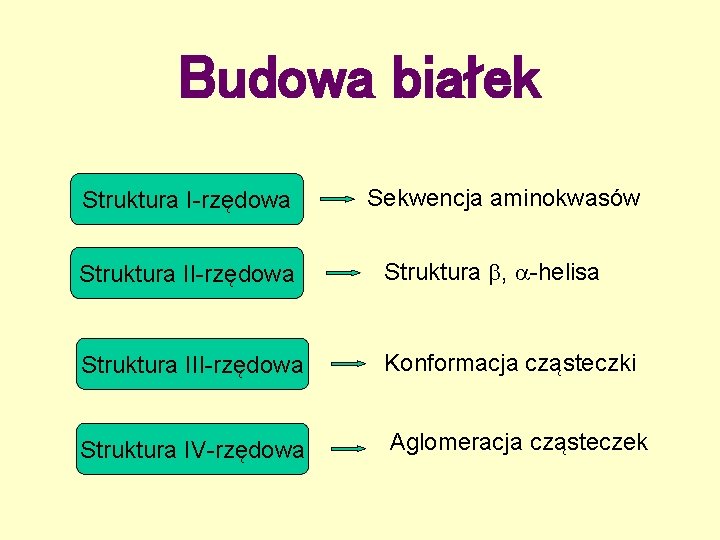
Budowa białek Struktura I-rzędowa Sekwencja aminokwasów Struktura II-rzędowa Struktura , -helisa Struktura III-rzędowa Konformacja cząsteczki Struktura IV-rzędowa Aglomeracja cząsteczek
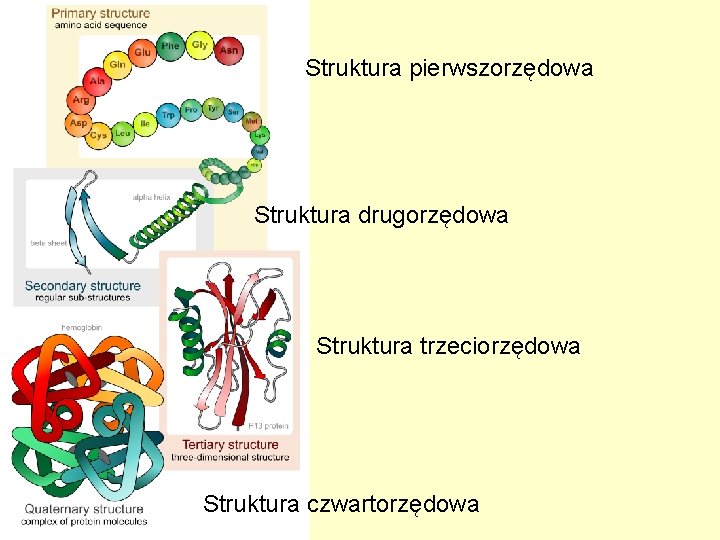
Struktura pierwszorzędowa Struktura drugorzędowa Struktura trzeciorzędowa Struktura czwartorzędowa

Biologiczne funkcje białek • Enzymy • Białka transportujące • Hormony • Białka ochronne • Białka zapasowe • Białka kurczliwe • Białka budulcowe • Toksyny

Właściwości białek • GLOBULARNE (rozpuszczalne w H 2 O) • FIBRYLARNE (nierozpuszczalne w H 2 O) • Lizozym • Insulina • Mioglobina • Kolagen • Elastyna • Keratyna

Struktura białek globularnych Aminokwasy hydrofobowe – wewnątrz cząsteczki osłonięte przed kontaktem z wodą Aminokwasy hydrofilowe – na zewnątrz cząsteczki oraz w centrach katalitycznych enzymów Imidazol histydyny – donor lub akceptor protonu przy fizjologicznym p. H (centra katalityczne enzymów) Grupy – CH 2 OH i CH 2 SH (seryna, cysteina) działają jako nukleofile podczas katalizy enzymatycznej

Denaturacja białek Rozerwanie wiązań stabilizujących strukturę II i III-rzędową – utrata aktywności biologicznej Struktura I-rzędowa pozostaje nienaruszona Czynniki powodujące denaturację: • Podwyższona temperatura (60 -70 C) • Niskie i wysokie p. H • Promieniowanie • Ultradźwięki • Detergenty • Rozpuszczalniki organiczne • Wysokie stężenie jonów
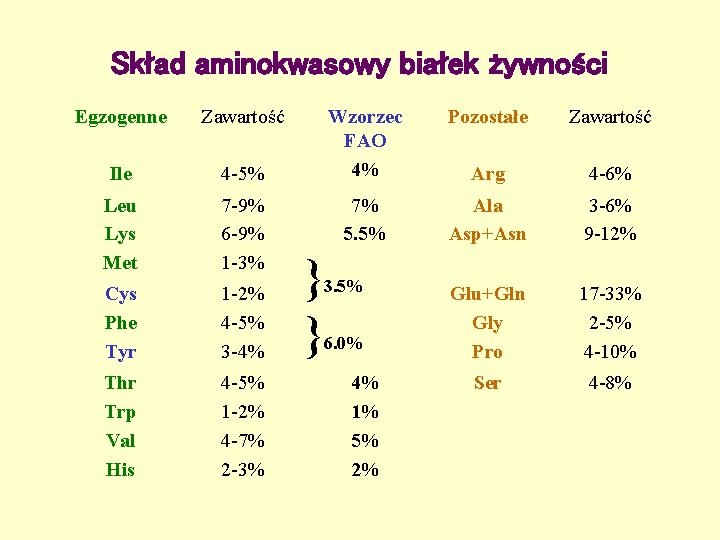
Skład aminokwasowy białek żywności Egzogenne Zawartość Ile 4 -5% Leu Lys Met 7 -9% 6 -9% 1 -3% Cys Phe Tyr 1 -2% 4 -5% 3 -4% Thr Trp Val His 4 -5% 1 -2% 4 -7% 2 -3% } } Wzorzec FAO 4% Pozostałe Zawartość Arg 4 -6% 7% 5. 5% Ala Asp+Asn 3 -6% 9 -12% Glu+Gln Gly Pro 17 -33% 2 -5% 4 -10% Ser 4 -8% 3. 5% 6. 0% 4% 1% 5% 2%

Reakcje białek podczas przetwarzania i przechowywania żywności • Działanie podwyższonej temperatury • Ekstremalne p. H • Obecność utleniaczy • Obecność węglowodanów, lipidów

Obróbka termiczna i przemysłowe przetwarzanie powodują: Skutki korzystne: • Ograniczenie psucia się • Przedłużenie czasu przechowywania Efekty niekorzystne: • Obniżenie wartości odżywczej • Utrata właściwości funkcjonalnych • Powstawanie produktów toksycznych • Niekorzystne zmiany cech sensorycznych

Obróbka termiczna w temp. do 100 C: • Zmniejszenie rozpuszczalności białek globularnych • Struktura pierwszorzędowa nienaruszona • Inaktywacja enzymów • Destrukcja toksyn i czynników przeciwżywieniowych • Poprawa przyswajalności

Obróbka termiczna > 115 C: • Degradacja cysteiny i cystyny (powstaje H 2 S, (CH 3)2 S, kwas cysteinowy • Reakcje deamidacji w resztach Asn i Gln (powstaje NH 3, zmiana p. I, kowalencyjne sieciowanie) • W obecności tlenu – degradacja tryptofanu

Obróbka termiczna > 200 C oraz zasadowe środowisko: • Izomeryzacja (obniżenie przyswajalności i wartości odżywczej) • Powstawanie cyklicznych pochodnych o działaniu mutagennym) • Degradacja w środowisku zasadowymj (Arg, Cys, Ser, Thr, Lys)

Obróbka termiczna 200 -300 C • Sieciowanie – grupy aminowe Lys i Arg reagują z karboksylowymi Glu i Asp (obniżenie przyswajalności, zmiany wł. funkcjonalnych) • Powstawanie cyklicznych pochodnych o działaniu mutagennym, kancerogennym
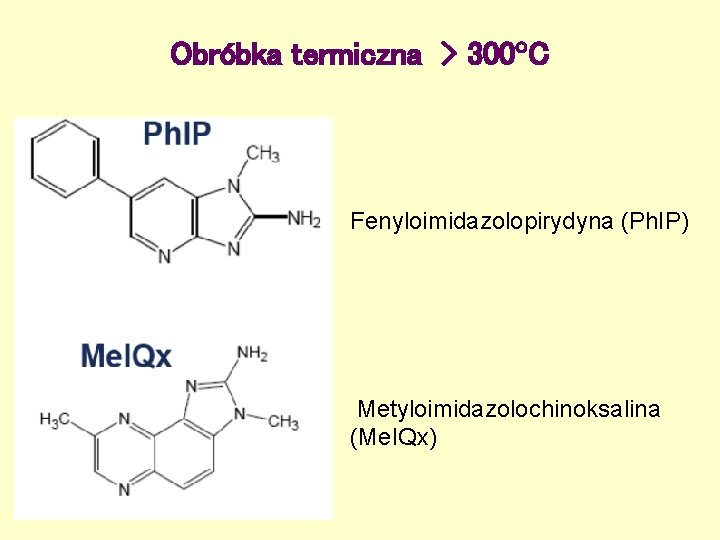
Obróbka termiczna > 300 C Fenyloimidazolopirydyna (Ph. IP) Metyloimidazolochinoksalina (Me. IQx)
- Slides: 23