www agamenonquimica com agamenonrobertogmail com PROF AGAMENON ROBERTO

www. agamenonquimica. com agamenonroberto@gmail. com

PROF. AGAMENON ROBERTO

Como medir átomos e moléculas? PROF. AGAMENON ROBERTO

UNIDADE DE MASSA ATÔMICA (u. m. a. ) 1 12 do carbono 12 ou CARBONO 12 1 u. m. a. PROF. AGAMENON ROBERTO
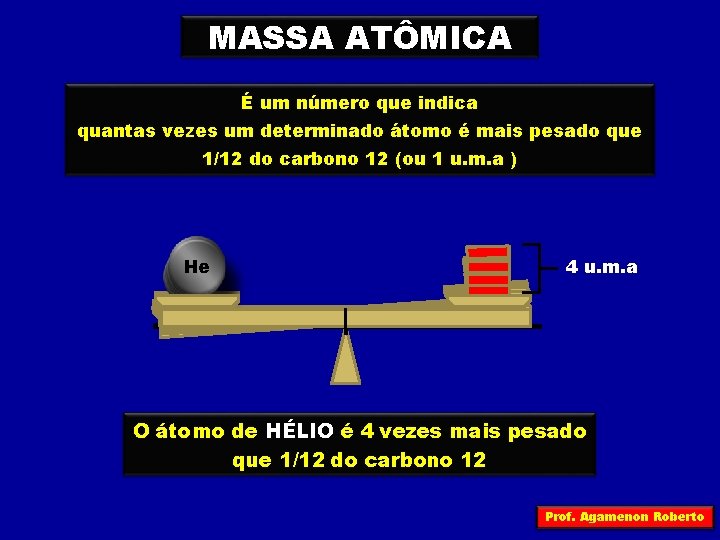
MASSA ATÔMICA É um número que indica quantas vezes um determinado átomo é mais pesado que 1/12 do carbono 12 (ou 1 u. m. a ) He He e H 4 u. m. a O átomo de HÉLIO é 4 vezes mais pesado que 1/12 do carbono 12 Prof. Agamenon Roberto

01) (UFPB) A massa de três átomos do isótopo 12 do carbono é igual à massa de dois átomos de um certo elemento X. Pode-se dizer, então, que a massa atômica de X, em unidades de massa atômica, é: Dado: massa atômica do carbono = 12 u. a) 12. X b) 36. X C C C c) 18. d) 3. e) 24. 2 x m. X = 3 x m. C 2 x m. X = 3 x 12 m. X = 36 2 m. X = 18 Prof. Agamenon Roberto

MASSA DO ELEMENTO QUÍMICO 35 Cl 17 37 Cl 17 É a média ponderada das massas atômicas de seus isótopos, onde a porcentagem com que cada aparece na natureza é o peso PROF. AGAMENON ROBERTO

O cloro possui dois isótopos de pesos atômicos 35 u e 37 u, com porcentagens, respectivamente, iguais a 75% e 25%. m = 35 Cl 75% 37 Cl 25% 35 x 75 + 37 x 25 100 2625 + 925 100 = 3550 100 m = 35, 50 u. m. a. PROF. AGAMENON ROBERTO

01) (Fuvest – SP) O carbono ocorre na natureza como uma mistura de átomos dos quais 98, 90% são 12 C e 1, 10% são de a) Explique o significado das representações 12 C e 13 C. Pág. 435 Ex. 10 13 C. 12 C Isótopo do carbono com número de massa 12. 13 C Isótopo do carbono com número de massa 13. b) Com esses dados, calcule a massa atômica do carbono natural. Dados: massa atômica do m = 12 x 98, 9 + 13 100 x 12 C 1, 1 = 12, 000 u. ; do = 13 C = 13, 003 u. 1186, 8 + 14, 3 100 = 1201, 1 100 m = 12, 011 u. PROF. AGAMENON ROBERTO

02) Um elemento X tem massa atômica igual a 35, 5 e é constituído de dois isótopos X 1, de massa 35, 8, e X 2, de massa 35, 4. Logo, a porcentagem do isótopo X 1 é igual a: a) 5. b) 10. c) 20. d) 25. 35, 8 X x% 1 35, 4 X Pág. 434 Ex. 07 (100 – x )% 2 e) 50. 35, 8 35, 5 = x x + 35, 4 x (100 – x) 100 35, 8 x + 3540 – 35, 4 x = 3550 0, 4 x = 3550 – 3540 x = 10 0, 4 x = 25% PROF. AGAMENON ROBERTO
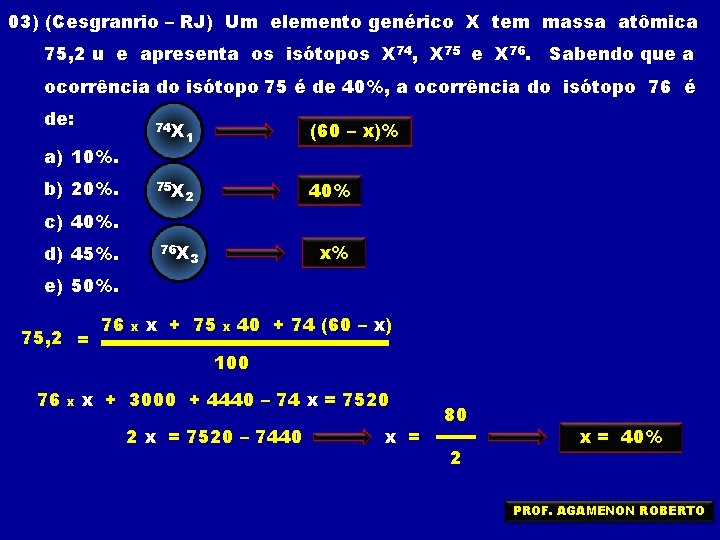
03) (Cesgranrio – RJ) Um elemento genérico X tem massa atômica 75, 2 u e apresenta os isótopos X 74, X 75 e X 76. Sabendo que a ocorrência do isótopo 75 é de 40%, a ocorrência do isótopo 76 é de: 74 X a) 10%. b) 20%. (60 – x)% 1 75 X 40% 2 c) 40%. 76 X d) 45%. x% 3 e) 50%. 75, 2 = 76 x x + 75 x 40 + 74 (60 – x) 100 x + 3000 + 4440 – 74 x = 7520 2 x = 7520 – 7440 x = 80 2 x = 40% PROF. AGAMENON ROBERTO

MASSA MOLECULAR (M) É um número que indica quantas vezes uma molécula é mais pesada que 1/12 do carbono 12 De uma maneira prática, calculamos a massa molecular somando-se todos os pesos atômicos dos átomos que formam a molécula PROF. AGAMENON ROBERTO
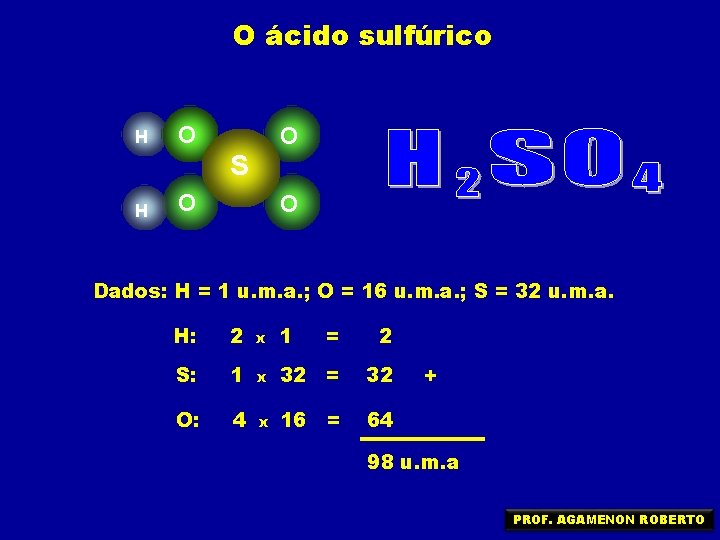
O ácido sulfúrico H O O S H O O Dados: H = 1 u. m. a. ; O = 16 u. m. a. ; S = 32 u. m. a. H: 2 x 1 = 2 S: 1 x 32 = 32 O: 4 x 16 = 64 + 98 u. m. a PROF. AGAMENON ROBERTO

01) A massa molecular da sulfanilmida, C 6 H 8 N 2 O 2 S, é: Dados: H = 1 u. ; C = 12 u. ; N = 14 u. ; O = 16 u. ; S = 32 u. a) 196 u. 6 x H: 8 x d) 112 u. N: 2 e) 172 u. b) 174 u. c) 108 u. C: 12 = 1 72 = 8 x 14 = 28 O: 2 x 16 = 32 S: 1 x 32 = 32 Pág. 435 Ex. 15 + 172 u. PROF. AGAMENON ROBERTO

02) (Ufac) A massa fórmula do composto abaixo é: Na 2 SO 4. 3 H 2 O Dados: H = 1 u. ; Na = 23 u. ; S = 32 u. ; O = 16 u. a) 142 u. b) 196 u. c) 426 u. d) 444 u. Na: 2 x 23 = 46 S: 1 x 32 = 32 O: 4 x 16 = 64 + 142 u. m. a e) 668 u. H: 2 x 1 = 2 O: 1 x 16 = 16 + 18 u. m. a M = 142 + 3 x 18 = 196 u. m. a Pág. 435 Ex. 16
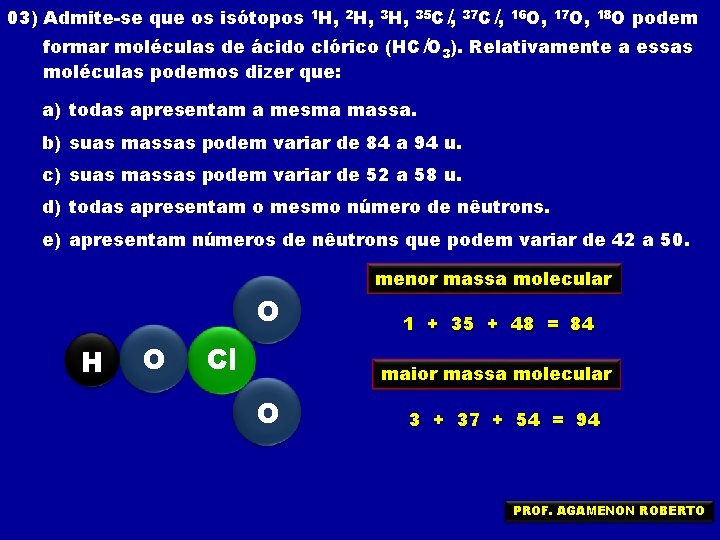
03) Admite-se que os isótopos 1 H, 2 H, 3 H, 35 C l, 37 Cl, 16 O, 17 O, 18 O podem formar moléculas de ácido clórico (HCl. O 3). Relativamente a essas moléculas podemos dizer que: a) todas apresentam a mesma massa. b) suas massas podem variar de 84 a 94 u. c) suas massas podem variar de 52 a 58 u. d) todas apresentam o mesmo número de nêutrons. e) apresentam números de nêutrons que podem variar de 42 a 50. O H O Cl menor massa molecular 1 + 35 + 48 = 84 maior massa molecular O 3 + 37 + 54 = 94 PROF. AGAMENON ROBERTO

04) (U. ANÁPOLIS – GO) Um composto Al 2(XO 4)3 apresenta uma “massa molecular” igual a 342 u. Determine a massa atômica do elemento “ X ”. Dados: O = 16 u. ; Al = 27 u. a) 8 u. b) 16 u. c) 32 u. d) 48 u. e) 96 u. Al : 2 x X: 3 x O : 12 x DESAFIO 27 = 54 x = 3 x 16 = 192 54 + 3 x + 192 = 342 3 x = 342 – 246 3 x = 96 x = Prof. Agamenon Roberto 96 3 = 32 u

NÚMERO DE AVOGADRO É o número de entidades (moléculas ou átomos) existentes em uma massa, em gramas, igual à massa molecular ou massa atômica Este número é igual a 6, 02 x 1023 Prof. Agamenon Roberto

Em uma massa de 56 g de átomos Fe de ferro (peso atômico 56 u. ) existem 6, 02 x 1023 átomos de ferro Em uma massa igual a 18 g de H 2 O O H H (massa molecular 18 u) existem 6, 02 x 1023 moléculas de água. A quantidade 6, 02 x 1023 é chamada de MOL PROF. AGAMENON ROBERTO

RESUMO M é o peso molecular 11 mol de de moléculas átomos 1 mol dede cálcio CO 2 (PA) é o peso atômico pesa contém M 44 g g ou (PA) 40 gg 6, 02 x 1023 entidades A massa (em gramas) de um mol de átomos ou a massa (em gramas) de um mol de moléculas chama-se MASSA MOLAR PROF. AGAMENON ROBERTO
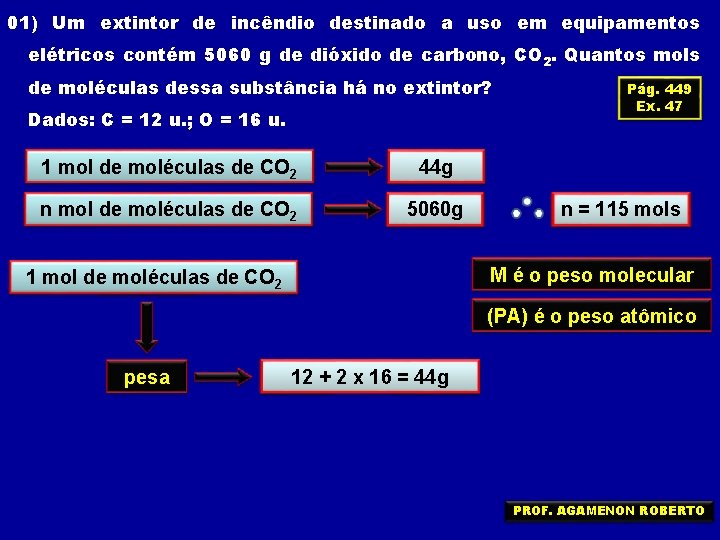
01) Um extintor de incêndio destinado a uso em equipamentos elétricos contém 5060 g de dióxido de carbono, CO 2. Quantos mols de moléculas dessa substância há no extintor? Dados: C = 12 u. ; O = 16 u. 1 mol de moléculas de CO 2 44 g n mol de moléculas de CO 2 5060 g 1 mol de moléculas de CO 2 1 mol Pág. 449 Ex. 47 n = 115 mols M é o peso molecular (PA) é o peso atômico pesa M 12 g + 2 ou x 16 =(PA) 44 g g PROF. AGAMENON ROBERTO

02) Dentre as amostras listadas abaixo, indique aquela que possui maior quantidade de matéria: Dados: Ag = 108 u. ; Ca = 40 u. ; Pb = 207 u. a) 10, 8 g de prata; b) 4, 0 g de cálcio; Pág. 449 Ex. 50 c) 20, 7 g de chumbo; 1 mol 108 g 1 mol 40 g 1 mol 207 g n mol 10, 8 g n mol 4 g n mol 20, 7 g n = 10, 8 108 n = 0, 1 mol n = 4 40 n = 0, 1 mol n = 20, 7 207 n = 0, 1 mol PROF. AGAMENON ROBERTO
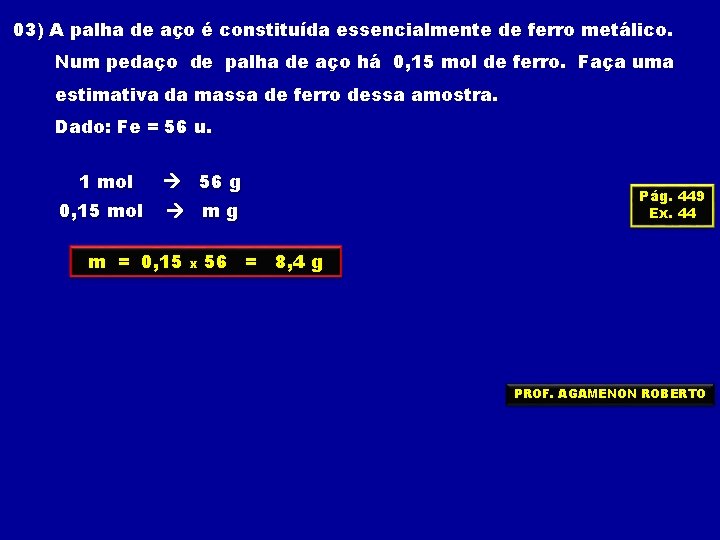
03) A palha de aço é constituída essencialmente de ferro metálico. Num pedaço de palha de aço há 0, 15 mol de ferro. Faça uma estimativa da massa de ferro dessa amostra. Dado: Fe = 56 u. 1 mol 0, 15 mol 56 g mg m = 0, 15 x Pág. 449 Ex. 44 56 = 8, 4 g PROF. AGAMENON ROBERTO

04) (UFRJ) Um balão de oxigênio contendo 3, 01 x 1026 átomos foi completamente utilizado por uma equipe médica durante uma cirurgia. Admitindo-se que havia apenas gás oxigênio (O 2) nesse balão, a massa utilizada do referido gás foi equivalente a: Dado: O 2 = 32 g/mol. 23 entidades Contém x 10 6, 02 x 1023 moléculas a) 8, 0 kg. 1 mol b) 4, 0 kg. pesa c) 12, 0 kg. d) 16, 0 kg. e) 10, 0 kg. 32 g m m = 32 2 x x 3, 01 6, 02 x x 1026 2 x 6, 02 3, 01 = 8 x x x (PA)g (PM) 32 g g 1023 átomos 1026 átomos 103 g = 8 kg 1023 PROF. AGAMENON ROBERTO

Dizemos que um gás se encontra nas CNTP quando: P = 1 atm ou 760 mm. Hg e T = 0 °C ou 273 K É o volume ocupado por um mol de um gás Nas CNTP o volume molar de qualquer gás é de 22, 4 L

01) Assinale a alternativa correspondente ao volume ocupado por 0, 25 mol de gás carbônico (CO 2) nas condições normais de temperatura e pressão (CNTP): a) 0, 25 L. b) 0, 50 L. c) 5, 60 L. 1 mol 0, 25 mol 1 d) 11, 2 L. e) 22, 4 L 0, 25 1 x V = 22, 4 V V = 0, 25 x 22, 4 V = 5, 6 L Prof. Agamenon Roberto
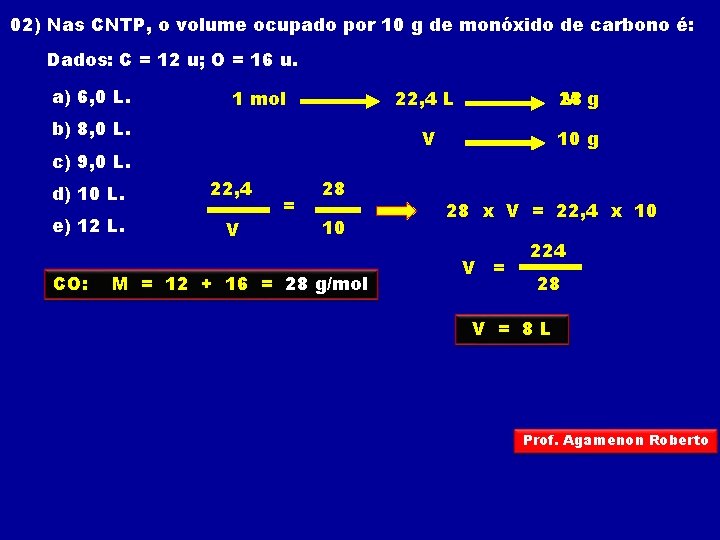
02) Nas CNTP, o volume ocupado por 10 g de monóxido de carbono é: Dados: C = 12 u; O = 16 u. a) 6, 0 L. 1 mol b) 8, 0 L. c) 9, 0 L. d) 10 L. 22, 4 e) 12 L. V CO: = 28 10 M = 12 + 16 = 28 g/mol 22, 4 L 28 M g V 10 g 28 x V = 22, 4 x 10 V = 224 28 V = 8 L Prof. Agamenon Roberto
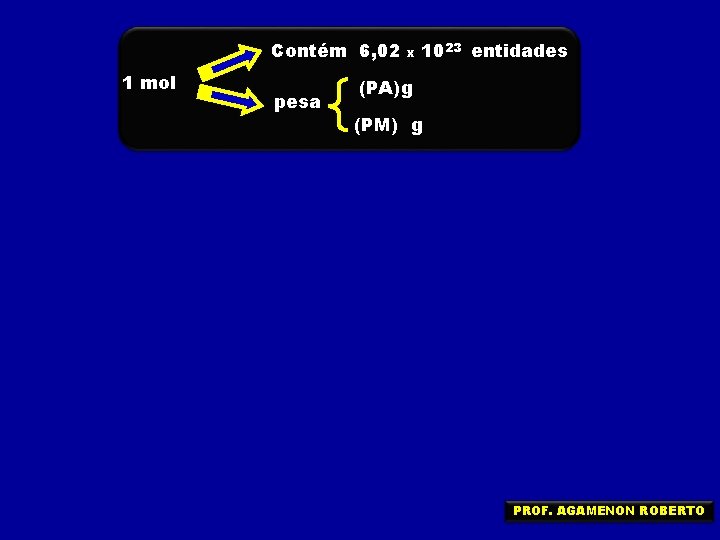
Contém 6, 02 1 mol pesa x 1023 entidades (PA)g (PM) g PROF. AGAMENON ROBERTO
- Slides: 28