Wodorotlenki waciwoci chemiczne Klasa 1 CP 1 DP










![Wodorotlenki amfoteryczne Na 3[Al(OH)6] czyli heksahydroksoglinian sodu to sól kompleksowa Jak się tworzy nazwy Wodorotlenki amfoteryczne Na 3[Al(OH)6] czyli heksahydroksoglinian sodu to sól kompleksowa Jak się tworzy nazwy](https://slidetodoc.com/presentation_image_h2/604ec111e8099f33cfde21891f50ae0d/image-12.jpg)
![Wodorotlenki amfoteryczne – sole kompleksowe Na 3[Al(OH)6] czyli heksahydroksoglinian sodu to sól kompleksowa Jak Wodorotlenki amfoteryczne – sole kompleksowe Na 3[Al(OH)6] czyli heksahydroksoglinian sodu to sól kompleksowa Jak](https://slidetodoc.com/presentation_image_h2/604ec111e8099f33cfde21891f50ae0d/image-13.jpg)





- Slides: 20

Wodorotlenki właściwości chemiczne Klasa 1 CP, 1 DP, 1 FP 30 marca – 1 kwietnia 2020 r. Marta Sawicka


Z poprzednich lekcji wiemy : � co to są wodorotlenki n Me(OH)n liczba grup wodorotlenkowych = wartościowość metalu � jak tworzyć nazwy wodorotlenków na podstawie ich wzoru i jak napisać wzór wodorotlenku na podstawie jego nazwy; np. Na. OH – wodorotlenek sodu Al(OH)3 – wodorotlenek glinu Cr(OH)3 – wodorotlenek chromu(III) tu: mamy jedną grupę wodorotlenkową, bo potas leży w grupie 1 układu okresowego i jego wartościowość zawsze wynosi I tu: podajemy wartościowość bo chrom w związkach może przyjmować różne wartościowości wodorotlenek potasu – KOH wodorotlenek żelaza(II) – Fe(OH)2 tu: mamy dwie grupy wodorotlenkowe, bo wartościowość żelaza w tym związku, zgodnie z jego nazwą, wynosi II

Z poprzednich lekcji wiemy : � co to są zasady Wodorotlenki rozpuszczalne w wodzie i ich wodne roztwory nazywamy zasadami � jakie są metody otrzymywania wodorotlenków metal aktywny + woda wodorek metalu + woda tlenek metalu aktywnego + woda wodorotlenek+ wodór wodorotlenek oraz (dla wodorotlenków praktycznie nierozpuszczalnych w wodzie) sól metalu 1 + zasada metalu 2 wodorotlenek metalu 1 + sól metalu 2

Z tej lekcji dowiesz się: � jaki charakter chemiczny mają wodorotlenki, � jak określić charakter chemiczny wodorotlenków na podstawie wyników doświadczenia, � jak przebiegają reakcje chemiczne potwierdzające charakter chemiczny wodorotlenków

Podział wodorotlenków ze względu na ich charakter chemiczny : WODOROTLENKI zasadowe amfoteryczne

Wodorotlenki zasadowe � to wodorotlenki litowców i niektórych berylowców, np. Na. OH, KOH, Sr(OH)2, Ba(OH)2 � ich wodne roztwory mają odczyn zasadowy więc barwią fenoloftaleinę na malinowo fenoloftaleina woda + Na. OH

Wodorotlenki zasadowe � reagują z kwasami dając odpowiednie sole wodorotlenek + kwas → sól + woda np. Na. OH + HCl wodorotlenek sodu → kwas chlorowodorowy Na. Cl + H 2 O chlorek sodu woda Zapoznaj się z przebiegiem takiej reakcji oglądając film: https: //www. youtube. com/watch? v=8 n. BSL 90 z. YUw źródło: youtube. com

A co to są wodorotlenki amfoteryczne?

Wodorotlenki amfoteryczne � � to np. Al(OH)3 , Be(OH)2 , Pb(OH)2 , Cr(OH)3 , Sn(OH)2 , Sn(OH)4 i inne; zauważ, że wszystkie te związki nie rozpuszczają się w wodzie (sprawdź w tabeli rozpuszczalności) czyli w wodzie występują w postaci osadu; reagują zarówno z kwasami, kwasami jak i zasadami dając odpowiednie sole wodorotlenek + kwas → sól + woda wodorotlenek + zasada → sól + woda amfoteryczny kompleksowa

� np. Wodorotlenki amfoteryczne reakcja z kwasem Al(OH)3 + 3 HCl wodorotlenek glinu � np. → Al. Cl 3 + 3 H 2 O kwas chlorowodorowy chlorek glinu woda reakcja z zasadą Al(OH)3 + 3 Na. OH wodorotlenek glinu wodorotlenek sodu → Na 3[Al(OH)6] heksahydroksoglinian sodu
![Wodorotlenki amfoteryczne Na 3AlOH6 czyli heksahydroksoglinian sodu to sól kompleksowa Jak się tworzy nazwy Wodorotlenki amfoteryczne Na 3[Al(OH)6] czyli heksahydroksoglinian sodu to sól kompleksowa Jak się tworzy nazwy](https://slidetodoc.com/presentation_image_h2/604ec111e8099f33cfde21891f50ae0d/image-12.jpg)
Wodorotlenki amfoteryczne Na 3[Al(OH)6] czyli heksahydroksoglinian sodu to sól kompleksowa Jak się tworzy nazwy takich soli: • heksa - bo we zorze jest obecnych 6 grup wodorotlenkowych • hydrokso - bo obecne są grupy wodorotlenkowe, które nazywane są też grupami hydroksylowymi • glinian - bo to sól glinu • sodu – bo kationem metalu w tej soli jest właśnie sód
![Wodorotlenki amfoteryczne sole kompleksowe Na 3AlOH6 czyli heksahydroksoglinian sodu to sól kompleksowa Jak Wodorotlenki amfoteryczne – sole kompleksowe Na 3[Al(OH)6] czyli heksahydroksoglinian sodu to sól kompleksowa Jak](https://slidetodoc.com/presentation_image_h2/604ec111e8099f33cfde21891f50ae0d/image-13.jpg)
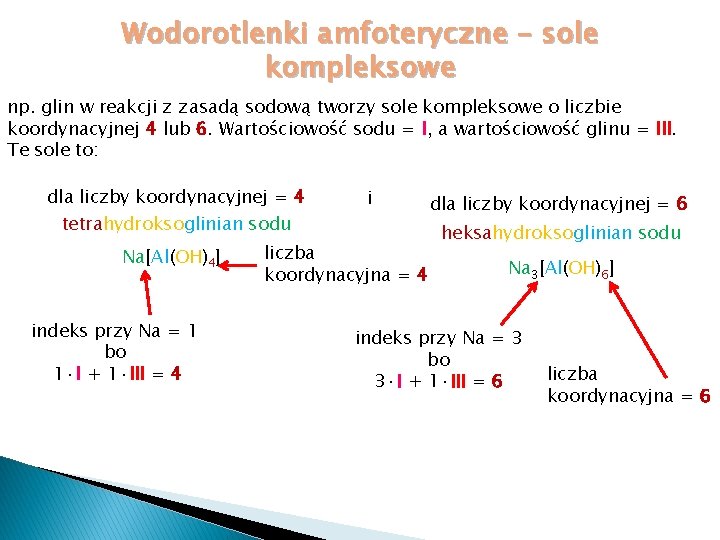
Wodorotlenki amfoteryczne – sole kompleksowe Na 3[Al(OH)6] czyli heksahydroksoglinian sodu to sól kompleksowa Jak się tworzy wzory takich soli: • musisz znać tzw. liczbę koordynacyjną - czyli liczbę np. grup OH, które mogą występować w soli kompleksowej • musisz pamiętać, że : suma iloczynów wartościowości metali i ich indeksów stechiometrycznych = liczba koordynacyjna

Wodorotlenki amfoteryczne – sole kompleksowe np. glin w reakcji z zasadą sodową tworzy sole kompleksowe o liczbie koordynacyjnej 4 lub 6. Wartościowość sodu = I, a wartościowość glinu = III. Te sole to: dla liczby koordynacyjnej = 4 tetrahydroksoglinian sodu Na[Al(OH)4] indeks przy Na = 1 bo 1·I + 1·III = 4 i liczba koordynacyjna = 4 dla liczby koordynacyjnej = 6 heksahydroksoglinian sodu Na 3[Al(OH)6] indeks przy Na = 3 bo 3·I + 1·III = 6 liczba koordynacyjna = 6

Wodorotlenki amfoteryczne Zapoznaj się z przebiegiem reakcji wodorotlenku amfoterycznego z kwasem i zasadą oglądając film: https: //www. youtube. com/watch? v=r 5 fn. GBq-EJM (źródło: youtube. com) UWAGA: przerwij oglądanie filmu w 1. 42 min oglądania ! *Zwróć uwagę, że tym razem, o zajściu reakcji wodorotlenku amfoterycznego z kwasem i zasadą świadczy zanik (czyli roztworzenie się) osadu wodorotlenku. Nie ma więc potrzeby dodawania żadnego wskaźnika.

A teraz wykonaj zadania znajdujące się na kolejnych slajdach. Odpowiedzi przepisz do zeszytu. Zadania pochodzą z Kart pracy ucznia z kartami laboratoryjnymi dla liceum ogólnokształcącego i technikum 1 To jest chemia, wydawnictwa Nowa Era.

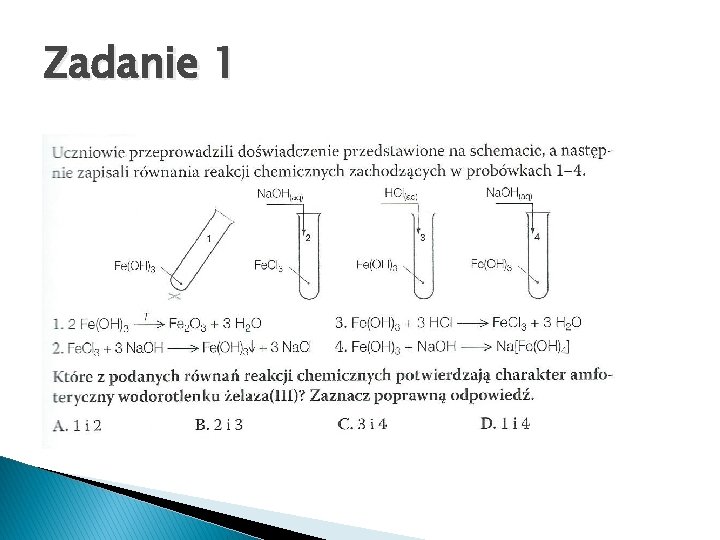
Zadanie 1

Zadanie 2 Uczniowie przeprowadzili doświadczenie chemiczne, którego celem było zbadanie właściwości wodorotlenku potasu. Polegało ono na tym, że na początku, w dwóch zlewkach umieścili wodny roztwór tego wodorotlenku. Wykonane w dalszych krokach czynności oraz towarzyszące im obserwacje umieścili w poniższej tabeli.

To wszystko na dziś Dzwonek Przepraszam, jeszcze tylko jeden slajd……
