Woda jest niezbdna do ycia wszystkim ywym organizmom


Woda jest niezbędna do życia wszystkim żywym organizmom , a ich ciała charakteryzują się dużą zawartością wody




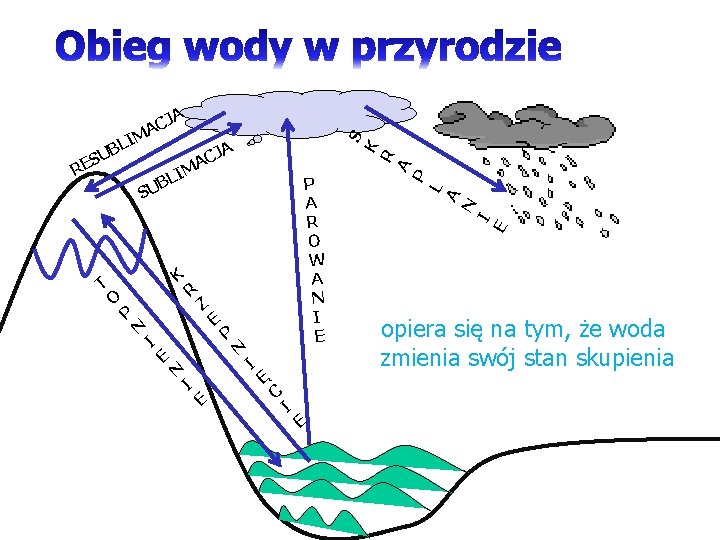
T A CJ A LIM K O P N I E N R I Z E E P N I Ę C I E E I A N P A R O W A N I E L B SU P A R R ES K I L UB S JA C MA opiera się na tym, że woda zmienia swój stan skupienia

WODA • Jest cieczą, ciałem stałym lub gazem w zależności od temperatury i ciśnienia • Jest przezroczysta, bez smaku i zapachu • Jest rozpuszczalnikiem dla soli kuchennej, cukru krystalicznego, spirytusu i kwasu octowego • W wodzie nie rozpuszczają się: piasek, mąka, olej, kreda, benzyna
temperatura +4 100 o. C
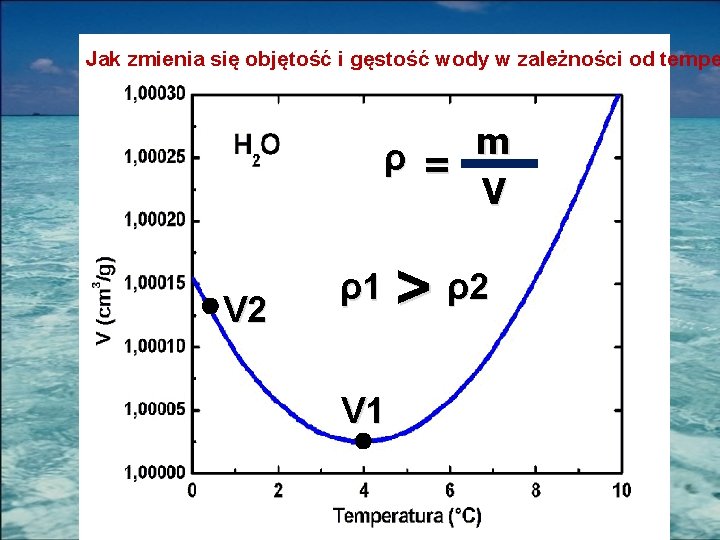
Jak zmienia się objętość i gęstość wody w zależności od tempe m ρ = V V 2 ρ1 V 1 > ρ2

Dzięki temu, że woda jest dobrym rozpuszczalnikiem możliwe jest rozpuszczanie się w niej tlenu czy soli mineralnych niezbędnych organizmom do zachowania życia i zdrowia

Największa gęstość wody w temp. +4°C powoduje, że zimna woda na dnie dużych zbiorników nie zamarza, co umożliwia wielu organizmom wodnym przetrwanie. Zmiana gęstości wody w zależności od temperatury, sprzyja także ruchowi wody, co ułatwia przemieszczanie się w niej różnych substancji
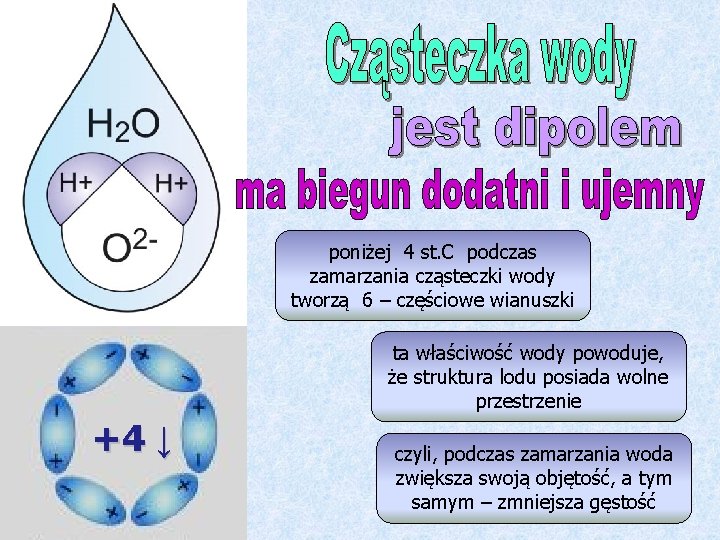
poniżej 4 st. C podczas zamarzania cząsteczki wody tworzą 6 – częściowe wianuszki ta właściwość wody powoduje, że struktura lodu posiada wolne przestrzenie +4 ↓ czyli, podczas zamarzania woda zwiększa swoją objętość, a tym samym – zmniejsza gęstość



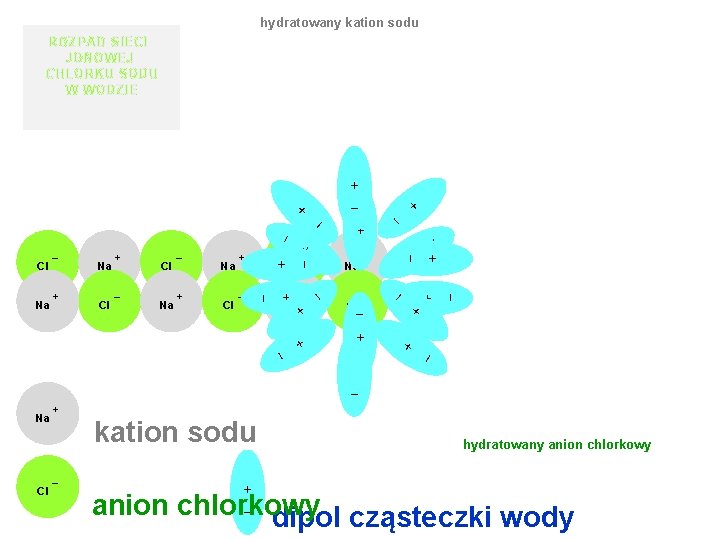
hydratowany kation sodu ROZPAD SIECI JONOWEJ CHLORKU SODU W WODZIE _ + + Na _ Cl + – + _ _ + + _ Na + – + _ – Cl + _ Cl + + _ + Na – _ – Cl + _ Cl + + + Na + _ Na – _ _ Cl + + _ Na Cl + kation sodu – + _ hydratowany anion chlorkowy dipol cząsteczki wody

Pojawienie się jonów soli zakłóca tworzenie sieci krystalicznej lodu i dlatego sól jest używana do posypywania jezdni w czasie zimy. Cl Na – + Na Zorganizowana sieć krystaliczna jonów w strukturze lodu nadaje wodzie, w temperaturze poniżej zera, wygląd ciała stałego. Cl – +

Wysokie ciepło właściwe wody ma duże znaczenie dla organizmów żyjących w wodach, gdyż nie są narażone na częste zmiany temperatury i duże jej wahania. Sprzyja też ustabilizowaniu klimatu na obszarach bogatych w zbiorniki wodne


Wysokie napięcie powierzchniowe wody umożliwia unoszenie się wody w kapilarach (co ułatwia jej cyrkulację w glebie czy ruch soków w roślinach) oraz utrzymanie się owadów na jej powierzchni

To napięcie powierzchniowe polegające na występowaniu dużych sił przyciągania się cząsteczek wody Sprzyja tworzeniu się kropel wody

Niepożądane substancje w wodach nawozy sztuczne detergenty produkty ropy naftowej Dopuszczalne substancje w wodach tlen drobiny piasku dwutlenek węgla sole mineralne
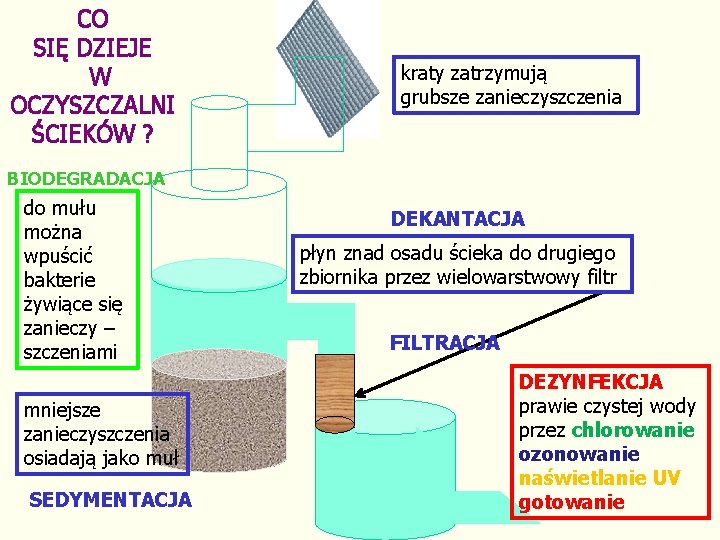
CO SIĘ DZIEJE W OCZYSZCZALNI ŚCIEKÓW ? kraty zatrzymują grubsze zanieczyszczenia BIODEGRADACJA do mułu można wpuścić bakterie żywiące się zanieczy – szczeniami mniejsze zanieczyszczenia osiadają jako muł SEDYMENTACJA DEKANTACJA płyn znad osadu ścieka do drugiego zbiornika przez wielowarstwowy filtr FILTRACJA DEZYNFEKCJA prawie czystej wody przez chlorowanie ozonowanie naświetlanie UV gotowanie
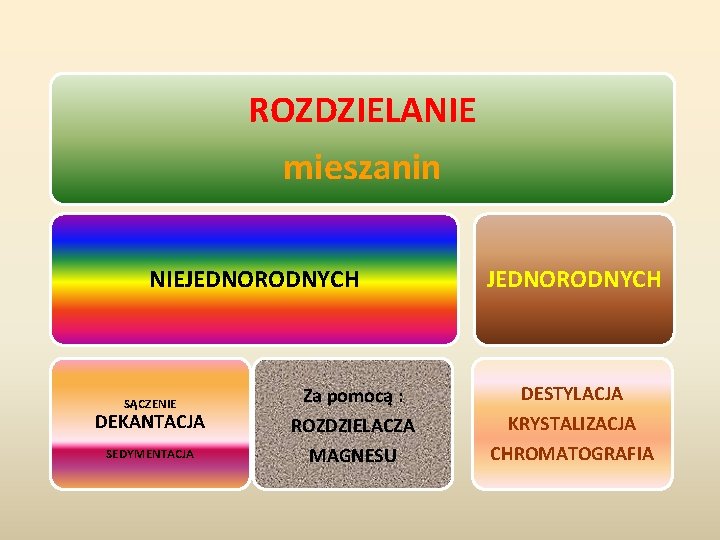
ROZDZIELANIE mieszanin NIEJEDNORODNYCH SĄCZENIE DEKANTACJA SEDYMENTACJA Za pomocą : ROZDZIELACZA MAGNESU JEDNORODNYCH DESTYLACJA KRYSTALIZACJA CHROMATOGRAFIA

Rozpuszczanie to mieszanie się wzajemne cząsteczek substancji rozpuszczanej w rozpuszczalniku (np. w wodzie) Ten proces można przyśpieszyć przez : mieszanie ogrzewanie (ciała stałe) oziębianie (gazy) PODZIAŁ ROZTWORÓW ze względu na wielkość i rodzaj cząsteczek substancji rozpuszczonej ZAWIESINA KOLOID RZECZYWISTY woda z białkiem lub kleik mieszanina niejednorodna mieszanina jednorodna skrobiowy ze względu na ilość substancji rozpuszczonej NIENASYCONY mniej substancji dokładnie tyle substancji rozpuszczonej niż wskazuje rozpuszczonej co wskazuje krzywa rozpuszczalności PRZESYCONY więcej substancji rozpuszczonej niż wskazuje krzywa rozpuszczalności

ROZPUSZCZALNOŚĆ • Maksymalna masa substancji – w gramach, jaką da się rozpuścić w 100 g rozpuszczalnika np. wody w określonej temperaturze

Gdy użyjemy więcej substancji rozpuszczonej niż każe krzywa rozpuszczalności PRZESYCONY Gdy sporządzimy roztwór zgodnie z krzywą rozpuszczalności NASYCONY Gdy użyjemy mniej substancji rozpuszczonej niż każe krzywa rozpuszczalności NIENASYCONY
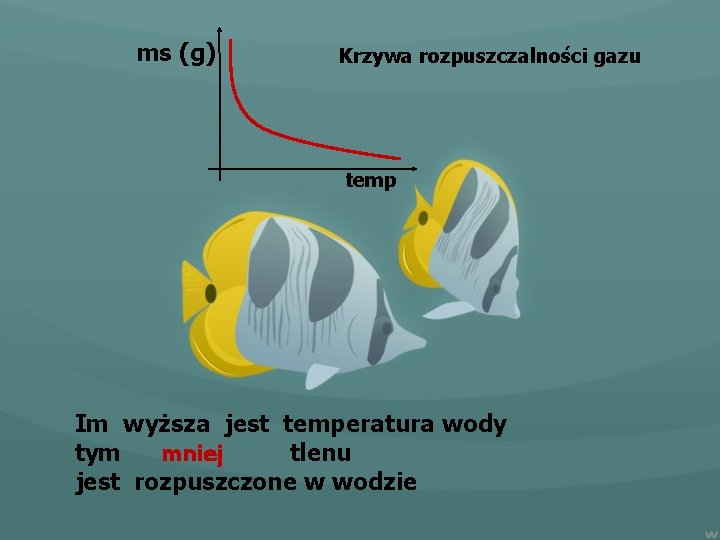
ms (g) Krzywa rozpuszczalności gazu temp Im wyższa jest temperatura wody mniej tym tlenu jest rozpuszczone w wodzie

ROZPUSZCZALNOŚĆ Maksymalna masa substancji – w gramach, jaką da się rozpuścić w 100 g rozpuszczalnika np. wody w określonej temperaturze.
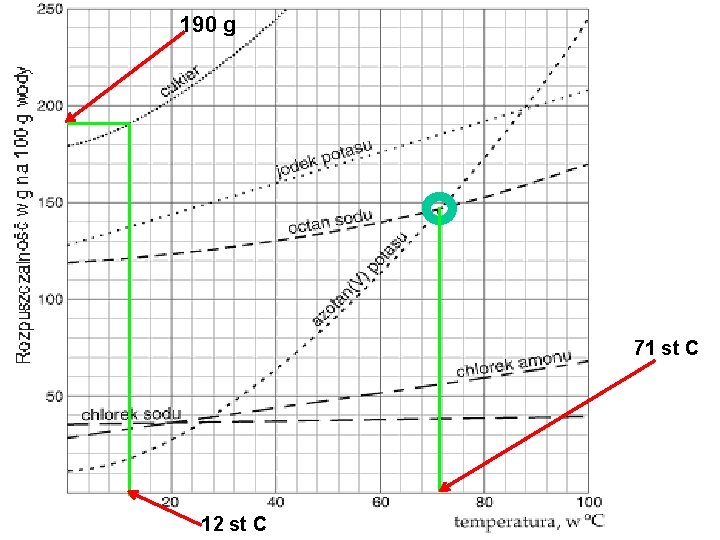
190 g 71 st C 12 st C
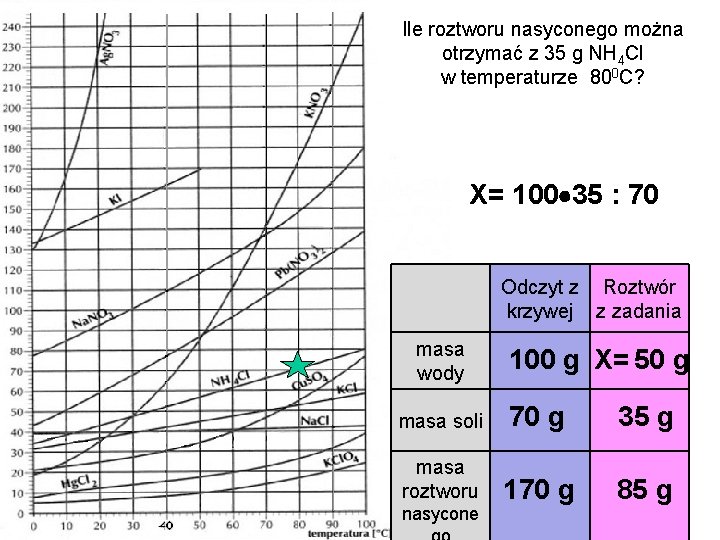
Ile roztworu nasyconego można otrzymać z 35 g NH 4 Cl w temperaturze 800 C? X= 100 35 : 70 Odczyt z Roztwór krzywej z zadania masa wody 100 g X= 50 g masa soli 70 g 35 g masa roztworu 170 g 85 g nasycone
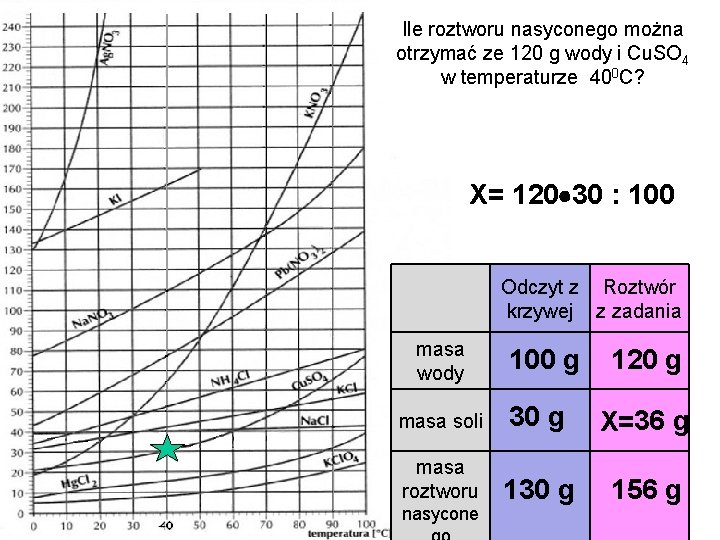
Ile roztworu nasyconego można otrzymać ze 120 g wody i Cu. SO 4 w temperaturze 400 C? X= 120 30 : 100 Odczyt z Roztwór krzywej z zadania masa wody 100 g 120 g masa soli 30 g X=36 g masa roztworu 130 g 156 g nasycone
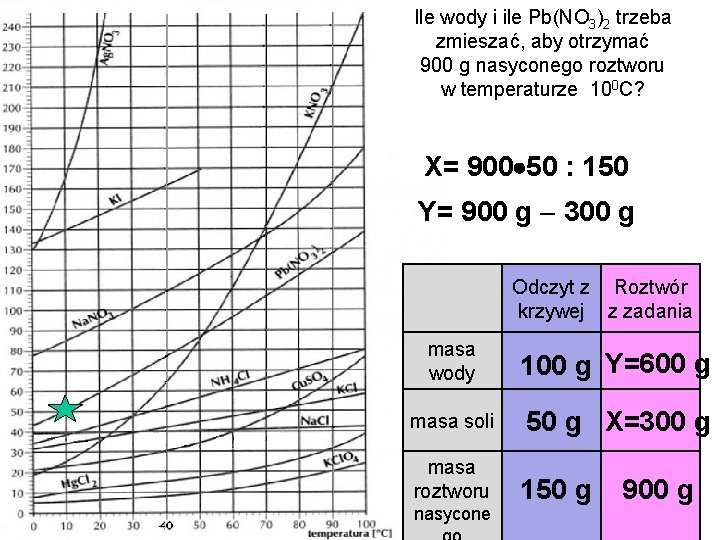
Ile wody i ile Pb(NO 3)2 trzeba zmieszać, aby otrzymać 900 g nasyconego roztworu w temperaturze 100 C? X= 900 50 : 150 Y= 900 g 300 g Odczyt z Roztwór krzywej z zadania masa wody 100 g Y=600 g masa soli 50 g X=300 g masa roztworu 150 g nasycone 900 g
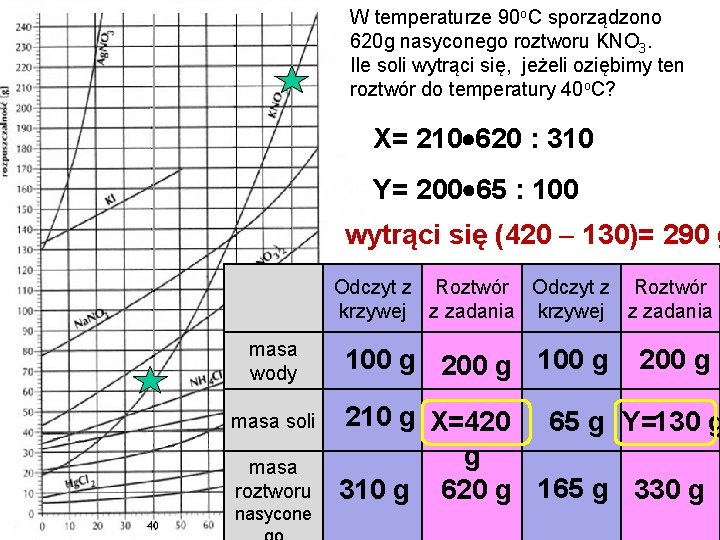
W temperaturze 90 o. C sporządzono 620 g nasyconego roztworu KNO 3. Ile soli wytrąci się, jeżeli oziębimy ten roztwór do temperatury 40 o. C? X= 210 620 : 310 Y= 200 65 : 100 wytrąci się (420 130)= 290 g Odczyt z Roztwór krzywej z zadania masa wody masa soli masa roztworu nasycone 100 g 200 g 210 g X=420 65 g Y=130 g g 310 g 620 g 165 g 330 g
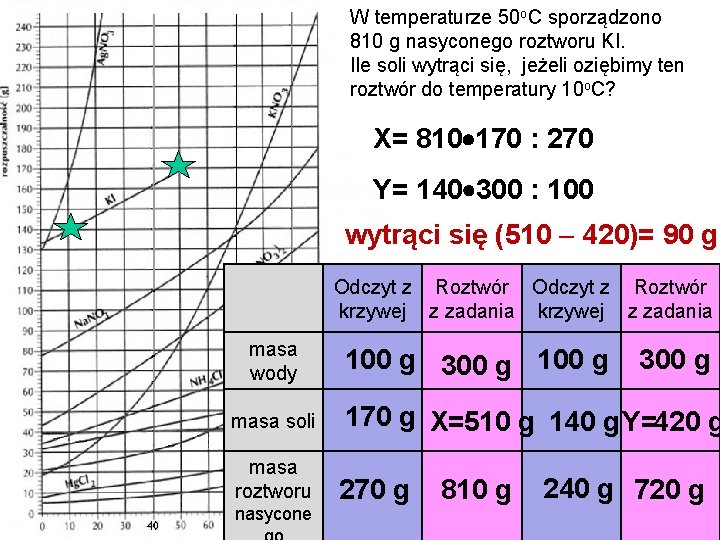
W temperaturze 50 o. C sporządzono 810 g nasyconego roztworu KI. Ile soli wytrąci się, jeżeli oziębimy ten roztwór do temperatury 10 o. C? X= 810 170 : 270 Y= 140 300 : 100 wytrąci się (510 420)= 90 g Odczyt z Roztwór krzywej z zadania masa wody 100 g 300 g masa soli 170 g X=510 g 140 g Y=420 g masa roztworu 270 g nasycone 810 g 240 g 720 g
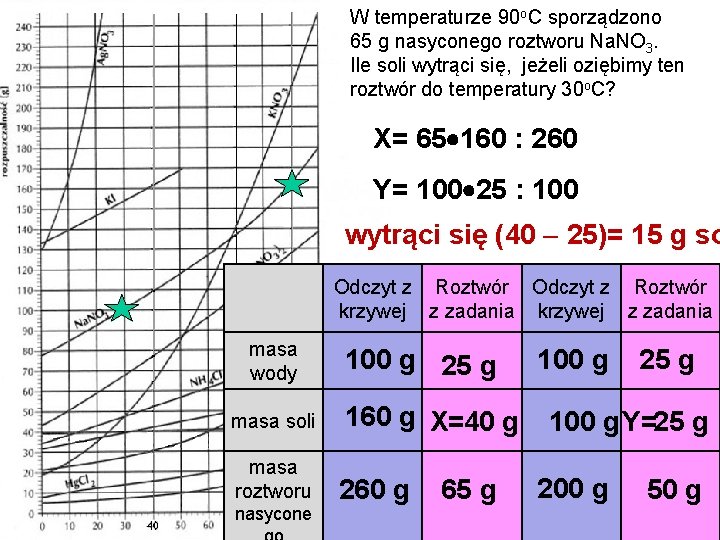
W temperaturze 90 o. C sporządzono 65 g nasyconego roztworu Na. NO 3. Ile soli wytrąci się, jeżeli oziębimy ten roztwór do temperatury 30 o. C? X= 65 160 : 260 Y= 100 25 : 100 wytrąci się (40 25)= 15 g so Odczyt z Roztwór krzywej z zadania masa wody 100 g 25 g masa soli 160 g X=40 g masa roztworu 260 g nasycone 65 g 100 g 25 g 100 g Y=25 g 200 g 50 g

Rozwiązywanie zadań dotyczących stężeń procentowych soli z wykorzystaniem proporcjonalności

100 % – Cp Oblicz stężenie procentowe 280 g roztworu, mw jeżeli po jego odparowaniu pozostało 70 g soli. X = 70 100 / : 280 ms 70 g X = Cp mr 280 g 100 % X = 25 % Odp. Stężenie procentowe tego roztworu wynosi 25 %
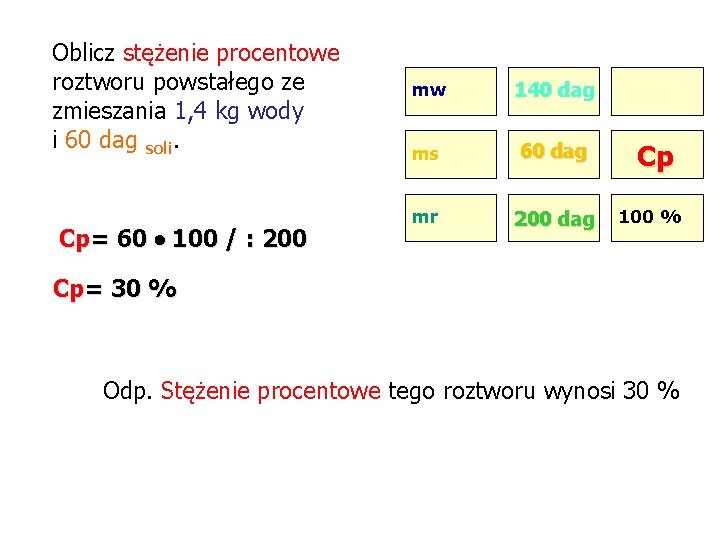
Oblicz stężenie procentowe roztworu powstałego ze zmieszania 1, 4 kg wody i 60 dag soli. Cp= 60 100 / : 200 mw 140 dag ms 60 dag mr 200 dag Cp 100 % Cp= 30 % Odp. Stężenie procentowe tego roztworu wynosi 30 %

Ile wody i ile soli potrzeba do otrzymania 8 kg 5 % -owej solanki Y= 8 5 / : 100 = 0, 4 kg X 95 % ms Y 5% mr 8 kg mw X = 8 kg – 0, 4 kg = 7, 6 kg Odp. Potrzeba 7, 6 kg wody i 0, 4 kg soli. 100 %

Ile wody wlać do 400 g soli, aby otrzymać solankę o stężeniu 20 % X = 400 80 / : 20 = 1600 g mw X ms 400 g mr 80 % 100 % Odp. Trzeba wlać 1600 g wody. Ile cukru trzeba wsypać do 3 litrów wody, aby otrzymać roztwór o stężeniu 40 % X = 40 3 / : 60 = 2 kg mw 3 kg 60 % ms X 40 % mr Odp. Trzeba wsypać 2 kg cukru. 100 %
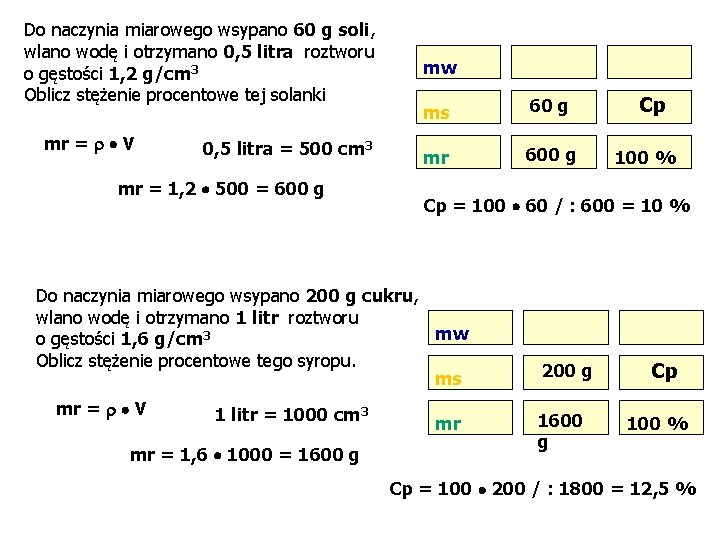
Do naczynia miarowego wsypano 60 g soli, wlano wodę i otrzymano 0, 5 litra roztworu o gęstości 1, 2 g/cm 3 Oblicz stężenie procentowe tej solanki mr = V 0, 5 litra = 500 cm 3 mr = 1, 2 500 = 600 g mw ms 60 g mr 600 g 1 litr = 1000 cm 3 mr = 1, 6 1000 = 1600 g 100 % Cp = 100 60 / : 600 = 10 % Do naczynia miarowego wsypano 200 g cukru, wlano wodę i otrzymano 1 litr roztworu mw o gęstości 1, 6 g/cm 3 Oblicz stężenie procentowe tego syropu. ms mr = V Cp mr 200 g 1600 g Cp 100 % Cp = 100 200 / : 1800 = 12, 5 %
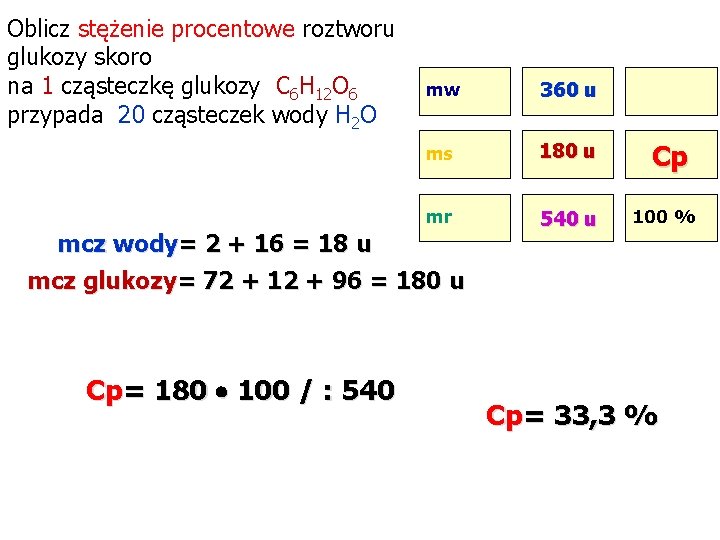
Oblicz stężenie procentowe roztworu glukozy skoro na 1 cząsteczkę glukozy C 6 H 12 O 6 przypada 20 cząsteczek wody H 2 O mw 360 u ms 180 u mr 540 u mcz wody= 2 + 16 = 18 u Cp 100 % mcz glukozy= 72 + 12 + 96 = 180 u Cp= 180 100 / : 540 Cp= 33, 3 %

Rozcieńczanie roztworów przez dolanie wody Oblicz stężenie procentowe roztworu powstałego przez dolanie 20 g wody do 140 g 40 % - owej solanki. 60 % mw ms mr X =56 g 40 % 140 g 100 % X = 140 40 / : 100 X = 56 g soli mw ms 56 g Cp mr 160 g 100 % Cp = 100 56 / : 160 Cp = 35 %

Rozcieńczanie roztworów przez wytrącenie soli Oblicz stężenie procentowe roztworu powstałego przez wytrącenie 20 g soli z 240 g 25 % - owej solanki 75 % mw ms mr X = 60 g 25 % 240 g 100 % X = 240 25 / : 100 X = 60 g soli mw ms 40 g Cp mr 220 g 100 % Cp = 100 40 / : 220 Cp = 18, 2 %

przez dosypanie soli Zatężanie roztworów Oblicz stężenie procentowe roztworu powstałego przez dosypanie 30 g soli do 45 dag 4 % - owej solanki 96 % mw ms mr X = 18 g 4 % 450 g 100 % X = 450 4 / : 100 X = 18 g soli mw ms 48 g Cp mr 480 g 100 % Cp = 100 48 / : 480 Cp = 10 %
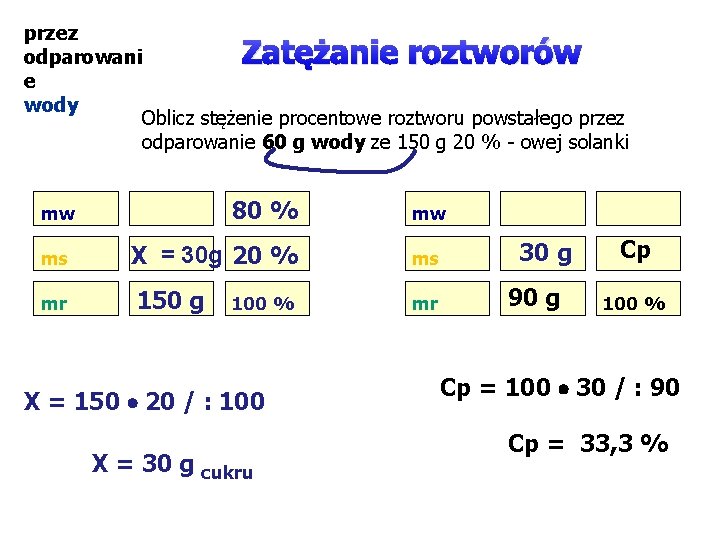
przez odparowani e wody Oblicz stężenie procentowe roztworu powstałego przez odparowanie 60 g wody ze 150 g 20 % - owej solanki Zatężanie roztworów 80 % mw ms mr X = 30 g 20 % 150 g 100 % X = 150 20 / : 100 X = 30 g cukru mw ms mr 30 g 90 g Cp 100 % Cp = 100 30 / : 90 Cp = 33, 3 %

Mieszanie roztworów Oblicz stężenie procentowe roztworu powstałego przez zmieszanie dwóch solanek : 60 g 5 %- owego roztworu z 75 g 20 % - owego roztworu. 95 % mw ms mr X = 3 g 5 % 60 g X = 15 g 20 % ms 100 % 75 g mr X = 60 5 / : 100 % X = 75 20 / : 100 X = 3 g soli Cp = 80 % mw X = 15 g soli ( 3 g + 15 g ) ● 100 % 60 g + 75 g Cp = 13, 3 %

Ile wody trzeba wlać do 1 kg solanki (10%) aby otrzymać 4 % - owy roztwór soli mw m kwasu 900 g + X 96 % 100 g mr 4% 1000 g + X X = dolana woda 1000 g + X = 10000 : 4 1000 g + X = 2500 g 0% 10 % 4% 6 jm = 1, 5 kg 4 jm = 1 kg X = 1500 g Odp. Do 1 kg 10 % - owej solanki trzeba wlać 1500 g wody

Ile mw (10%) trzeba wlać do 2 kg wody aby otrzymać 5 % - owy roztwór solanki 2 kg + 0, 9 X m kwasu 95 % 0, 1 X 5% 100 % mr 0% X = dolana solanka 0, 1 X = 5 (2 + 0, 9 X) / : 95 95 • 0, 1 X = 5 (2 + 0, 9 X) 9, 5 X = 10 + 4, 5 X 10 % 5 X = 10 5% 5 jm = 2 kg 5 jm = 2 kg X = 2 kg Odp. Do 2 kg wody trzeba wlać 2 kg solanki 10 % - owej.
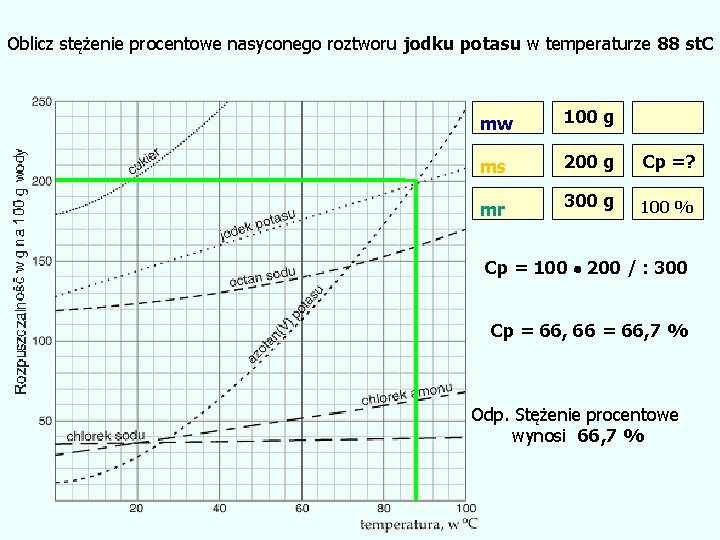
Oblicz stężenie procentowe nasyconego roztworu jodku potasu w temperaturze 88 st. C mw 100 g ms 200 g Cp =? mr 300 g 100 % Cp = 100 200 / : 300 Cp = 66, 66 = 66, 7 % Odp. Stężenie procentowe wynosi 66, 7 %
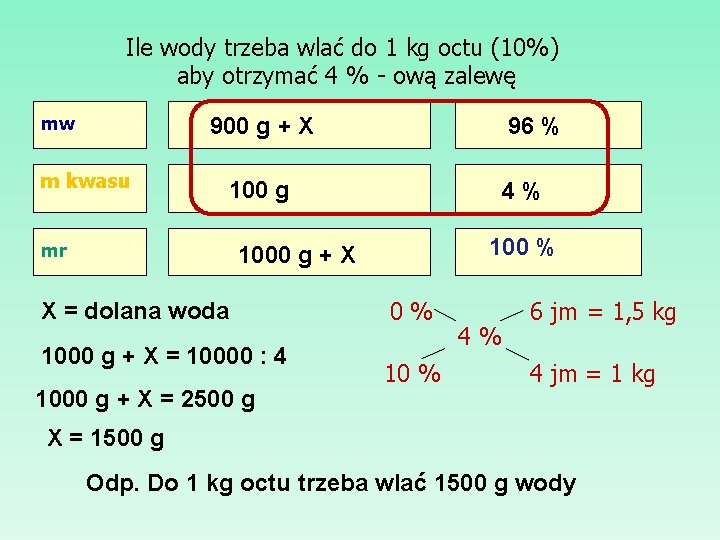
Ile wody trzeba wlać do 1 kg octu (10%) aby otrzymać 4 % - ową zalewę mw 900 g + X m kwasu 96 % 100 g mr 4% 1000 g + X X = dolana woda 1000 g + X = 10000 : 4 1000 g + X = 2500 g 0% 10 % 4% 6 jm = 1, 5 kg 4 jm = 1 kg X = 1500 g Odp. Do 1 kg octu trzeba wlać 1500 g wody

Ile octu (10%) trzeba wlać do 2 kg wody aby otrzymać 5 % - ową zalewę mw 2 kg + 0, 9 X m kwasu 95 % 0, 1 X 5% 100 % mr 0% X = dolany ocet 0, 1 X = 5 (2 + 0, 9 X) / : 95 95 • 0, 1 X = 5 (2 + 0, 9 X) 9, 5 X = 10 + 4, 5 X 10 % 5 X = 10 5% 5 jm = 2 kg 5 jm = 2 kg X = 2 kg Odp. Do 2 kg wody trzeba wlać 2 kg octu.
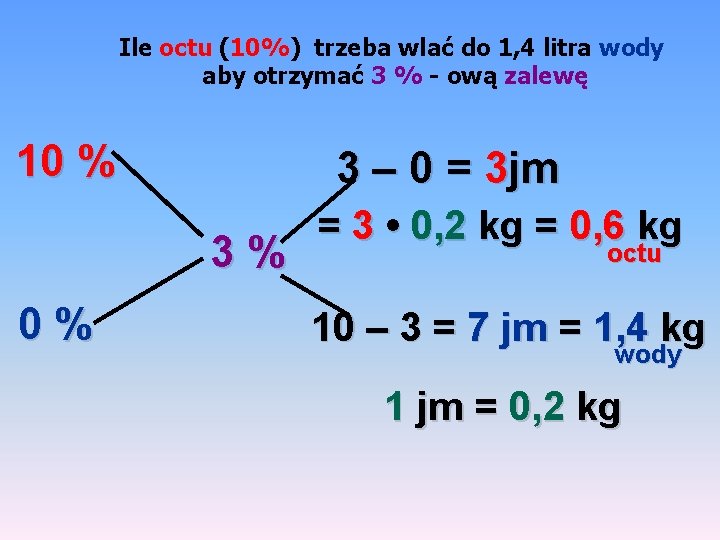
Ile octu (10%) trzeba wlać do 1, 4 litra wody aby otrzymać 3 % - ową zalewę 10 % 3 – 0 = 3 jm 3% 0% = 3 • 0, 2 kg = 0, 6 kg octu 10 – 3 = 7 jm = 1, 4 kg wody 1 jm = 0, 2 kg
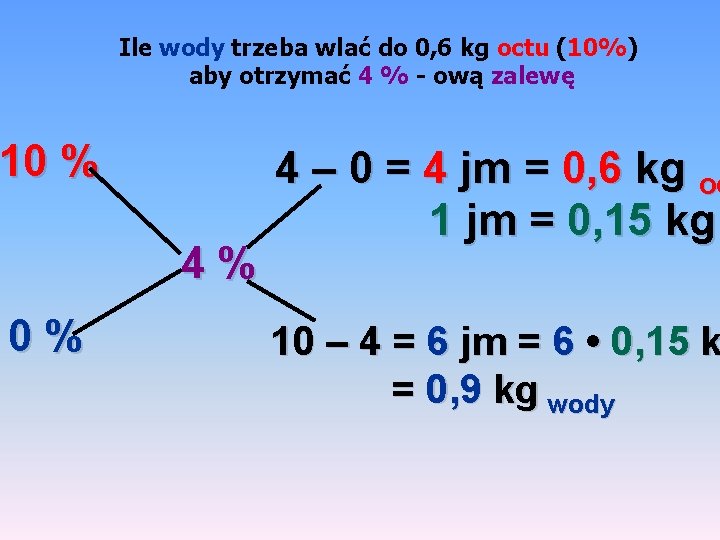
Ile wody trzeba wlać do 0, 6 kg octu (10%) aby otrzymać 4 % - ową zalewę 10 % 4% 0% 4 – 0 = 4 jm = 0, 6 kg oc 1 jm = 0, 15 kg 10 – 4 = 6 jm = 6 • 0, 15 k = 0, 9 kg wody
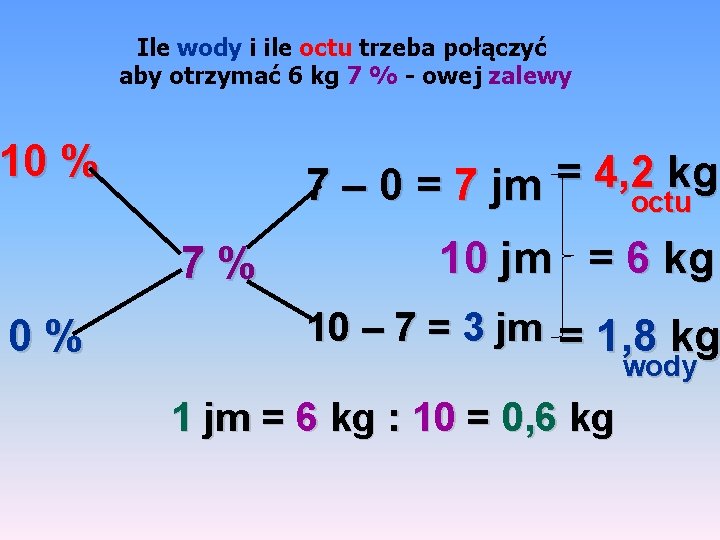
Ile wody i ile octu trzeba połączyć aby otrzymać 6 kg 7 % - owej zalewy 10 % kg 7 – 0 = 7 jm = 4, 2 octu 7% 0% 10 jm = 6 kg 10 – 7 = 3 jm = 1, 8 kg wody 1 jm = 6 kg : 10 = 0, 6 kg


Gejzer - rodzaj gorącego źródła, które gwałtownie wyrzuca słup wody i pary wodnej o temperaturze około 100° C






Zapora wodna może być postawiona dla różnych celów: * dla ochrony przeciwpowodziowej * dla uzyskania energii * jako rezerwuar wody * dla walorów rekreacyjnych



ms • 100% _____ Cp = mr ms • 100% mr =_____ Cp ms • 100% = Cp • mr _____ ms = 100% Ile 4% - owej solanki otrzymano z 1 kg Ile soli trzeba wsypać do wody, aby otrzymać 300 g 15 % - owej solanki? 15% • 300 g _____ ms = 100% ms = 45 g 25 1 kg • 100% mr =_____ 4% mr = 25 kg

ms • 100% _____ Cp = ms + mw ms • 100% ms + mw =_____ Cp ms • 100% –ms • Cp _________ mw = Cp ms (100% – Cp ________ mw = Cp ms • (100% – Cp ) = mw • ms • 100% _____ – ms mw = Cp ms • 100% ms • Cp __________ – mw = Cp Cp mw • Cp _____ ms = 100% – Cp
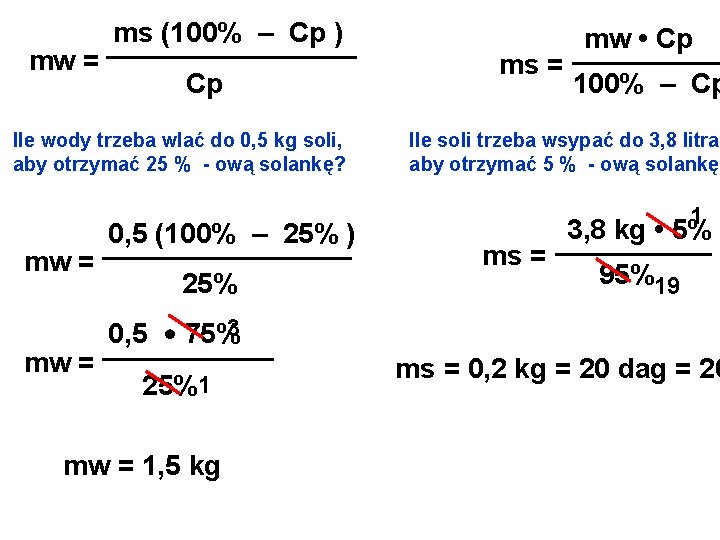
ms (100% – Cp ) ________ mw = Cp Ile wody trzeba wlać do 0, 5 kg soli, aby otrzymać 25 % - ową solankę? 0, 5 (100% – 25% ) ________ mw = 25% 3 0, 5 • 75% ______ mw = 25%1 mw = 1, 5 kg mw • Cp _____ ms = 100% – Cp Ile soli trzeba wsypać do 3, 8 litra aby otrzymać 5 % - ową solankę? 1 3, 8 kg • 5% _____ ms = 95%19 ms = 0, 2 kg = 20 dag = 20

soli trzeba dosypać do 10 kg 4% - owej sola Ile wody odparuje z 1 tony 9% - owej Ile solanki aby powstał 20%- owy roztwór soli? Skoro w wyniku tego odparowania powstaje 30%- owy roztwór soli? Cp • mr _____ ms = 100% 9 • 1000 kg _____ ms = 100 ms = 90 kg 90 • 100 _____ 30 = 1000 – x 30 (1000 – x) = 9000 30 000 – 30 x = 9000 21 000 = 30 x x = 700 kg 4 • 10 000 g _____ ms = 100 ms = 400 g (400 + x) • 100 _______ 20 = 10 000 + x 20 (10 000 + x) = 40 000 + 100 x 200 000 + 20 x = 40 000 + 100 x 160 000 = 80 x x = 160 000 : 80 = 2 000 g = 2 kg
- Slides: 72