Wet van BoyleMariotte 1 e wet van GayLussac
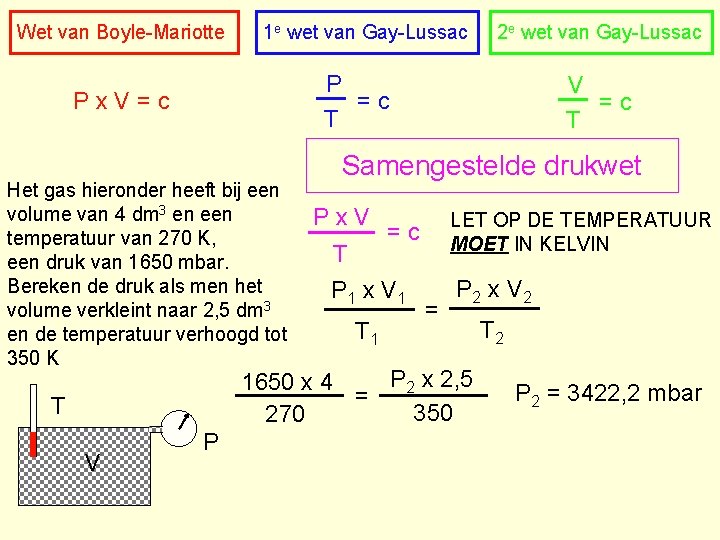
Wet van Boyle-Mariotte 1 e wet van Gay-Lussac P =c T Px. V=c Het gas hieronder heeft bij een volume van 4 dm 3 en een temperatuur van 270 K, een druk van 1650 mbar. Bereken de druk als men het volume verkleint naar 2, 5 dm 3 en de temperatuur verhoogd tot 350 K V =c T Samengestelde drukwet Px. V T P 1 x V 1 T 1 LET OP DE TEMPERATUUR MOET IN KELVIN =c = P 2 x V 2 P 2 x 2, 5 1650 x 4 = 350 270 T V 2 e wet van Gay-Lussac P T 2 P 2 = 3422, 2 mbar

Voorbeeldopgave 1 Een afgesloten hoeveelheid ideaal gas heeft bij een temperatuur van 150 0 C een volume van 40 L en een druk van 300 h. Pa. Bereken de spanning van het gas als men het afkoelt tot -70 0 C en het volume verkleint tot 5 L. P 1 x V 1 T 1 300 x 40 423 = = P 2 x V 2 150 0 C =. . . K T 2 P 2 x 5 203 P 2 = 1151, 8 h. Pa T = t + 273 T = 150 + 273 T = 423 K -70 0 C =. . . K T = t + 273 T = -70 + 273 T = 203 K

Voorbeeldopgave 2 Een afgesloten hoeveelheid ideaal gas heeft bij een temperatuur van -23 0 C een druk van 3 bar. Bereken de druk van het gas als men het bij gelijkblijvend volume verhit tot 227 0 C. P 1 x V 1 T 1 3 x V 1 250 = = P 2 x V 2 T 2 P 2 x V 2 500 P 2 = 6 bar

Voorbeeldopgave 3 Een afgesloten hoeveelheid ideaal gas heeft een volume van 40 dm 3 en een druk van 2, 5 N/cm 2. Bereken de gasdruk die dit gas bij de onderstaande volumes krijgt. De temperatuur blijft tijdens het veranderen van de volumes op 270 C. V(dm 3) P(N/cm 2) 10 20 40 60 80 10 5 2, 5 1, 67 1, 25 1 Teken met behulp van de gegevens uit de tabel een P - V diagram
- Slides: 4