Webapplikcik s mobilapplikcik a kmiai ktsek tantsban Webbased

Web-applikációk és mobil-applikációk a kémiai kötések tanításában Web-based a mobilné aplikácie vo vyučovaní teórie chemickej väzby Dr. habil. Paed. Dr. Juhász György, Ph. D. • Projekt KEGA č. 002 UJS-4/2016 • „Web-based aplikácie v transdisciplinárnom vzdelávaní budúcich učiteľov“

Kötéselméletek - bevezetés • • Az atomok és a molekulák egymás közti kölcsönhatásainak az eredménye azon erők összessége, amelyek a kémiai kötés kialakulásához vezetnek, meghatározzák a molekulák térszerkezetét és ezzel az egyes molekulák tulajdonságait és funkcióit. Klasszikus kötéselméletek: Kössel féle kötéselmélet : az atomok a külső elektronhéjon (vegyértékhéj)lévő elektronok segítségével kötődnek és a legközelebbi nemesgáz konfigurációját igyekeznek felvenni – ionok keletkezése – elektrosztatikus kölcsönhatás - kötés kialakulása Lewis féle kötéselmélet: két azonos atom közti kötés kialakulásánál a 2 atomtól származó 2 kötőelektron a két atom közös elektronpárját alkotja (Lewis féle kötőelektronpár). Lewis bevezette a kovalens kötés fogalmát és a többszörös kötés fogalmát is. Ezek az elméletek azonban nem magyarázzák meg a kémiai kötés kialakulásának lényegét. Ezt csak a hullámmechanikai ismeretek tették lehetővé.

Kötéselméletek - bevezetés • A de Broglie egyenlet a mikrorészecskék hullámmechanikájának alapegyenlete. Ha az elektron E összenergiája a kinetikai és a potenciális energiából tevődik össze, akkor a v sebességel mozgó elektronr λ hullámhosszára a következő kifejezést kapjuk: • Az elektron hullámjellegét 1925 -ben Erwin Schrödinger fogalmazta meg az ő nevét viselő hullámegyenletében (Schrödinger egyenlet - SE): • Ebben az egyenletben egy új változó szerepel – hullámfüggvény ψ, amely az elektront írja le, miközben az elektron helyzetének a függvénye. A klasszikus mechanikában a hullámfüggvény négyzete az energiasűrűséget adja meg, a hullámmechanikai értelmezés szerint a ψ2 a statisztikailag vett átlagos elektronsűrűséget adja meg. •

Kötéselméletek - bevezetés • A SE megoldásaként az energiaminimumokhoz tartozó különböző E energiaértékeket kapunk a hozzátartozó ψ hullámfüggvényekkel. A alakban felírt hullámfüggvényt atomi pályának (atomorbitálnak) nevezzük, ahol a n, l, ml a kvantumszámok • Ha az elektron állapotát a hullámfüggvény írja le, akkor azt mondjuk, hogy az elektron a megfelelő kvantumszámokkal megadott atomi pályán tartózkodik. A kép forrása: http: //chem. libretexts. org/@api/deki/files/8855/Single_electron_orbitals. jpg
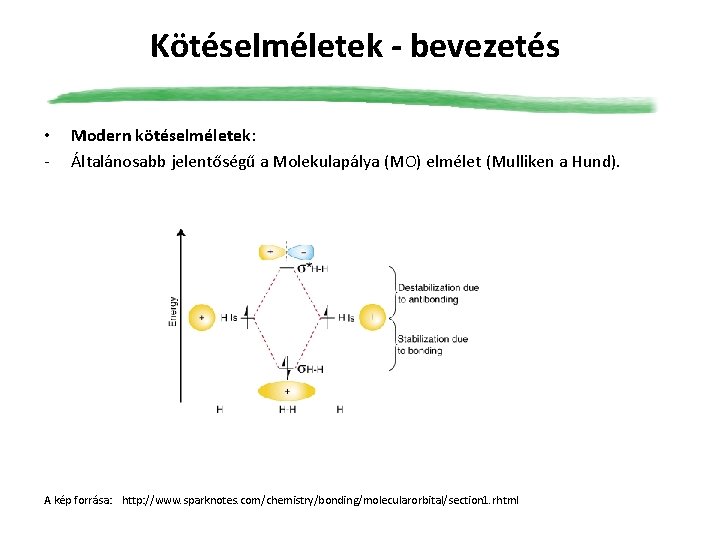
Kötéselméletek - bevezetés • - Modern kötéselméletek: Általánosabb jelentőségű a Molekulapálya (MO) elmélet (Mulliken a Hund). A kép forrása: http: //www. sparknotes. com/chemistry/bonding/molecularorbital/section 1. rhtml

Kötéselméletek – Hückel féle MO elmélet A konjugált molekulák –molekulapályáinak számításaival Erich Hückel foglalkozott. Az általa bevezetett közelítő módszer segítségével megszerkeszthetjük a – molekulapályák energiadiagramját, és kiszámíthatjuk az egyes pályakoefficienseket is. A Hückel-féle megközelítésben a –molekulapályákat a σ– molekulapályáktól függetlenül vizsgáljuk. A σ– molekulapályák adják az egyes molekulák vázát, amely meghatározza a molekula térbeli elrendeződését is.

Kötéselméletek – Hückel féle MO elmélet A molekula vázában minden C atomot azonos módon kezelünk, így a kételektronintegrálokat (Coulombintegrálokat), melyekben a pályák egy atomon vannak, azonosnak tekintjük és -val jelöljük. A Coulomb-féle integrál egyszerűsített formában az elektron potenciális energiájaként interpretálható. A kétatomos kételektronintegrálok közül azokat, melyek egymáshoz σ-kötéssel kötött atomok között vannak, β -val jelöljük. Pl. az etén esetében, ha a σ–vázat rögzítettnek vesszük, akkor a számításokat csak a 2 – molekulapálya jellemzőinek meghatározására összpontosítjuk.

Kötéselméletek – Hückel féle MO elmélet • Az egyenletekben a ψA, ψB, ψC, ψD, az A, B, C, D szénatomokon centrált 2 pz atompályák hullámfüggvényei a c. A, c. B, c. C, c. D pedig az adott C atomok kiszámított együtthatói.

Kötéselméletek – Hückel féle MO elmélet • • A Hückel féle megközelítésnél az optimális energiákat és együtthatókat az ún. variációs módszerrel határozzuk meg, amelynél felírjuk az ún. szekuláris determinánst ( A= B= C= D= egyszerűsítéssel), amely egyenlő nullával. Az etén esetében a szekuláris determináns a következő:

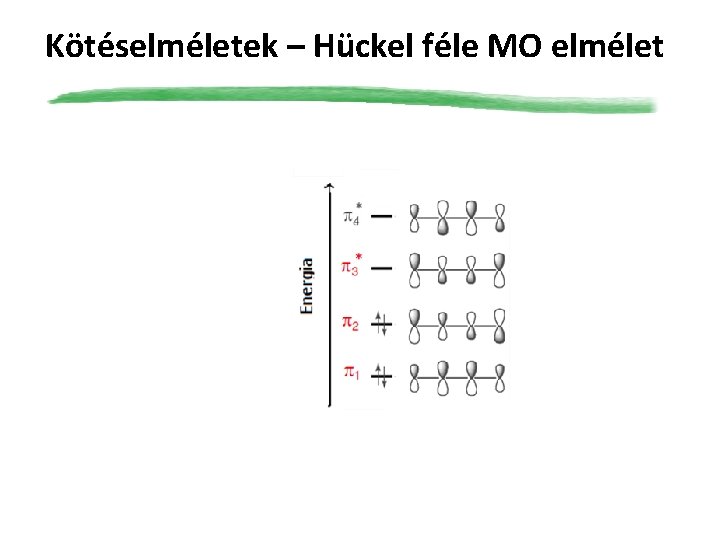
Kötéselméletek – Hückel féle MO elmélet
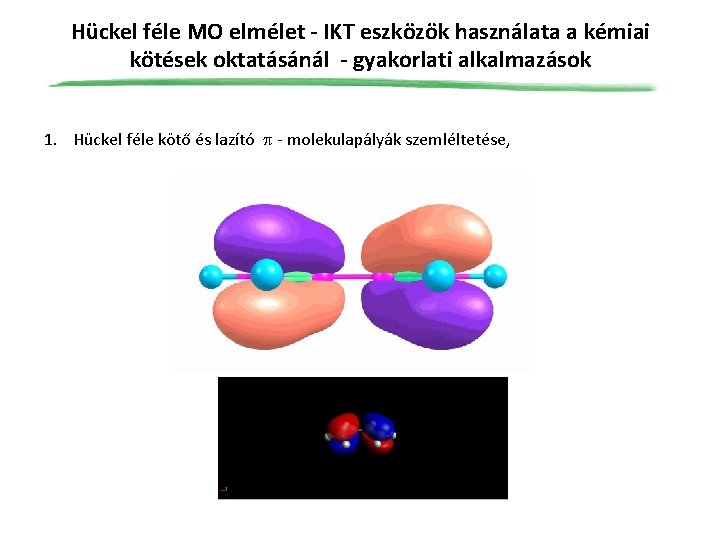
Hückel féle MO elmélet - IKT eszközök használata a kémiai kötések oktatásánál - gyakorlati alkalmazások 1. Hückel féle kötő és lazító - molekulapályák szemléltetése,

Hückel féle MO elmélet - IKT eszközök használata a kémiai kötések oktatásánál - gyakorlati alkalmazások 2. Woodward, Hoffmann és Fukui péle szabályok - periciklusos reakciók Juhász, J. , Matulík, D. , Obrcian, M. , : Pericyklické reakcie - počítačom podporovaná výučba, In: Zborník 1 príspevkov 51. zjazdu Chemických spoločností, Nitra, 1999, K-P 15

Köszönöm a figyelmet! Paed. Dr. Juhász György, Ph. D.
- Slides: 14