Wat is het verband tussen p H en

Wat is het verband tussen p. H en concentraties? Uitleg over p. H, p. OH, [H+] en [OH−]
![De p. H-schaal is een logaritmische (exponentiële) schaal: [H 3 O+] (M) p. H De p. H-schaal is een logaritmische (exponentiële) schaal: [H 3 O+] (M) p. H](http://slidetodoc.com/presentation_image_h2/78b050b0741925cac0e2035d1ec78a7e/image-2.jpg)
De p. H-schaal is een logaritmische (exponentiële) schaal: [H 3 O+] (M) p. H 1 100 0 0, 1 10− 1 1 0, 01 10− 2 2 etc. … 10− 7 7 etc. … 10− 12 12 10− 13 13 10− 14 14 0, 0000001

De definitie van p. H is dus: p. H = − log [H 3 O+] Wat hetzelfde is als: p. H = − log [H+]
![Er is in water en in oplossingen een verband tussen [H 3 O+] en Er is in water en in oplossingen een verband tussen [H 3 O+] en](http://slidetodoc.com/presentation_image_h2/78b050b0741925cac0e2035d1ec78a7e/image-4.jpg)
Er is in water en in oplossingen een verband tussen [H 3 O+] en [OH−] : [H 3 O+] x [OH−] = 1, 00 x 10− 14 (bij 298 K) dus…
![Hiermee kunnen we in elke oplossing een verband aangeven tussen [H 3 O+] en Hiermee kunnen we in elke oplossing een verband aangeven tussen [H 3 O+] en](http://slidetodoc.com/presentation_image_h2/78b050b0741925cac0e2035d1ec78a7e/image-5.jpg)
Hiermee kunnen we in elke oplossing een verband aangeven tussen [H 3 O+] en [OH−] : [H 3 O+] (M) p. H [OH−] (M) 1 100 0 10− 14 0, 1 10− 13 0, 01 10− 2 2 10− 12 … … … 10− 7 7 10− 7 … … … 10− 12 12 10− 13 13 10− 14 14 100 0, 0000001 [OH−] (M)
![De definitie van p. OH is: p. OH = − log [OH−] dus… De definitie van p. OH is: p. OH = − log [OH−] dus…](http://slidetodoc.com/presentation_image_h2/78b050b0741925cac0e2035d1ec78a7e/image-6.jpg)
De definitie van p. OH is: p. OH = − log [OH−] dus…
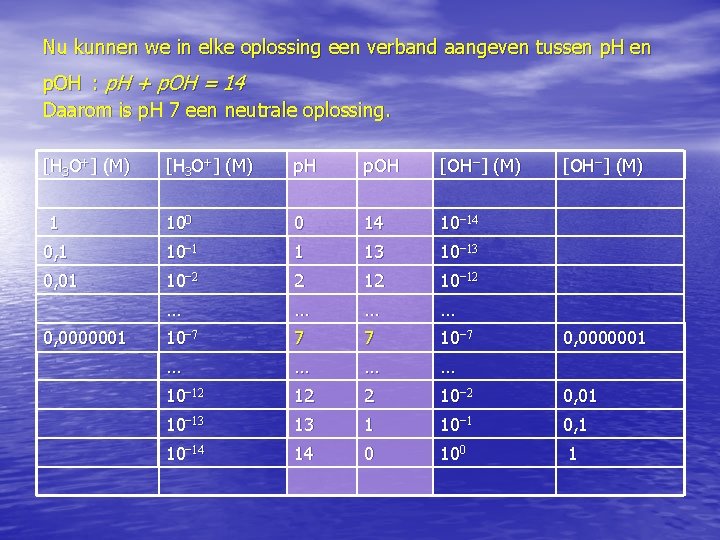
Nu kunnen we in elke oplossing een verband aangeven tussen p. H en p. OH : p. H + p. OH = 14 Daarom is p. H 7 een neutrale oplossing. [H 3 O+] (M) p. H p. OH [OH−] (M) 1 100 0 14 10− 14 0, 1 10− 1 1 13 10− 13 0, 01 10− 2 2 12 10− 12 … … 10− 7 7 7 10− 7 … … 10− 12 12 2 10− 2 0, 01 10− 13 13 1 10− 1 0, 1 10− 14 14 0 100 1 0, 0000001 [OH−] (M) 0, 0000001
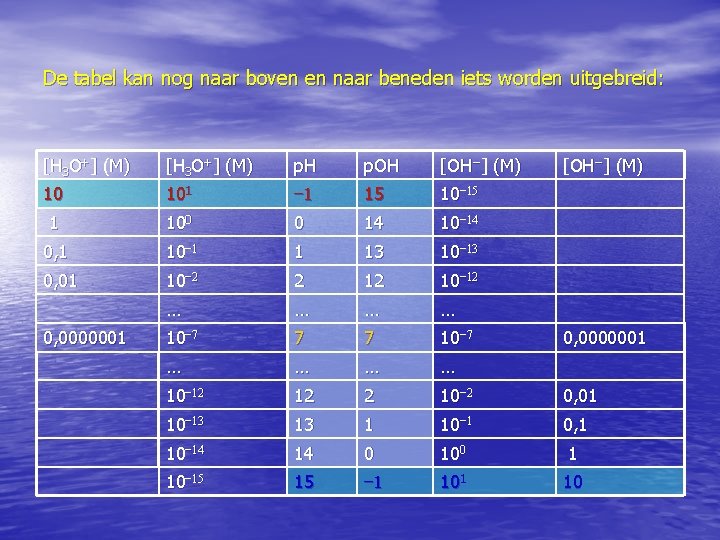
De tabel kan nog naar boven en naar beneden iets worden uitgebreid: [H 3 O+] (M) p. H p. OH [OH−] (M) 10 101 − 1 15 10− 15 1 100 0 14 10− 14 0, 1 10− 1 1 13 10− 13 0, 01 10− 2 2 12 10− 12 … … 10− 7 7 7 10− 7 … … 10− 12 12 2 10− 2 0, 01 10− 13 13 1 10− 1 0, 1 10− 14 14 0 100 1 10− 15 15 − 1 10 0, 0000001 [OH−] (M) 0, 0000001

Bij andere waarden voor de concentraties dan 1 - 0, 01 etc. gebruik je de formule en je rekenmachine: • Om de p. H uit te rekenen van zure oplossingen: p. H = − log [H+] • Om de p. H uit te rekenen van basische oplossingen: p. OH = − log [OH−] en p. H + p. OH = 14, 00
![dus… bijvoorbeeld: [H+] = 0, 030 M → p. H = − log(0, 030) dus… bijvoorbeeld: [H+] = 0, 030 M → p. H = − log(0, 030)](http://slidetodoc.com/presentation_image_h2/78b050b0741925cac0e2035d1ec78a7e/image-10.jpg)
dus… bijvoorbeeld: [H+] = 0, 030 M → p. H = − log(0, 030) = 1, 52 [OH−] = 0, 0065 M → p. OH = − log(0, 0065) = 2, 19 p. H = 14, 00 − 2, 19 = 11, 81

Om uit de p. H de concentraties te berekenen, gebruik je de formules (staan ook in BINAS 38 A): [H 3 O+] = 10−p. H M en [OH−] = 10−p. OH M
![dus… bijvoorbeeld: • Bij een zure oplossing: p. H = 3, 3 → [H+] dus… bijvoorbeeld: • Bij een zure oplossing: p. H = 3, 3 → [H+]](http://slidetodoc.com/presentation_image_h2/78b050b0741925cac0e2035d1ec78a7e/image-12.jpg)
dus… bijvoorbeeld: • Bij een zure oplossing: p. H = 3, 3 → [H+] = 10− 3, 3 M = 5 x 10− 4 M • Bij een basische oplossing: p. H = 10, 3 → p. OH = (14, 00 − 10, 3) = 3, 7 [OH−] = 10− 3, 7 M = 2 x 10− 4 M →
- Slides: 12