Wasserstoff Andreas Bachofner01 27 03 2015 Andreas Bachofner01

Wasserstoff Andreas Bachofner/01 27. 03. 2015 Andreas Bachofner/01 Wasserstoff 1

Geschichte �Entdeckung im 16. Jahrhundert �Hydrogéne von hydro=Wasser und gennáo=erzeugen �Entdeckung der Isotope in den frühen 1930 er Jahren Andreas Bachofner/01 Wasserstoff 2

Allgemeine Eigenschaften �Besteht aus 1 Proton und 1 Elektron �Ordnungszahl 1 �Geringste Dichte �Farb- und geruchlos bei Zimmertemperatur �Sehr tiefe Schmelz- und Siedetemperatur �Kommt meist als H 2 -Molekül vor � 2 Isotope: Deuterium und Tritium Andreas Bachofner/01 Wasserstoff 3

Löslichkeit von Wasserstoff �Löst sich nur schlecht in Flüssigkeiten �Löst sich gut in Metallen �Möglichkeit zur Wasserstoffspeicherung �Wasserstoff macht Metall Ø Spröde Ø Unempfindlich gegen Luft und Wasser Ø Eventuell zu Supraleitern Andreas Bachofner/01 Wasserstoff 4

Hydride �Kovalente Hydride �Salzartige Hydride �Metallische Hydride �Komplexe Übergangsmetallhydride Andreas Bachofner/01 Wasserstoff 5

Quelle: http: //www. youtube. com/watch? v=En 2 hk. Te. ICrc Andreas Bachofner/01 Wasserstoff 6

Vorkommen �Neunthäufigstes Element der Erde Ø Vorhanden in Meeren, fossilen Brennstoffen… Ø Erdmasse ist Grund für relativ geringe Häufigkeit �Fast ausschließlich in gebunder Form vorhanden �Häufigstes Element im Weltall Ø Vorhanden in Gasplaneten, Sonnen… Andreas Bachofner/01 Wasserstoff 7

Gewinnung �Spaltung von Wasser Ø Elektrolyse Ø Thermochemisches Verfahren �Gewinnung aus Kohlenwasserstoffen Ø Dampfreformierung Ø Partielle Oxidation Ø Wasserstoff aus Biomasse Ø Kvaerner-Verfahren �Biologische Verfahren �Sonstige Verfahren Ø Wasserstoff aus Metallen Andreas Bachofner/01 Wasserstoff 8

Elektrolyse �Anode und Kathode in Wasser �Sauerstoff bildet sich an Anode �Wasserstoff bildet sich an Kathode �Anschließendes Auffangen der Gase �Vorteile Ø Gute Umweltverträglichkeit Ø Sauerstoff kann auch abgefüllt werden �Nachteile Ø Hohe Kosten durch hohen Energiebedarf Andreas Bachofner/01 Wasserstoff 9
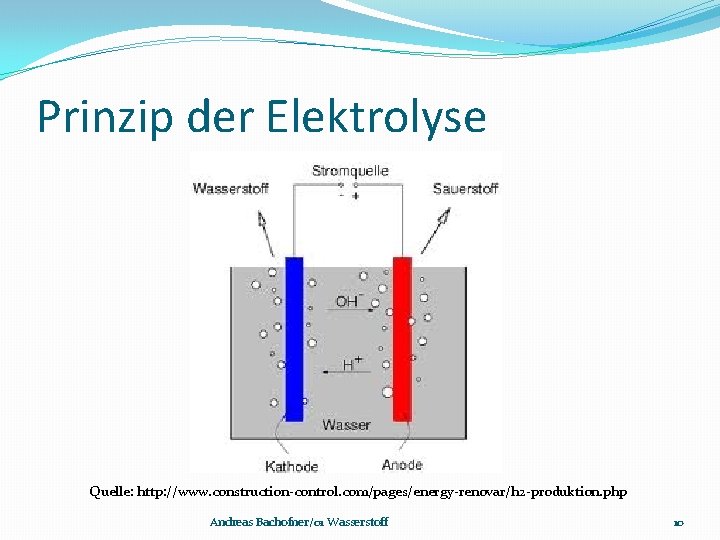
Prinzip der Elektrolyse Quelle: http: //www. construction-control. com/pages/energy-renovar/h 2 -produktion. php Andreas Bachofner/01 Wasserstoff 10

Thermochemisches Verfahren �Spaltung von Wasserdampf mithilfe von Hitze und Chemikalien �Benötigte Temperatur durch Katalysatoren bei 900°C �Schwefelsäure-Iod-Verfahren Ø 1. Schritt: Schwefeldioxid und Iod reagieren bei 120°C mit Wasserdampf zu Schwefelsäure und Iodwasserstoff Ø 2. Schritt: Iodwasserstoff spaltet sich bei 300° und Schwefelsäure bei 850°C Andreas Bachofner/01 Wasserstoff 11

Dampfreformierung �Umsetzung von Erdgas, Propan, Butan… � 1. Schritt: Ausgangsstoffe werden unter hohem Druck und hohen Temperaturen aufgespalten � 2. Schritt: Methan wird bei 800 -900°C unter 25 -30 bar mit Wasser zu Kohlenstoffmonoxid und Wasserstoff umgesetzt � 3. Schritt: Übriges Kohlenstoffmonoxid wird mit Wasser zu Wasserstoff und Kohlenstoffdioxid umgesetzt Andreas Bachofner/01 Wasserstoff 12

Dampfreformierung �Vorteile Ø Sehr wirtschaftliche Methode Ø Sehr weit verbreitet �Nachteile Ø Schadstoffemissionen sind mit Verbrennung der Ausgangsprodukte zu vergleichen Allgemeine Gleichung: Cn. Hm + n H 2 O (n + m/2) H 2 + n CO Beispiel Methan: CH 4 + H 2 O CO + 3 H 2; CO + H 2 O CO 2 + H 2 Andreas Bachofner/01 Wasserstoff 13

Partielle Oxidation �Umsetzen von Erdgas oder Heizöl unter Sauerstoffmangel durch teilweise Verbrennung in einem exothermen Prozess �Allgemeine Gleichung: Cn. Hm + n/2 O 2 n CO + m/2 H 2 �Beispiel Heizöl: C 12 H 24 + 6 O 2 12 CO + 12 H 2 Andreas Bachofner/01 Wasserstoff 14

Wasserstoff aus Biomasse �Funktioniert nach dem Prinzip der Dampfreformation �Statt fossilen Brennstoffen wird Biomasse umgesetzt �Vorteile Ø Hoher Sauerstoffgehalt von Biomasse Ø Beruht auf erneuerbaren Rohstoffen �Nachteile Ø Wirkungsgrad von 30 -40% Ø Starke Konkurrenz mit Biomasseverflüssigung Andreas Bachofner/01 Wasserstoff 15

Kvaerner-Verfahren �Spaltung von Kohlenwasserstoffen mit einem Plasmabrenner �Vorteile Ø Kohlenstoffdioxidfreie Produktion Ø Sehr hoher Wirkungsgrad (98%) Ø Wasserstoff, Aktivkohle und Heißdampf nutzbar Ø Mögliche Reaktionsgleichung: CH 4 C + 2 H 2 Andreas Bachofner/01 Wasserstoff 16

Biologische Verfahren �Produktion von Wasserstoff mithilfe von Algen �Vorteile Ø Komplette Umweltverträglichkeit �Nachteile Ø Große, sonnenbeschienene Flächen notwendig Ø Sehr kleiner Nutzungsgrad Andreas Bachofner/01 Wasserstoff 17

Wasserstoff aus Metallen �Erzeugung durch Lösen von Metallen in verdünnten Säuren �Geeignet für Erzeugung kleiner Mengen Wasserstoff für Labore �Beispiel: Zinkgranulat in verdünnter Salzsäure Andreas Bachofner/01 Wasserstoff 18

Verwendung �Energieträger �Kohlehydrierung �Reduktionsmittel �Ammoniakerzeugung �Lebensmittelzusatzstoff �Fetthärtung �Kühlmittel �Traggas Andreas Bachofner/01 Wasserstoff 19

Wasserstoff als Energieträger �Sekundärenergieträger �Gilt als möglicher Energieträger der Zukunft �Keine Energiequelle, da Wasserstoff erst produziert werden muss Andreas Bachofner/01 Wasserstoff 20

Wasserstoffverbrennungsmoto r �Funktioniert nach Prinzip des Otto-Motors �Zwei Verfahren Ø Saugrohr-Einspritzung Wasserstoff mit geringem Überdruck wird vergast und gezündet Ø Direkt-Einspritzung Wasserstoff mit hohem Druck wird direkt in die Brennkammer eingespritzt und gezündet bessere Füllung Andreas Bachofner/01 Wasserstoff 21

Wasserstoffverbrennungsmoto r �Vorteile Ø Verbrennungsprodukte sind Wasserdampf und Stickoxide (NOx) und nur Spuren von Kohlendioxid und Kohlenwasserstoffen Ø Besserer Wirkungsgrad als reine Benzinmotoren Ø Saubere Abgase; kein Feinstaub enthalten �Nachteile Ø Schlechtere Leistung als Benzinmotoren Ø Fehlzündungen möglich (bezieht sich nur auf Hubkolbenmotoren) Ø Wasserstoff greift Schmierstoffe an Ø Flüssiger Wasserstoff ist sehr kalt (ca. -250°C) Probleme bei Werkstoffwahl Andreas Bachofner/01 Wasserstoff 22

Brennstoffzelle �Prinzip der galvanischen Zelle �Verbunden durch äußeren Stromkreis �Getrennt durch protonendurchlässiges Membran �Vorteile Ø hoher Wirkungsgrad ( >50%; bei Abwärmenutzung bis zu 80%) Ø Keine Schadstoffemissionen Ø Geräuscharmut �Nachteile Ø Kurze Lebensdauer Ø Hohe Investitionskosten (Reduzierung durch Serienfertigung) Andreas Bachofner/01 Wasserstoff 23

Funktion der Brennstoffzelle Quelle: http: //www. diebrennstoffzelle. de/zelltypen/pemfc/funktion. shtml Andreas Bachofner/01 Wasserstoff 24

Wasserstoff als Raketentreibstoff �Bekanntes Beispiel: Space Shuttle-Programm �Vorteile Ø Hohe Energiedichte Ø Niedrige Masse �Nachteile Ø Schwierige kryogene Lagerung Andreas Bachofner/01 Wasserstoff 25

Kohlehydrierung �Verflüssigung von Kohle zu Treib- und Brennstoffen � 1. Möglichkeit Kohlenwasserstoffe werden direkt aus Wasserstoff und Kohle produziert � 2. Möglichkeit Kohle wird vergast und mit Wasserdampf und Sauerstoff zu Synthesegas umgesetzt das in Wasser und Kohlenwasserstoffe aufgespalten wird �Heute kaum von Bedeutung �Fand im Dritten Reich und in Südafrika Anwendung Andreas Bachofner/01 Wasserstoff 26

Wasserstoff als Reduktionsmittel und -schutz �Wasserstoff reagiert mit Metallen und entzieht Sauerstoff �Erhitzte Metalle reagieren leicht mit Sauerstoff Härtungsvorgänge in Öfen werden unter einer Schutzschicht durchgeführt �Schutzschicht kann z. T. aus Wasserstoff bestehen �Auch schon vorhanden Oxidschichten können mit Wasserstoff beseitigt werden �Allgemeine Gleichung : �Beispiel: Andreas Bachofner/01 Wasserstoff Me. O + H 2↔Me + H 2 O Cu. O + H 2 ↔ Cu + H 2 O 27

Einsatzgebiete von Wasserstoff als Reduktionsmittel �Glühen von Stahl �Reinigung von Metalloberflächen �Glühen von NE-Legierung �Steigern der Kühlleistung von Öfen (in Kombination mit flüssigem Stickstoff) �Sintern �Reduktion von Metalloxiden, (z. B. Wolframoxid) Andreas Bachofner/01 Wasserstoff 28

Herstellung von Ammoniak NH 3 �Besteht aus Stickstoff und Wasserstoff �Verhältnis 1: 3 �Wird mit Haber-Bosch-Verfahren hergestellt �Rohstoff hauptsächlich Erdgas � 1. Schritt: Erdgas wird entschwefelt � 2. Schritt: Erdgas wird mit Wasserdampf zur Reaktion gebracht � 3. Schritt: Erdgas spaltet sich bei 1000°C; Luft wird solange zugeführt bis Stickstoffkonzentration richtig ist � 4. Schritt: Verbleibendes Gemisch aus Wasserstoff, Stickstoff und Kohlenmonoxid wird mit Wasser umgesetzt, um Kohlenmonoxid in Wasserstoff umzuwandeln � 5. Schritt: Kohlendioxid wird aus Gemisch gefiltert Andreas Bachofner/01 Wasserstoff 29

Ammoniakherstellung �Eigentliche Ammoniaksynthese bei hohem Druck und unter katalytischen Verhältnissen � 6. Schritt: Gasgemisch wird in röhrenförmigem Reaktor unter 25 -30 bar und 450 -500°C � 7. Schritt: Ammoniak unter kritische Temperatur bringen und abscheiden �Wirkungsgrad liegt bei ca. 25% �Wasserstoff kann wiedergewonnen werden �Alle anderen Gase werden als Abgase abgegeben �Jahresproduktion 2011: 136 Mio. Tonnen Andreas Bachofner/01 Wasserstoff 30

Anwendungen von Ammoniak �Basis für Sprengstoffe �Basis für Stickstoffdünger �Produktion von Salpetersäure �Bestandteil von Reinigungsmitteln Andreas Bachofner/01 Wasserstoff 31

Wasserstoff in Luftschiffen �Kurz nach Heißluftballon verwendet �Konzept wurde durch Graf von Zeppelin weiterentwickelt �Einsatz im Ersten Weltkrieg �Später eingesetzt als Linienverkehrsflugzeuge �Aufgrund von Unfällen (Lakehurst 1937) keine Verwendung von Wasserstoff in Luftschiffen mehr �Ersatz durch Helium Andreas Bachofner/01 Wasserstoff 32
- Slides: 32