Waldsterben und Sterben der Seen in Skandinavien gestoppt

Waldsterben und Sterben der Seen in Skandinavien gestoppt! Bild: Wetzel

Rauchgasentschwefelung � � � Es gibt mehr als 100 verschiedene Verfahren, am häufigsten angewendet wird das Calciumcarbonatverfahren: Nasswäsche mit wässrigen, schwach basisch reagierenden Suspensionen von fein gemahlenem, natürlichem Kalkstein (Ca. CO 3) Reaktionen: (1) SO 2 + Ca. CO 3 + H 2 O Ca. SO 3 ∙ 1/2 H 2 O + CO 2+1/2 H 2 O (2) Ca. SO 3 ∙ 1/2 H 2 O+1/2 O 2 + 2 H 2 O Ca. SO 4 ∙ 2 H 2 O + ½ H 2 O Heutige Deutungen des Waldsterbens als „Umwelt-Fehlalarm“ ignorieren, dass die Erholung unserer Wälder das Ergebnis großer Anstrengungen zur Luftreinhaltung ist

Weltkarte der Luftverschmutzung mit SO 2, 2015, Satellit Envisat Universität Heidelberg
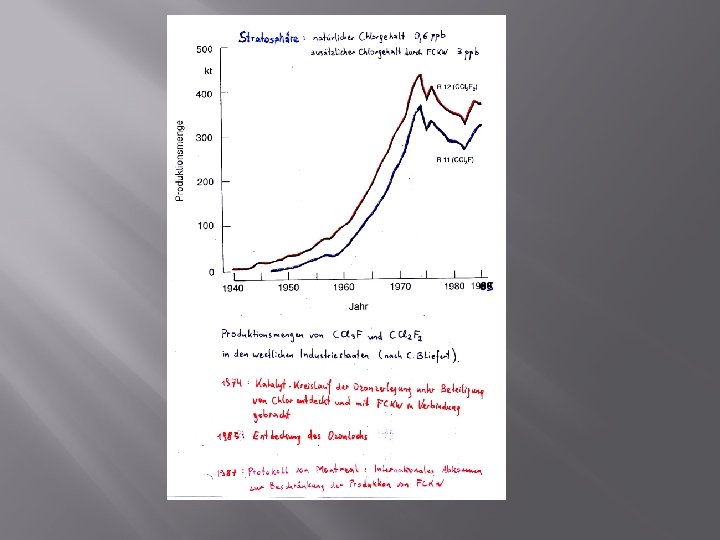

Kurze Geschichte der Lithosphäre, Hydrosphäre und Atmosphäre � Am Beginn steht der Urknall, nach heutigen kosmologischen Theorien der Beginn des Universums aus einem singulären Zustand mit enorm hoher Temperatur und Dichte. � 380 000 Jahre nach dem Urknall bildeten sich die ersten Atome (90% H, 10% He, etwas Deuterium) � Alter des Universums: 13, 8 Milliarden Jahre

Sterne � Entstehen bis heute dadurch, dass sich kosmische Materie irgendwo überdurchschnittlich stark verdichtet � und sich aufgrund der Gravitation in Richtung auf ihren Schwerpunkt hin kontrahiert. � Gravitationsenergie wird frei, der Himmelskörper heizt sich während seiner Schrumpfung adiabatisch auf. � Ab 107 K setzt die Fusion von Wasserstoff zu Helium ein.

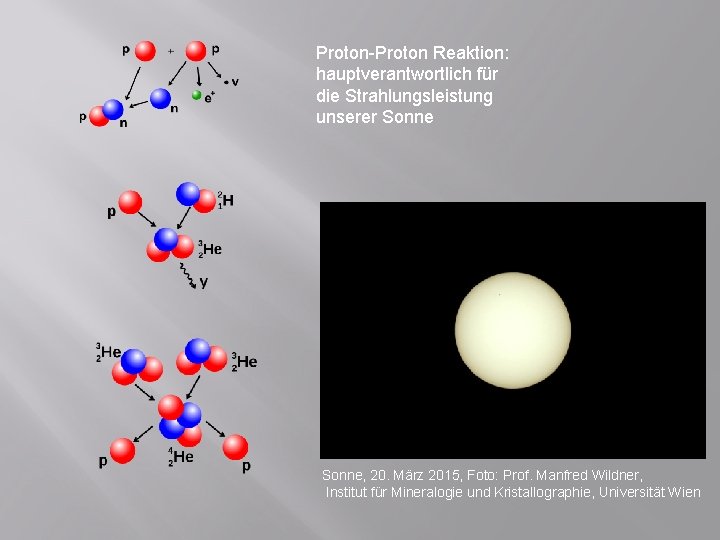
Proton-Proton Reaktion: hauptverantwortlich für die Strahlungsleistung unserer Sonne, 20. März 2015, Foto: Prof. Manfred Wildner, Institut für Mineralogie und Kristallographie, Universität Wien

� Seit der Entstehung unserer Sonne (vor 4, 6 Milliarden Jahren) sind erst 10 % des vorhandenen nutzbaren Wasserstoffs verbraucht worden � Die Sonne hat noch ein mehrere Milliarden Jahre langes unverändertes Leben vor sich � Durch die bei der Wasserstofffusion freiwerdende Energie wird der weitere Gravitatationskollaps aufgehalten � Wenn in einem Stern von 1, 5 Sonnenmassen oder größer 10% des Wasserstoffs aufgebraucht sind, kommt es zu einer weiteren gravitatationsbedingten wärmeliefernden Kontraktion

Temperatur in Millionen Kelvin Brennmaterial H Wasserstoffbrennen H mit H zu He Brenndauer 40 10 Milliarden J. 190 1 Million Jahre C Kohlenstoffbrennen C mit C zu Mg u. a. Sterne mit mindestens 4 Sonnenmassen 740 10. 000 Jahre Ne Neonbrennen Sterne mit mindestens 8 Sonnenmassen 1. 600 10 Jahre 2. 100 5 Jahre Si Siliciumbrennen Si mit Si zu Ni u. a. Endprodukt vor allem Fe-56 3. 400 1 Woche Fe-Kerne Kernfusion schwerer Elemente (endotherm) 10. 000 Supernova-Explosion He O Heliumbrennen He mit He zu Be, Be mit He zu C C mit He zu O Sauerstoffbrennen O mit O zu S u. a. Sterne mit mindestens 8 Sonnenmassen

Beteigeuze: Heliumbrennen hat begonnen
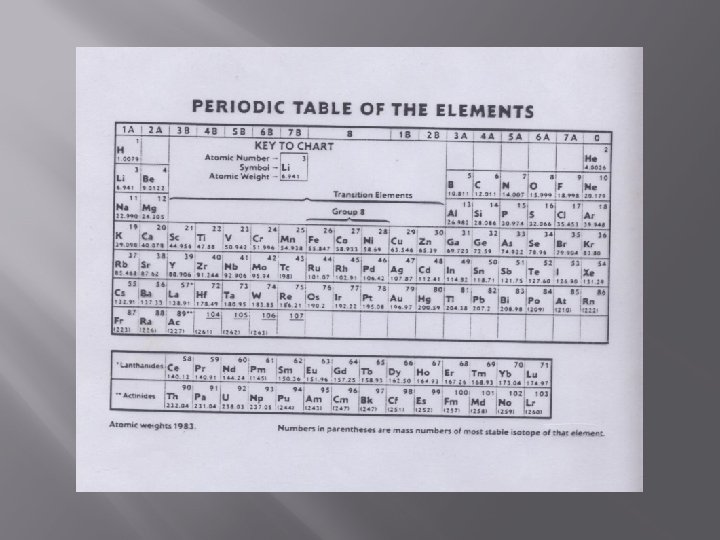
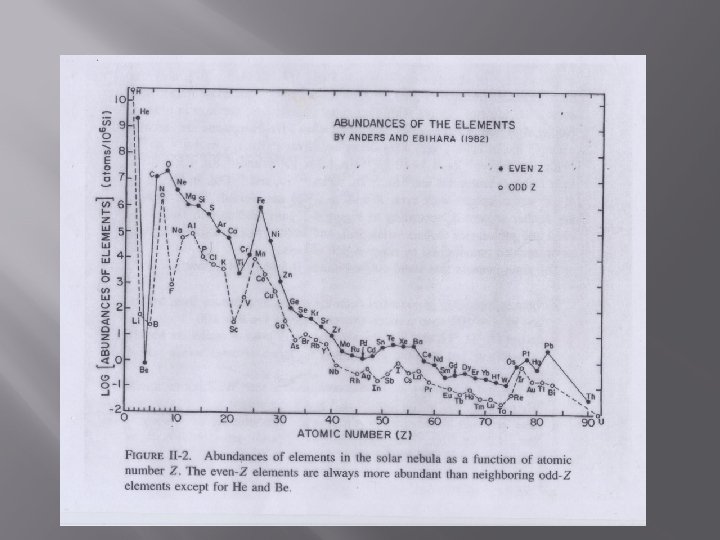
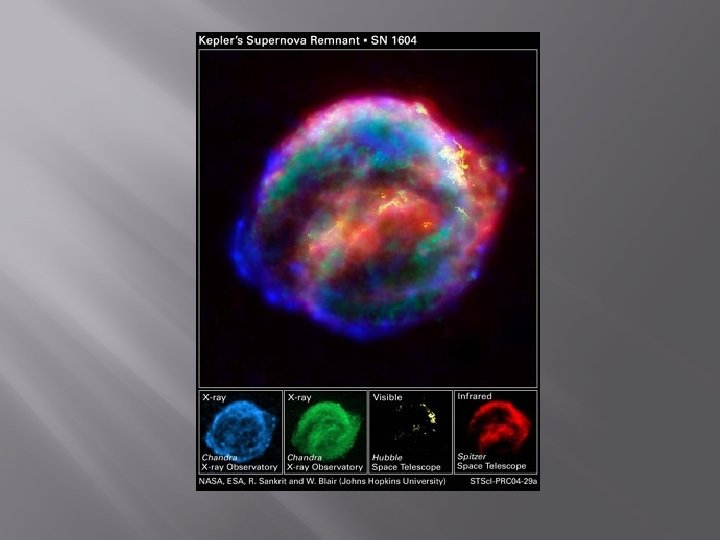


Kosmische Uhr � Man nimmt an, dass bei der Bildung des Urans in heißen Sternen die Isotope U-235 und U-238 in gleichen Mengen entstehen. � Dann errechnet sich aus ihren Halbwertszeiten und relativen Häufigkeiten auf der Erde, dass der Zeitpunkt ihrer Erzeugung 6 Milliarden Jahre zurückliegt.
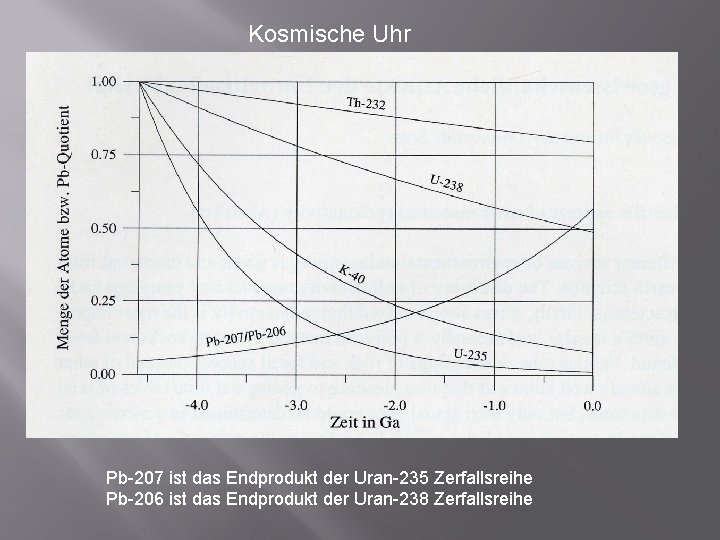
Kosmische Uhr Pb-207 ist das Endprodukt der Uran-235 Zerfallsreihe Pb-206 ist das Endprodukt der Uran-238 Zerfallsreihe

� � � Primordial radionuclides = Initial radionuclides existing since the earth was formed and which have not completely decayed due to their long half-life e. g. U 238, U 235 and Th 232 and K 40 and 25 other radionuclides

Der Urnebel fällt in sich zusammen und beginnt zu rotieren. Dabei bildet sich eine Gas- und Staubscheibe um die Protosonne

� � � Nahe dem heißen Zentrum dieser Wolke konnten nur die schweren und schwerflüchtigen Stoffe kondensieren Weiter außen in kühleren Zonen konnten sich auch Substanzen mit größerer Flüchtigkeit niederschlagen Daher sind bei den inneren Planeten Merkur, Venus, Erde und Mars die leichten und leichtflüchtigen Elemente (H, He, C, N) stark abgereichert Die schweren und schwerflüchtige Verbindungen bildenden Elemente stark angereichert (Fe, Ni, Si, Mg, O) Auch die Edelgase Ne, Ar-36 und Ar-38, Kr, Xe sind abgereichert (bilden keine schwerflüchtigen Verbindungen) Das viele Ar-40 in der Atmosphäre kommt aus dem Zerfall von K-40 im Erdmantel im Laufe der Erdgeschichte

Relative Häufigkeit der Elemente im Kosmos und im Erdkörper Element Ordnungszahl Häufigkeit im Kosmos [%] Häufigkeit im Erdkörper [%] <0. 1 Wasserstoff (H) 1 92. 48 Helium (He) 2 7. 399 Sauerstoff (O) 8 0. 00629 Kohlenstoff (C) 6 0. 0292 Stickstoff (N) 7 0. 00777 Neon (Ne) 10 0. 00518 Magnesium (Mg) 12 0. 00374 11. 2 Silizium (Si) 14 0. 00370 14. 7 Eisen (Fe) 26 0. 00318 37. 4 Schwefel (S) 16 0. 00178 Argon (Ar) 18 0. 00081 Aluminium (Al) 13 0. 00030 1. 3 Calcium (Ca) 20 0. 00022 1. 4 Natrium (Na) 11 0. 00021 0. 6 Nickel (Ni) 28 0. 00018 3. 0 Chrom (Cr) 24 0. 00005 0. 3 Phosphor (P) 15 0. 00003 0. 1 Mangan (Mn) 25 0. 00003 0. 2 29. 5

NASA

� Die Erde ballte sich aus kosmischem Staub (aus Planetesimalen=gashaltige feste Teilchen) zusammen. Das war stark strahlender „radioaktiver Müll“ der Supernova-Explosion � Adiabatische Materieverdichtung, radioaktive Prozesse: die junge Erde erwärmte sich auf einige Tausend Grad und schmolz: durch Abdampfen weiterer Verlust von leichtflüchtigen Elementen � Abkühlung, Entmischung, vor 4 Milliarden Jahren erstarrt die Erdkruste. � Die Gesteine der Erdkruste und des Erdmantels konnten bei ihrer Bildung große Mengen leichtflüchtiger Bestandteile binden und daher vor dem Verlust ins All retten (Wasser in Form von -OH Gruppen in zahlreichen Mineralien, CO 2 in Karbonatiten und in Spuren in allen primären Gesteinen, Kohlenwasserstoffe und Stickstoff in Feldspäten � Durch Ausgasen entstand die Uratmosphäre (Primordialatmosphäre)

Gigantischer „Hochofenprozess“: Die äußere Hülle der Urerde enthielt genügend zweiwertiges Eisen (Fe. O) aus kosmischem Staub, um Methan und Ammoniak während des Ausgasens zu Stickstoff, CO 2 und Wasser umzusetzen. 4 Fe. O + CH 4 3 Fe. O + 2 NH 3 CO 2 + 2 H 2 O + 4 Fe N 2 + 3 H 2 O + 3 Fe

Zusammensetzung heutiger vulkanischer Exhalationen: 80% H 2 O 10% CO 2 7% H 2 S 0. 5% N 2 0. 5% H 2 0. 5% CO CH 4 und NH 3 nur in Spuren HCl, HF, SO 2, Edelgase in Spuren kein O 2 Foto: US National Park Service

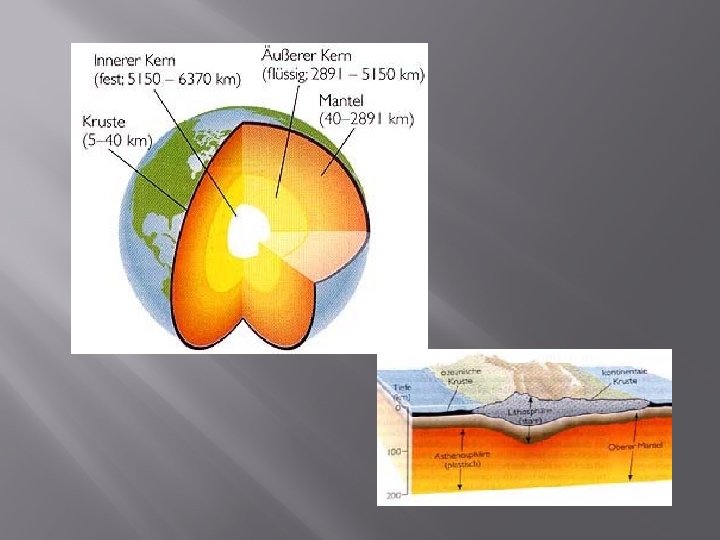
� Damals (vor 4 Milliarden Jahren) stammte die Erdwärme ebenso wie heute aus dem Zerfall radioaktiver Nuklide, nur wurde damals noch ca. 3 x so viel Wärme erzeugt � diese innere Wärme hatte schon damals wenig Einfluss auf die Oberflächentemperatur der Erde � aber viel auf Vulkanismus, Bildung der Atmosphäre und Hydrosphäre � Der heutige Erdkern hat 6500°C ! Der äußere Erdkern ist flüssig, die in ihm stattfindenden Konvektionsströme verursachen das erdmagnetische Feld. � Dieses schützt und vor der kosmischen Strahlung.
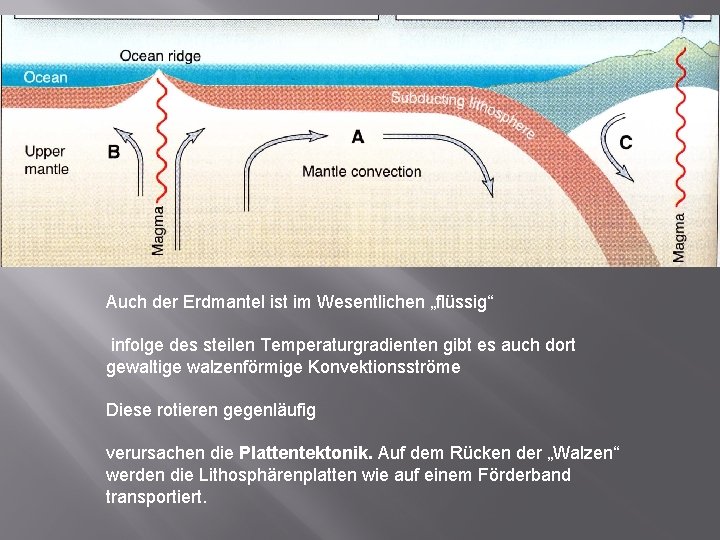
Auch der Erdmantel ist im Wesentlichen „flüssig“ infolge des steilen Temperaturgradienten gibt es auch dort gewaltige walzenförmige Konvektionsströme Diese rotieren gegenläufig verursachen die Plattentektonik. Auf dem Rücken der „Walzen“ werden die Lithosphärenplatten wie auf einem Förderband transportiert.

Die Erdkruste (Lithosphäre) � � „Schwimmt“ auf dem Erdmantel Dicke unter dem Ozean 5 -7 km, unter Kontinentalebenen 30 -40 km, unter Gebirgen 50 km Besteht zu 48, 8% aus Sauerstoff, zu 26, 3% aus Silizium Bausteine: Ca-, Na-, Mg-, K-, Ti-, Fe- und Phaltige Silicate und Alumosilicate

Saure, basische und ultrabasische Silicatgesteine bzw. Magmen � � � 70% Si. O 2 „sauer“ (Erdkruste) 50% Si. O 2 „basisch“ <50% Si. O 2 „ultrabasisch“ (Erdmantel)

Der Erdkern � 86% Fe, 7% Ni, 1% Co, 6% S � Der innere Teil mit Radius 1400 km ist fest, Druck 3, 5 Millionen Bar, Temperatur 6500°C Bei 6500°C und 1 Bar Druck wäre Eisen gasförmig � � Der innere Erdkern hat erst vor 2, 5 Milliarden Jahren zu kristallisieren begonnen � Durch die Kristallisation wird ebenfalls ständig Wärme frei

Infolge der in der Tiefe herrschenden hohen Drucke zeichnen sich die Strukturen der Verbindungen durch höhere Koordinationszahlen der Gitterbausteine aus: Stishovit (Si. O 2, Hochdruckmodifikation, Rutil-Typ (Ti. O 2), tetragonal) KZ=6, Dichte 4, 5 g/cm 3 Cristobalit (Si. O 2, unter Normaldruck beständig) KZ=4, Dichte 2, 32 g/cm 3 Dominantes Mineral des tiefen Erdmantels in 2300 km Tiefe: Mg, Fe(Si. O 3) KZ=6, Perowskit-Struktur (Ca. Ti. O 3 -Typ, rhombisch)
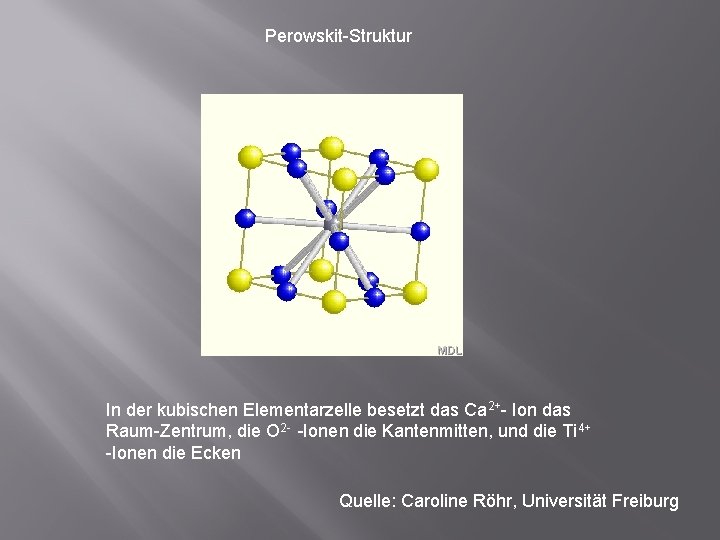
Perowskit-Struktur In der kubischen Elementarzelle besetzt das Ca 2+- Ion das Raum-Zentrum, die O 2 - -Ionen die Kantenmitten, und die Ti 4+ -Ionen die Ecken Quelle: Caroline Röhr, Universität Freiburg
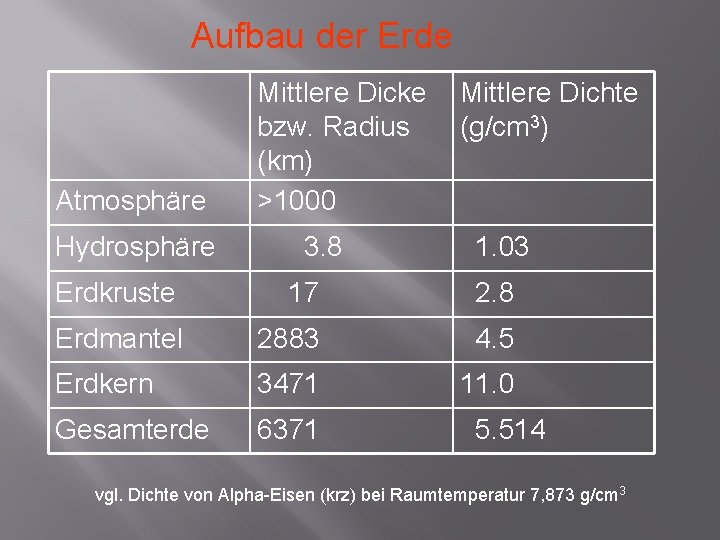
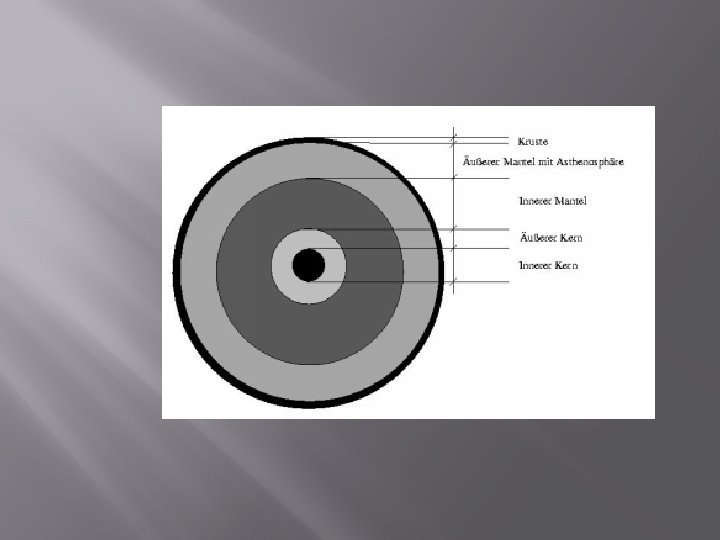
Aufbau der Erde Atmosphäre Hydrosphäre Mittlere Dicke bzw. Radius (km) >1000 3. 8 Mittlere Dichte (g/cm 3) 1. 03 Erdkruste 17 2. 8 Erdmantel 2883 4. 5 Erdkern 3471 11. 0 Gesamterde 6371 5. 514 vgl. Dichte von Alpha-Eisen (krz) bei Raumtemperatur 7, 873 g/cm 3
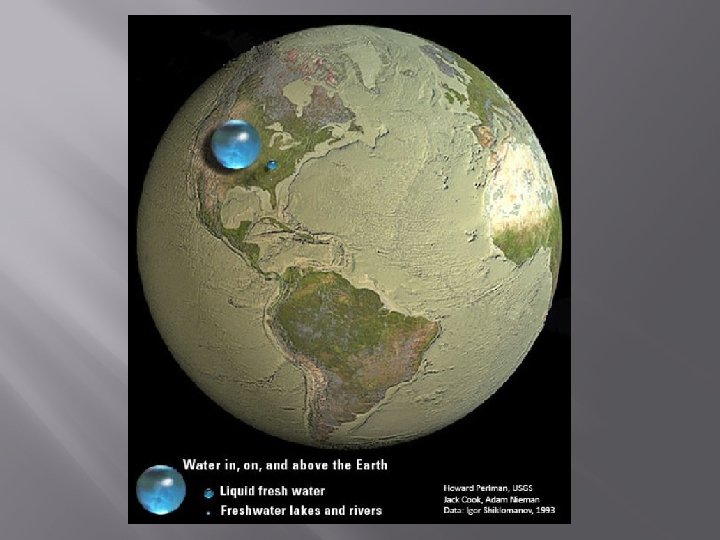

Bild: Niedersächsisches Landesamt für Bodenforschung durchschnittlicher geothermischer Gradient: 3°C pro 100 m Tiefe Wärmestrom 0, 06 Watt/m 2 Erdoberfläche (Solarkonstante: 1367 Watt/m 2) (Mensch erzeugt durch Verbrennen fossiler Brennstoffe 0, 03 Watt/m 2 Erdoberfläche)

Evolution der Hydrosphäre und Atmosphäre

� Wasserdampf konnte sich nie in hohen Konzentrationen in der Atmosphäre sammeln, die Erdkruste war schon bei der Entstehung (Ausgasung) des H 2 O genügend abgekühlt, sodass das Wasser kondensierte… aber trotzdem nicht weltweit einfror � Die Kondenstation des Wasserdampfes war mit der Auswaschung von CO 2 verbunden, das verhinderte einen zu hohen Treibhauseffekt („Wärmehölle“) durch CO 2 � Das CO 2 gelangte als Carbonat in die Sedimente des Ur-Ozeans

The faint young Sun paradox The landscape during the early Archean could have looked like this: small continents on a planet mostly covered by oceans, illuminated by the much fainter young Sun, and with a Moon that appears larger in the sky because of its smaller distance to Earth. Potsdam Institute for Climate Impact Research


Quelle: NASA Venus und Erde (Größenvergleich) Venus-Atmosphäre: 95% CO 2, 100 Bar an der Oberfläche, 480°C (durch den CO 2 Treibhauseffekt) Erde: 15°C mittlere Temp. An der Erdoberfläche (Temp. wäre ohne CO 2 Treibhauseffekt -18°C)
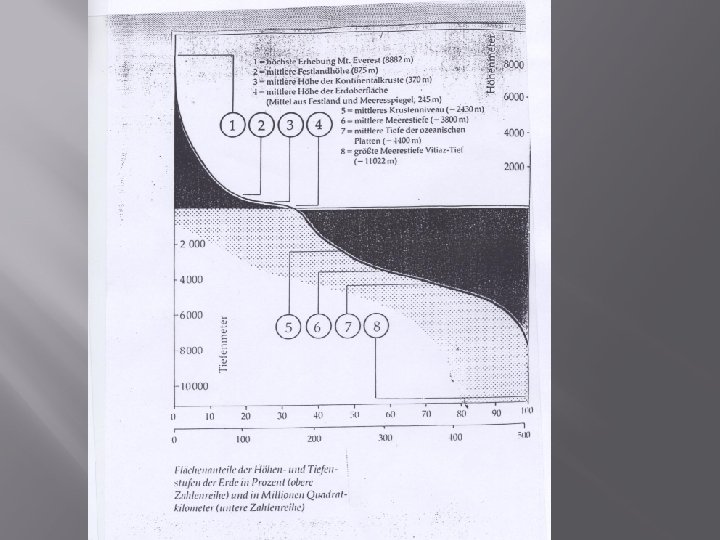
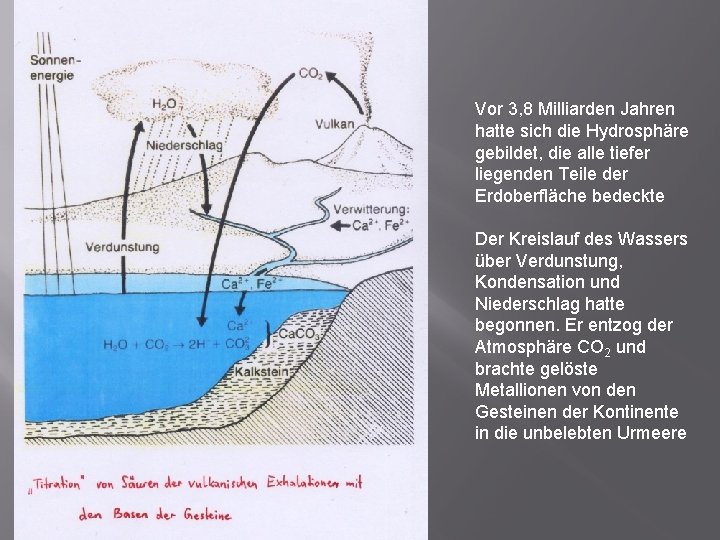
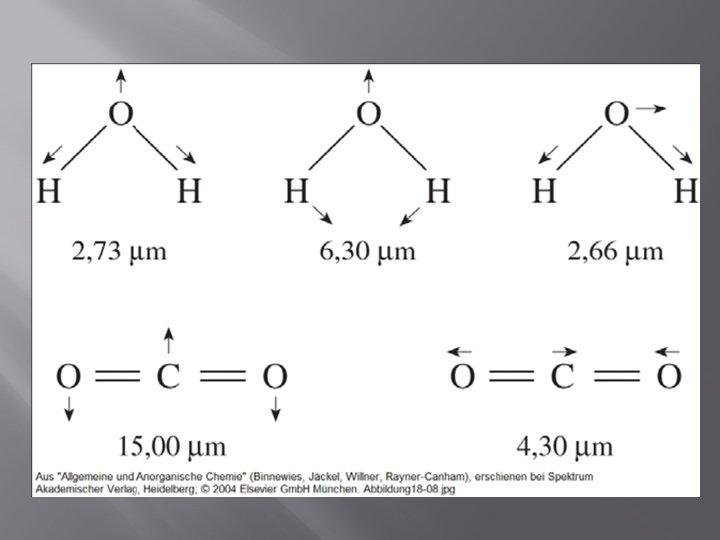
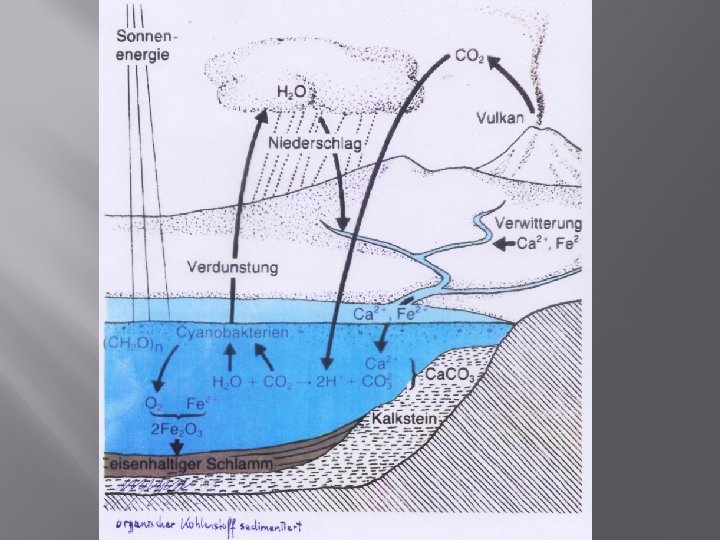
Vor 3, 8 Milliarden Jahren hatte sich die Hydrosphäre gebildet, die alle tiefer liegenden Teile der Erdoberfläche bedeckte Der Kreislauf des Wassers über Verdunstung, Kondensation und Niederschlag hatte begonnen. Er entzog der Atmosphäre CO 2 und brachte gelöste Metallionen von den Gesteinen der Kontinente in die unbelebten Urmeere

Beweis dafür, dass es in der frühen Erdatmosphäre keinen Sauerstoff (O 2) gab: In 2, 5 x 109 Jahre alten Flussschottern (Konglomeraten) fand man Uraninit UO 2. Die Körnchen wurden von Flüssen im Geröll weite Strecken transportiert und dabei charakteristisch abgerundet. Hätte die Atmosphäre Sauerstoff enthalten, so wäre das Uran(IV) rasch zu Uran(VI) oxidiert worden. Die Körnchen hätten sich aufgelöst, weil das entstehende [UO 2]2+ (Uranyl- Ion) im Gegensatz zum Uraninit gut wasserlöslich ist. Auch Schottersteine aus Pyrit Fe. S 2 in solchen Sedimenten beweisen die Abwesenheit von Sauerstoff.

Wieso enthält die heutige Atmosphäre so viel O 2? � Die heutige Zusammensetzung der Atmosphäre ist eine Folge des Lebens auf der Erde.

Entscheidende Bedeutung der Ozeane für die Entstehung des Lebens � � � Wasser ist der Träger aller chemischen Lebensvorgänge in den Organismen Wasser löste das atmosphärische CO 2 und verhinderte zu großen Treibhauseffekt Wasser löste CO 2 und alle anderen Nährstoffe Wasser wirkte aufgrund seiner hohen Wärmekapazität 4200 J/(kg·K) stabilisierend auf das irdische Klima Wasser absorbierte das kurzwellige UV (200 nm – 290 nm) (die ersten Organismen lebten unter einer 10 m dicken Wasserschicht (UV Filter entspricht der heutigen Atmosphäre)
![Photosynthese CO 2 + 2 H 2 S + Licht [CH 2 O] + Photosynthese CO 2 + 2 H 2 S + Licht [CH 2 O] +](http://slidetodoc.com/presentation_image_h2/93b45a792d87493a90e7642904d728de/image-50.jpg)
Photosynthese CO 2 + 2 H 2 S + Licht [CH 2 O] + H 2 O + 2 S 2 CO 2 + 2 H 2 O + H 2 S + Licht 2 [CH 2 O] + H 2 SO 4 CO 2 + 2 H 2 + Licht [CH 2 O] + H 2 O CO 2 + 2 H 2 O + Licht [CH 2 O] + H 2 O + O 2

Viele Prozesse wie die N 2 - CO 2 - und S-Assimilation waren bereits von Anbeginn des Lebens mit Lichtreaktionen, einem Elektronenfluss und ATP verbunden. Aber erst die Kopplung zweier lichtgetriebener Reaktionen, d. h. die Kopplung zweier Photosysteme erzeugte die notwendige Energie für die Spaltung von Wasser und die Freisetzung von Sauerstoff. Die mikropaläontologisch-morphotypischen Funde in ältesten Gesteinen (3, 5 Milliarden Jahre alt) weisen darauf hin, dass cyanobakterielle Ökosysteme sehr bald die frühe Erde beherrscht haben. (Manfred Schidlowski, 1998)


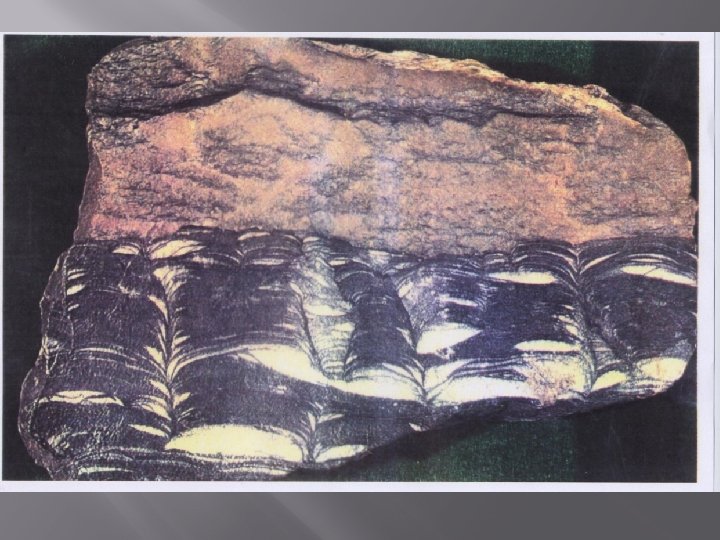
� Die biologische Kohlenstoff-Fixierung durch die archaischen Stromatolithen zeigt, dass prokaryotisches Mikrobenthos die Erde schon vor etwa 3, 5 Milliarden Jahren beherrscht hat. Die Archaisch-Proterozoischen Funde bestehen hauptsächlich aus Cyanobakterien. � Vergleichbare mikrobielle Gesellschaften gehören zu den produktivsten Ökosystemen der heutigen Biosphäre. Besonders die benthischen (= auf dem Meeresboden lebenden) Cyanobakterien können die erstaunliche Primärproduktivität von 10 g C/m² am Tag erreichen. � Die Photosynthese hat daher in quantitativer Hinsicht während der nachfolgenden Evolution des Leben nur wenig an Wichtigkeit dazu gewonnen.

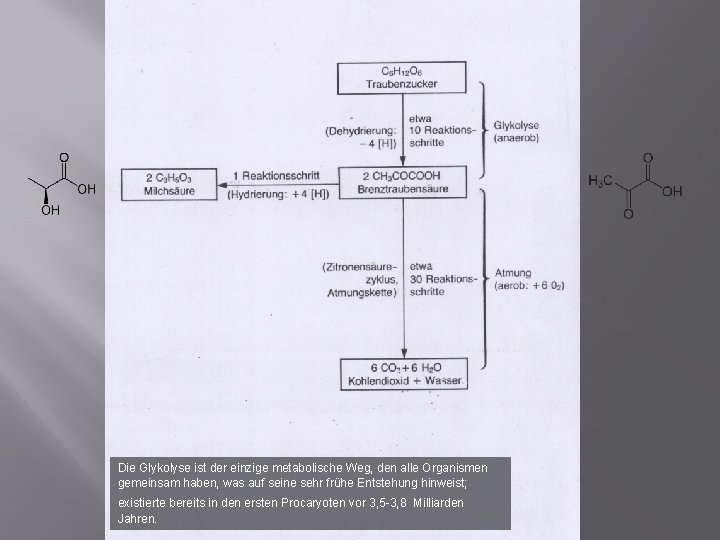
Die Glykolyse ist der einzige metabolische Weg, den alle Organismen gemeinsam haben, was auf seine sehr frühe Entstehung hinweist; existierte bereits in den ersten Procaryoten vor 3, 5 -3, 8 Milliarden Jahren.

� Die Sauerstoff-Atmung bedeutet gegenüber der Gärung eine 14 x effektivere Ausnutzung der in den Kohlenhydraten gespeicherten Energie. � Atmung ist schon bei 1% des heutigen O 2 Partialdrucks möglich. � Infolge dieses Fortschritts nahm die biologische Aktivität und damit auch die Sauerstoff-Produktion sprunghaft zu.



Mangel an bioessentiellen Metallen im Ozean vor 2 Milliarden Jahren bis vor 1 Milliarde Jahren fehlte weitgehend eine globale Zirkulation des Weltozeans. Gleichzeitig begann vor 2 Milliarden Jahren die Sulfat-Zufuhr zum Ozean durch die einsetzende oxidative Verwitterung der Gesteine der Kontinente. Durch dissimilatorische Sulfatreduktion entstanden hohe H 2 S Gehalte in tieferen sauerstofffreien Wasserschichten, dies führte zur Bildung schwerlöslicher Sulfide von Mo, Fe, Cu, Zn. Durch den Mangel an Mikronährstoffen im Ozean verzögerte sich die Entwicklung der Eukaryoten, die bereits vor 2, 1 Milliarden Jahren erstmals die Bildfläche betraten (Gabonionta, 2010 entdeckt).
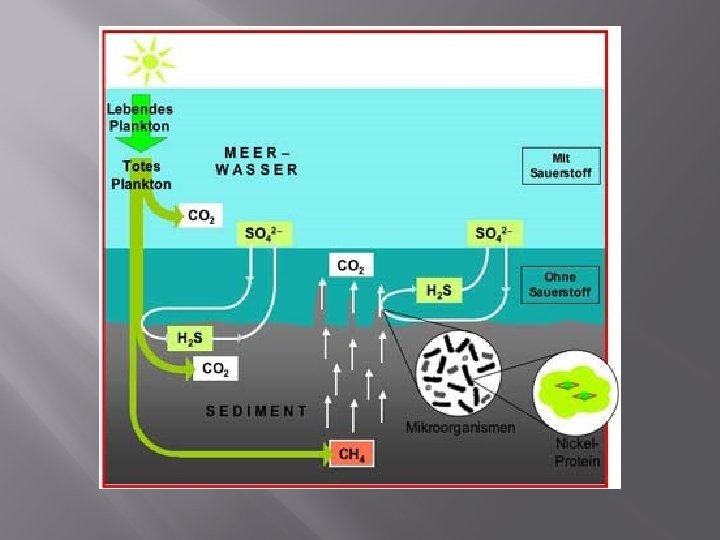

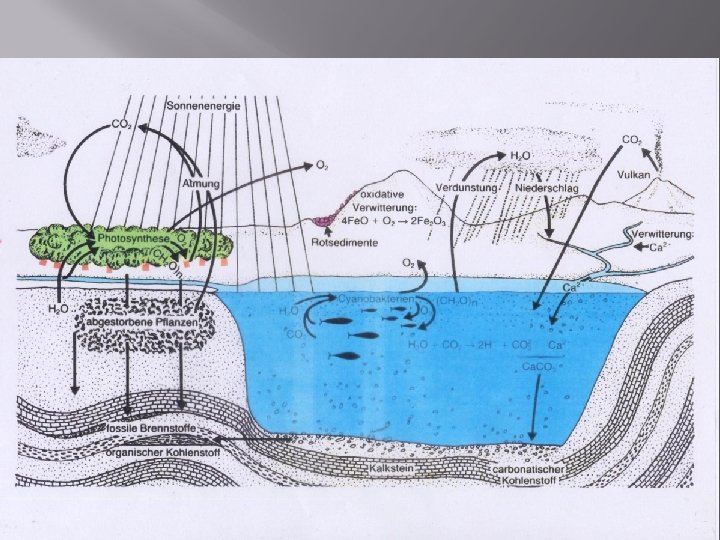
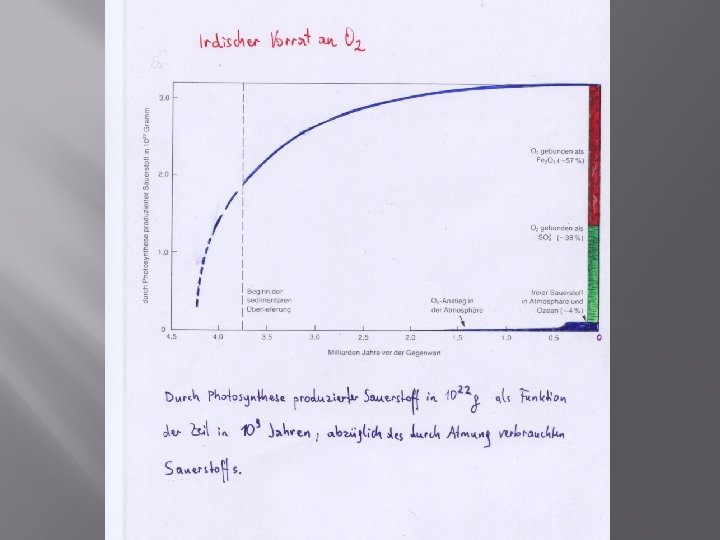

Es bedarf eines Überschusses der Photosyntheserate über die Atmungsrate: Der reduzierte Kohlenstoff wird nicht zur Gänze wieder zu CO 2 oxidiert, sondern wandert zum Teil ins Sediment, wo er vor Oxidation geschützt ist. So kann der Sauerstoffverbrauch durch die Oxidation reduzierender Krustenbestandteile und reduzierender vulkanischer Gase ausgeglichen werden.



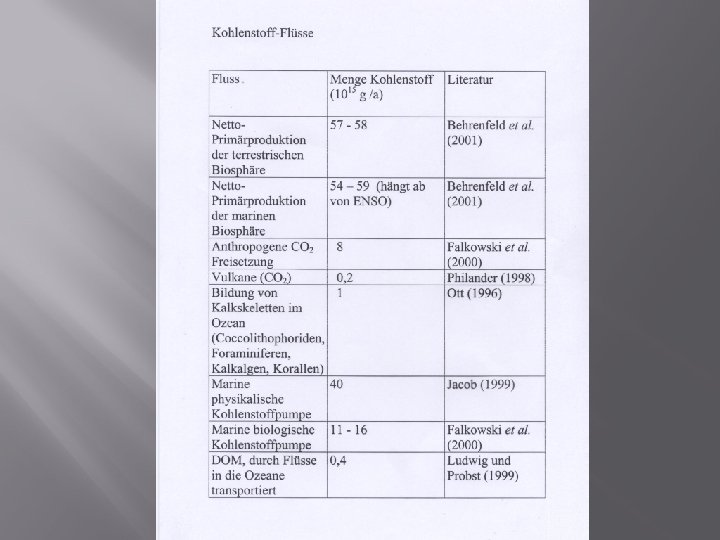
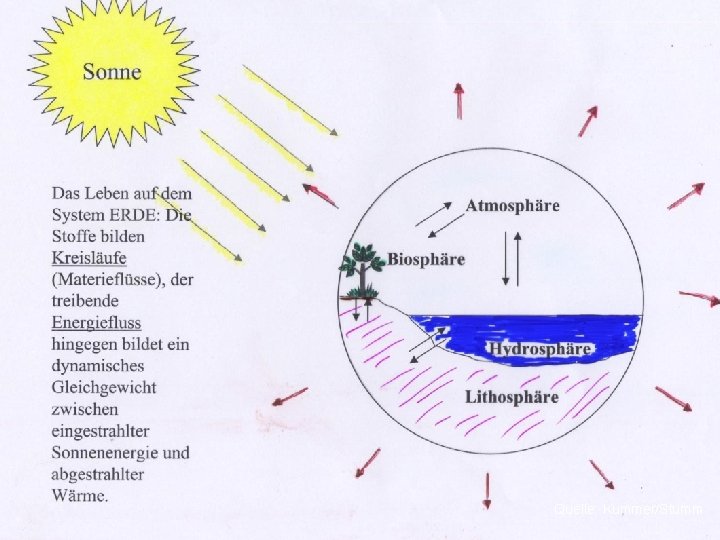
Quelle: Kummer/Stumm

Biogeochemische Stoffkreisläufe � � � Ein wichtiges Konzept der Umweltforschung ist es, globale und regionale Materieflüsse und Stoffkreisläufe in den Vordergrund zu stellen Insbesondere die biogeochemischen Stoffkreisläufe der Elemente Intensiv erforscht wurden der globale Kohlenstoffkreislauf, Stickstoffkreislauf, Phosphorkreislauf, Schwefelkreislauf , Quecksilberkreislauf, Eisenkreislauf u. a.
- Slides: 72