VYETEN FUNKCE LEDVIN Magdalna Fotov stav klinick biochemie

VYŠETŘENÍ FUNKCE LEDVIN Magdaléna Fořtová Ústav klinické biochemie a patobiochemie 2. LF UK a FN Motol, Klinika nefrologie 1. LF UK a VFN

Fyziologické funkce ledvin 1. Syntetická renin, erytropoetin, kalcitriol 2. Regulační koncentrace elektrolytů plazmatický objem osmolalita krevní tlak acidobazická rovnováha 3. Vylučovací močovina, kys. močová, kreatinin, kyseliny a zásady hormony a jejich metabolity léky, toxiny

Práce ledvin 180 litrů ultrafiltrátu 1, 5 litru moči p. H plazmy: 7, 4 p. H moče: až 4, 6

Vyšetřovací metody v nefrologii • Anamnéza a objektivní vyšetření • Laboratorní krevní testy • Vyšetření moče (proteinurie, hematurie…) • Hodnocení renální funkce (GFR…) • Zobrazovací metody (USG. . ) • Renální biopsie

Anamnéza • Rodinná anaméza: Dědičné choroby • Autosomálně dominantní polycystická choroba ledvin • Alportův syndrom • Osobní anaméza: • Diabetes mellitus • Hypertenze • Ateroskleróza • Dna • Systémové choroby • Urolitiáza, reflux, onemocnění prostaty • Infekce: cystitis, pyelonefritis, HBV, HCV, chronické bakteriální choroby • Tumory

Anamnéza • Léky, nefrotoxiny: • Diuretika, ACEI, ARB: prerenální selhání • NSA, antibiotika: akutní intersticiální nefritida • Penicilamin, zlato: membranózní GN • Analgetika: analgetická nefropatie • Cytostatika – cisplatina: ATN • Immunosupresiva – Cy. A: prerenální selhání, ATN, chronická intersticiální TIN • Radiokontrastní látky: ATN • Lithium: tubulární dysfuknce • Ethylenglykol: tubulární obstrukce krystaly • Gynekologická anamnéza: • Těhotenství: preeklampsie, asymptomatická bakteriurie, pravostranná pyelonefritis
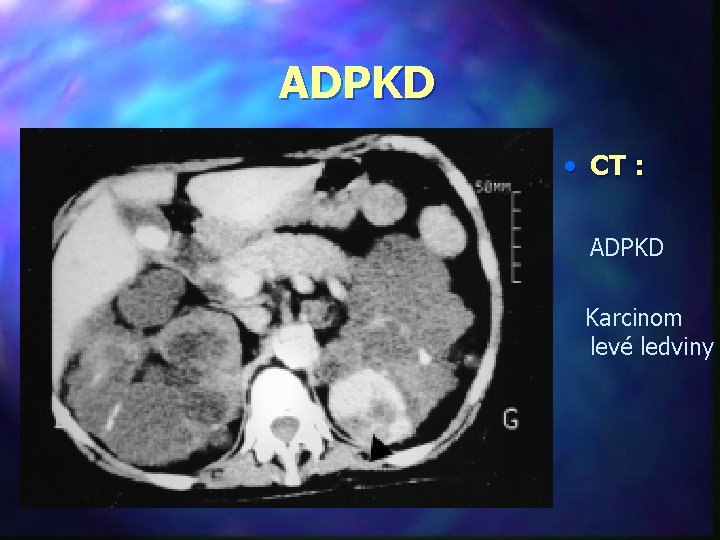
ADPKD • CT : ADPKD Karcinom levé ledviny
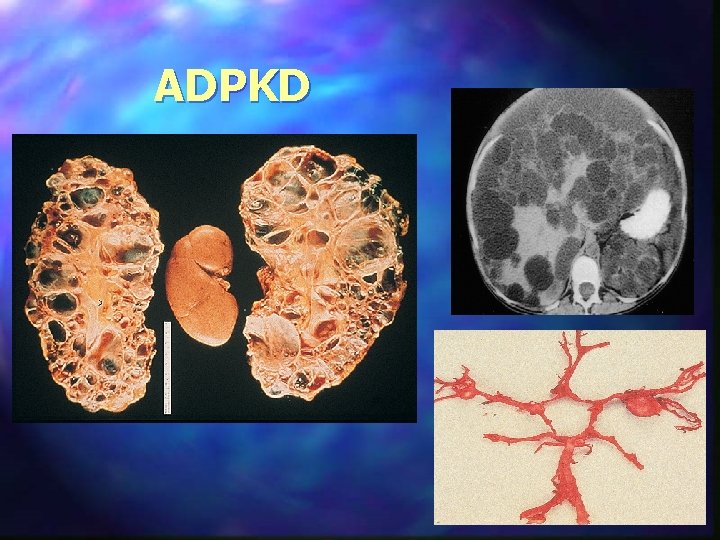
ADPKD

Možné symptomy onemocnění ledvin • Teplota, třesavka, bolest v podbřišku, bolest v bedrech (pyelonephritis, cystitis) • Makroskopická hematurie (Ig. A GN, cystitis) • Otoky (nefrotický syndrom) • Dušnost • Změny barvy a množství moče (diabetes mellitus, Ig. A GN) • Dysurie, urgence • Hluchota, poruchy visu (Alportův syndrom, HT) • Fotosenzitivita, teploty, noční poty, artralgie, myalgie (SLE) • Epistaxe, hematemeza (WG, HT)

Fyzikální vyšetření • • • Otoky Dušnost Hypertenze Šelest v epigastriu (stenóza a. renalis) Perikardiální třecí šelest (urémie, SLE) Hmatné ledviny, event. hepatomegalie (ADPKD) • Otoky kloubů, kožní výsev, Raynaudův fenomén, teploty, alopecie (systémové choroby) • Bledost (chronická renální insuficience, systémové choroby) • Foetor ex ore
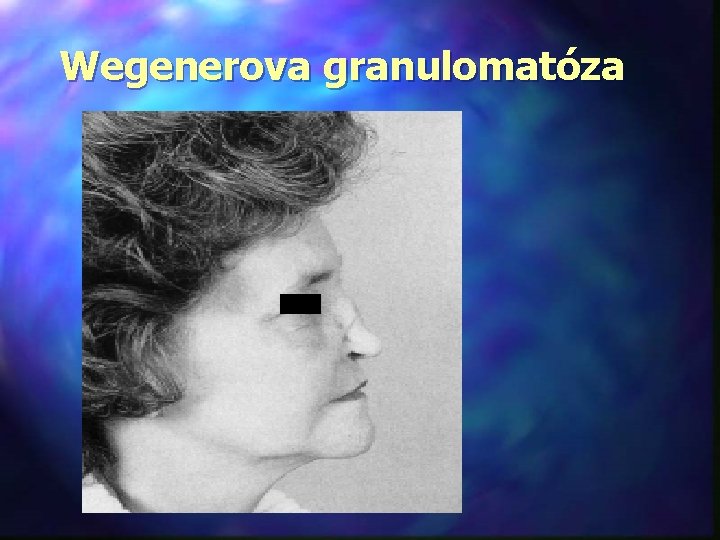
Wegenerova granulomatóza

Možné laboratorní odchylky • • urea, kreatinin, kyselina močová, Na, K Ca, Pi, parathormon p. H, HCO 3 CRP, FW, leukocytóza anémie D-dimery haptoglobin, myoglobin • imunologie: autoprotilátky – ANCA, anti. GBM, ANA, antids. DNA, komplement

Moč chemicky a sediment

Moč chemicky a sediment • • Změna barvy: - Červená moč – erytrocyty, hemoglobin, myoglobin, porfyriny, senna, levodopa, fenacetin, metronidazol, červená řepa - Bílá moč – přítomnost chylu, hnisu, fosfátových krystalů - Oranžová moč – rifampicin, fenytoin, sulfasalazin, nitrofurantoin, bilirubin, urobilin, rebarbora - Hnědá moč – methemoglobin, bilirubin, levodopa, melanin - Modrozelená moč – biliverdin, infekce pseudomanádami, vitamin B Specifická hmotnost moči: 1001 -1035 kg/m 3 (osmolalita 50 -1000 mmol/kg H 2 O) 1010 = izostenurie, >1018 zachovalá koncentrační schopnost ledvin hustotu zvyšuje výrazněji než osmolalitu přítomnost bílkoviny, glukózy, rtg kontr. latek • Chemické charakteristiky • Sediment: Vyšetření dg proužkem: specifická hmotnost, p. H, krev, bílkovina, leukocyty, nitrity, glukóza, urobilinogen, bilirubin, ketolátky - > 10 erytrocyty/ul - > 20 leukocytů/ul Addisova Hamburgerova metoda - > 150 mg/l bílkovin Erytrocyty do 2 mil. /24 h do 2 000/min Leukocyty do 4 mil. /24 h do 4 000/min Válce do 100 000/24 h do 70/min

Močový sediment • Erytrocyty Dysmorfní – m. j. akantocyty(„pučící“ery), původem z glomerulů Isomorfní – neglomerulární – z vývodných močových cest • Leukocyty (neutrofily, lymfocyty, eosinofily) • Válce – matrix=shluky Tamm-Horsfallova mukoproteinu – hyalinní (nespecifické) – erytrocytární (glomerulární hematurie) - leukocytární (TIN, infekce moč. cest) - granulované (jemné granulace-sérové proteiny, hrubé -alterované buňky, ATN, GN, TIN) - voskové (široké válce, vznikají v dilatovaných atrofických tubulech u nemocných s CHRI) granulace Lipidurie: oválná tuková tělíska nebo válce s tubulárními bb. naplněnými tukovými kapénkami u NS • Mikroorganismy: bakterie (E. coli, Staphylococcus epidermidis), kvasinky, trichomonas, Schistosoma haematobium • Tubulární buňky, epitelie, krystaly

Bakteriurie • střední proud moče po očištění periuretrální oblasti • z infekce močových cest (IMC) je podezdřelý 2 x po sobě zjištěný průkaz >105 bakterií/ml moče • nevýhoda: časté kontaminace • výhoda: screeningový test, jednoznačný výsledek u negativního nálezu
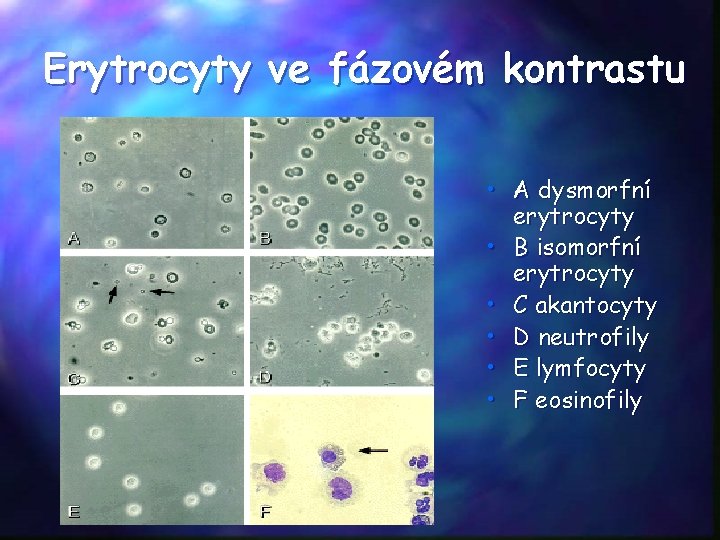
Erytrocyty ve fázovém kontrastu • A dysmorfní erytrocyty • B isomorfní erytrocyty • C akantocyty • D neutrofily • E lymfocyty • F eosinofily
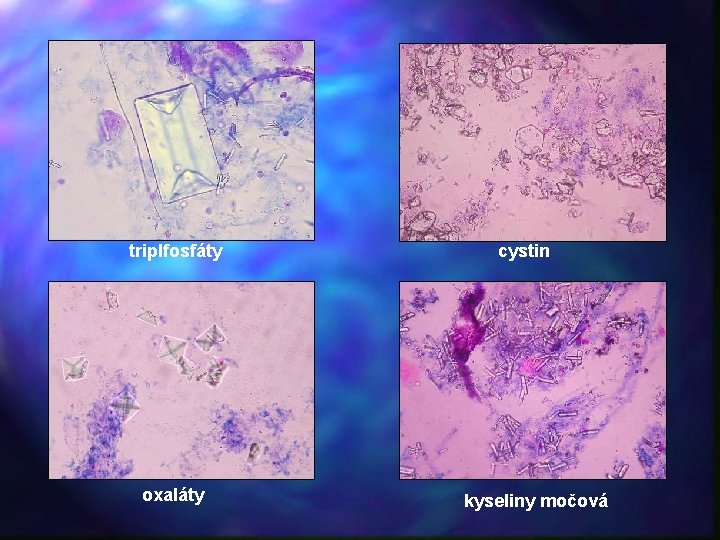
triplfosfáty oxaláty cystin kyseliny močová

hyalinní válec granulovaný válec leukocytární válec voskový válec erytrocytární válec „buněčné“ válce

Proteinurie

Proteinurie • I za fyziologických okolností proniká malé množství bílkovin (do Mr 200 000) bazální membránou glomerulů do ultrafiltrátu, v tubulech nastává různě velká zpětná resorpce, v definitivní moči zdravého dospělého jedince do 150 mg/d • plazmatické bílkoviny, bílkoviny pocházející z ledvinného parenchymu nebo z močových cest (např. uromukoid = glykoprotein Tamm-Horsfallův)

Proteinurie • Hlavní manifestace chorob ledvin • Rizikový faktor progrese renální insuficience, kardiovaskulární morbidity a mortality • Vyšetření dg proužkem (kys. sulfosalicylová)– semikvantitativní – detekuje pouze albumin • Kvantitativní stanovení (biuretová metoda, turbidimetrie- v prostředí imidazolového pufru je bílkovina denaturována alkylbenzyl –dimetyl amonium chloridem. . . zákal) • Selektivita PU – elektroforéza v polyakrylamidovém gelu • Albumin / creatinine ratio (ACR) - koncentrace albuminurie z jednoho vzorku

1. 2. Na glomerulární ultrafiltraci se podílejí 2 mechanizmy: systém molekulové bariéry (vnitřní část glomerulární membrány a mesangium) – brání průniku větších molekul než Mr 70 000 -100 000 a více postižení = neselektivní glomerulární PU –chronické proliferující GN, diabetická GN, amyloidóza ledvin systém elektrostatického odpuzování (podocyty a vnější část glomerulární membrány) – brzdí prostup proteinovým molekulám jako je albumin (Mr 67 000) postižení = selektivní glomerulární PU (albumin+transferin) NS s min. změnami, poč. stadia membranózní nefropatie, FSGS mikroproteiny (10 000 -40 000) se sice dostávají do primární moči, ale jsou tubulárními buňkami rezorbovány a hydrolyzovány na aminokyseliny postižení = tubulární mikroproteinurie (α 1 -mikroglobulin, α 2 -mikroglobulin, β 2 -mikroglobulin, lehké řetězce imunoglobulinů) kompletní forma (mikroproteiny o Mr 10 000 -70 000)- CHTIN, akutní tubulární selhání, rejekce transplantované ledviny, dědičné tubulopatie nekompletní forma (10 000 -40 000) –renální vaskulární poruchy

Proteinurie • • • d. U-protein „Mikroalbuminurie“ Jednotlivé proteiny • • • albumin postižení glomerulů transferin α 1 -mikroglobulin α 2 -mikroglobulin β 2 - mikroglobulin retinol-vázající globulin postižení tubulů lehké řetězce Ig (κ, λ), Bence-Jonesova proteinurie Ig. G α 2 -makroglobulin postrenální proteinurie α 1 -lipoprotein ELFO proteinů v moči Polyakrylamidová gelová ELFO IMUNOELFO, Imunofixace (U-Ig. G/S-Ig. G) x (S-trf/U-trf) index selektivity (<0, 1 selektivní PU, >0, 2 neselektivní PU) U-Ig. G/Ig. G 4 nebo p. AMS/s. AMS nábojová selektivita


sel. gl. nesel. gl. tub. smíšená
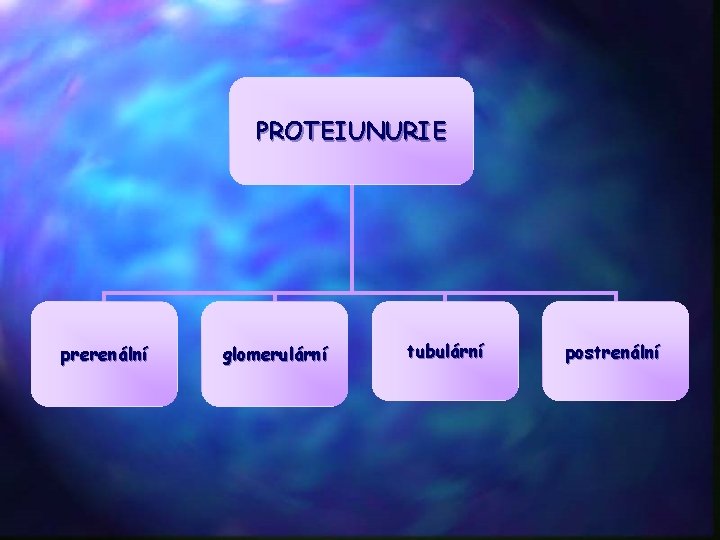
PROTEIUNURIE prerenální glomerulární tubulární postrenální

Proteinurie • Prerenální – při nadměrné produkci nízkomolekulárních proteinů jako • lehké řetězce imunoglobulinů (myelom, AL amyloidóza) • myoglobin (rhabdomyolýza) • Glomerulární – díky zvýšené glomerulární permeabilitě proteiny – primární a sekundární GN • Selektivní – albumin (př. minimální změny) • Neselektivní - albumin + proteiny o vyšší molekulové hmotnosti jako gamaglobuliny (př. membranózní nefropatie)

Proteinurie • Tubulární – při snížené reabsorbci v tubulech (α 1 -mikroglobulin, NAG, př. u TIN) • Glomerulotubulární (smíšená) – CHSL • Postrenální – močové cesty (α 2 -makroglobulin, př. tumory močového měchýře, prostatitida) • Posturální (orthostatická) proteinurie • Febrilní proteinurie

Tubulární proteinurie • β 2 - mikroglobulin • Mr 11 500, 100 Ak • v plazmě v nízké koncentraci (asi 1, 6 mg/l) • snadno přechází do glomerulárního filtrátu, většina zpětně resorbována PT a degradována v lysosomech • jen malá část se dostává do definitivní moči (cca 0, 11 mg/d) • při poruše tubulární zpětné resorpce a degradace zvýšení v moči • v kyselých močích se však rozkládá !!! • α 1 -mikroglobulin • MR 26 000 -33 000 • část molekuly GP produkovaného v játrech, který v plazmě tvoří komplex s Ig. A • v moči jako „mikroprotein“, stálý i při kyselém p. H lépe se hodí pro dg tubulárních lézí • NAG (N-acetyl- β-D-glukosaminidáza) • lyzosomální enzym uvolňující se nefrotoxickým účinkem na PT (např. aminoglykosidy) s následnou cytolýzou a nekrózou

Tamm-Horsfallův protein (uromodulin) • glykoprotein (asi 30% sacharidů), makromolekulový polymer (Mr 7 -28. 106) • lokalizován na stěně tlustého raménka vzestupné kličky a nejproximálnější části DT (v moči 50 mg/d) • fyziologická funkce? • imunosupresivní funkce (brání adhezi mikroorganismů na povrch epitelových buněk moč. ústrojí, vysoká vazebná afinita pro IL-1, TNF, IL-2) • význam při nepropustnosti tlustého raménka pro vodu • za patologických stavů: matrix válců
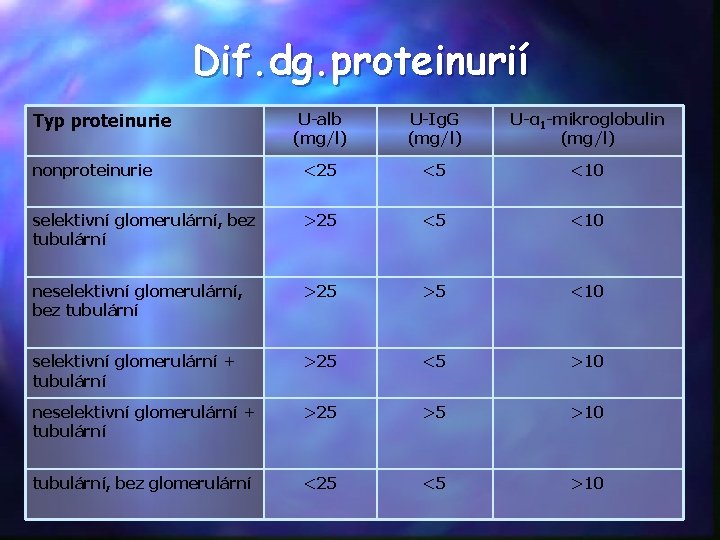
Dif. dg. proteinurií Typ proteinurie U-alb (mg/l) U-Ig. G (mg/l) U-α 1 -mikroglobulin (mg/l) nonproteinurie <25 <5 <10 selektivní glomerulární, bez tubulární >25 <5 <10 neselektivní glomerulární, bez tubulární >25 >5 <10 selektivní glomerulární + tubulární >25 <5 >10 neselektivní glomerulární + tubulární >25 >5 >10 tubulární, bez glomerulární <25 <5 >10

Albuminurie

Albuminurie • • • časná predikce diabetické nefropatie kontrola těhotenského diabetu patologické těhotenství (preeklampsie) nefropatie u hypertenze časná diagnostika glomerulární proteinurie jiného původu (hereditární, renovaskulární, infekční nefropatie) • rizikový faktor kardiovaskulárních onemocnění (u diabetiků atd. ) • „mikroalbuminurie“ není detekovatelná metodami kvalitativní analýzy (např. testovacími proužky)

Typ vzorku „mikroalbuminurie“ Sběr moči 30 -300 mg/24 hod Časovaný vzorek 20 -200 ug/min Náhodný vzorek 2, 8 -28 g/mol kreat Prokázaná „mikroalbuminurie“: dosažení uvedených hodnot ve dvou ze tří po sobě následujících vzorcích v intervalu 3 -6 měsíců

Preanalytické podmínky • Národní doporučení: - vzorek 2. ranní moči - stanovení ve sběru moči získaném během nočního odpočinku • Mezinárodní doporučení: - sběr moči za 24 hod - akceptovány i jednorázové (1. ranní moč) či časované vzorky (sběr za 4 hodiny či vzorek sebraný přes noc)

Stabilita albuminu • Při teplotě 4 -20 o. C minimálně 1 týden • Při teplotě -20 o. C mírné snižování albuminurie!!! • Při teplotě -70 o. C a nižší 6 měsíců

Koncentrace albuminu v moči se zvyšuje: při fyziologických dějích: • zvýšená fyzická námaha • zvýšený příjem bílkovin v dietě • těhotenství při patologických dějích: • akutními chorobné stavy • infekce močových cest • zvýšená koncentrace glukózy v krvi • infekce GIT • kardiální choroby • arteriální hypertenze

Cirkadiální variabilita • ve dne albuminurie cca o 25% vyšší než v noci • rozdíly mezi jednotlivými dny mohou být až 40% noční sběr moči • u diabetiků nevykazuje albumin v moči cirkadiální variabilitu!!

Metody stanovení: • • Imunoturbidimetrie, imunonefelometrie RIA, ELISA HPLC Elektroforéza (PAGE, kapilární)

Imunoturbidimetrie • Vzorek obsahující lidský albumin je vhodně naředěn a poté reaguje se specifickou protilátkou za tvorby precipitátu • Tvorba precipitátu je měřena turbidimetricky při 340 nm • Výpočet provádí systém automaticky z naměřené absorbance a kalibrační křivky

prostředí s rozptýlenými částicemi zdroj světla detektor procházejícího záření TURBIDIMETRIE detektor odraženého záření NEFELOMETRIE měřící cela zdroj světla detektor procházejícího světla optika detektor rozptýleného světla

• Imunochemické metody hrubě podhodnocují koncentrace albuminu v moči • Příčinou je fragmentace albuminu v moči, změna konformace molekuly a ztráta části imunoreaktivity

Ztráta imunoreaktivity albuminu: • fragmenty albuminu určitý podíl intaktního albuminu (Mr 66 500) při průchodu proximálními tubuly ledvin proteolyticky štěpen lyzozomálními enzymy na fragmenty o Mr 500 -15000 • „nicked albumin“ konformačně změněný albumin (v důsledku přítomnosti fragmentů albuminu), velikost molekuly zůstává nezměněna, pravděpodobně dojde ke ztrátě některých disulfidových můstků

• U zdravých jedinců peptidy odvozené od albuminu tvoří pravděpodobně i více než 90% celkového množství albuminu v moči (intaktní albumin méně než 10%) • Rozdíl imunochemické metody vs HPLC podstatně výraznější u diabetiků než u nediabetiků

• Detekce zvýšených koncentrací imunochemicky nereaktivního albuminu v moči metodou HPLC umožní diagnostikovat diabetickou nefropatii v průměru o 4 roky dříve u DM I. typu a o 2, 5 roku u DM II. typu ü Comper, W. D. , Osicka, T. M. , Jerums, G. High prevalence of immuno-unreactive albumin in urine of diabetic patients. Am. J. Kidney Dis. , 2003, 41, p. 336 -342. ü Comper, W. D. , Osicka, T. M. , Clark, M. , Maclssac, R. J. , Jerums, G. Earlier detection of microalbuminuria in diabetic patients using a new urinary albumin assay. Kidney Int. , 2004, 65, p. 1850 -1855. ü Osicka, T. M. , Comper W. D. Characterization of immunochemically nonreactive urinary albumin. Clin. Chem. , 2004, 50, p. 2286 -2291.

• Kontroverzní zjištění: zvýšené hodnoty albuminu získané HPLC nejsou způsobeny imunochemicky nereaktivním albuminem, ale koelucí některých močových proteinů z kolony (orosomukoid, transferrin, inhibitor proteináz alfa 1) HPLC tedy není schopna rozlišit albumin od těchto močových proteinů a poskytuje falešně zvýšené výsledky ü Sviridov, D. , Meilinger, B. , Drake S. K. , Hoehn G. T. , Hortin G. L. Coelution of other proteins with albumin during site-exclusion HPLC: Implications for analysis of urinary albumin. Clin. Chem. , 2006, 52, p. 389 -397.

HPLC High performance liquid chromatography Vysokoúčinná kapalinová chromatografie metoda umožňující separaci a stanovení látek ve směsi § rozdělení látek ve směsi podle jejich chemických a fyzikálních vlastností § vzorek nesený mobilní fází protéká přes kolonu § eluát z kolony protéká detektorem § detektor měří některou z fyzikálních vlastností eluátu absorbci v UV fluorescenci schopnost oxidace či redukce

Další biomarkery diabetické nefropatie

Podocytární proteiny a jejich fragmenty • podocyty = klíčové strukturální elementy glomerulární filtrační bariéry • detekovány i v moči pacientů (diabetiků či pacientů s CHRI) bez (mikro)albuminurie • nefrin • nebyly detekovány u zdravých kontrol

Glykosaminoglykany • přítomnost diabetu ovlivňuje metabolismus extracelulární matrix • močová exkrece GAG pozitivně koreluje s délkou trvání diabetické nefropatie

Kolagen typu IV • hlavní komponentou extracelulární matrix • byl nalezen v moči diabetiků s (mikro)albuminurií, nikoliv u jiných pacientů s albuminurií • není citlivějším markerem než albumin (detekovatelný pouze v přítomnosti albuminurie)

Polyklonální volné lehké řetězce imunoglobulinů • by-produkty normální syntézy imunoglobulinů • z cirkulace odstraňovány převážně ledvinami • diabetici II. typu mohou mít významně zvýšené koncentrace polyklonálních volných lehkých řetězců v séru a v moči ještě před rozvojem zjevného onemocnění ledvin

Produkty pokročilé glykace • heterogenní skupina látek • vzniká neenzymovou glykací a vlivem oxidačního stresu • souvisí s rozvojem diabetických komplikací

Funkční vyšetření ledvin
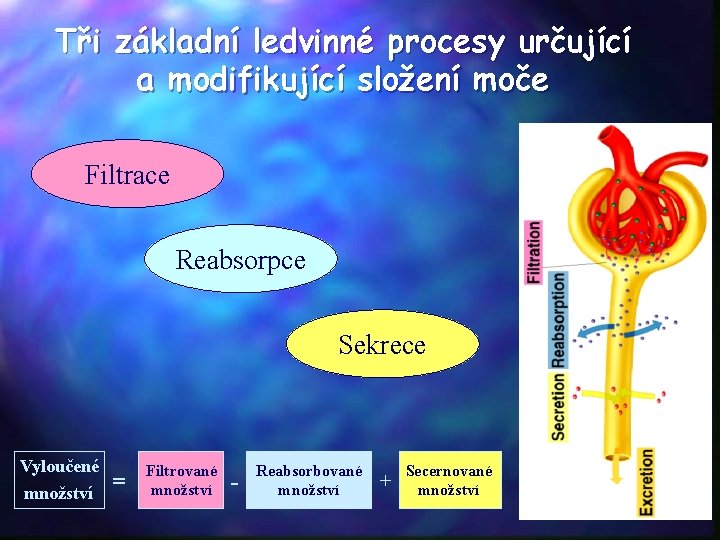
Tři základní ledvinné procesy určující a modifikující složení moče Filtrace Reabsorpce Sekrece Vyloučené množství = Filtrované množství - Reabsorbované množství + Secernované množství

Úkoly funkčního vyšetření ledvin učinit si představu o: • velikosti fungujícího parenchymu • o progresi onemocnění (opakovaným vyšetřením v malých časových intervalech) • o charakteru patologického procesu probíhajícího v ledvině (pomáhá stanovit přesnou dg)

Funkční vyšetření ledvin • sledování diurézy • glomerulární filtrace • koncentrační schopnost ledvin • renální vylučování iontů (Na, K, Ca, Pi, kyseliny močové, šťavelové, cystinu. . ) • renální vylučování všech osmoticky aktivních látek • acidifikační činnost ledvin

Sledování diurézy • anurie: diuréza < 100 ml/d • oligurie: diuréza < 500 ml/d zdravým ledvinám stačí k vyloučení denní dávky osmoticky aktivních látek (asi 600 mmol) cca 0, 5 l moči u nemocných v hyperkatabolickém stavu (sepse, stavy po operacích, úrazech) je produkce osmoticky aktivních látek mnohem vyšší (až přes 3000 mmol/d) a množství tekutiny potřebné k jejich vyloučení ledvinami neschopnými koncentrovat moč až přes 10 l/d (každá menší diuréza – “oligurie“)

Glomerulární filtrace Pasivní děj - krevní plazma je filtrována přes molekulární síto: • endotel kapilár • bazální membrána: kolagen IV, glykoproteiny (fibronektin a laminin), GAG • výběžky podocytů • neomezeně prochází molekuly do Mr 5000 bez výrazného náboje • negativní náboj bariéry odpuzuje negativně nabité částice (albumin)
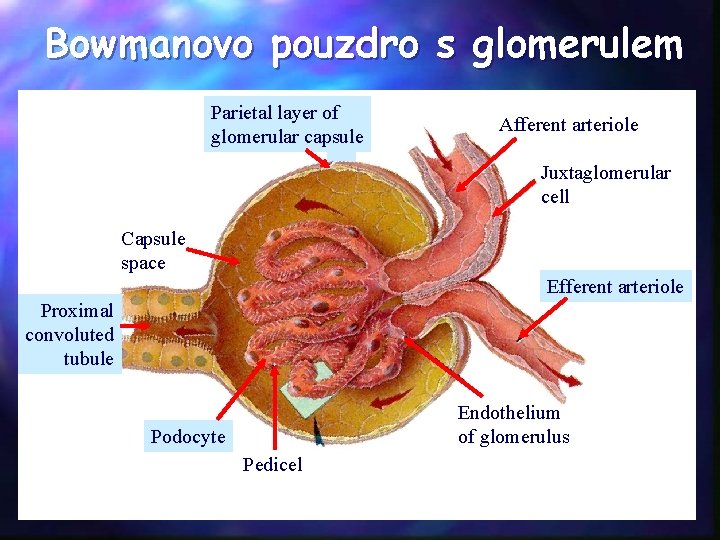
Bowmanovo pouzdro s glomerulem Parietal layer of glomerular capsule Afferent arteriole Juxtaglomerular cell Capsule space Efferent arteriole Proximal convoluted tubule Endothelium of glomerulus Podocyte Pedicel
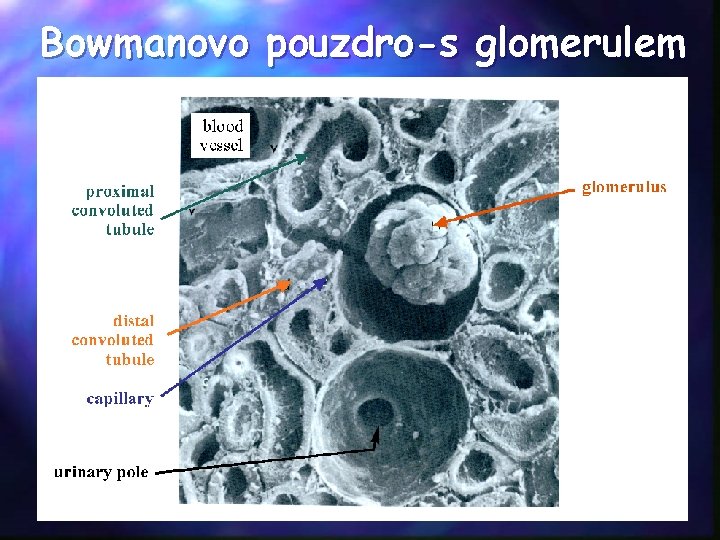
Bowmanovo pouzdro-s glomerulem
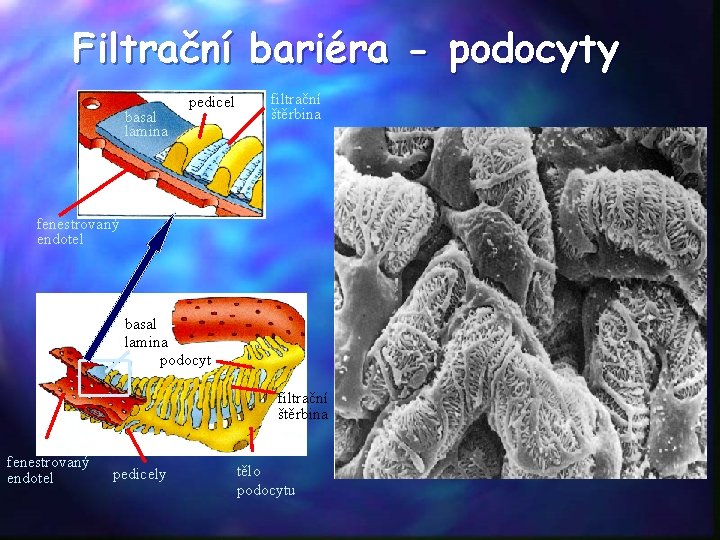
Filtrační bariéra - podocyty basal lamina pedicel filtrační štěrbina fenestrovaný endotel basal lamina podocyt filtrační štěrbina fenestrovaný endotel pedicely tělo podocytu

Glomerulární filtrace (GF) • Glomerulární filtrát = filtrát plazmy, která prochází glomerulární bariérou do močového prostoru (1 000 ml/min=20% srdečního minutového výdeje) • Faktory rozhodující o filtraci v glomerulárních kapilárách: • rozsah kapilárního řečiště (velikost filtrační plochy) • permeabilita kapilár • gradienty hydrostatických a onkotických tlaků přes kapilární membránu • Celková GF = součet GF každého nefronu (po 1 mil. nefronů v každé ledvině) metody přímé metody výpočtové

Glomerulární filtrace (GF) • GF vyjádřená jako renální clearance (C): virtuální objem plazmy, který je v určité časové jednotce (ml/s, ml/min) ledvinami od sledované látky zcela očištěn CA = UA. V PA • V = objem moči za jednotku času (ml/s, ml/min) • UA = močová koncentrace látky • PA = plazmatická koncentrace látky

Glomerulární filtrace (GF) Užitečná pro • odhad renální funkce • monitorace progrese renální insuficience • umožní předvídat potřebu náhrady funkce ledvin • určuje redukci dávek léčiv – ATB při ren. insuf. Ideální látka pro měření clearance : • bezpečná, levná, jednoduché měření • volně filtrována v glomerulu (bez vazby na bílkoviny) • bez reabsorbce, sekrece v ledvinách • bez extrarenální eliminace

Odhad GF v klinické praxi • Měření: 1. clearance inulinu/polyfruktosanu 2. clearance kreatininu 3. izotopové metody • Odhad dle vzorců: 1. pro dospělé (muž/žena/rasa): MDRD, (Cockcroft Gault) 2. pro děti (Schwartz) 3. výpočet GF z koncentrace cystatinu C

Clearance inulinu (Cin) • nejpřesnější metoda měření GF, „zlatý standard“, referenční metoda • inulin = fruktózový polysacharid (32 molekul fruktózy, Mr 5200) volně prochází glomerulární membránou, v tubulech není ani resorbován ani seceronován, nevýhoda: nerozpustný ve studené vodě • syntetický polyfruktosan = jeho Mr o 1000 menší než inulinu, je rozpustný ve studené vodě • podmínkou meření: udržení konstantní hladiny v plazmě (200 -300 mg/l, kontinuální intravenózní infuze), přesný sběr moči (dříve: cévkování močového měchýře, dnes: zvyšování diurézy požitím vody před zahájením vyšetření, prodloužení sběrné močové periody na 60 -90 min) procedura je náročná a nehodí se pro rutinní vyšetření Fyziologické hodnoty (Smith, 1957): • Muži: 2, 07 ± 0, 43 ml/s / 1, 73 m 2 ( = 124 ± 25, 8 ml/min/1, 73 m 2) • Ženy: 1, 82 ± 0, 23 ml/s /1, 73 m 2 (= 109 ± 13, 5 ml/min/1, 73 m 2)

Plazmatická clearance inulinu • je-li během infuze při vyšetření plazmatická hladina stabilizována (na hodnotě P, která je v rozmezí 200 -300 mg/l), pak močové vylučování (UV) je stejně velké, jako je množství inulinu dodávaného infuzí (Iinf) a platí vztah: Cin = Iinf/ P • dojde-li k zakolísání P během vyšetřování, počítá se Cin podle vzorce: Cin = celkové množství inulinu infundované během vyšetření/ AUC=plocha vymezená plazmatickými koncentracemi a časovou osou

Plazmatická clearance inulinu • po jednorázovém i. v. podání inulinu následuje exponenciální pokles jeho koncentrace, podíl dávky a AUC určuje Cin • jednorázová intravenózní aplikace (50 mg/kg) inulinu • odběr vzorku venózní krve obvykle v 30. , 60. a 90. minutě • pokles plazmatických koncentrací probíhá v exponenciální závislosti na čase (po nanesení hodnot na semilogarimický papír dostáváme křivku) • podle sklonu křivky určíme obvykle graficky t 1/2 • není nutný sběr moče!!

Clearance kreatininu CKr = UCr. V SKr • částečné vylučování kreatininu sekrecí proximálním tubulem (nadhodnocuje GF - je falešně vyšší), s klesající GF podíl tubulární sekrece stoupá progresívní nadhodnocení GF při jejím zhoršování • kompetitivní inhibice tubulární sekrece (cimetidin, trimetoprim, spironolakton) • • • u zdravého dospělého člověka CKr jen lehce přesahuje GF (o 10 -20%) v důsledku nevelké tubulární sekrece u jedinců s CHRI (CKD 4 a 5) se tubulární sekrece relativně zvyšuje (vzhledem k velmi snížené GF), v konečných stádiích CHSL může CKr přesahovat GF o 100 i více % přepočet na ideální tělesný povrch (1, 73 m 2)

Příklad výpočtu clearance kreatininu • S-Cr: 200 umol/l • U-Cr: 4 mmol/l • V: 2, 4 l/24 h • CKr = UV/S = (4 x 2400/24/60/60)/0, 2 = 0, 55 ml/s

Vztah mezi PKr a GF hyperbolický PKr indikátor málo senzitivní


Kreatinin • vzniká v organizmu dehydratací kreatinu uvolněného při svalové činnosti z kreatinfosfátu v množství, které je úměrné svalové hmotě • při normální funkci ledvin jeho koncentrace v séru nepodléhá větším změnám • vylučuje se ledvinami glomerulární filtrací a protože jeho vylučování během 24 hodin je téměř konstantní, používá se pro sledování funkce ledvin • při poklesu glomerulární filtrace pod 50 % dochází k vzestupu sérového kreatininu. věk sérum [umol/l] moč [mmol/l] 0 -6 týdnů 12 -48 1, 2 -4, 4 6 tý-1 rok 21 -55 0, 4 -5, 4 1 -15 let 27 -88 5, 7 -14, 7 >15 let M: 44 -115 Ž: 44 -97 5, 7 -14, 7

Koncentrace kreatininu v séru • Extrarenální faktory působící na hodnotu SKr: • extrarenální vylučování kreatininu (především střevem u jedinců s pokročilejší chron. renální insuf. ) • změny distribučního prostoru kreatininu (zvláště u jedinců s velkými otoky) • rozdíly v objemu svalové hmoty • příjem masa, proteinů a aminokyselin v dietě • produkce kreatininu závisí též na funkci jater CAVE: pacienti se svalovou atrofií, malnutricí, závažnějším jaterním postižením !!!

Stanovení kreatininu • Jaffého reakce (popsána v roce 1886) kreatinin reaguje v alkalickém prostředí s kyselinou pikrovou za vzniku oranžového komplexu (enol forma kreatin pikrátu), který však není specifický pouze pro kreatinin (s kys. pikrovou reaguje také glukóza, kyselina močová, askorbát, acetát, pyruvát, ale i léky zvyšujícící sérový kreatinin-cefalosporiny, trimetoprim, cimetidin) • Enzymatické stanovení kreatininu (specifičtější, ale nákladnější) Taganelliho metoda, měří se pokles absorbance při 340 nm způsobený oxidací NADPH (pokles absorbance je nepřímo úměrný obsahu kreatininu ve vzorku). Kreatinin je za přítomnosti kreatinindeiminázy přeměněn na amoniak a N-methylhydantoin. Amoniak reaguje s 2 - oxoglutamátem a NADPH. Reakce je katalyzována glutamátdehydrogenázou a vzniká při ní glutamát a NADP. • Hmotnostní spektrometrie s izotopovou dilucí = referenční metoda Výsledky měření kreatininu pomocí Jaffého metody jsou zatíženy systematickou chybou v závislosti na koncentraci kreatininu: v oblasti koncentrací menších než cca 130 umol/l pozitivní, ve vyšších koncentracích negativní !!!

Koncentrace cystatinu C • užívána i při rychlých změnách GF (nejlepší korelace s GF je do úrovně lehčího poškození tubulární funkce) • cystatin C = polypeptid patřící do velké „rodiny“ cysteinových proteáz • vytvářen všemi jadernými buňkami, volně prochází glomerulární membránou, zachycován tubulárními buňkami • molekuly cystatinu C, které pronikly do nitra tubulárních buněk, jsou však v jejich nitru metabolizovány, do peritubulární extracelulární tekutiny žádný cystatin C nepřechází očišťování extracelulární tekutiny od cystatinu C je přímo úměrné GF Rovnice podle Grubba (PETIA): e. GFR = 1, 4115. Scyst -1, 68. F [ml. s-1. 1. 73 m-2] Rovnice podle Leveyova (PENIA): e. GFR = 1, 278. Scyst -1, 19. F [ml. s-1. 1. 73 m-2] Scyst [mg/l], F. . . koeficient (děti do 14 let F 1, 384, muži F=1, ženy F=0, 948) • nález cystatinu C v definitivní moči = tubulopatie
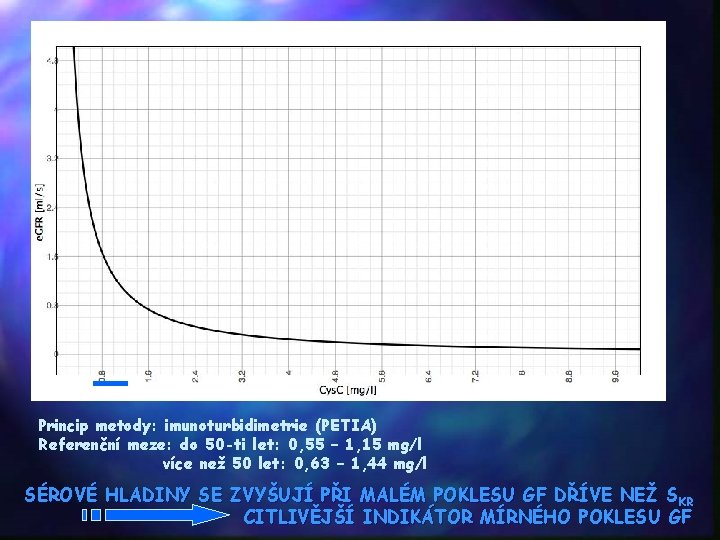
Princip metody: imunoturbidimetrie (PETIA) Referenční meze: do 50 -ti let: 0, 55 – 1, 15 mg/l více než 50 let: 0, 63 – 1, 44 mg/l SÉROVÉ HLADINY SE ZVYŠUJÍ PŘI MALÉM POKLESU GF DŘÍVE NEŽ S KR CITLIVĚJŠÍ INDIKÁTOR MÍRNÉHO POKLESU GF

• sérové koncentrace cystatinu C v průběhu 24 h téměř konstantní • výpočet GF pomocí cystatinu C nelze použít: • při podávání glukokortikoidů (zvyšují Cyst. C) • u pacientů s nekompenzovanou hyperthyreózou (zvýšení cyst. C) či hypothyreózou (snížení Cyst. C) • u pacientů s progresí melanomu, lymfoproliferativních procesů a kolorektálního CA (zvýšení Cyst. C)

Izotopové metody vyšetření GF • • • 99 m. Tc-DTPA (diethyltriaminopentaoctová kyselina) 51 Cr-EDTA (ethylendiaminotetraoctová kyselina) 125 I-thalamát • vylučování izotopem značených látek ledvinami • rychlost poklesu aktivity v plazmě dána velikostí GF, resp. tubulární sekrece • dynamická scintigrafie: možnost posouzení odděleně funkce P a L ledviny (99 m. Tc-MAG 3 (merkaptoacetyltriglycin), 99 m. Tc-DTPA) • použitá látka značená izotopem jednorázově aplikována i. v. a ve stanovených časových intervalech sledován exponenciální pokles plazmat. koncentrace plazmat. clearance (pro látky vylučované pouze GF identická s její renální clearancí - 51 Cr-EDTA, 99 m. Tc-DTPA) • 123 I-OIH, 131 I-OIH (orthoiodhippuran)-efektivní průtok plazmy ledvinami • GF/ERPF = filtrační frakce (18 -22%)

Renální clearance močoviny • urea: • • • primárním produktem detoxikace amoniaku, vzniká jako jeden z hlavních produktů při metabolizmu bílkovin tvorba probíhá v játrech denní produkce je asi 0, 5 – 0, 7 mol/den cca 90 % se vylučuje ledvinami (vylučována GF, tubulární sekrecí, je zpětně resorbovánastoupá při omezení GF pod 30%), 30% 10 % trávicím traktem a kůží koncentrace v krvi závisí na denním příjmu proteinů, jejich katabolizmu a vylučování • stanovení urey (enzymatická reakce Roch Ramelova): ureasa urea + 2 H 2 O 2 NH 4+ + CO 322 -oxoglutarát + NH 4+ glutamátdehydrogenasa L-glutamát +H 2 O NADH+H+ NAD+ oxidace NADH na NAD se sleduje kineticky jako pokles absorbance při 340 nm věk sérum [mmol/l] moč [mmol/d] 0 -6 týdnů 0, 7 – 5, 0 2 -17 6 tý-1 rok 0, 4 -5, 4 29 -123 1 -15 let 1, 8 -6, 7 67 -333 >15 let M: 2, 8 -8, 0 Ž: 2, 0 -6, 7 167 -583

Renální clearance močoviny • podhodnocuje GF z závislosti na diuréze • při hodnotách diurézy > 2 ml/min klesá zpětná resorpce urey v závislosti na osmotickém gradientu a pak se Curea blíží hodnotě GF • málo používaná metoda (většinou ji lze použít ke zhodnocení stupně katabolismu bílkovin) • z vyloučeného množství urey v moči/24 h lze odhadnout i množství metabolizované tělesné bílkoviny- při vyrovnané dusíkové bilanci množství přijímaných bílkovin v dietě (0, 25. Uurea V/24 h) Aproximace CKr a Curea: GF = CKr + Curea 2 ve stadiu 4 a 5 CKD je přesnější vztah: GF = 0, 4 Ckr + 0, 6 Curea (zvýšená tubulární sekrece kreatininu, snížená zpětná resorpce urey při polyurii v reziduálních nefronech)

Výpočtové metody odhadu GF (e. GF) 1. rovnice podle Cockcrofta a Gaulta 2. rovnice MDRD: Modification of Diet in Renal Disease (Levey A. S. & spol. , 1999) 3. rovnice podle Schwartze pro děti

Odhad clearance kreatininu dle Cockcrofta a Gaulta CKr = (140 -věk). hmotnost 48, 9. SKr . 0, 85 (ženy) [ml. s-1. 1, 73 m-2 ] věk. . roky tělesná hmotnost v kg SKr v umol/l SKr (mg/dl) x 72 → (umol/l) při přesném měření hodnot GF zvláště u jedinců s vysokou tělesnou hmotností a vyšších věkových kategorií zaznamenány větší rozptyly hodnot změřených vs. vypočtených ODBORNOU VEŘEJNOSTÍ JIŽ METODA POVAŽOVÁNA ZA OBSOLENTNÍ!

Odhad GF pomocí MDRD • • • Modification of Diet in Renal Disease velká multicentrická studie, která sledovala vliv příjmu bílkovin v potravě na rychlost progrese chronických renálních onemocnění krokovou multivariantní regresní analýzou odvozeny následující vzorce: e. GF = 100, 6339. SKr-0, 999. věk-0, 176. Surea-0, 170. Salb 0, 318. 0, 762 (ženy). 1, 18 (černá populace) [ml. s-1. 1, 73 m-2] e. GF = 547, 1535. SKr-1, 154. věk-0, 203. 0, 742 (ženy). 1, 21 (černá populace) [ml. s-1. 1, 73 m-2] e. GF = 515, 3832. (stand SKr)-1, 154. věk-0, 203. 0, 742 (ženy). 1, 21 (černá populace) [ml. s-1. 1, 73 m-2] věk [roky], SKr [umol/l], Surea. [mmol/l], Salb [g/l] • • u vypočtených hodnot vyšších než 1, 5 ml. s-1. 1, 73 m-2 se doporučuje uvádět hodnotu ≥ 1, 5 ml. s-1. 1, 73 m-2 vzhledem k nepřesnosti rovnice v této oblasti hodnoty 1 až 1, 5 ml. s-1. 1, 73 m-2 nutno individuálně hodnotit ve vztahu ke klinickému obrazu hodnota nižší než 1 ml. s-1. 1, 73 m-2 považována za patologickou od 40 let věku hodnota e. GF klesá přibližně o 0, 17 ml. s-1. 1, 73 m-2 na dekádu

CKD-EPI rovnice • Chronic Kidney Disease Epidemiology Collaboration formula • Publikováno v květnu 2009, Levey et al. • Nahrazuje dnes již nedoporučovanou rovnici MDRD, zvláště je-li GF větší než 1 ml/s/ 1, 73 m 2 Černé ženy: SKr (mg/dl) ≤ 0, 7 e. GFR=166 x (SKr/0, 7)-0, 329 x 0, 993 věk SCr (mg/dl) > 0, 7 e. GFR=166 x (SKr/0, 7)-1, 209 x 0, 993 věk Bílé ženy: SKr (mg/d. L) ≤ 0, 7 e. GFR=144 x (SKr/0, 7) SKr (mg/d. L) > 0, 7 e. GFR=144 x (SKr/0, 7) Černí muži: SKr (mg/d. L) ≤ 0, 9 e. GFR=163 x (SKr/0, 9)-0, 411 x 0, 993 věk SKr (mg/d. L) > 0, 9 e. GFR=163 x (SKr/0, 7)-1, 209 x 0, 993 věk Bílí muži: SKr (mg/d. L) ≤ 0, 9 e. GFR=141 x (SKr/0, 9) -0, 411 x 0, 993 věk SKr (mg/d. L) > 0, 9 e. GFR=144 x (SKr/0, 9) -1, 209 x 0, 993 věk -0, 329 x 0, 993 věk -1, 209 x 0, 993 věk

Rovnice Lund-Malmö • Odvozena pro standardizované stanovení kreatininu • Je možné ji použít jak pro dospělé, tak pro děti od 1 roku života • Odpovídá dobře instrumentálním metodám • Lze ji použít v rozsahu kreatininu 45 -545 μmol/l • Odvozena na evropské populaci SKr < 150 μmol/l e. GFR = EXP ((4, 62 -0, 0112*SKr)- 0, 0124*věk+0, 339*(LN(věk))0, 226*pohlaví)/60 (ml/s/1, 73 m 2) SKr ≥ 150 μmol/l e. GFR = EXP ((8, 17+0, 0005*SKr -1, 07*LN(SKr))0, 0124*věk+0, 339*(LN(věk))-0, 226*pohlaví)/60 Pohlaví je 0 pro muže, 1 pro ženy EXP= základ přirozeného logaritmu umocněný na zadané číslo LN= přirozený logaritmus

Rovnice Lund-Malmö s korekcí na LBM • Korekce na „libovou“ hmotu (lean body mass), která se určuje postupem podle Jamese z tělesné výšky (v cm, doporučený interval 67 -189 cm) a hmotnosti (v kg, doporučený interval 8 -111 kg) SKr < 150 μmol/l e. GFR = EXP ((4, 95 -0, 011*SKr)- 0, 00587*věk+0, 00977*LBM)/60 (ml/s/1, 73 m 2) SKr ≥ 150 μmol/l e. GFR = EXP ((8, 58+0, 0005*SKr -1, 08*LN(SKr))0, 00587*věk+0, 00977*LBM))/60 LBM podle Jamese Ženy: LBM=1, 07*hmotnost-148*(hmotnost/výška)2 Muži: LBM=1, 1*hmotnost-120*(hmotnost/výška)2

Kvadratická rovnice Mayo Clinic • Rule et al. • Lépe stanoví GFR u pacientů se zachovanou renální funkcí e. GFR= exp(1, 911+5, 249/SKr -2, 114/SKr 2 0, 00686 x věk-[0, 205 u žen]) • Je-li SKr< 0, 8 mg/d. L, užije se hodnota 0, 8 mg/d. L pro SKr

Odhad GF u dětí pomocí rovnice dle Schwartze F. výška e. GF = [ml. s-1. 1, 73 m-2 ] SKr výška [cm], SKr [umol/l] Maximální koncentrace sérového kreatininu pro jedince dané tělesné výšky: SKr(max) = vcm. 0, 54 [umol/l] =poslední, ještě normální koncentrace sérového kreatininu při dolní hranici GF (1, 5 ml. s-1. 1, 73 m-2) Podmínka Faktor F věk do 1 roku 0, 663 0, 487 u předčasně narozených dívky, věk od 1 do 18 let 0, 810 chlapci, věk od 1 do 12 let 0, 810 chlapci, věk od 12 do 18 let 0, 959 velký význam pro orientační odhad hladiny sérového kreatininu: např. u 3 -letého dítěte s výškou 100 cm je SKr(max) pouze 54 umol/l, u 2 -letého s výškou 86 cm pouze 46, 5 umol/l

Chronické poškození ledvin Definice chronického poškození ledvin podle doporučení National Kudney Foundation (K/DOQI) z roku 2002: 1. Strukturální nebo funkční postižení ledvin trvající déle než 3 měsíce s poklesem nebo bez poklesu GF 2. GF <1, 0 ml. s-1. 1. 73 m-2 déle než 3 měsíce s nebo bez postižení ledvin Stupeň Klinický popis GF [ml. s-1. 1. 73 m-2] 1 normální GF, ale známky poškození ledvin ≥ 1, 5 2 mírná CHRI 1 -1, 49 3 střední CHRI 0, 50 -0, 99 4 těžká CHRI 0, 25 -0, 49 5 konečné stadium CHRI, léčba selhání funkce ledvin <0, 25 (histol. , moč. sediment)
![Akutní poškození ledvin Acute Kidney Injury (AKI) RIFLE SKr [umol/l] GF [ml/s] Diuréza [ml. Akutní poškození ledvin Acute Kidney Injury (AKI) RIFLE SKr [umol/l] GF [ml/s] Diuréza [ml.](http://slidetodoc.com/presentation_image/1c4317a80dc00047228daa6ac47e9000/image-93.jpg)
Akutní poškození ledvin Acute Kidney Injury (AKI) RIFLE SKr [umol/l] GF [ml/s] Diuréza [ml. kg-1. h-1] Riziko (Risk) SKr> o 50% (1, 5 x) oligurie-D <0, 5 GF < o 25% minimálně 6 h v průběhu 1 -7 dnů neoligoanurie-D zachována I. Poškození ledvin (Injury) SKr > o 100% (2 x) GF < o 50% II. Selhání ledvin (Failure) SKr> o 200% (3 x) nebo oligurie-D <0, 5 III. -ASL SKr> 350 umol/lpři delší než 24 h vzestupu o 50 umol/l/d či anurie minimálně 12 h GF < o 75% neoligoanurie-výjimečně D zachována Ztráta funkce ledvin (Loss) ASL s afunkcí delší než 4 tý anurie či oligurie Terminální selhání funkce (End-stage kidney disease) afunkce trvající déle než 3 m anurie či oligurie-D <0, 5 minimálně 12 h neoligoanurie-D zachována AKI stádia s výhodou výpočet GF pomocí cystatinu C !!!

Nové biomarkery u akutního poškození ledvin 1) Neutrofilní lipokalin asociovaný s gelatinázou (NGAL, lipocalin-2, siderocalin) • původně identifikován jako složka neutrofilních granulí • 25 k. Da protein kovalentně vázaný na gelatinázu z neutrofilů (matrix metalloproteinázu-9, MMP-9) • význam v imunitní odpovědi (působí bakteriostaticky ovlivněním transportu železa), pro diferenciaci buněk a jejich přežití • za fyziologických podmínek exprimován ve velmi malém množství v řadě tkání a orgánech (v ledvině, plicích, žaludku, střevě) • zvýšení exprese indukováno poškozením epitelu • syntéza indukována v ledvinách po ischemickém a nefrotoxickém poškození • jeho zvýšení v séru a v moči 24 -48 h před zvýšením kreatininu • AKI, CHRI • zvýšení též u pacientů s akutní bakteriální infekcí či infekcí moč. cest, CA pankreatu či prsu

2) Interleukin 18 • prozánětlivý cytokin, indukován po akutním poškození ledvin, štěpen v proximálním tubulu • jeho pro-forma je přeměňována intracelulární cysteinovou proteázou (kaspázou-1) na aktivní formu, která opouští buňku a vylučuje se do moči • zvýšení u pacientů s AKI (x nikoliv u CHSL, infekce moč. cest, NS, SL prerenální etiologie) • v moči se objevuje cca o 4 h později než NGAL 3) Molekula poškození ledvin (kidney injury molekule, KIM-1) • transmembránový protein, zvýšeně exprimován v nediferencovaných buňkách proximálního tubulu po ischemickém nebo nefrotoxickém poškození • jeho zkrácená doména vzniklá proteolytickým štěpením detekovatelná v moči • specifičtější pro ischemické poškození, není významně ovlivněn CHRI nebo infekcí moč. cest

Vyšetření průtoku krve ledvinami • látky, které jsou (téměř) kompletně extrahovány z krevního oběhu při jediné pasáži ledvinou • p-aminohippurová kyselina (PAH) • kombinuje se GF (16% plazmatické koncentrace PAH volně filtrováno) s tubulární exkrecí (tubulární buňky jsou schopny odebírat PAH z peritubulární krve a transportovat ji do tubulární tekutiny) • PAH je extrahována ledvinou z více než 90%

Vyšetření tubulárních funkcí

• v tubulech se normálně zpětně resorbuje 97 -98% glomerulárního filtrátu (cca 170 -180 l) • konečná moč-cca 1, 5 l, její složení závisí na zpětné resorpci a na sekreci solutů do lumen tubulů • pasivní (volná difuze), aktivní charakter (selektivní transport vyžadující dodání energie) • pouze zpětná resorpce (glukóza), sekrece (p-aminohippurová kyselina) • pasivní zpětná resorpce: osmotický gradient, p. H gradient, tok solventů

Proximální tubulus • místo obligatorní (na hormonech nezávislé) resorpce: • většiny Na+, Cl-, K+ a HCO 3 • asi 70% vody • veškeré glukózy a aminokyselin Na+ je resorbován aktivně, voda, chloridy a hydrogenkarbonát jej pasivně sledují • glukóza a AA jsou resorbovány sekundárně aktivním transportem přes specifické transportéry • močovina se do krve vrací pasivně (difúze)

Henleova klička • její funkcí je vytvářet hyperosmolární prostředí ve dřeni ledvin, které pak umožní koncentrovat moč ve sběracím kanálku • Protiproudový multiplikační systém • sestupné raménko propustné pro vodu, naopak se do tubulu dostává močovina → ↑osmolarita • vzestupné raménko je nepropustné pro vodu, ale je propustné pro Na+ a Cl- → ↓osmolarita • zde se resorbuje 20% filtrované vody
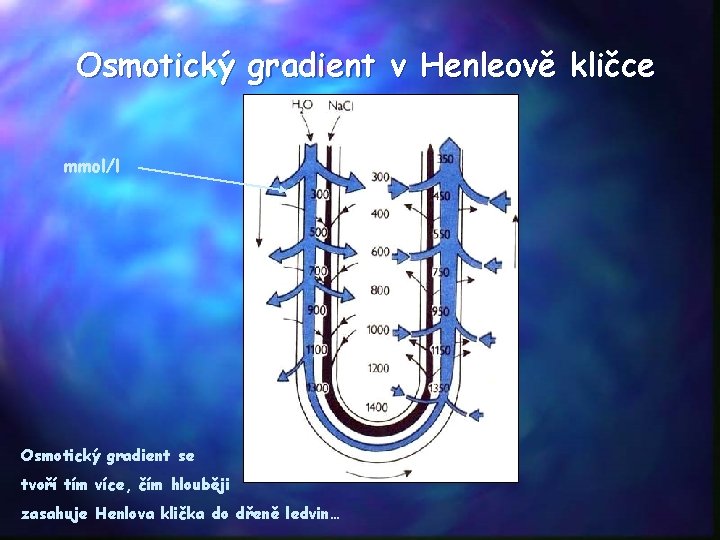
Osmotický gradient v Henleově kličce mmol/l Osmotický gradient se tvoří tím více, čím hlouběji zasahuje Henlova klička do dřeně ledvin…

Distální tubulus • resorpce Na+ a exkrece K +, závislá na aldosteronu • Aldosteron: • zvyšuje zadržování Na+ a tekutin, zvyšuje vylučování K + • působí v jádře indukci Na+/ K+ ATPázy na bazolaterální membráně • zvyšuje sekreci H+

Sběrací kanálek • finálně rozhoduje o objemu a osmolaritě definitivní moči • ADH ovlivňuje propustnost sběracího kanálku (aquaporiny) pro vodu: • v jeho přítomnosti se moč koncentruje, jak prochází hyperosmolární dření • v nepřítomnosti ADH se voda neresorbuje, moč zůstává hypotonická

Metabolismus vody – obligátní resorpce • ze 180 l glomerulárního filtrátu denně: • 60 - 70% (110 -130 l) je obligátně resorbováno v proximálním tubulu • asi 20% (40 l) v protiproudovém systému Henleovy kličky • zbyde asi 20 l hypotonické moči, která přijde do distálního tubulu…. . . zde začíná prostor pro možnou regulaci (aldosteron, ADH)

Tubulární resorpce (intenzitu možno měřit) 1. 2. stanovíme součin GF x plazmatická koncentrace látky GF. P (pouze část nenavázaná na proteiny) stanovíme množství látky vyloučené močí = objem moči (v čase) x koncentrace látky v moči U. V Výpočet: T = (GF. P) – (U. V) je-li látka v tubulech resorbována, je U. V menší než GF. P

Tubulární sekrece • • Jde o transport z peritubulární krve do lumen Sekrece endogenních organických látek se děje v konečné části proximálního tubulu (v pars recta), je tak možno vyloučit i látky vázané na proteiny Jsou 2 transportní systémy: Transportní systém pro organické kyseliny (anionty) Transportní systém pro organické báze (kationty) Je-li látka především secernována, pak U. V je větší než GF. P

• Zánik nefronu je spojen s adaptivními změnami v reziduálních nefronech • Pokles GF je kompenzován změnami v tubulární zpětné resorpci nebo tubulární sekreci • Z krátkodobého hlediska to umožňuje přechodnou stabilizaci vnitřního prostředí (pokles GF na 10% může být ještě vyrovnán u Na+, K+ nebo osmolality při dodržení dietních opatření, hladina urey a kreatininu však stoupá, stejně jako patologie Ca-Pi metabolismu a ABR) ABR • Dlouhodobě to vede k progresi poškození glomerulů a tubulů a k jejich skleróze

Koncentrační schopnost ledvin • správná funkce tubulů, dřeňový protiproudový systém, dřeňový osmotický gradient (Henleova klička, sběrné kanálky), propustnost sběracích kanálků pro vodu (ADH) • maximální koncentrační schopnost závislá na zachování integrity renálního parenchymu u nemocí postihující renální intersticium může být koncentrační schopnost snížena již u nemocných, kteří mají zcela normální GF • vyšetření u polyurických pacientů-rozlišení centrální vs. nefrogenní diabetes insipidus vs. psychogenní polydipsie

Koncentrační testy • Klasický test žízněním (obsolentní): • nemocný nepije a nepřijímá tekutiny obsahující větší množství vody (ovoce, zeleninu) • moč se sbírá ve čtyřhodinových intervalech po 12 -ti hod žíznění, (poslední vzorek-ne déle než 36 h žíznění, odebere se i vzorek žilní krve pro určení koncentračního indexu (Uosm/S-osm)) • zdraví jedinci: • 15 -30 let moč o osmolalitě 1000 mmol/kg H 2 O (specif. hmotnost 1030) • 31 -50 let moč o osmolalitě 900 mmol/kg H 2 O (specif. hmotnost 1028) • 51 -70 let moč o osmolalitě 800 mmol/kg H 2 O (specif. hmotnost 1026) • Zkrácený (Adiuretinový) test: • noc bez příjmu tekutin • ráno (cca za 13 h) se vymočí, poté je aplikováno intranasálně 10 -40 ug Adiuretinu (analog vasopresinu) • moč je sbíraná ve čtyřech 1 -hodinových intervalech, omezen příjem tekutin • zdraví jedinci • • • 15 -20 let 21 -50 let 51 -60 let 61 -70 let 71 -80 let osmolalita osmolalita moče moče >970 mmol/kg H 2 O >940 mmol/kg H 2 O >830 mmol/kg H 2 O >790 mmol/kg H 2 O >780 mmol/kg H 2 O

Osmolární clearance, exkreční frakce osmoticky aktivních látek • Osmolární clearance (COsm) • účinnost vylučování všech osmoticky aktivních látek • do 0, 05 ml/s • zvýšení: vyšší intenzita exkrece osmot. akt. l. např. u hyperkatabolických stavů, při výrazné hyperglykémii, při zvýšení urey v plazmě, obvykle provázeno polyurií (osmotická diuréza) • při sníženém příjmu Na. Cl, u hypoproteinémie nastává pokles • nemocní v kritických stavech: COsm nejdříve zvýšena, po poklesu GF klesá • Exkreční frakce osmolární: osmolární EFOsm = Cosm/CKr • norma do 0, 035 • zvýšení: tubulární resorpce osm. akt. l. je snížena, relativně větší část vylučována močí • stavy s výrazným snížením GF a zvýšením EFOsm: vylučování osm. akt. l. umožněno snížením resorpce v reziduálních nefronech (osmotická diuréza v těchto nefronech)

Clearance bezsolutové vody (CH 2 O) CH 2 O = V – COsm (V. . . objem moči v ml/s) • resorpce osmoticky aktivních látek v distálním úseku nefronu • udává, jaké množství vody bychom museli odstranit z moči hypotonické vůči plazmě, abychom její osmolalitu upravili na hodnotu plazmatickou (v tomto případě má CH 2 O hodnotu pozitivní) pozitivní • při tvorbě hypertonické moči (tj. běžná moč) je naopak v moči z tohoto hlediska nedostatek H 2 O a CH 2 O má hodnotu negativní • norma: -0, 027 až -0, 007 ml/s • při poruše dřeňového gradientu se CH 2 O zvyšuje na hodnoty ≥ 0, 004 ml/s • vzestup patologický při současném zvýšení osmolality plazmy (u pacientů v kritických stavech při hrozícím renálním selhání se CH 2 O a CKr mohou patologicky měnit již 12 -24 h před zvyšováním urey či kreatininu v plazmě a ještě před nástupem oligurie )

Acidifikační schopnost ledvin • měření p. H ranní moči p. H metrem (nemocný nesmí mít močovou infekci-např. Proteus produkuje ureázu, která rozkládá ureu na amonné ionty a zvyšuje p. H moči, p. H musí být změřeno bezprostředně po vymočení) • má-li nemocný s chronickou metabolickou acidózou p. H ranní moči > 6, dle pp. o distální renální tubulární acidózu • vyšetření p. H moči po zátěži acidifikujícími látkami (NH 4 Cl, Ca. Cl 2 v cca 0, 1 g/kg hmotnosti) • p. H moči by mělo klesnout na ≤ 5, 4 • sleduje se tzv. titrovatelná acidita a exkrece amonných iontů • vyšetření exkreční frakce hydrogenkarbonátu • dg. proximální tubulární acidózy
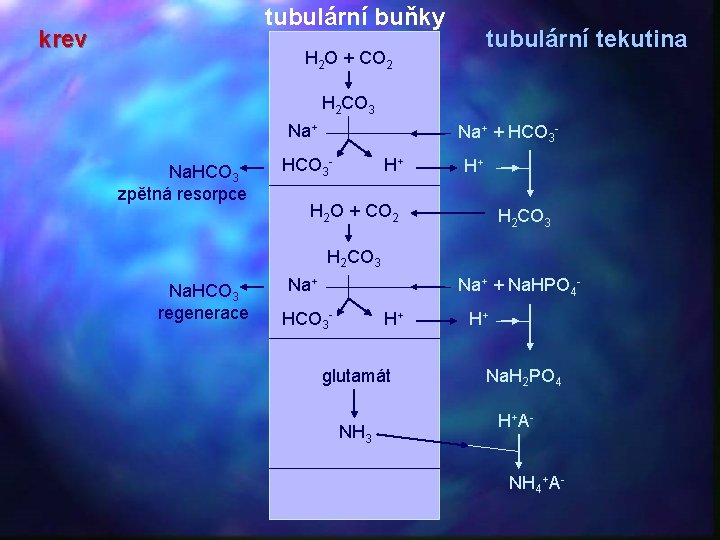
tubulární buňky krev tubulární tekutina H 2 O + CO 2 H 2 CO 3 Na+ Na. HCO 3 zpětná resorpce Na+ + HCO 3 - H+ H+ H 2 O + CO 2 H 2 CO 3 Na. HCO 3 regenerace Na+ + Na. HPO 4 - HCO 3 - H+ glutamát NH 3 H+ Na. H 2 PO 4 H+ A NH 4+A-

Sledování močových odpadů iontů • Na+, K+, Ca 2+, urátů, oxalátů, cystinu (urolitiáza), urey (příjem bílkovin v potravě) • frakční exkrece (FE) FEX = [UX/SX]/[UKr/SKr] [ %] • FE udává, jaká část sledované látky profiltrované v glomerulech se vyloučí do moči • u pacientů s ASL svědčí FENa<1% pro prerenální azotémii (ledviny mají schopnost retinovat v hypovolémii Na) • u pacientů s ASL, známkami hypovolémie a FENa>2% jde pp. o renální příčinu (akutní tubulární nekróza-poškozené tubuly nejsou schopny retinovat Na) (nelze použít u nemocných léčených furosemidem)

Rozlišení akutní nedostatečnosti ledvin prerenální FE Na+ pod 1% nad 2, 5% FE Cl- pod 1% nad 1, 3% S-kreat. norm. (+) ++ až ++++ S-urea ++ (+) ++ až ++++ U-Na pod 15 mmol nad 30 mmol
![Maximální hodnoty FE Analyt [ %] Na+ 20 -30 K+ 150 -200 voda 30 Maximální hodnoty FE Analyt [ %] Na+ 20 -30 K+ 150 -200 voda 30](http://slidetodoc.com/presentation_image/1c4317a80dc00047228daa6ac47e9000/image-116.jpg)
Maximální hodnoty FE Analyt [ %] Na+ 20 -30 K+ 150 -200 voda 30 -35 osm 30 -35 urea 90 -100 FE určuje adaptabilitu reziduálních funkčních nefronů

Markery tubulárního poškození • např. po léčbě aminoglykosidy, cytostatiky, při rejekci transplantované ledviny • „Enzymurie“ –např. aktivita N-acetyl-β-D-glukosaminidázy (NAG) v moči • některé malé proteiny, jejichž močová exkrece se zvyšuje v důsledku jejich nedostatečné tubulární reabsorpce (β 2 -mikroglobulin, α 1 -mikroglobulin, retinol vázající globulin)

Zobrazovací metody

Zobrazovací metody • Sonografické metody • Rtg metody (s nebo bez použití kontrastní látky) • Scintigrafické metody • Nukleární magnetická rezonance

Ultrazvuk • přednost před rtg vyšetřeními pro možnost častých kontrol bez radiační zátěže • vyšetření vlastních či transplantovaných ledvin • určení polohy, tvaru, velikosti ledvin (již prenatálně) • průkaz cyst, kamenů, nádorů • posouzení arteriálního a venózního průtoku (detekce stenosy a. renalis) • průkaz močového rezidua • sonografická kontrola při renální biopsii • vyšetření příštítných tělísek (2 a 3 HPT)
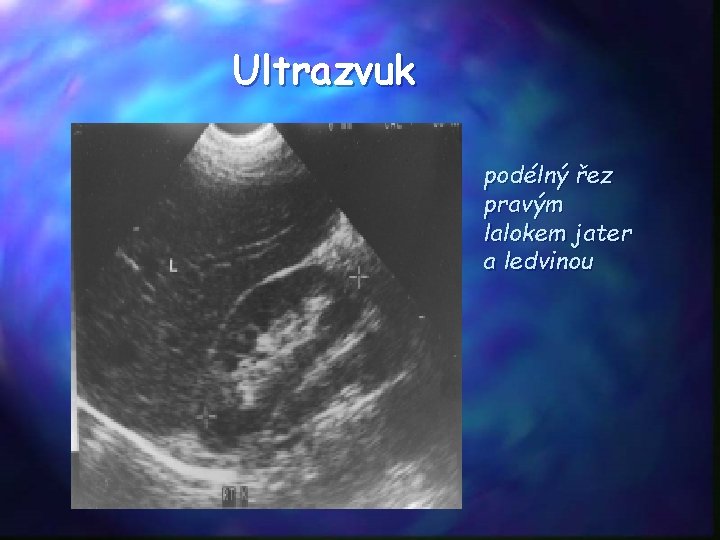
Ultrazvuk podélný řez pravým lalokem jater a ledvinou

RTG metody • nativní snímek • vylučovací urografie • mikční cystoureterografie • arteriografie • (venografie) • CT
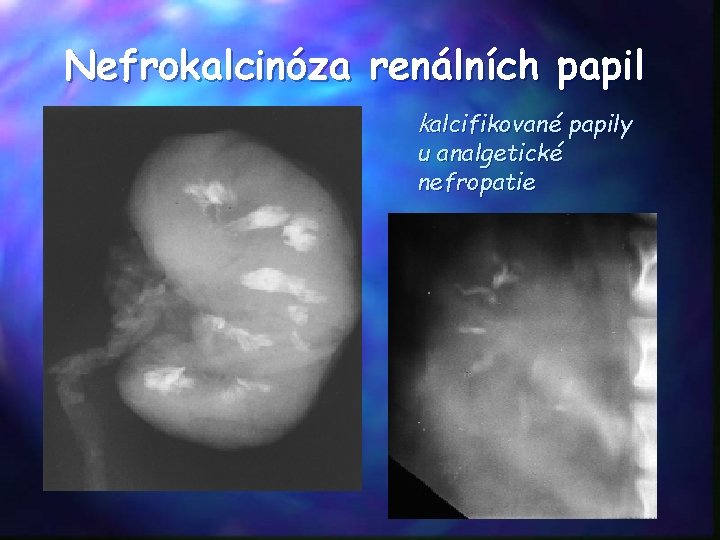
Nefrokalcinóza renálních papil kalcifikované papily u analgetické nefropatie
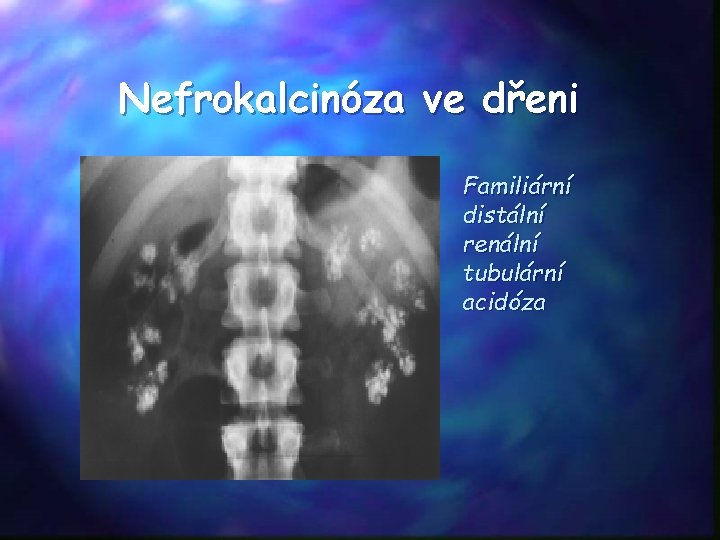
Nefrokalcinóza ve dřeni Familiární distální renální tubulární acidóza

Intravenózní vylučovací urografie • poloha, velikost, tvar ledvin • průkaz anatomických anomálií • průkaz deformace kalichopánvičkového systému u pyelonefritidy, průkaz defektů papil • průkaz komprese kalichového systému u expanzivních procesů • průkaz obstrukce močových cest, kamenů • oboustranné posouzení vylučování kontrastní látky (časný a pozdní snímek) • Překonána CT, USG • Kontrastní látky: neionizované, isoosmolární lépe tolerované • Riziko nefrotoxicity (ATN): DM, věk, CHRI, dehydratace

CT (HRCT, spirální CT) • Široce používané • Indikace: renální, perirenální masy, cysty x tumory, staging tumoru, abscesy, lithiáza, retroperitoneální choroby, obstrukce, pyelonefritis • CT angiografie • Kontraindikace, riziko nefrotoxicity a příprava – jako u IVU

CT polycystické ledviny
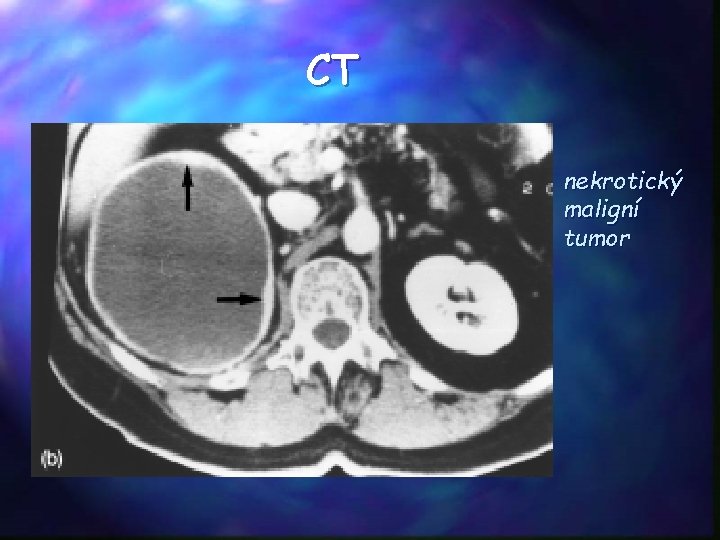
CT nekrotický maligní tumor
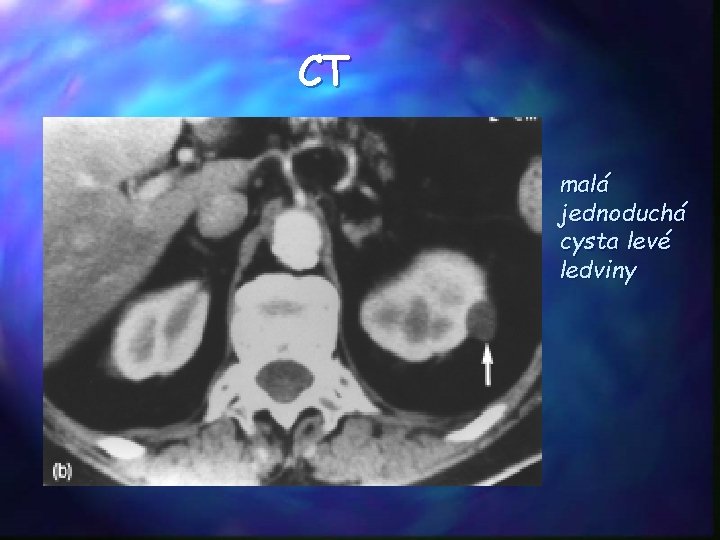
CT malá jednoduchá cysta levé ledviny

Angiografie • Zlatý standard v dg. renovaskulární hypertenze • Invazívní – cestou a. femoralis • Indikace: průkaz stenózy arteria renalis • vaskularizace tumoru • trombóza renální žíly (opožděný snímek) • jako komplikace nefrotického syndromu (MGN) • komplikace tu ledvin
Intravenózní digitální subtrakční angiografie
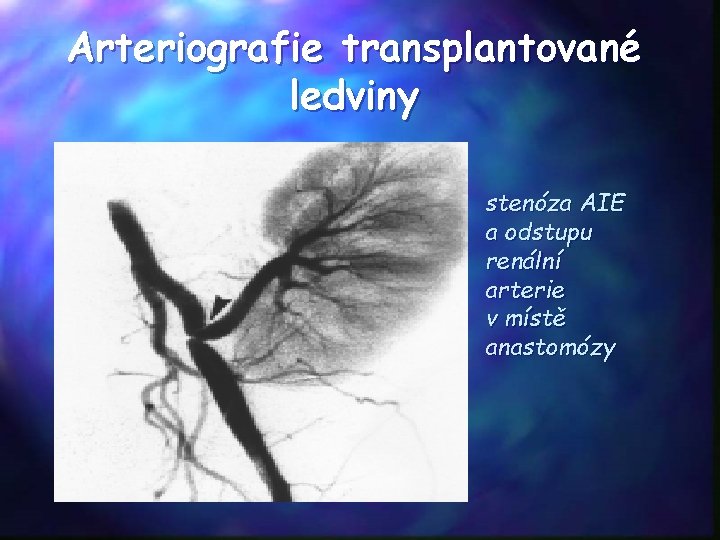
Arteriografie transplantované ledviny stenóza AIE a odstupu renální arterie v místě anastomózy
Arteriografie

Scintigrafie • Neinvazivní metoda • Funkční a strukturální zhodnocení • • Dynamická (Tc-DTPA, Tc-MAG 3) – přesně GFR, GFR jednotlivé ledviny, perfuze štěpu, event. hydronefroza při obstrukci, po kaptoprilu-stenosa renální tepny • Statická (Tc-DMSA) – vychytává se ve funkčním parenchymu – zachycuje jizvy, zánětlivá ložiska, vrozené abnormity
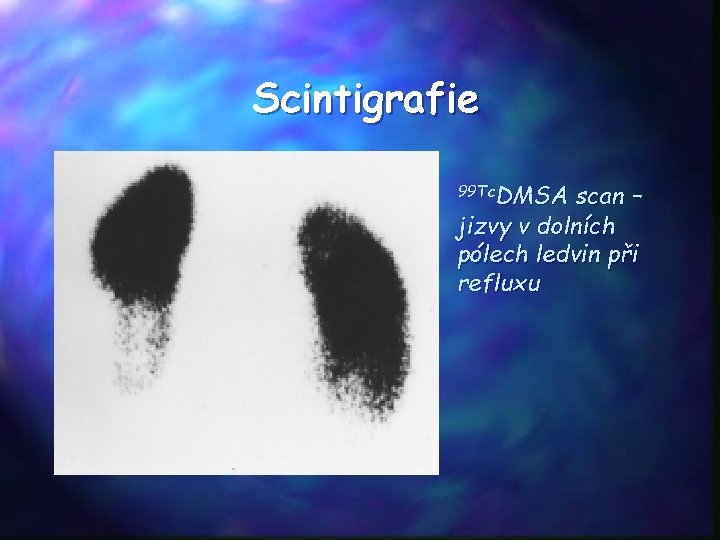
Scintigrafie 99 Tc. DMSA scan – jizvy v dolních pólech ledvin při refluxu

Magnetická rezonance • Zhodnocení renálních tumorů, staging • Drahá, nedostupná • Výhody – výborná rozlišitelnost pro měkké tkáně, lze použít u renální insuficience (gadolinium méně nefrotoxické a nealergenní), lze použít v graviditě • Kontraindikace – některé kovy v těle (pacemakery. . ) • MR angiografie – dg. renovaskulární choroby

MR MR angiografie aa. renales

Renální biopsie - indikace Nevysvětlitelná akutní nebo chronická choroba ledvin s normální velikostí ledvin, zvláště : • Nefrotický syndrom • Významná proteinurie • Mírná PU a hematurie • Akutní renální selhání • Nevysvětlitelné chronické renální selhání • Susp. systémové onemocnění s pozitivním močovým sedimentem • Dysfunkce štěpu

Renální biopsie – příprava • • 2 normální ledviny dle zobrazovacích metod TK < 140/90 mm Hg Hb > 100 g/l Normální koagulace a počet trombocytů Vyšetřit krevní skupinu Antiagregancia stop 5 dní předem Sterilní moč Informovaný souhlas

RB – kontraindikace • Chronické renální selhání + malé ledviny • Sklon ke krvácení • Dekorigovaná hypertenze • IMC • Solitární ledvina • Četné cysty • Nespolupráce • Susp. tumor ledviny • Hydronefróza

RB – technika • Transkutánní přístup (obvykle) • lokalizace místa vpichu sonograficky • Transjugulární přístup (vzácně) • při krvácivých stavech • při kombinované biopsii (s játry) za současného měření tlaků

RB – zhodnocení • Vyšetření bioptického materiálu: • Světelnou mikroskopií • Imunofluorescencí • Elektronovým mikroskopem • Konečná diagnóza (korelace s klinickými nálezy), staging postižení, odhad prognózy, indikace k ISU léčbě

RB – komplikace • Bolest • Krvácení – makroskopická hematurie 5%, velký subkapsulární hematom 1%, malý hematom 85% • Arteriovenózní fistule 10% • Jiný orgán – sval, tuk, játra, slezina, perforace kolon • Úmrtí (0, 1%)
- Slides: 143