Vybran metody analytick chemie ELEKTROFORZA Princip elektroforetickch separac

Vybrané metody analytické chemie ELEKTROFORÉZA

Princip elektroforetických separací n n Jsou založeny na migraci nabitých částic v elektrickém poli Kulová částice o poloměru r náboji z je hnána gradientem elektrického pole mezi dvěma elektrodami směrem k elektrodě opačného znaménka a bržděna třením n n Hnací síla je úměrná intenzitě elektrického pole E a celkovému náboji částice Q FE=QE Třecí síla je podle Stokesova zákona přímo úměrná poloměru a rychlosti částice FF=-6πηrν

Princip elektroforetických separací n V ustáleném stavu se obě síly vyrovnávají QE = 6πηrν (E=U/Lc) (V/m) a z toho vyplývá, že νef = E. (Q/ 6πηr) (m/s) Q/ 6πηr = μef (m 2/Vs) μef - efektivní elektroforetická pohyblivost (získaná z experimentu), u kationtů kladné, u aniontů záporné n Nabité částice migrují v elektrickém poli tím rychleji, čím jsou menší a čím větší nesou náboj
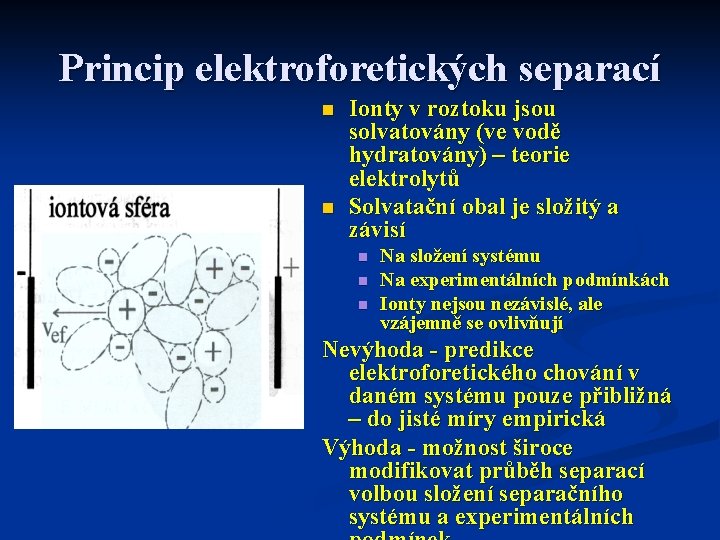
Princip elektroforetických separací n n Ionty v roztoku jsou solvatovány (ve vodě hydratovány) – teorie elektrolytů Solvatační obal je složitý a závisí n n n Na složení systému Na experimentálních podmínkách Ionty nejsou nezávislé, ale vzájemně se ovlivňují Nevýhoda - predikce elektroforetického chování v daném systému pouze přibližná – do jisté míry empirická Výhoda - možnost široce modifikovat průběh separací volbou složení separačního systému a experimentálních

Princip elektroforetických separací n Při práci s velmi zředěnými roztoky platí Kohlrauschův zákon o neodvislé vodivosti (pohyblivosti) iontů, který je definován pro nekonečné zředění Λ 0=Σλ 0 i n Λ 0 -celková molární vodivost roztoku λ 0 -molární vodivosti iontů při ∞ zředění v analytických elektroforetických separacích se migrující separované ionty vzájemně neovlivňují Pohyblivost jednotlivých iontů regulujeme manipulací hodnot Q a r n n Náboj iontů slabých elektrolytů měníme změnou stupně disocace (p. H), u silných i slabých elektrolytů koordinačními reakcemi s vhodnými ligandy – tvorba komplexů

Princip elektroforetických separací Elektroosmotický tok - elektroosmóza n n Na každém rozhraní fází které obsahuje nabité částice vznikne na základě elektrostatických zákonů elektrická dvojvrstva – kompaktní Helmholtzova vrstva a difúzní vrstva Tato vrstva má vlastnosti deskového kondenzátoru – potenciálový rozdíl mezi vnitřní a vnější hranicí difúzní vrstvy se nazývá elektrokinetický potenciál – zeta (ξ) potenciál
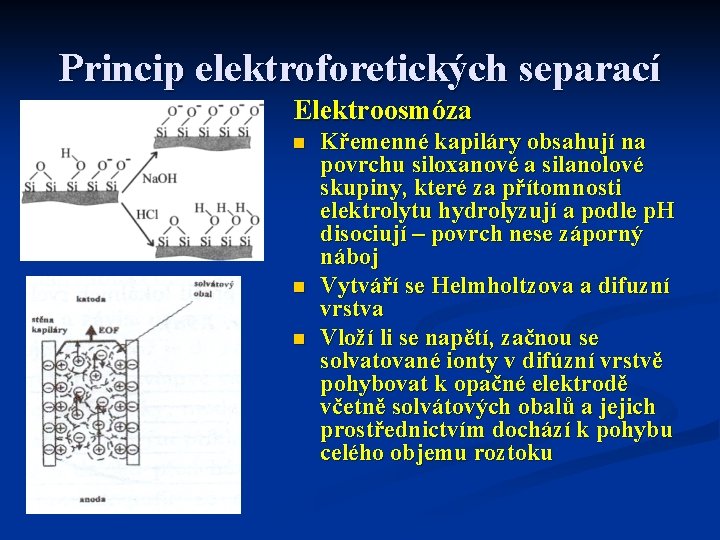
Princip elektroforetických separací Elektroosmóza n n n Křemenné kapiláry obsahují na povrchu siloxanové a silanolové skupiny, které za přítomnosti elektrolytu hydrolyzují a podle p. H disociují – povrch nese záporný náboj Vytváří se Helmholtzova a difuzní vrstva Vloží li se napětí, začnou se solvatované ionty v difúzní vrstvě pohybovat k opačné elektrodě včetně solvátových obalů a jejich prostřednictvím dochází k pohybu celého objemu roztoku
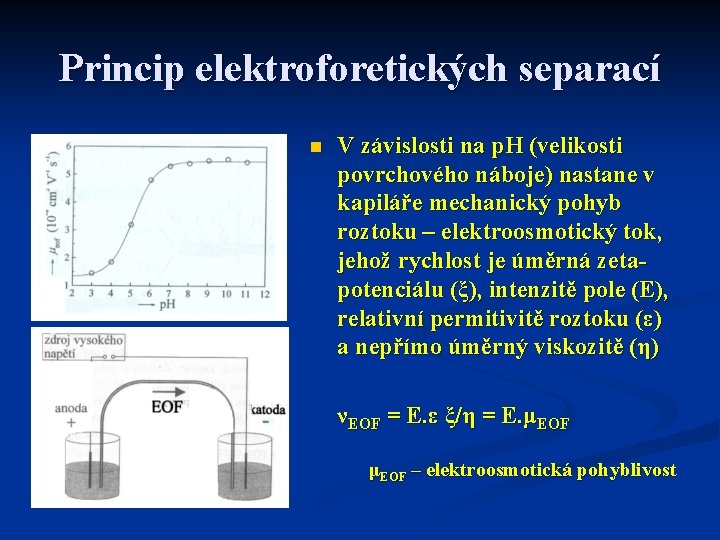
Princip elektroforetických separací n V závislosti na p. H (velikosti povrchového náboje) nastane v kapiláře mechanický pohyb roztoku – elektroosmotický tok, jehož rychlost je úměrná zetapotenciálu (ξ), intenzitě pole (E), relativní permitivitě roztoku (ε) a nepřímo úměrný viskozitě (η) νEOF = E. ε ξ/η = E. μEOF – elektroosmotická pohyblivost

Princip elektroforetických separací n n n Rychlost EOF se přičítá k migrační rychlosti částic pokud migrují stejným směrem a odečítá od rychlosti částic, které migrují opačným směrem Vlivem EOF se kapilárou pohybují kationty, anionty, ale i neutrální molekuly EOF - další významný parametr, kterým lze ovlivnit separaci – lze měnit rychlost i směr EOF, případně ho vyloučit (neutrální povrch) n n Změnou složení roztoku (p. H) Modifikací povrchu kapiláry

n n Kapilární elektroforéza x chromatografie Elektroforeogramy formálně podobné chromatogramům Základní rozdíl je hnací síla, která způsobí pohyb solutů v systému n n Chromatografie – mechanický přetlak Elektroforéza – elektrostatické síly které vedou k n n n Migraci solutů Elektroosmotickému toku Liší se profily průtoků n n Chromatografie parabolický Elektroosmotický je plochý - menší rozmytí zón- účinnější

Elektroforetické techniky n n n Volná elektroforéza proteinů v trubici (Tiselius)- migraci v elektrickém poli ruší pohyb částic způsobený teplotní konvekcí a difúzí Elektroforéza na papíře (málo používaná) nebo na tenké vrstvě gelu – rutinní technika pro separaci velkých molekul (DNA) Kapilární zónová elektroforéza (CZE) n n n Kapilární gelová elektroforéza (CGE) Afinitní kapilární elektroforéza (ACE ) Micelární elektrokinetická kapilární chromatografie (MEKC) Elektrochromatografie v naplněných kapilárách (CEC) Kapilární izoelektrické fokuzování Kapilární izotachoforéza

Kapilární zónová elektroforéza (CZE) n n n Vhodná pro separaci iontů lišících se svou molekulovou hmotností, tvarem a nábojem Nabité molekuly dělí na základě rozdílných elektroforetických pohyblivostí (mobilit) Elektroosmotický tok tlumivého roztoku unáší nabité ionty k detektoru a tyto ionty migrují uvnitř tlumivého roztoku různými elektroforetickými rychlostmi a tím se vzájemně dělí Běhe jednoho experimentu lze tedy dělit, detegovat a stanovit jak kationty, tak i anionty CZE lze použít pouze pro molekuly s nábojem. Nenabité molekuly a částice se pohybují elektroosmotickým tokem a vzájemně se nedělí

Kapilární zónová elektroforéza (CZE) n n Separace se provádí v kapiláře z taveného křemene s vnitřním průměrem 25 -100μm, vnějším nejčastěji 375 μm pokryté vrstvou polyimidu Využívá se elektroforetické migrace a osmotického toku kapaliny kapilárou na kterou je vloženo vysoké napětí (desítky k. V) V zásaditých pufrech je EOF srovnatelný s lineární rychlostí mobilní fáze v HPLC, v kyselých je výrazně nižší EOF závisí i na koncentraci pufru – vyšší koncentrace generují pomalejší EOF a naopak. Velmi nízké koncentrace pufrů (pod 10 mmol/l) nejsou schopny zajistit konstantní p. H v systému a vedou k nereprodukovatelným výsledkům

Kapilární zónová elektroforéza (CZE) n n Rychlostní profil v kapalině hnané elektroosmózou je plochý a proto je dosahováno vyšších účinností než v HPLC Vlivem elektrického proudu (desítky až stovky μA) vzniká Jouleovo teplo, které je nutno odvést stěnou kapiláry do okolí a deformuje rychlostní profil. Čím vodivější pufr a čím větší průměr kapiláry, tím více Jouleova tepla vzniká a to vede ke zhoršení separace – kapiláru ochlazovat kapalinou nebo proudícím vzduchem
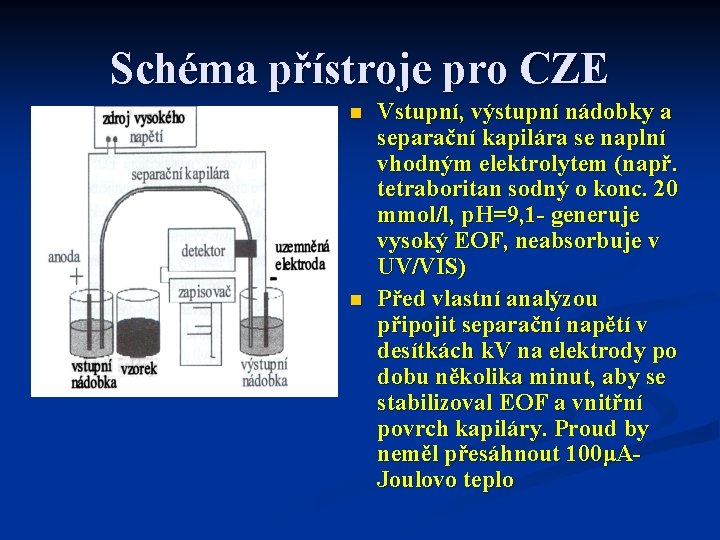
Schéma přístroje pro CZE n n Vstupní, výstupní nádobky a separační kapilára se naplní vhodným elektrolytem (např. tetraboritan sodný o konc. 20 mmol/l, p. H=9, 1 - generuje vysoký EOF, neabsorbuje v UV/VIS) Před vlastní analýzou připojit separační napětí v desítkách k. V na elektrody po dobu několika minut, aby se stabilizoval EOF a vnitřní povrch kapiláry. Proud by neměl přesáhnout 100μAJoulovo teplo
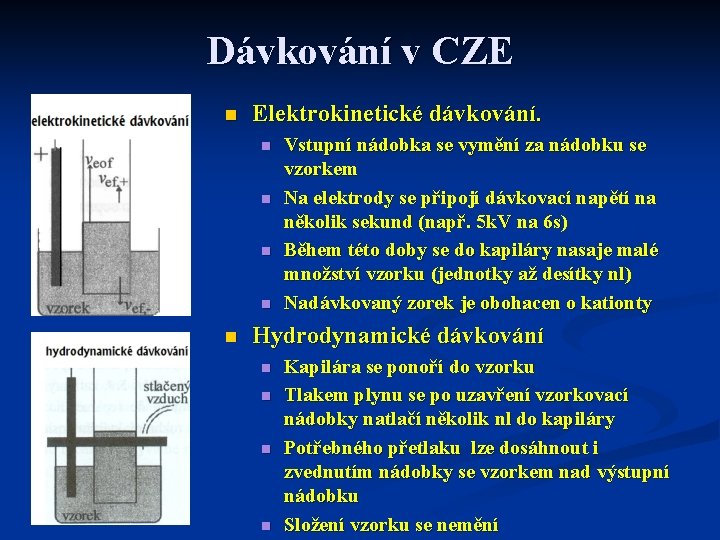
Dávkování v CZE n Elektrokinetické dávkování. n n n Vstupní nádobka se vymění za nádobku se vzorkem Na elektrody se připojí dávkovací napětí na několik sekund (např. 5 k. V na 6 s) Během této doby se do kapiláry nasaje malé množství vzorku (jednotky až desítky nl) Nadávkovaný zorek je obohacen o kationty Hydrodynamické dávkování n n Kapilára se ponoří do vzorku Tlakem plynu se po uzavření vzorkovací nádobky natlačí několik nl do kapiláry Potřebného přetlaku lze dosáhnout i zvednutím nádobky se vzorkem nad výstupní nádobku Složení vzorku se nemění

Zakoncentrování (sample stacking) n n Při dávkování zředěného vzorku, který má menší vodivost než separační elektrolyt dochází po vložení separačního napětí k zakoncentrování na rozhraní mezi vzorkem a separačním elektrolytem Zóna vzorku o menší vodivosti si vynutí větší intenzitu pole než je v elektrolytu. Kationty uvnitř zóny pak migrují větší rychlostí na přední rozhraní, kde se zpomalí, nakupí a zakoncentrují a do separačního elektrolytu migrují menší rychlostí. Anionty se naopak koncentrují na zadním rozhraní

Analýza CZE n n Po nadávkování se kapilára opět ponoří do vstupní nádobky s elektrolytem a připojí se separační napětí (desítky k. V) Celá nadávkovaná zóna je unášena EOF ke katodě (detektoru) Látky s nábojem navíc migrují elektroforetickými rychlostmi uvnitř elektrolytu a vytváří vlastní zóny Neutrální látky se nedělí a pohybují se v jediné zóně EOF

Detekce v CZE n Fotometrický detektor UV/VIS měří absorpci uvnitř kapiláry na jejím konci před výstupní nádobkou. V místě měření je nutno kapiláru zbavit polyimidové vrstvy (okénko několik mm) n n Přímá absorpční detekce- dělené látky absorbují v UV/VIS oblasti a elektrolyt málo, nebo vůbec Nepřímá detkce – pro ionty, které neabsorbují (anorganické Na+, Ca 2+, . . , Cl-, SO 42 - atd. ) přidáme elektrolyt který obsahuje silně absorbující kationt (např. Cu 2+) pro detekci kationtů, nebo aniont (Cr. O 42 -) pro detekci aniontů. Dostanee negativní pík, neboť v zóně neadsorbující iont vytěsní barevný

Detekce v CZE n n n Detektor s diodovým polem (DAD) Fluorescenční detektor využívající laserem indukovanou fluorescenci – nejcitlivější pro fluoreskující analyty Bezkontaktní vodivostní detektor –měří vodivost uvnitř kapiláry, která se průchodem zón mění – pro neasorbující analyty (cukry, aminokyseliny, . . ) Elektrochemický detektor (ampérometrický)pro elektrochemicky aktivní analyty Hmotnostní detektor

Elektroferogram CZE n n n Kvalitativní informace – migrační čas příslušné sloučeniny a z něho lze vypočítat elektroforetickou pohyblivost analytu Kvantitativní informace – plocha píku. Vzhledem k často kolísajícímu EOF se místo ploch vyhodnocuje korigovaná plocha píku, což je plocha píku dělená migračním časem analytu Pro kvatifikaci lze využít všechny běžné postupy (metoda vnějšího i vnitřního standardu, vnitřní normalizace, standardního přídavku). Pracujeme s korigovanými plochami píků

Využití CZE Využívá se ke stanovení nejrůznějších anorganických i organických sloučeni iontové povahy n Separaci lze výrazně ovlivňovat volbou elektrolytu n Volba p. H ovlivňuje stupeň disociace látek a tí i jejich efektivní pohyblivosti n Přídavkem chirálního selektoru do elektrolytu (cyklodextrin) lze separovat i enantiomery opticky aktivních látek n

Kapilární gelová elektroforéza (CGE) n n Elektroforéza v matrici gelu umožňuje separace vysokomolekulárních biologicky aktivních látek (peptidů, bílkovin, polynukleotidů, . . ) na základě velikosti jejich molekul Lze ji realizovat na desce, koloně nebo v separační kapiláře naplněné gelem – kapilární gelová elektroforéza. Analyty, lišící se velikostí a tvarem molekul migrují póry gelu, což zvyšuje rozdíly jejich elektroforetických rychlostí Gel v kapiláře brání vzniku EOF a proto může být separován jeden typ iontů (buď kationty, nebo anionty)

Kapilární gelová elektroforéza (CGE) n Nejčastěji používaným gelem v CGE je polyakrylamid n Chemický gel – radikálovou polymerací akrylamidu a bisakrylamidu (síťující složka) uvnitř separační kapiláry n n n Fyzikální gely – vzájemným propletením lineárních řetězců (polyakrilamid, agarosa, methylcelulosa, polyethylenglykol aj. ) n n Vzájemným poměrem obou monomerů lze řídit velikost pórů Obtížná příprava bez bublinek vzduchu a nemožnost výměny náplně Výhodou je menší viskozita, možnost výměny gelu před každou analýzou – lepší reprodukovatelnost Nachází uplatnění pro vysokoúčinné separace a určování molekulových hmotností velkých nabitých

Micelární elektrokinetická chromatografie (MEKC) n n n Metoda vyvinutá pro analýzu neutrálních molekul hydrofobní i hydrofilní povahy Využívá solvatace těchto látek v micelách, které vzniknou v separačním tlumivém roztoku po přidání povrchově aktivní látky (tenzidu) – nejčastěji SDS (dodecylsíran sodný) Ve vodném prostředí se molekuly po překročení kritické micelární koncentrace začnou organizovat do kulovitých útvarů-micel a vytváří micelární fázi, která má polární povrch tvořený sulfátovými skupinami a nepolární dutinu (kavitu)

Micelární elektrokinetická chromatografie (MEKC) n n n Hydrofobní dutiny micel SDS jsou schopny do sebe pojmout nepolární molekuly a tím dochází k jejich solvataci a rozpouštění v micelární fázi Ve vodném pufru s micelami tenzidu se budou molekuly analytů podle své polarity dělit mezi vodnou a micelární fázi Disociované síranové skupiny na povrchu micel SDS způsobují záporný povrchový náboj micel a tyto v elektrickém poli migrují k anodě Neutrální analyty se podle své polarity více či méně rozpouštějí v kavitách micel a ty je unášejí k anodě Micelární fáze se chová jako stacionární fáze v HPLC s tím rozdílem, že se pohybuje vlastní elektroforetickou rychlostí – označuje se proto jako pseudostacionární fáze

Micelární elektrokinetická chromatografie (MEKC) n n Všechny micely migrují stejnou rychlostí k anodě Čím více analytu je v micelární fázi, tím rychleji se pohybuje k anodě Separační elektrolyt včetně micel a analytů je však EOF unášen ke katodě (detektoru) Rychlost EOF je vyšší než elektroforetická rychlost micel a proto jsou všechny analyty transportovány k detektoru i přes to, že pseudostacionární fáze se pohybuje opačným směrem
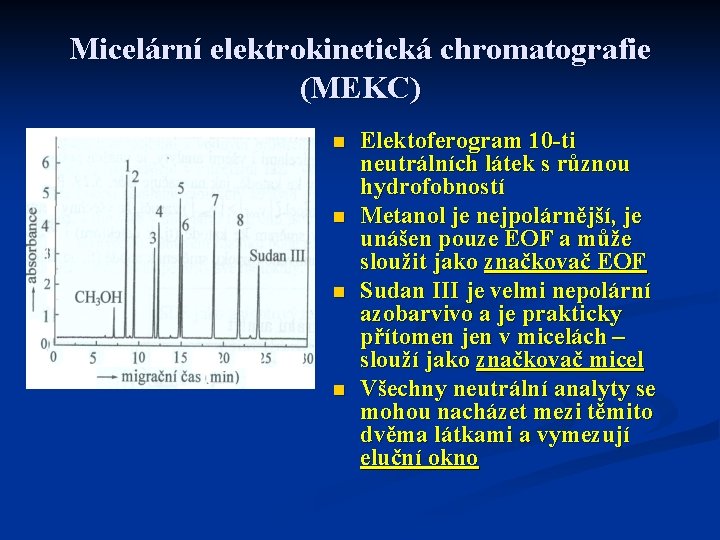
Micelární elektrokinetická chromatografie (MEKC) n n Elektoferogram 10 -ti neutrálních látek s různou hydrofobností Metanol je nejpolárnější, je unášen pouze EOF a může sloužit jako značkovač EOF Sudan III je velmi nepolární azobarvivo a je prakticky přítomen jen v micelách – slouží jako značkovač micel Všechny neutrální analyty se mohou nacházet mezi těmito dvěma látkami a vymezují eluční okno

Micelární elektrokinetická chromatografie (MEKC) n n Lze použít i jiné detergenty. Aniontové se chovají jako SDS Katiotové tenzidy se organizují do micel s kladným nábojem na povrchu a putují ke katodě Při přidání kationtového tenzidu do separačního elektrolytu však dojde k převrácení EOF. Tenzid změní náboj na povrchu kapiláry Pseudostacionární fáze tvořená micelami kationtového tenzidu opět proudí proti EOF

Micelární elektrokinetická chromatografie (MEKC) n n Analyty, které mohou protonizovat či disociovat a nést náboj se vedle distribuce mezi vodnou a pseudostacionární fázi v nabité formě pohybují vlastní elektroforetickou rychlostí Migrační čas zóny slabě kyselého či bazického analytu bude dán součtem všech transportních mechanizmů, které se u molekul i iontů uplatňují a analyt vytváří jedinou vlastní specifickou zónu

Kapilární elektrochromatografie (CEC) n n Kapilární elektrochromatografie (CEC) kombinuje elektroforetický a chromatografický separační mechanizmus Kapilára je vyplněna vhodnou stacionární fází n n Náplňová – fáze uzavřena mezi dvěma fritami Monolitická – zpolymerováním monomerů uvnitř kapiláry se vytvoří blok porézního polymeru – monolit (polybutylmethakrylát x ethylendimethylakrilát , polystyren x divinylbenzen)

Elektrochromatografie (EC) n Mobilní fáze uvnitř kapiláry je hnána EOF n n n Neutrální analyty interagují se stacionární fází v koloně obdobně HPLC Analyty iontové povahy interagují se stacionární fází jako neutrální látky a navíc je jejich separace ovlivňována rozdíly v jejich efektivních mobilitách CEC se díky vysoké separační schopnosti, snadné přípravě monolitických kolon a použitelnosti pro neutrální i nabité analyty využívá při n n n Analýze léčiv Opticky aktivních látek Biologických látek jako jsou proteiny a štěpy ribonukleových kyselin

Izoelektrická fokusace (IEF) n n IEF dělí látky amfolytické povahy na základě jejich izoelektrického bodu v lineárním gradientu p. H Lze realizovat n n n v plošném uspořádání v gelu v křemenné separační kapiláře bez gelu naplněné vhodným nosným amfolytem – kapilární izoelektrické fokusování Aby se eliminoval EOF pokrývá se vnitřní povrch kapiláry vrstvičkou hydroxyethylcelulosy Amfolyty mohou podle p. H nést kladný, záporný nebo žádný náboj (bílkoviny, peptidy, aminokyseliny) Izoelektrickým bodem rozumíme takové p. H, při kterém má molekula nulový náboj a proto žádnou elektroforetickou pohyblivost

Izoelektrická fokusace (IEF) n n n n Před separací se naplní kapilára roztokem dělených analytů rozpuštěných v nosném amfolytu, který je schopen tlumit celý rozsah p. H Jako nosné amfolyty se používají směsi polyaminopolykarboxylových nebo sulfonových kyselin Konce kapiláry se ponoří do nádobky s katolytem a katodou(20 mm/l Na. OH) a anolytem a anodou (6 mmol/l H 3 PO 4). Po vložení separačního napětí migrují na vstupu OH- ionty a z opačného konce H 3 O+ a vytvoří v nosném amfolytu klesající spojitý lineární gradient p. H Analyty migrují podle náboje do svého izoelektrického podu (p. H=p. I), kde se zastaví a fokuzují Po fokuzaci se nahradí anolyt (H 3 PO 4) roztokem Na. Cl a do výstupního konce začnou migrovat Na+ ionty místo H 3 O+ , začne se posouvat gradient p. H a zóny fokuzovaných analytů se vytlačí z kapiláry přes UV detektor Pro jednotlivé analyty se získají „píky“ různé šířky

Kapilární izotachoforéza (ITP) n n n Nejstarší kapilární metoda pro separaci iontů Používá se separační kapilára , která negeneruje EOF (PTFE, křemen s vrstvičkou hydroxyethylcelulózy) Dva separační tlumivé roztoky – vedoucí (leading) a koncový (terminatig) Vedoucí elektrolyt obsahuje koiont stejného znaménka jako analyty a velkou elektroforetickou pohyblivost Koncový elektrolyt obsahuje koiont opět stejného znaménka jako analyty, ale malou pohyblivost Vzorek se dávkuje mezi ně a vytvoří mezi nimi rozhraní

Kapilární izotachoforéza (ITP) n n n Po spuštění separačního napětí začnou všechny analyty a kionty putovat stejnou elektroforetickou rychlostí směrem k detektoru Během migračního procesu se ionty ze vzorku řadí za koiontem vedoucího elektrolytu podle svých elektroforetických pohyblivostí a vytváří vlastní, ostře ohraničené a na sebe navazující zóny Každý ion vytváří vlastní zónu. Zóny jsou seřazeny podle klesající elektroforetické pohyblivosti mezi zónami vedoucího a koncového elektrolytu a prochází detektorem Detegoval lze jen jeden druh ionů – kationty nebo anionty Detektor monitoruje elektrickou vodivost jednotlivých zón

Kapilární izotachoforéza (ITP) n n Izotachoforegram má schodovitý průběh, každý schod- jeden analyt. Koncentrace analytů v zónách se přizpůsobí koncentraci koiontu ve vedoucím elektrolytu Výška (vodivost) je mírou kvality, délka je mírou kvantity Nepolární látky a opačně nabité ioty neruší • Dnes se využívá hlavně • Obsah kyselin v silážích, rozbor vody • pro měření elektroforetických pohyblivostí • Prekoncentrační krok před CZE
- Slides: 37