Vybran metody ACh KAPALINOV CHROMATOGRAFIE Kapalinov chromatografie LC

Vybrané metody ACh KAPALINOVÁ CHROMATOGRAFIE

Kapalinová chromatografie (LC) n Nejdéle známá chromatografická metoda (Cvět). Téměř 80% známých látek lze analyzovat pomocí LC (iontové, polární i nepolární, mol. hm. 5 -106) Papírová chromatografie (PC) je starší technika a byla postupně nahrazena tenkovrstevnou chromatografií (TLC). n Pro obě techniky je stacionární fáze umístěna v ploše. V případě PC je tvořena speciálním papírem, u TLC tenkou vrstvou fáze na desce (sklo, hliníková či plastová folie) n

PC a TLC – stacionární fáze V PC je stacionární fází voda sorbovaná na papíře n V TLC stejné materiály jako v kolonové chromatografii n Pro lipofilní – adsorbenty oxid hlinitý (alumina), silikagel, polyamid, acetylovaná celulóza n Pro hydrofilní – celulóza, měniče iontů, křemelina, polyamidy a chemicky vázané fáze n n Desky pro TLC lze připravit v laboratoři, přednost se dává komerčně připraveným deskám pro klasickou TLC, HPTLC či preparativní TLC

PC a TLC – stacionární fáze n Vrstva fáze (0, 1 -0, 5 mm pro analytické a 0, 5 -2, 0 pro preparativní účely)je nanesena na skleněné, hliníkové nebo plastové desce. n n Přilnavost k desce se zvyšuje přídavkem pojiva 0, 1 -10% (sádra, škrob, polyakrylová kyselina a její soli) Pro snadnější vizualizaci skvrn se často přidává fluorescenční indikátor např. aktivovaný křemičitan hořečnatý o stejném zrnění (analyt zháší fluorescenci) Někdy stacionární fázi na desce předchází tzv. koncentrační zóna (2 -3 cm) tvořená inertním sorbentem Pro HPTLC se používají menší sférické částice (210μm)s jednotnou velikostí nebo monolitické ultratenké vrstvy – vysoká účinnost, délku lze zkrátit na několik cm, vyšší citlivost (pg)

PC – mobilní fáze n Jako mobilní fáze v PC se používají směsi rozpouštědel v závislosti na struktuře analytu. n n n Pro polární látky se často používají směsi butanolkyselina octová (hydroxid amonný)-voda Pro středně polární butylacetát, diisopropylether, chloroform s malým přídavkem polárních rozpouštědel a vody Pro zcela nepolární látky papír impregnovaný parafinovým olejem a vodné roztoky alkoholů nasycené stacionární fází jako mobilní fáze (RP-PC).

TLC – mobilní fáze n O volbě mobilní fáze v TLC rozhoduje použitá stacionární fáze Pro dělení na adsorpčním principu a chemicky vázaných fázích se volí rozpouštědla podle eluční schopnosti – eluotropní řady (n-pentan , ……. , voda) n Pro měniče iontů elektrolyty n Pro gely voda nebo organická rozpouštědla n

PCVzorek a TLC vyvíjení se nanese ve formě malých skvrn na n n n start pomocí mikropipetky, mikrostříkačky a nechá se odpařit rozpouštědlo Uspořádání vzestupné, sestupné (PC), kruhové v komoře nasycené parami rozpouštědel – rozpouštědlo vzlíná kapilárními silami. V HPTCL deska v hermetické „komoře“ s kontrolovaným přetlakem Vyvíjení n n n jednoduché (v jedné soustavě) vícenásobné – aplikují se různé mobilní fáze, na čele nové mobilní fáze dojde k zakoncentrování dvojrozměrné – skvrna se vyvine v jednom směru, deska se vysuší a otočí o 90° a vyvíjí se v jiné soustavě

PC a TLC – vyhodnocování kvality n Pokud nejsou dělené látky barevné, je nutno skvrny vizualizovat. n n n Postřik činidlem, nebo namočení do roztoku který poskytuje barevnou reakci (nespecifická – páry jódu, konc. kyselina sírová, acidobazické indikátory pro kyseliny a zásady, specifická pro funkční skupiny) Pozorování v UV záření – fluorescence či její zhášení na deskách s indikátorem (254 nebo 366 nm) Základní veličina, která charakterizuje polohu separovaných zón je retardační faktor RF definovaný jako poměr vzdáleností, které urazil analyt di a čelo mobilní fáze dm RF = di/dm= ui/um = 1/(1+k) u – příslušné rychlosti, k- retenční faktor

PC a TLC – vyhodnocování kvality n n Hodnota RF se pohybuje od 0 (látka nemigruje) do 1 (látka není zadržována a migruje s čelem rozpouštědla) Hodnoty RF jsou špatně reprodukovatelné n n n Stacionární, mobilní fáze a páry nejsou v rovnováze Kapilární síly záleží na průměru kanálků – průtok není konstantní Látky se v PC a TLC vyhodnocují na základě RF hodnot a jejich shodě se standardy Využívají se také hodnoty RM definované RM = log[(1/RF)-1 ]= log k hodnoty RM souvisejí se strukturou, v homologických řadách závisí lineárně na počtu strukturních jednotek Pro kruhové vyvíjení platí RF, lineární =R 2 F, kruhový.
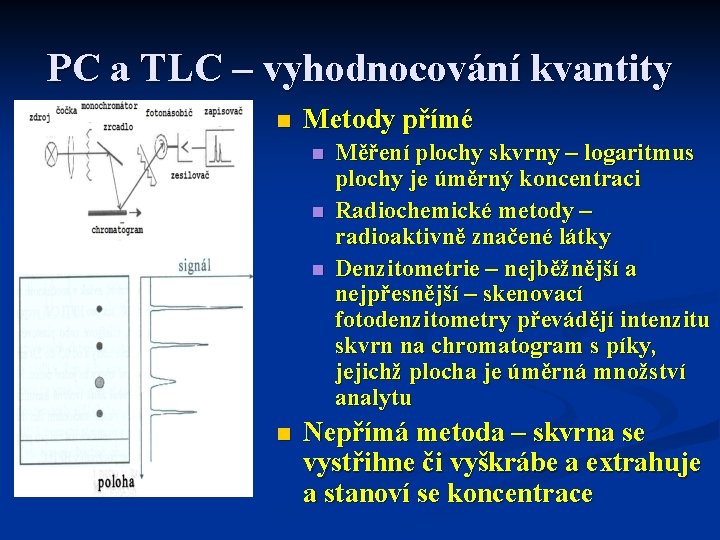
PC a TLC – vyhodnocování kvantity n Metody přímé n n Měření plochy skvrny – logaritmus plochy je úměrný koncentraci Radiochemické metody – radioaktivně značené látky Denzitometrie – nejběžnější a nejpřesnější – skenovací fotodenzitometry převádějí intenzitu skvrn na chromatogram s píky, jejichž plocha je úměrná množství analytu Nepřímá metoda – skvrna se vystřihne či vyškrábe a extrahuje a stanoví se koncentrace

Kolonová LC n n V klasickém provedení v kolonách 500 x 10 mm, částice 0, 05 -1, 0 mm + hydrostatický tlak – málo účinné, dlouhá doba analýzy (hodiny) – dodnes pro preparativní a jednoduchá dělení HPLC se vyvinula z GC na počátku 70. let. Vysoké účinnosti se dosahuje n n Použitím malých částic (2 -7μm) pravidelného tvaru a jednotné velikosti Průtok mobilní fáze musí být zajištěn vysokým tlakem (jednotky – desítky MPa) Lze zpracovávat malá množství (μl) Potřeba citlivých detektorů náročná instrumentace
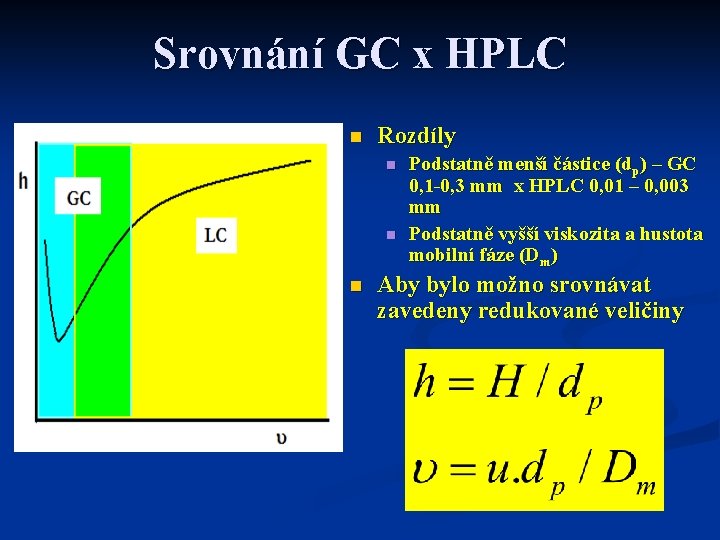
Srovnání GC x HPLC n Rozdíly n n n Podstatně menší částice (dp) – GC 0, 1 -0, 3 mm x HPLC 0, 01 – 0, 003 mm Podstatně vyšší viskozita a hustota mobilní fáze (Dm) Aby bylo možno srovnávat zavedeny redukované veličiny

Kolony HPLC n Tradiční analytické náplňové kolony n n n délka 5 -25 cm, vnitřní průměr několik mm, průtok mobilní fáze cca 1 ml/min objem vzorku 1 -20 μl částice náplně 5 -10 μm, kulovitého tvaru Během používání při vysokých tlacích se náplň sesedá n Mikronáplňové n n vnitřní průměr 1 mm a menší částice 2 -3 μm Objem vzorku cca 1 μl průtok mobilní fáze desítky μl/min Lze ještě používat běžnou instrumentaci
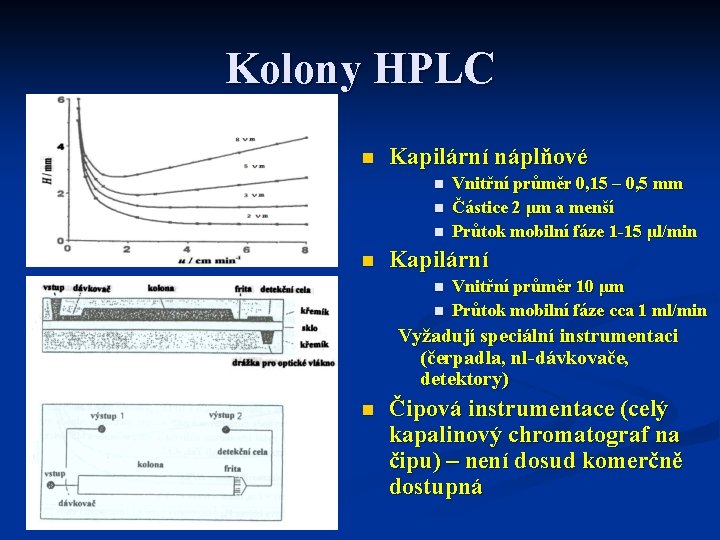
Kolony HPLC n Kapilární náplňové n n Vnitřní průměr 0, 15 – 0, 5 mm Částice 2 μm a menší Průtok mobilní fáze 1 -15 μl/min Kapilární n n Vnitřní průměr 10 μm Průtok mobilní fáze cca 1 ml/min Vyžadují speciální instrumentaci (čerpadla, nl-dávkovače, detektory) n Čipová instrumentace (celý kapalinový chromatograf na čipu) – není dosud komerčně dostupná

Monolitické kolony n n Kompaktnější náplň než klasické náplňové kolony Kolona je vyplněna polymerem organického či anorganického původu o definované pórovitosti, který se vytvoří přímo v koloně vhodnou polymerační reakcí v roztoku Monolitické kolony na bázi silikagelu mají vysokou pórovitost, která dovoluje vysoké průtoky a velký povrch pro interakce s analyty Monolitické kolony mají větší životnost, velkou mechanickou stabilitu, jsou odolnější ke změnám p. H a vykazují vysoké účinnosti při velkých průtocích mobilní fáze
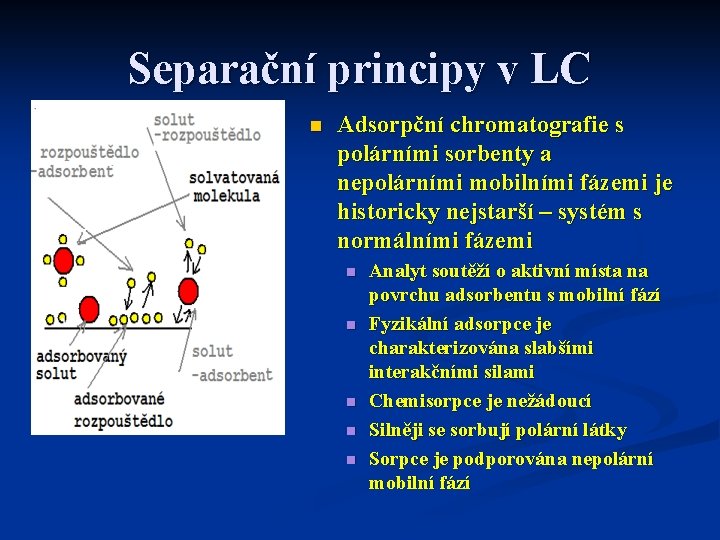
Separační principy v LC n Adsorpční chromatografie s polárními sorbenty a nepolárními mobilními fázemi je historicky nejstarší – systém s normálními fázemi n n n Analyt soutěží o aktivní místa na povrchu adsorbentu s mobilní fází Fyzikální adsorpce je charakterizována slabšími interakčními silami Chemisorpce je nežádoucí Silněji se sorbují polární látky Sorpce je podporována nepolární mobilní fází

LSC n Při velkém zředění solutu lze adsorpční děj popsat lineární izotermou danou Henryho zákonem, při vyšších koncentracích (preparativní HPLC) sorpčními izotemami n n n Silikagel-polární sorbent (silanolové skupiny –Si. OH) , siloxanové (Si-O-Si) jsou nežádoucí. Stabilní při p. H 2 -8 Alumina – stabilnější v alkalickém prostředí (p. H 2 -12), vhodná pro látky bazického charakteru Adsorbenty na bázi organických polymerů Mobilní fáze nepolární rozpouštědla (hexan, heptan, . . ) s malým množstvím (do 1%) modifikátoru (voda, alkoholy, acetonitril, tetrahydrofuran) Vhodná pro separaci látek lišících se funkčními skupinami a izomerů. Nevhodná pro dělení v homologických řadách.

LC na chemicky vázaných fázích n Chemicky vázané fáze (hlavně nepolární-reverzní) v součastné době nejpoužívanější n n n Umožňují aplikace pro analyty s širokým rozsahem polarity (80% všech aplikací) Široký sortiment fází Levné mobilní fáze a rychlé ustavování rovnováhy Reverzní chromatografie je jednodušší, rychlejší a reprodukovatelnější RP – umožňují přímé aplikace na biologické vzorky (vodné roztoky) Nevýhody n n n Složitý retenční mechanizmus Chemicky vázané fáze na silikagelu jsou stabilní v omezeném rozsahu p. H (2, 5 -8) Přítomnost nezreagovaných silanolových skupin vede k nežádoucí adsorpci a je příčinou kompllikovaného mechanizmu

LC na chemicky vázaných fázích n n Silikagel je nejběžnějším nosičem pro chemicky vázané fáze – obsahuje silanolové skupiny, ve kterých může být aktivní vodík snadno nahrazen různými funkčními skupinami –R. Většina fází je siloxanového typu Si-O-Si-R Reakcí s monochlororganosilany vznikají fáze s monomolekulární vrstvou vázané fáze, zatímco reakcí s di- a trichlorsilany dochází k sesíťování a vzniku polymerní vrstvy v poslední době se používají i jiné materiály jako oxid zirkoničitý a titaničitý, které jsou stálé v širším rozsahu p. H Lze použít i polymerní nosiče, které jsou stálé v širokém rozsahu p. H, neobsahují zbytkové aktivní skupiny, ale mohou
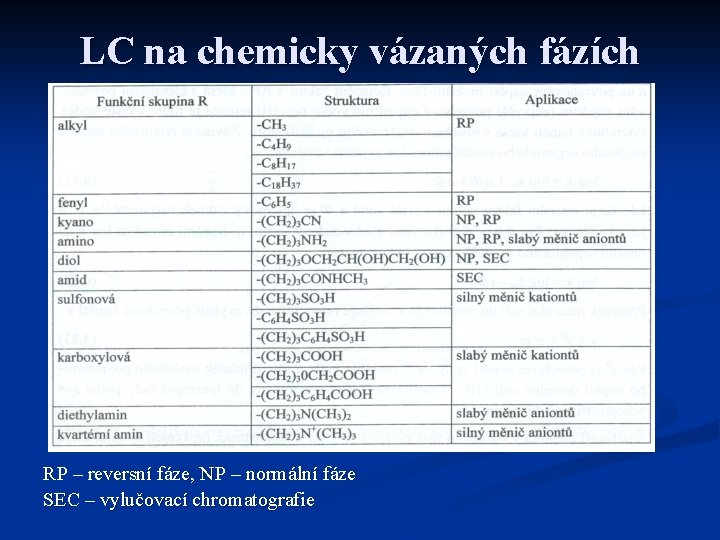
LC na chemicky vázaných fázích RP – reversní fáze, NP – normální fáze SEC – vylučovací chromatografie

LC na chemicky vázaných fázích n Mechanizmus separace na reversních chemicky vázaných fázích je kombinací tří interakcí n Interakce solutu s mobilní fází (vodou) – rozhodující n n n Přídavkem organických rozpouštědel povrchové napětí vody klesá a klesá i retence Přídavkem solí povrchové napětí roste a zvyšuje se i retence Interakce mobilní fáze se stacionární fází - při větším obsahu organického rozpouštědla (nad 50%)jsou alkyly solvatovány a slut reaguje s celým řetězcem Rozdělování solutu mezi mobilní a stacionární fázi – retence roste s množstvím vázaného uhlíku (10 -60%) a délkou řetězce Nejpoužívanější je oktadecylová fáze (RP C-18) n n n Lze separovat nepolární látky (voda + organická rozpouštědla) Látky polarizovatelné a slabé kyseliny a báze (potlačit disociaci volbou p. H) Látky iontového charakteru, přidáme li do mobilní fáze iontově párové činidlo s opačným nábolem (laurylsulfát, tetraalkylamonné soli, . . ) – tvorba asociátu – iontově párová chromatografie

Iontově výměnná chromatografie n Jako stacionární fáze se používají n n n Využívají s následující funkční skupiny n n n organické polymery materiály na bázi silikagelu – jsou účinnější, rychleji se ustavuje rovnováha, umožňují práci s gradientovou elucí Karboxylová (-COOH) – slabý měnič kationtů Sulfoskupiny (-SO 3 H) – silný měnič kationtů Aminoskupina (-NH 2) – slabý měnič aniontů Tetraalkylamoniová (-N+(R)3) – silný měnič aniontů Jako mobilní fáze se používají vodné tlumivé roztoky, jejichž ionty jsou v dynamické rovnováze s ionty měniče – čím větší koncentrace, tím rychlejší eluce

Iontově výměnná chromatografie n Retenci lze ovlivňovat n n n Používá se pro n n n Koncentrací solí Hodnotou p. H Teplotou Přídavkem organického modifikátoru látky iontové povahy – silné i slabé elektrolyty Aminokyseliny – fáze ze silného katexu a C-18 Pro čištění peptidů a proteinů některé neutrální látky lze převést na nabité ionty (komplexy diolů a cukrů s kyselinou boritou) Speciální případ je iontová chromatografie na silných katexech či anexech s vodivostní detekcí. Aby byla detekce citlivá, je nutno potlačit vodivost mobilní fáze (uhličitany pro anionty a HCl pro kationty). Před detektor je zařazena potlačovací ionexová kolona opačného charakteru, která zamění disociovanou fázi za málo disociovanou- tedy málo vodivou.
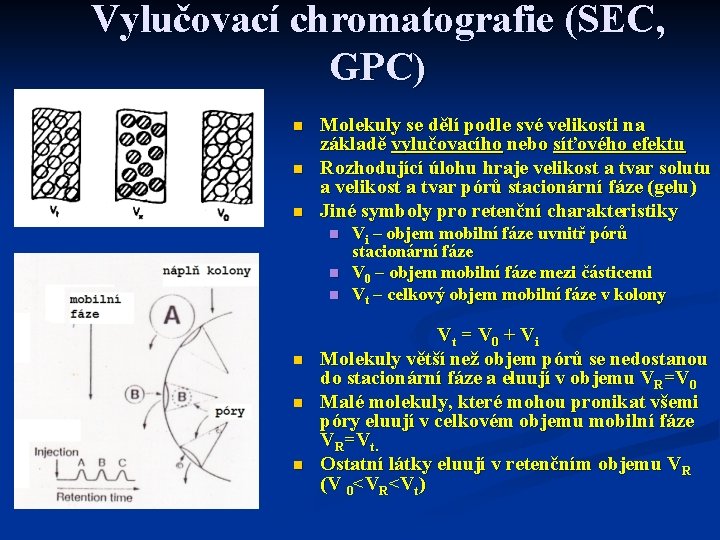
Vylučovací chromatografie (SEC, GPC) n n n Molekuly se dělí podle své velikosti na základě vylučovacího nebo síťového efektu Rozhodující úlohu hraje velikost a tvar solutu a velikost a tvar pórů stacionární fáze (gelu) Jiné symboly pro retenční charakteristiky n n n Vi – objem mobilní fáze uvnitř pórů stacionární fáze V 0 – objem mobilní fáze mezi částicemi Vt – celkový objem mobilní fáze v kolony Vt = V 0 + Vi Molekuly větší než objem pórů se nedostanou do stacionární fáze a eluují v objemu VR=V 0 Malé molekuly, které mohou pronikat všemi póry eluují v celkovém objemu mobilní fáze VR=Vt. Ostatní látky eluují v retenčním objemu VR (V 0<VR<Vt)

Vylučovací chromatografie (SEC, GPC) n Frakce objemu uvnitř pórů dosažitelná pro difúzi solutu se nazývá distribuční konstanta K 0 = (VR-V 0)/Vi VR = V 0 + K 0 Vi n n n Velké molekuly VR = V 0 a tedy K 0 = 0 malé molekuly VR= Vt a K 0 = 1 K 0 (0 – 1) Omezená separační kapacita (eluce mezi V 0 a Vi). Pro dosažení vyšší účinnosti separace nutno použít dlouhé kolony V případě ideálního chování v SEC (o retenci rozhoduje jen velikost a tvar pórů sttacionární fáze a analytu), je retenční čas (objem) přímo úměrný logaritmu molekulové hmotnosti Mr tr = a – b log Mr a, b - konstanty
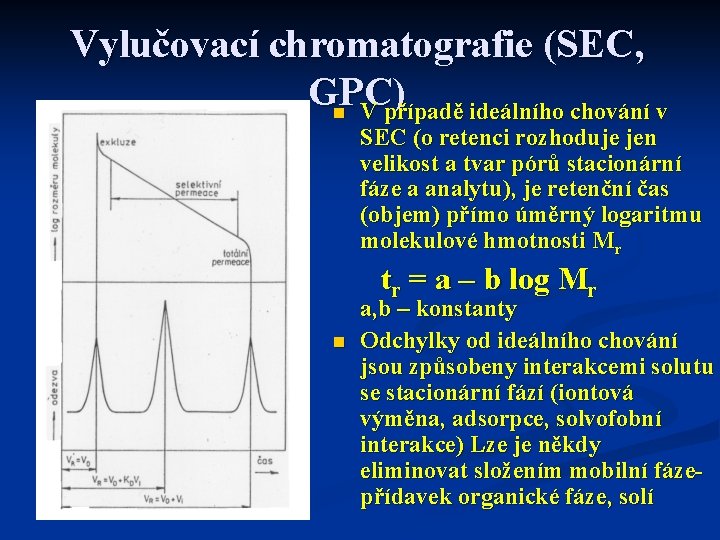
Vylučovací chromatografie (SEC, GPC) n V případě ideálního chování v SEC (o retenci rozhoduje jen velikost a tvar pórů stacionární fáze a analytu), je retenční čas (objem) přímo úměrný logaritmu molekulové hmotnosti Mr tr = a – b log Mr n a, b – konstanty Odchylky od ideálního chování jsou způsobeny interakcemi solutu se stacionární fází (iontová výměna, adsorpce, solvofobní interakce) Lze je někdy eliminovat složením mobilní fázepřídavek organické fáze, solí

Vylučovací chromatografie (SEC, GPC) n Stacionární fáze n n V klasické gelové chromatografii se používají hydrofilní zesíťované agarosové a dextranové gely – bobtnají a jsou stlačitelné – nelze používat v HPLC Pro HPLC semirigidní a rigidní náplně na bázi styrendivinylbenzenového kopolymeru nebo methakrylátových polymerů Pro biopolymery – hydrofilní polymery nebo anorganické stacionární fáze (porézní sklo, silikagel) – nebezpečí adsorpce solutů a složek mobilní fáze Mobilní fáze by neměla vykazovat interakce s analyty ani stacionární fází n n Musí rozpouštět analyty (vyšší pracovní teplota) Musí dobře smáčet povrch stacionární fáze, ale nesmí s ní interagovat Nemá solvatovat soluty – zvýšení jejich zdánlivé molekulové hmotnosti Kompatibilní s detektorem (pro UV nelze používat aromáty)

Vylučovací chromatografie (SEC, GPC) n SEC se využívá hlavně pro vysokomolekulární látky v polymerní chemii a biochemii s molekulovou hmotností nad 2 000. Pro předseparaci komplexních vzorků (štěpných produktů proteinů s tripsinem) n Oddělení nízkomolekulárních látek od vysokomolekulárních (gelová filtrace) n Určení molekulové hmotnosti látek a její distribuce n

Afinitní (biospecifická) chromatografie n n Je založena na silných biospecifických interakcích analytů s komplementárními látkami (ligandy) – interakce enzymů s inhibitory, substráty, kofaktory či efektory, komplexy protilátek s antigeny atd. Stacionární fáze- nosič s kovalentně navázaným ligandem (afinantem) Na takovou fázi se ze vzorku zadrží pouze látky s komplementární vazbou, ostatní se eluují s mrtvým časem Analyt se z vazby na ligand uvolní změnou p. H, koncentrace solí, změnou teploty, přídavkem činidel
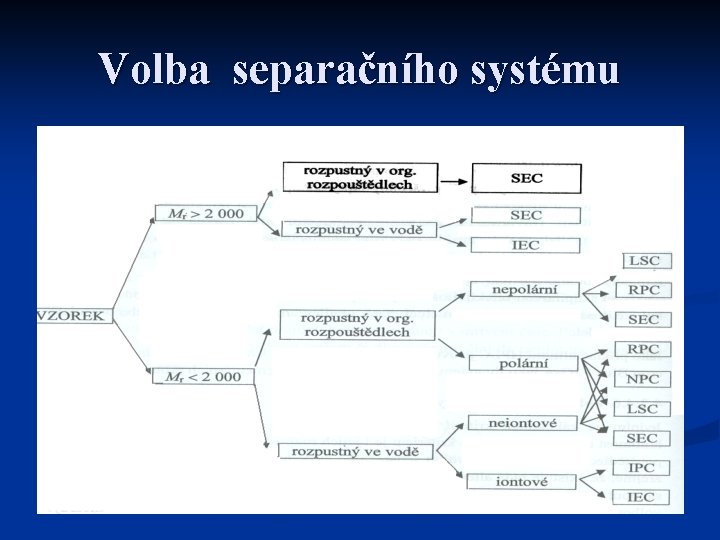
Volba separačního systému

Instrumentace v HPLC
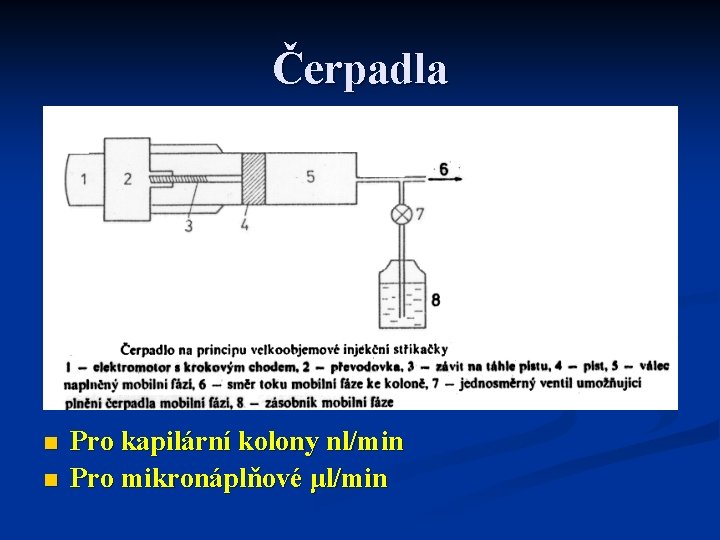
Čerpadla n n Pro kapilární kolony nl/min Pro mikronáplňové μl/min

Čerpadla n n Pro běžné náplňové kolem 1 ml/min Pro preparativní desítky ml/min
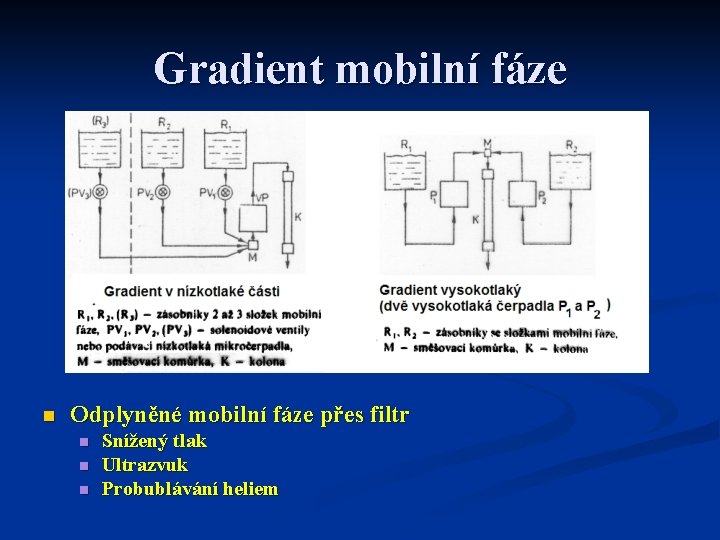
Gradient mobilní fáze n Odplyněné mobilní fáze přes filtr n n n Snížený tlak Ultrazvuk Probublávání heliem
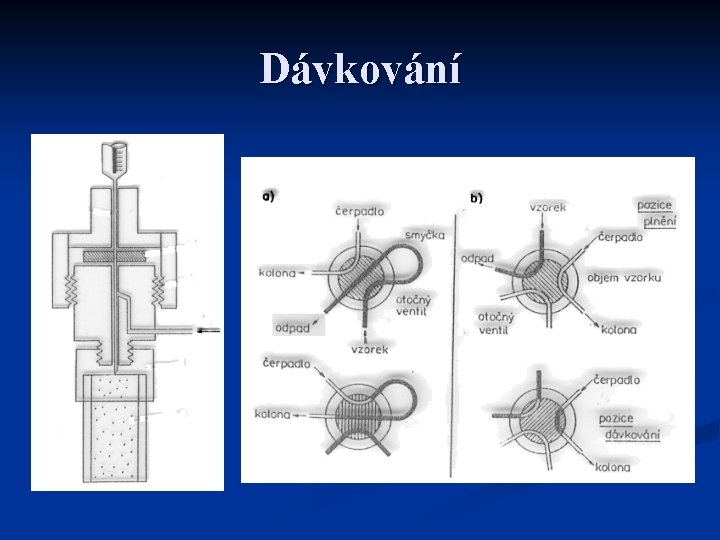
Dávkování
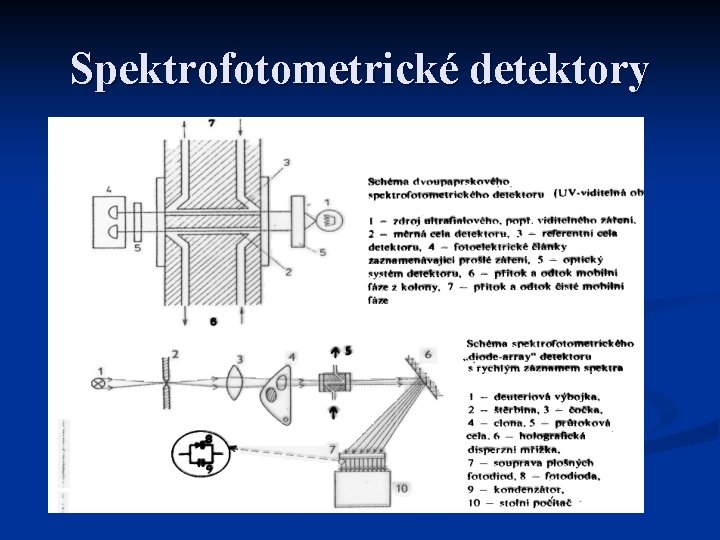
Spektrofotometrické detektory
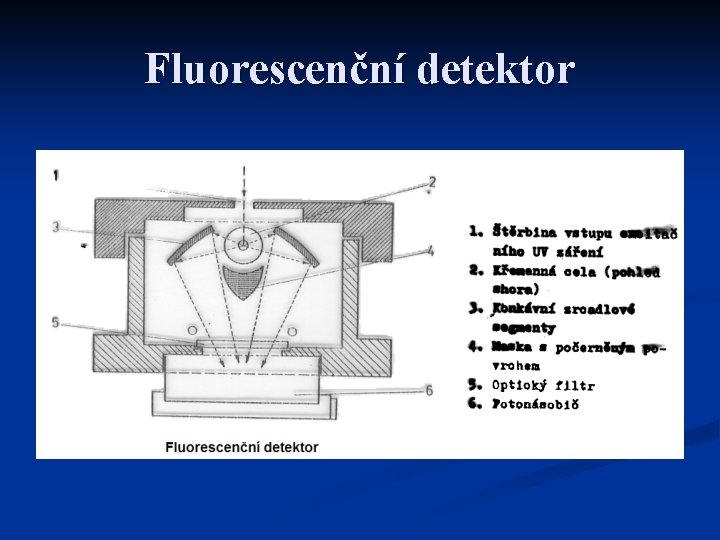
Fluorescenční detektor
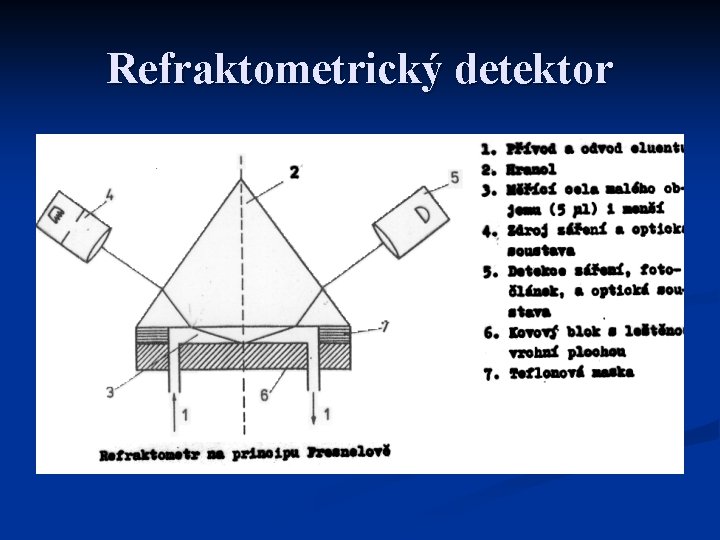
Refraktometrický detektor
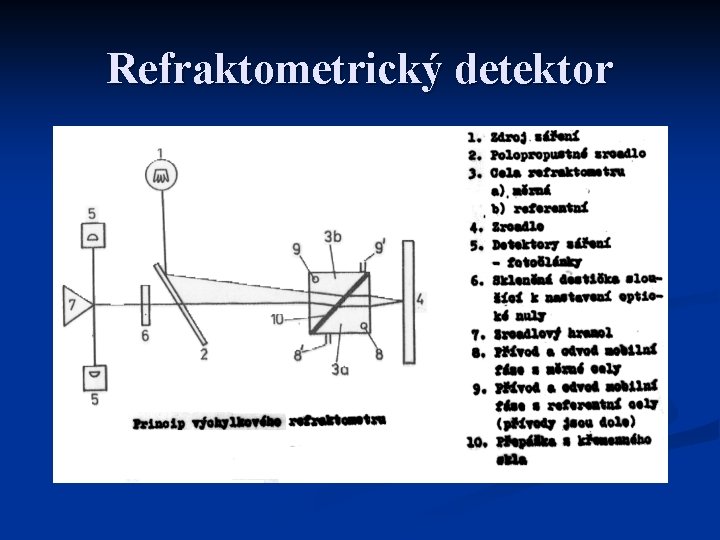
Refraktometrický detektor

Detektory pro HPLC n n Detektor založený na rozptylu světla s odpařením mobilní fáze (ELS – evaporative light scattering detektor). Použití je omezeno na netěkavé analyty a těkavé mobilní fáze – universální detektor Elektrochemické detektory (aminy, fenoly, …) n n n Měření vodivosti pro iontové látky Měření elektrického proudu elektrochemického děje (oxidace, redukce) Pracovní elektrody n n Ušlechtilý kov Au, Pt Různé formy uhlíku pro oxidace Rtuť a rtuťový film pro redukce Spojení s AAS, IPC, AES, NMR, MS

Gradientová eluce n Během analýzy se mění složení mobilní fáze. Používá se pro vzorky s velkými rozdíly v retenčních faktorech (10 < k < 1)
- Slides: 41