Vstavbov princip Periodickou tabulku lze vyut tak pro

Výstavbový princip • Periodickou tabulku lze využít také pro určení elektronové konfigurace prvku. • Př. : Popište elektronovou konfiguraci H a He H 1 s 1; He 1 s 2; • Př. : Popište elektronovou konfiguraci prvků ve čtvrté periodě. • Zkrácený zápis: např. elektronová konfigurace arsenu je [Ar]4 s 23 d 104 p 3.
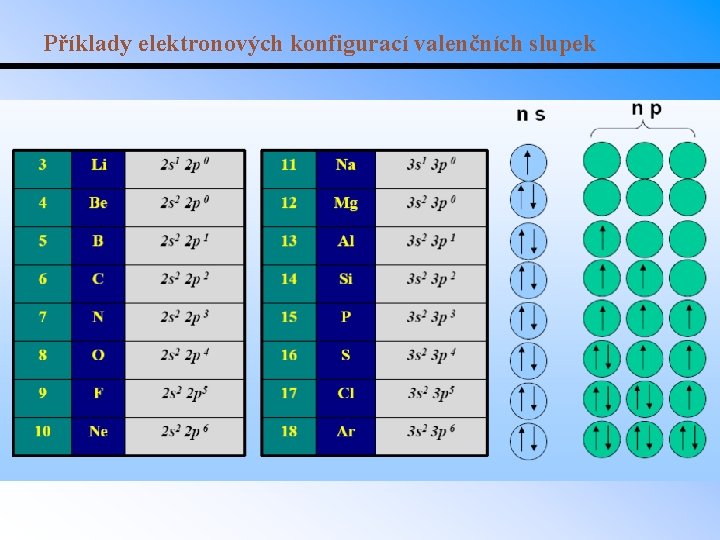
Příklady elektronových konfigurací valenčních slupek

Anomální elektronové konfigurace • Existuje několik výjimek z výstavbového principu. Stabilní konfigurace jsou např. také: – Z poloviny zaplněná podslupka d: • Cr má konfiguraci [Ar]4 s 13 d 5; • Mo má konfiguraci [Kr] 5 s 14 d 5 – Zcela zaplněná podslupka d: • Cu má konfiguraci [Ar]4 s 13 d 10 • Ag má konfiguraci [Kr]5 s 14 d 10. • Au má konfiguraci [Xe]6 s 14 f 145 d 10 • Výjimky se objevují u větších prvků které mají blízké energie orbitalů.
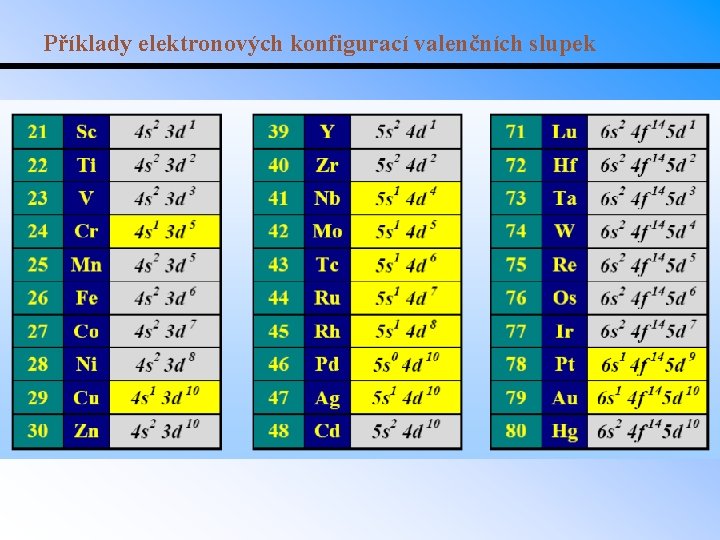
Příklady elektronových konfigurací valenčních slupek
![Příklady elektronových konfigurací iontů Na [Ne]3 s 1 Na+ [Ne] Ca [Ar]4 s 2 Příklady elektronových konfigurací iontů Na [Ne]3 s 1 Na+ [Ne] Ca [Ar]4 s 2](http://slidetodoc.com/presentation_image_h/d1400de59530dd29662dfd51346d5ddc/image-5.jpg)
Příklady elektronových konfigurací iontů Na [Ne]3 s 1 Na+ [Ne] Ca [Ar]4 s 2 Ca 2+ [Ar] Al [Ne]3 s 23 p 1 Al 3+ [Ne] H 1 s 1 H- 1 s 2 or [He] F 1 s 22 p 5 F- 1 s 22 p 6 ([Ne]) O 1 s 22 p 4 O 2 - 1 s 22 p 6 ([Ne]) N 1 s 22 p 3 N 3 - 1 s 22 p 6 ([Ne]) Fe: [Ar]4 s 23 d 6 Fe 2+: [Ar]4 s 03 d 6 ([Ar]3 d 6) Mn: Fe 3+: [Ar]4 s 03 d 5 ([Ar]3 d 5) Mn 2+: [Ar]4 s 03 d 5 ([Ar]3 d 5) [Ar]4 s 23 d 5

Periodicita chemických vlastností prvků • Chemické a mnohé fyzikální vlastnosti prvků jsou periodickou funkcí jejich atomových čísel. Periodické vlastnosti nacházíme i v řadách analogických sloučenin. • Mendělejev (1869) navrhl periodickou tabulku prvků seřazených podle atomového čísla (resp. Mr) horizontálně a podle chemických vlastností vertikálně. • Např. alkalické kovy tvoří ionty s nábojem +1, kovy alkalických zemin s nábojem + 2 • V tabulce zůstávaly neobsazené pozice prvků, které by měly existovat – postupně byly tyto prvky skutečně objeveny. • Univerzálnost vlastností je ve skutečnosti dána elektronovou konfigurací valenční sféry.

Periodická tabulka • Pořadí v tabulce je dáno výstavbovým principem (po řádcích). • Prvky ve stejných sloupcích mají stejnou elektronovou konfiguraci valenční slupky.
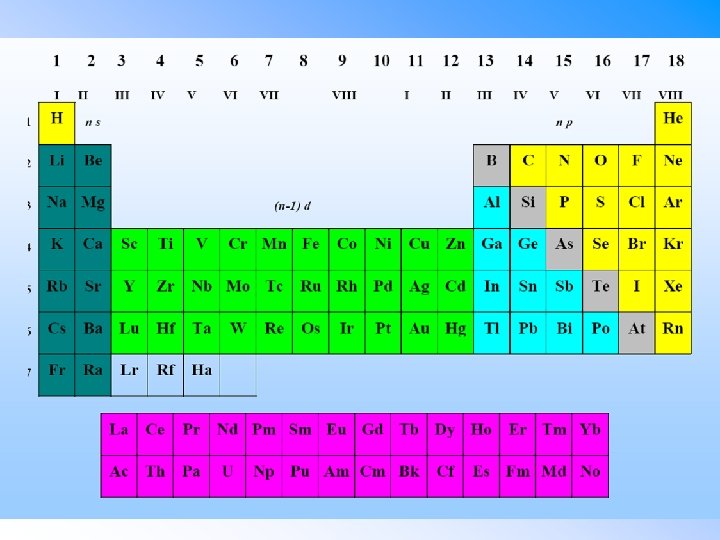

Základní trendy • Dominantní podobnost je vertikální: - klesá efektivní náboj jádra - vzrůstá velikost atomů - klesá ionizační energie a elektronová afinita - klesá elektronegativita - postupně zesilují kovové vlastnosti - vzrůstá reaktivita

Periodicita chemických vlastností • Protože mají prvky ve stejné skupině stejnou konfiguraci valenčních elektronů, měly by být podobné i jejich chemické vlastnosti. Př. : 2 Li(s) + Cl 2(g) 2 Li. Cl(s) 2 Na(s) + Cl 2(g) 2 Na. Cl(s) 2 K(s) + Cl 2(g) 2 KCl(s)

Izoelektronové látky a excitované stavy • Částice se stejným počtem elektronů jsou izoelektronové. • Př. : P 3 , S 2 , Cl , Ar, K+, Ca 2+. • V excitovaném (vybuzeném) stavu se alespoň jeden elektron nachází ve vyšší energetické hladině než odpovídá základnímu stavu. • Př. : [Ar]4 s 13 d 94 p 1 odpovídá konfiguraci excitovaného stavu Cu.

Orbitaly ve víceelektronových atomech • Elektrony jsou přitahovány k jádru ale také se navzájem odpuzují. • Repulzní síly způsobené dalšími elektrony stíní přitažlivý účinek atomového jádra. • Efektivní náboj jádra: náboj který je skutečně pociťován elektronem Zeff = Z Zshield Z – počet protonů Zshield – počet elektronů mezi jádrem a příslušným elektronem (nevalenční elektrony)
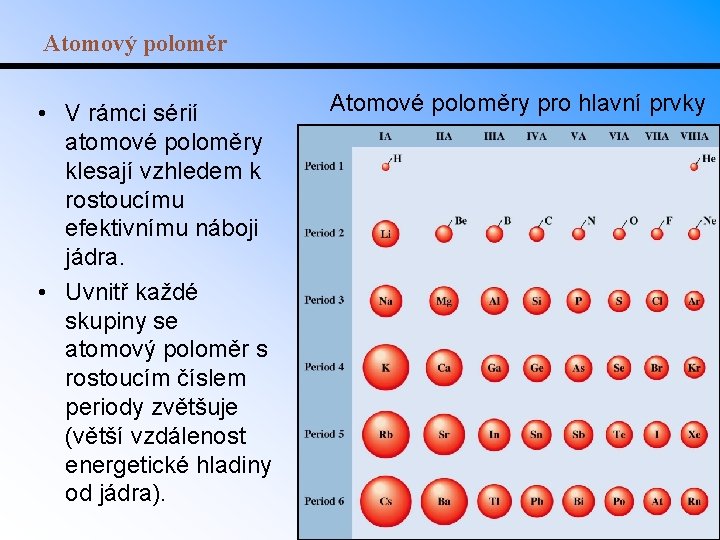
Atomový poloměr • V rámci sérií atomové poloměry klesají vzhledem k rostoucímu efektivnímu náboji jádra. • Uvnitř každé skupiny se atomový poloměr s rostoucím číslem periody zvětšuje (větší vzdálenost energetické hladiny od jádra). Atomové poloměry pro hlavní prvky
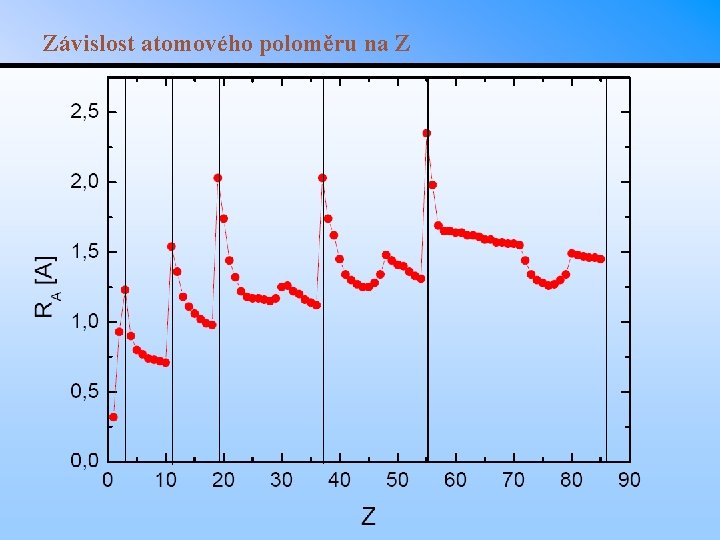
Závislost atomového poloměru na Z

Iontový poloměr • Pokud je iont kladně nabitý, jeho poloměr se zmenší, pokud záporně nabitý, zvětší se (vztaženo k poloměru elektroneutrálního atomu). • V rámci periody se kationty zmenšují. Když se objeví anionty, prudce se zvýší poloměr a následně pomalu klesá. Př. : Odhadněte která z následujících izoelektronových částic bude mít největší poloměr: P 3 , S 2 , Cl , Ar, K+, Ca 2+.
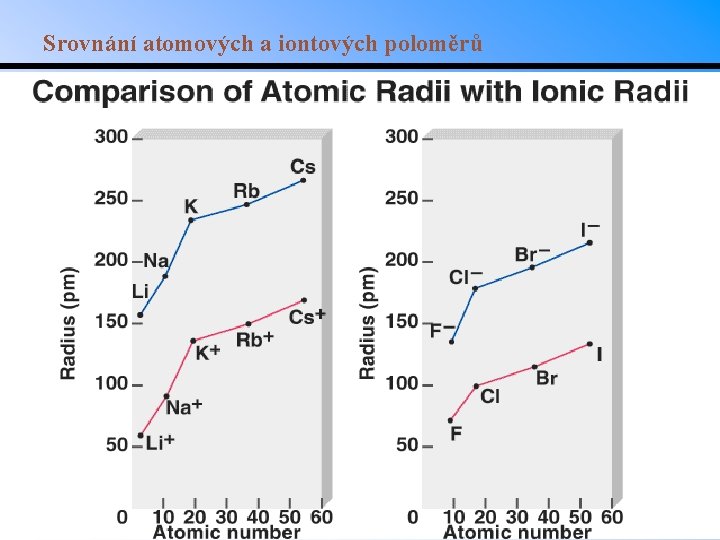
Srovnání atomových a iontových poloměrů
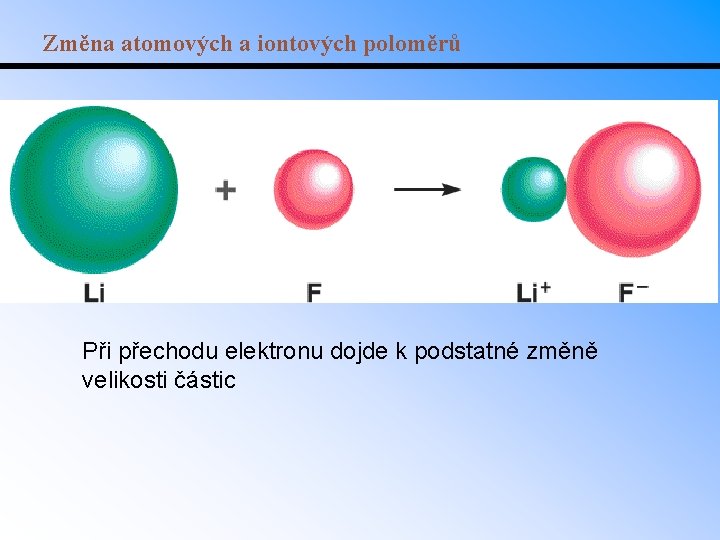
Změna atomových a iontových poloměrů Při přechodu elektronu dojde k podstatné změně velikosti částic

Iontové poloměry

Ionizační energie • • • Ionizační energie, Ei: minimální energie potřebná k odtržení elektronu od atomu v základním stavu v plynné fázi. M(g) + h M+ + e. Ei má přímý vztah k elektronové konfiguraci. Stabilnější základní stav odpovídá vyšší ionizační energii. Ionizační energie je vždy kladná, k ionizaci je tedy třeba dodat energii. Ionizační energie je nepřímo úměrná atomovému poloměru a přímo úměrná Zeff. Výjimky: B, Al, Ga, atd. : ionizační energie těchto prvků jsou o něco nižší než prvků v periodě předcházejících. • • – Před ionizací ns 2 np 1. Po ionizaci ns 2. Vyšší energie menší poloměr. Prvky skupiny 6 A. • • Před ionizací ns 2 np 4. Po ionizaci ns 2 np 3 a každý p elektron je v jiném orbitalu (Hundovo pravidlo).
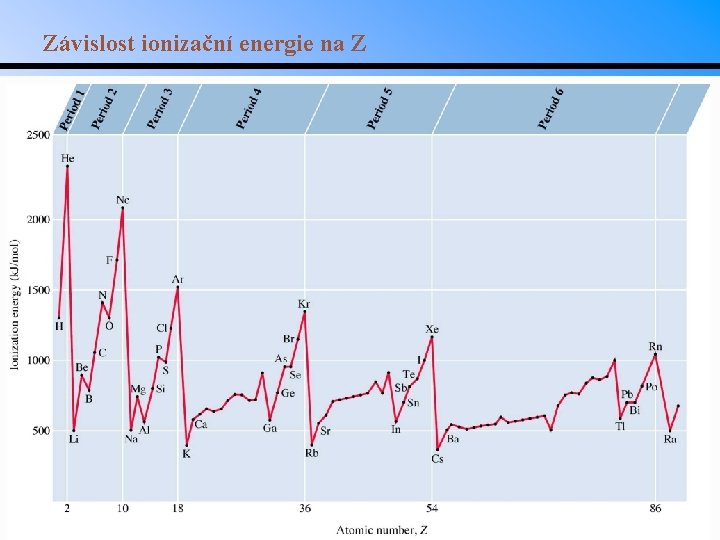
Závislost ionizační energie na Z

Vyšší ionizační energie • Energie potřebná k odtržení dalších elektronů od atomu se postupně zvyšuje. Např. druhá ionizace odpovídá reakci M+(g) + h M 2+ + e Ei 2. • Největší nárůst ionizační energie nastává u stabilních konfigurací typu vzácného plynu.
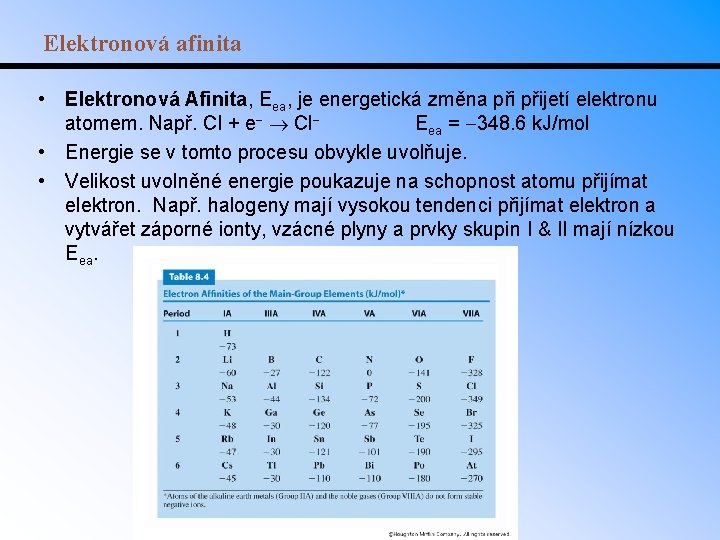
Elektronová afinita • Elektronová Afinita, Eea, je energetická změna přijetí elektronu atomem. Např. Cl + e Cl Eea = 348. 6 k. J/mol • Energie se v tomto procesu obvykle uvolňuje. • Velikost uvolněné energie poukazuje na schopnost atomu přijímat elektron. Např. halogeny mají vysokou tendenci přijímat elektron a vytvářet záporné ionty, vzácné plyny a prvky skupin I & II mají nízkou Eea.
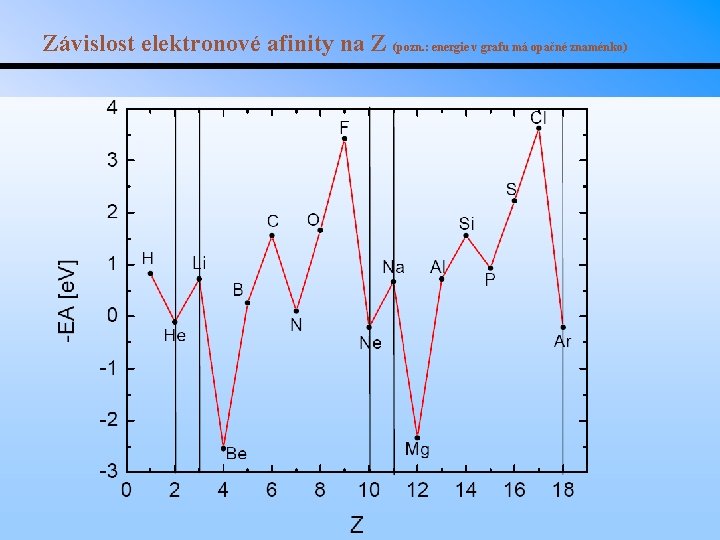
Závislost elektronové afinity na Z (pozn. : energie v grafu má opačné znaménko)

Elektronegativita • Elektronegativita je míra schopnosti atomu přijímat nebo ztrácet elektrony. Je přímo úměrná ionizační tendenci a schopnosti vytvářet konfiguraci vzácného plynu. Výpočet: kde Ei = ionizační energie Eea = elektronová afinita (obvykle záporná hodnota!) Např. Li má velmi nízkou ionizační energii i elektronovou afinitu, zatímco Cl má obě tyto hodnoty vysoké. Elektronegativita Cl bude tudíž vysoká a Li nízká. Nejvyšší elektronegativitu má fluor (4. 0). • Elektronegativita se zvyšuje v periodické tabulce diagonálně (odspodu nahoru a doprava). • Rozdíl elektronegativit dvou prvků poskytuje představu o charakteru případné chemické vazby mezi nimi: • Iontová vazba vzniká pokud 2 • Kovalentní vazba vzniká pokud 1 • Polárně kovalentní vazba vzniká pokud 1 2, vazba je přechodem mezi kovalentní a iontovou.
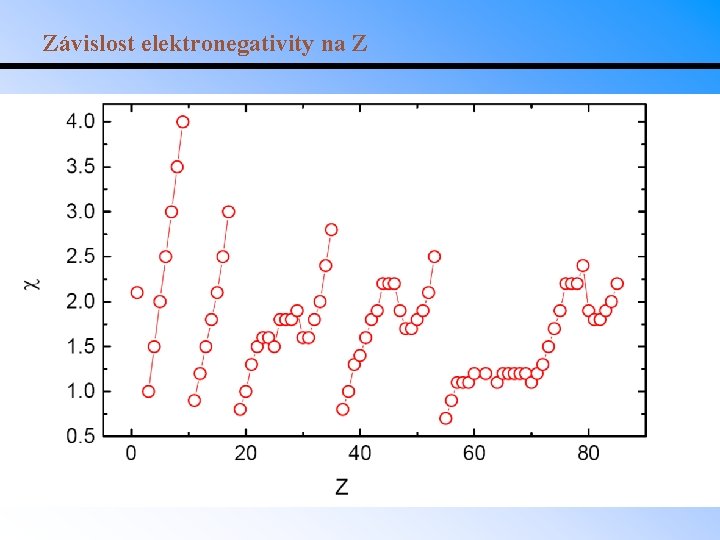
Závislost elektronegativity na Z
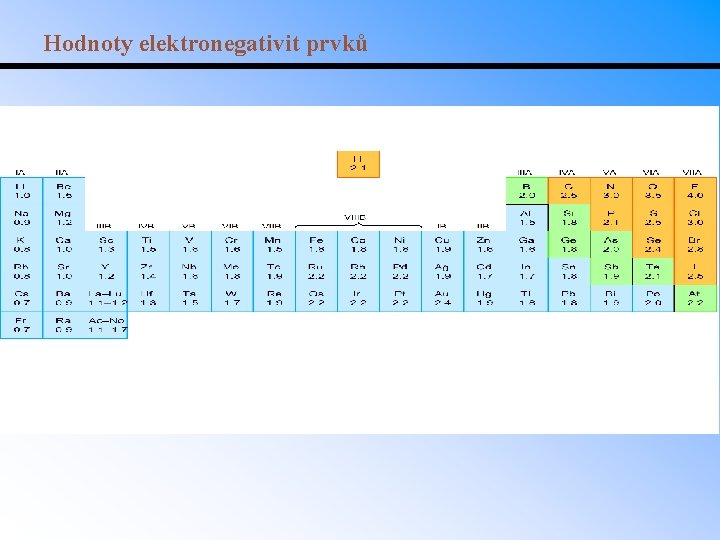
Hodnoty elektronegativit prvků
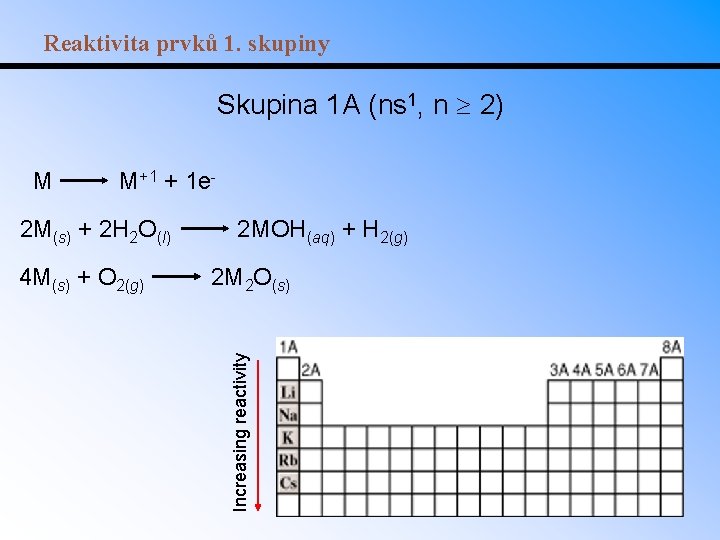
Reaktivita prvků 1. skupiny Skupina 1 A (ns 1, n 2) M+1 + 1 e- 2 M(s) + 2 H 2 O(l) 4 M(s) + O 2(g) 2 MOH(aq) + H 2(g) 2 M 2 O(s) Increasing reactivity M
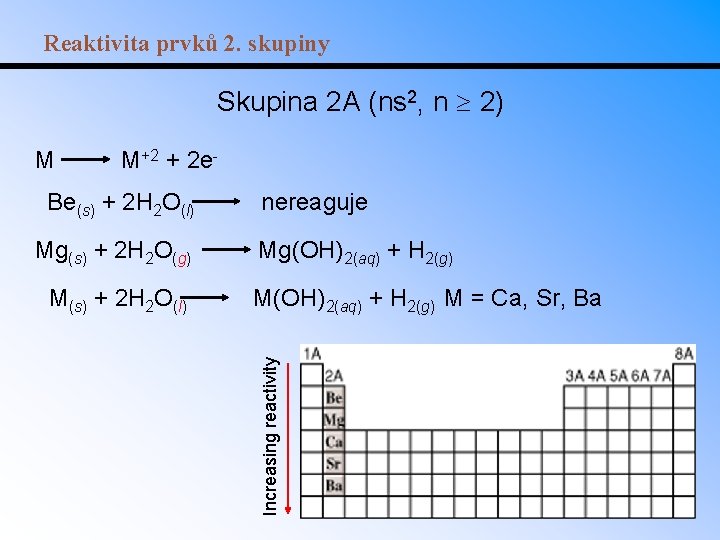
Reaktivita prvků 2. skupiny Skupina 2 A (ns 2, n 2) M+2 + 2 e- Be(s) + 2 H 2 O(l) Mg(s) + 2 H 2 O(g) M(s) + 2 H 2 O(l) nereaguje Mg(OH)2(aq) + H 2(g) M = Ca, Sr, Ba Increasing reactivity M
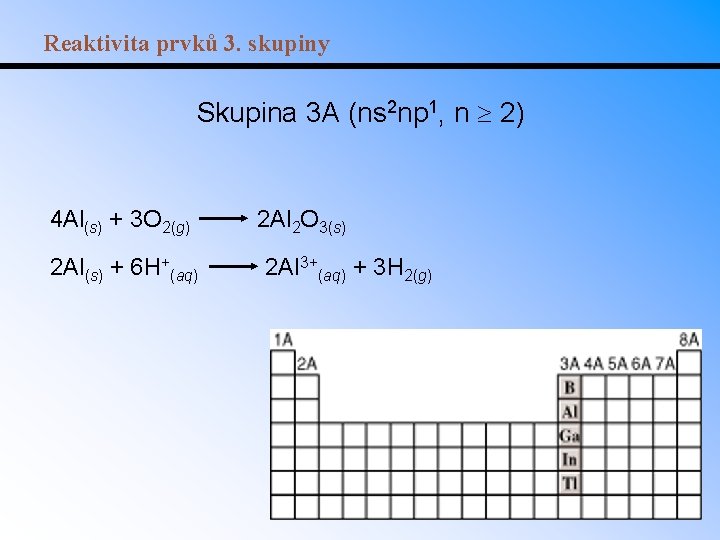
Reaktivita prvků 3. skupiny Skupina 3 A (ns 2 np 1, n 2) 4 Al(s) + 3 O 2(g) 2 Al(s) + 6 H+(aq) 2 Al 2 O 3(s) 2 Al 3+(aq) + 3 H 2(g)
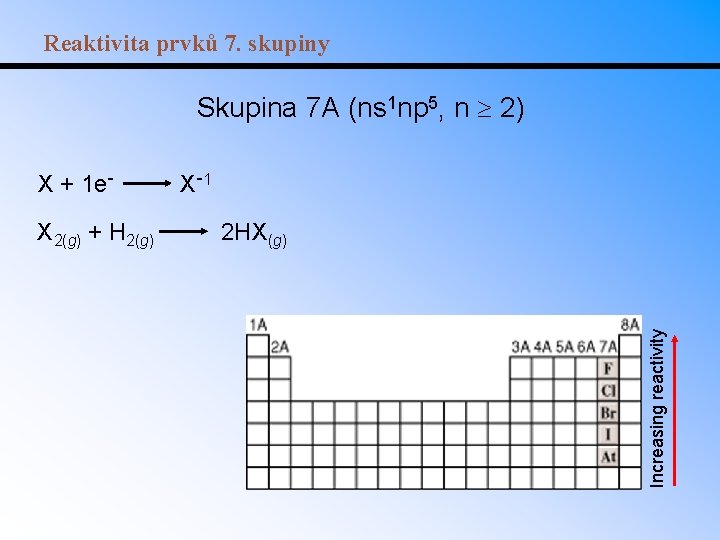
Reaktivita prvků 7. skupiny Skupina 7 A (ns 1 np 5, n 2) X 2(g) + H 2(g) X -1 2 HX(g) Increasing reactivity X + 1 e-
- Slides: 30