Vrus Antivirais Equipe de Virologia DEMIPICBS UFRGS Prof

Vírus & Antivirais Equipe de Virologia DEMIP/ICBS / UFRGS Prof Paulo Roehe Fonte: http: //www. google. com/imghp 1
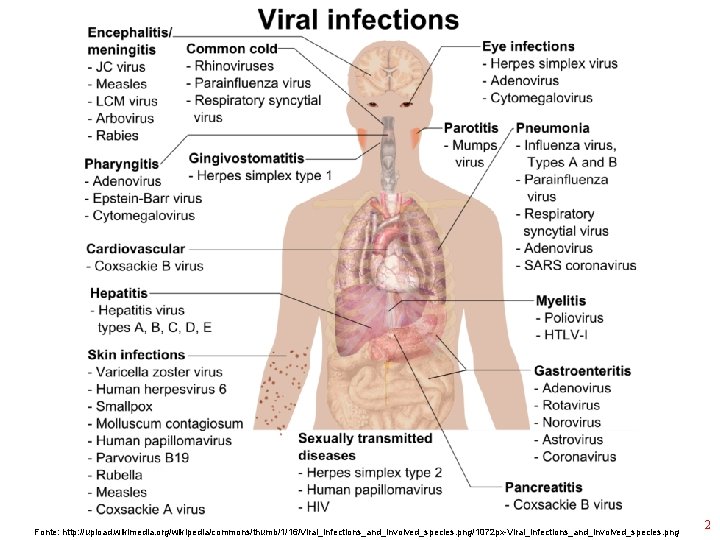
Fonte: http: //upload. wikimedia. org/wikipedia/commons/thumb/1/16/Viral_infections_and_involved_species. png/1072 px-Viral_infections_and_involved_species. png 2

O antiviral ideal • Deve interromper a replicação do vírus sem afetar significativamente o metabolismo de células do hospedeiro • A chave é a seletividade Fonte: http: //images. wisegeek. com/brass-key. jpg 3

O antiviral ideal • Deve ser capaz de penetrar nas células infectadas • Interferir com a síntese e/ou regulação de ácidos nucleicos virais • Interferir com a habilidade dos vírus se ligarem a célula • Estimular a resposta imune do organismo – Deve agir sinergicamente com o sistema imune para eliminar ou suprimir a atividade viral 91
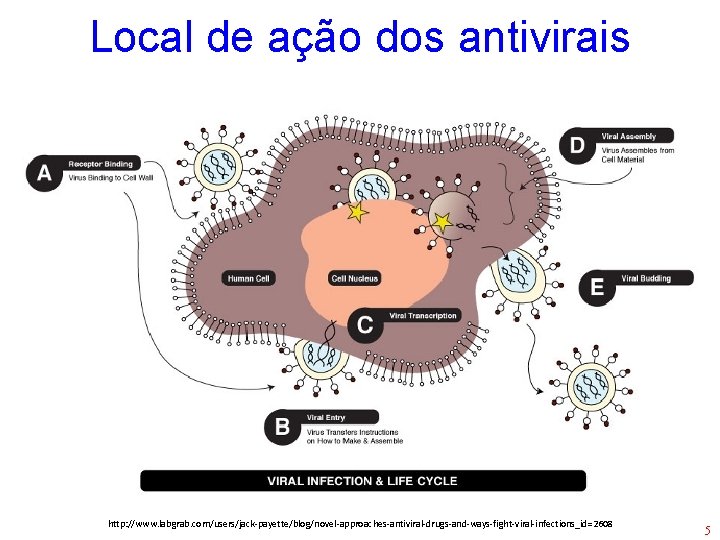
Local de ação dos antivirais http: //www. labgrab. com/users/jack-payette/blog/novel-approaches-antiviral-drugs-and-ways-fight-viral-infections_id=2608 5
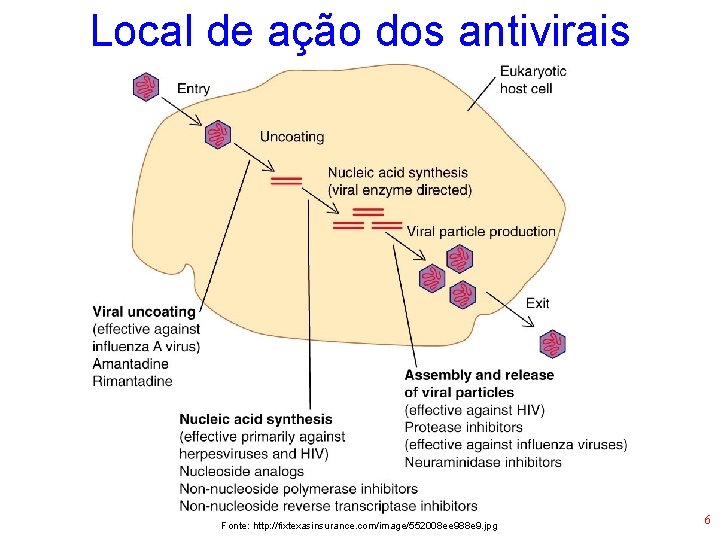
Local de ação dos antivirais Fonte: http: //fixtexasinsurance. com/image/552008 ee 988 e 9. jpg 6
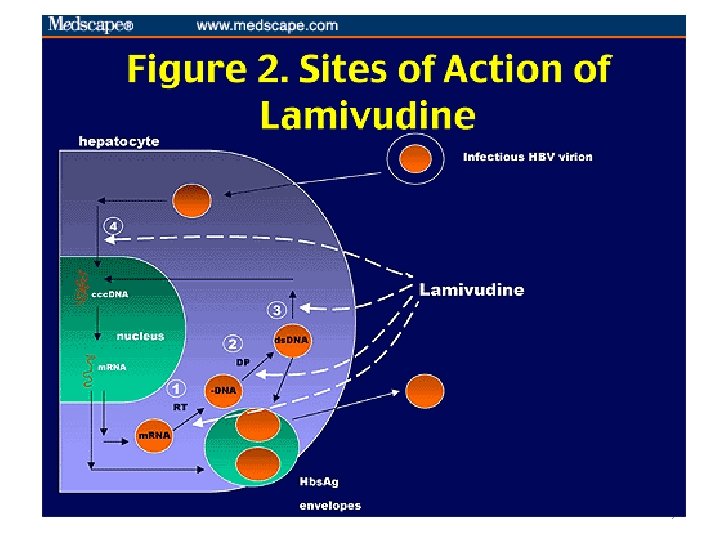
7

Pró-droga • Muitos antivirais são pró-drogas: devem ser modificados (ex: fosforilados) por enzimas virais ou celulares para se tornarem ativos 90
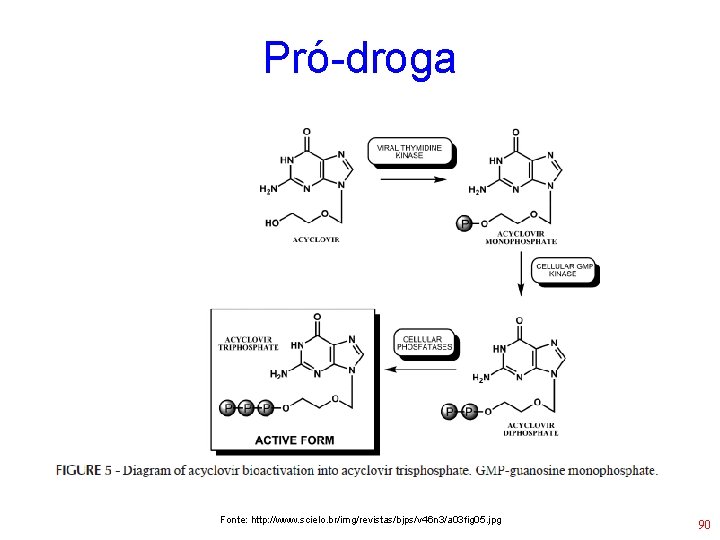
Pró-droga Fonte: http: //www. scielo. br/img/revistas/bjps/v 46 n 3/a 03 fig 05. jpg 90

Problemas dos antivirais • Inibem a replicação, mas após a remoção da droga o vírus volta a se replicar • Outros problemas: – Toxicidade – Rápido metabolismo – Baixa absorção – Rápida excreção 90
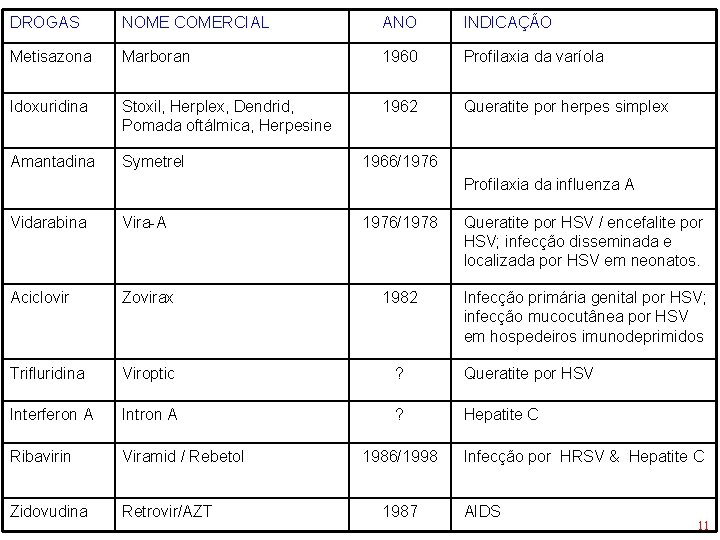
DROGAS NOME COMERCIAL ANO INDICAÇÃO Metisazona Marboran 1960 Profilaxia da varíola Idoxuridina Stoxil, Herplex, Dendrid, Pomada oftálmica, Herpesine 1962 Queratite por herpes simplex Amantadina Symetrel 1966/1976 Profilaxia da influenza A Vidarabina Vira-A 1976/1978 Queratite por HSV / encefalite por HSV; infecção disseminada e localizada por HSV em neonatos. Aciclovir Zovirax 1982 Infecção primária genital por HSV; infecção mucocutânea por HSV em hospedeiros imunodeprimidos Trifluridina Viroptic ? Queratite por HSV Interferon A Intron A ? Hepatite C Ribavirin Viramid / Rebetol Zidovudina Retrovir/AZT 1986/1998 1987 Infecção por HRSV & Hepatite C AIDS 11
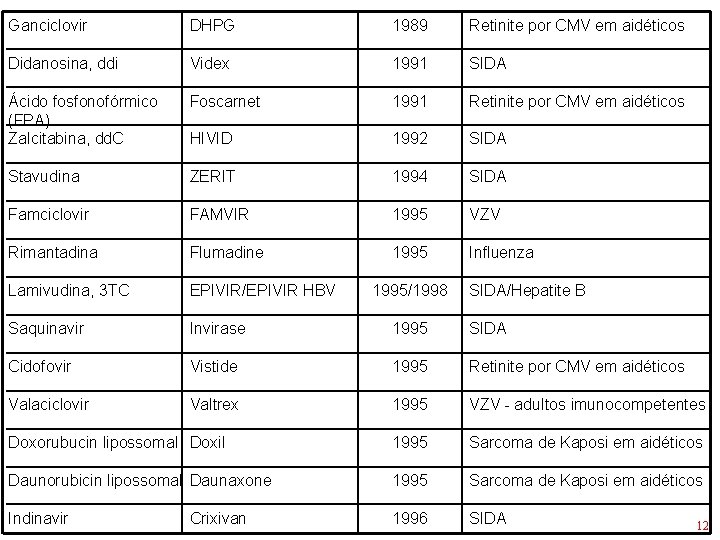
Ganciclovir DHPG 1989 Retinite por CMV em aidéticos Didanosina, ddi Videx 1991 SIDA Ácido fosfonofórmico (FPA) Zalcitabina, dd. C Foscarnet 1991 Retinite por CMV em aidéticos HIVID 1992 SIDA Stavudina ZERIT 1994 SIDA Famciclovir FAMVIR 1995 VZV Rimantadina Flumadine 1995 Influenza Lamivudina, 3 TC EPIVIR/EPIVIR HBV Saquinavir Invirase 1995 SIDA Cidofovir Vistide 1995 Retinite por CMV em aidéticos Valaciclovir Valtrex 1995 VZV - adultos imunocompetentes Doxorubucin lipossomal Doxil 1995 Sarcoma de Kaposi em aidéticos Daunorubicin lipossomal Daunaxone 1995 Sarcoma de Kaposi em aidéticos Indinavir 1996 SIDA Crixivan 1995/1998 SIDA/Hepatite B 12
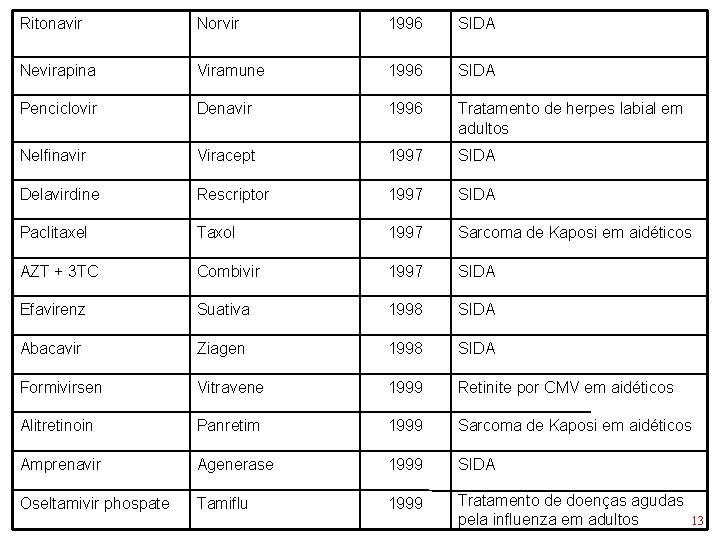
Ritonavir Norvir 1996 SIDA Nevirapina Viramune 1996 SIDA Penciclovir Denavir 1996 Tratamento de herpes labial em adultos Nelfinavir Viracept 1997 SIDA Delavirdine Rescriptor 1997 SIDA Paclitaxel Taxol 1997 Sarcoma de Kaposi em aidéticos AZT + 3 TC Combivir 1997 SIDA Efavirenz Suativa 1998 SIDA Abacavir Ziagen 1998 SIDA Formivirsen Vitravene 1999 Retinite por CMV em aidéticos Alitretinoin Panretim 1999 Sarcoma de Kaposi em aidéticos Amprenavir Agenerase 1999 SIDA Oseltamivir phospate Tamiflu 1999 Tratamento de doenças agudas pela influenza em adultos 13

Resposta imune a infecção • Os antivirais não eliminam vírus que não estejam replicando ou estejam latentes • Então a efetividade do sistema imune é essencial para se livrar da infecção viral • Importância do Interferon 14
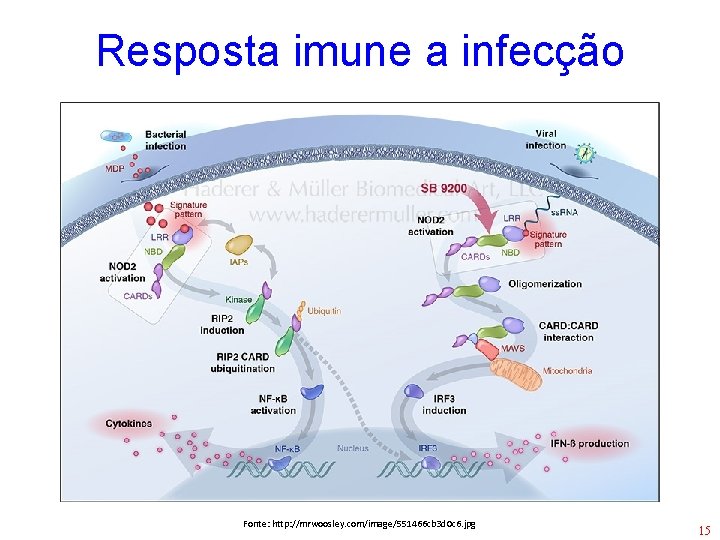
Resposta imune a infecção Fonte: http: //mrwoosley. com/image/551466 cb 3 d 0 c 6. jpg 15

Interferon • Proteínas naturais produzidas pelas células do sistema imune na resposta a vírus, bactéria, parasitas e céls tumorais • Ação antiviral que modula a resposta imune • Três classes: alfa, beta e gama 16

Interferon • Alfa e Beta: produzidos por todas as células em resposta a infecção viral • Gama: produzido somente por linfócitos T e células NK em resposta a citocinas • Alfa e Beta são mais efetivos que o Gama na atividade antiviral 17

Interferon • Mecanismos de ação – Induz a proteína quinase que inibe a síntese proteica – Induz a oligoadenilato sintetase que comanda para a degradação do m. RNA viral – Induz a fosfodiesterase que inibe o t. RNA inibindo a transdução 18
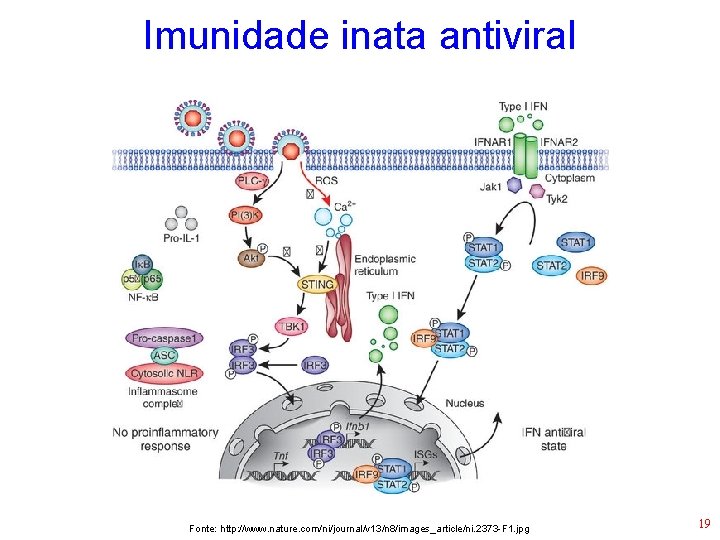
Imunidade inata antiviral Fonte: http: //www. nature. com/ni/journal/v 13/n 8/images_article/ni. 2373 -F 1. jpg 19

Interferon • Farmacocinética Fonte: http: //hepatite. org. br/hepatite/tratamento-e-cura – Biodisponibilidade oral: menor que 1% – Administrado IV e SC (injetável) – Distribuição em todos os tecidos, exceto SNC e olhos – Meia vida: 1 a 4 horas 20

Interferon • Efeitos colaterais – Febre, dor de cabeça, prurido – Supressão da medula óssea (anemia) – Neuro e cardiotoxicidade – Perda de fertilidade 21

Interferon • Alguns usos – Hepatite B e C crônicas – Infecções por CMV em pacientes transplantados – Sarcoma de Kaposi em pacientes com Aids • Interferon peguilado – Modificado através da adição de uma molécula de polietilenoglicol 22

Interferon + Ribavirina => HCV • Interferon peguilado • Ribavirina: análogo nucleosídeo sintético • Tratamento: de 6 (genótipo 2 e 3) a 12 meses (genótipo 1) • Muitos efeitos colaterais – Cefaleia, febre, dores musculares, cansaço, perda de apetite, perda de peso, prurido, depressão, queda de glóbulos brancos, plaquetas e anemia 23
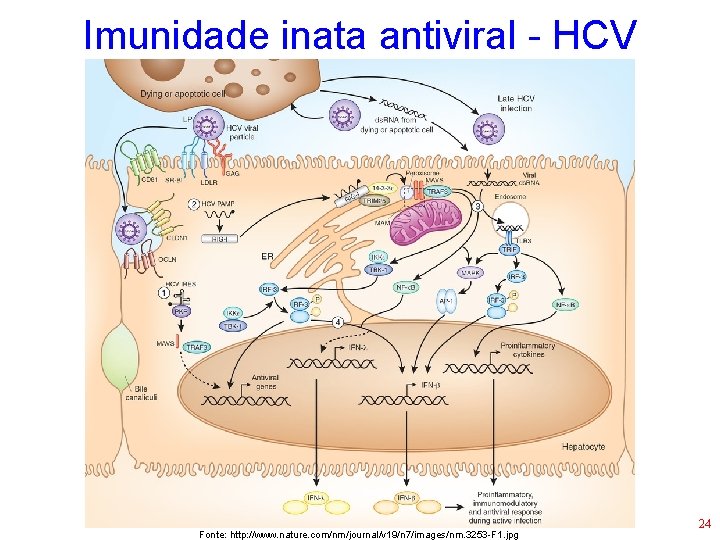
Imunidade inata antiviral - HCV Fonte: http: //www. nature. com/nm/journal/v 19/n 7/images/nm. 3253 -F 1. jpg 24

Análogos de nucleosídeos • Muitas drogas antivirais são nucleosídeos sintéticos que interferem de alguma maneira com a síntese de DNA ou RNA • Exemplos: – – – Ribavirina - Ganciclovir Aciclovir - Trifluridina Cidofovir - Didanosina (ddl) Famciclovir - Lamivudina (3 TC) Idoxuridina - Zidovudina (AZT) 25
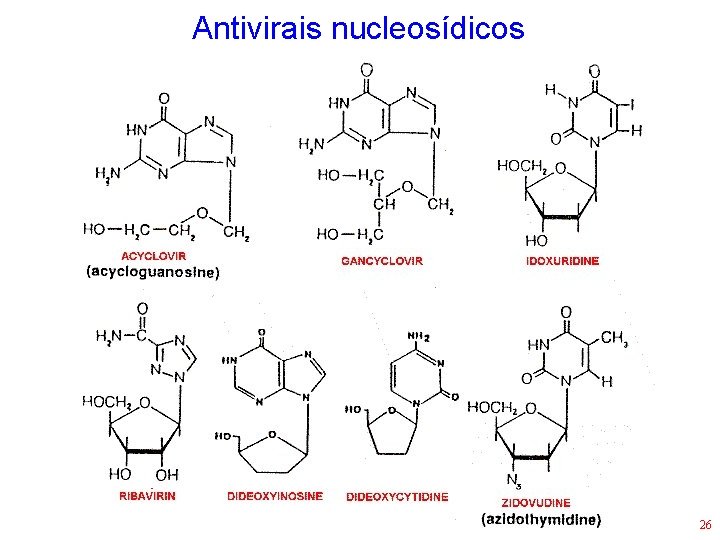
Antivirais nucleosídicos 26

Fonte: http: //www. toomuchof. com/wp-content/uploads/2014/02/acyclovir-toxicity-1. jpg 27
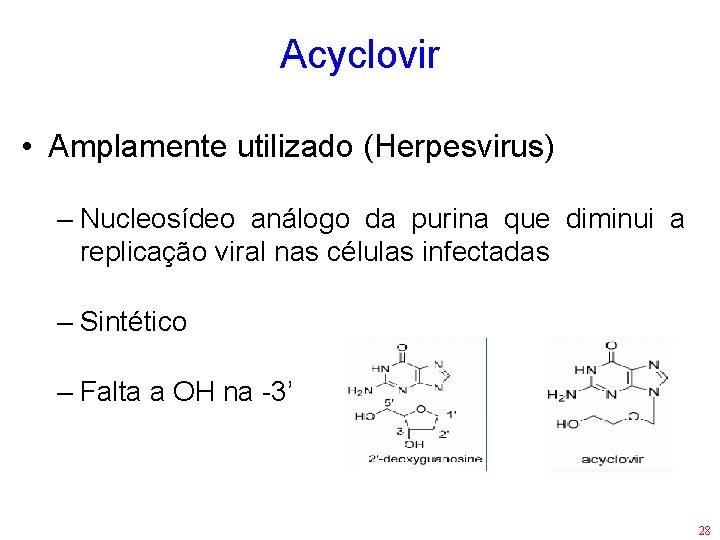
Acyclovir • Amplamente utilizado (Herpesvirus) – Nucleosídeo análogo da purina que diminui a replicação viral nas células infectadas – Sintético – Falta a OH na -3’ 28
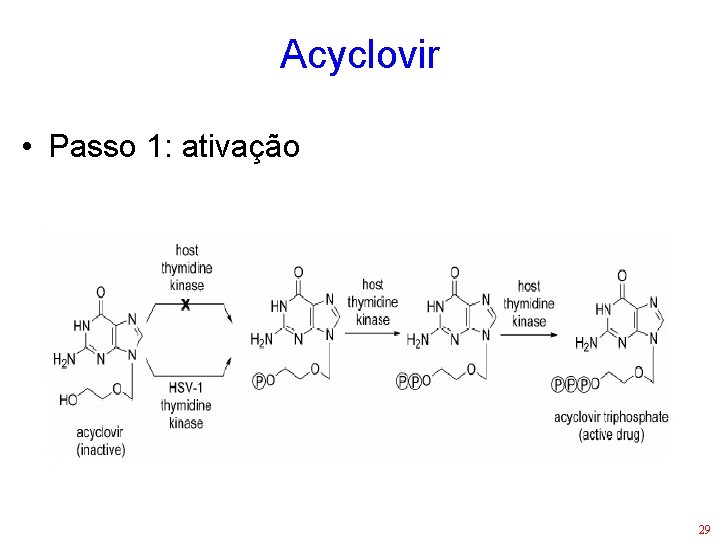
Acyclovir • Passo 1: ativação 29
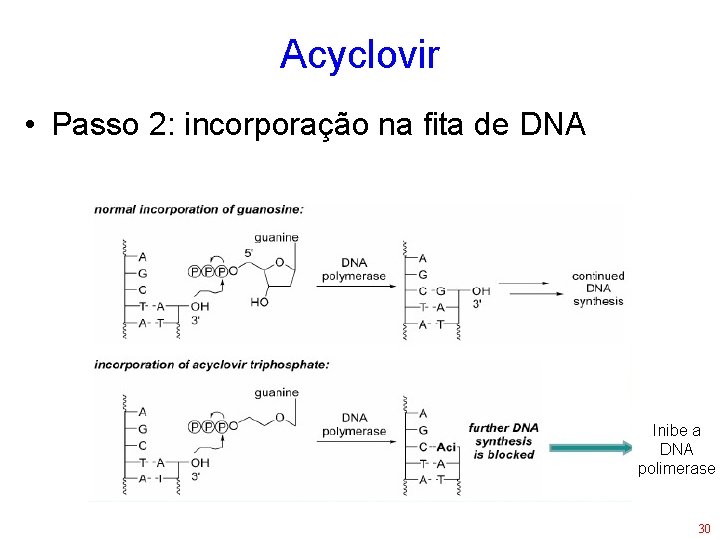
Acyclovir • Passo 2: incorporação na fita de DNA Inibe a DNA polimerase 30

Acyclovir • Efetivo contra – HHV-1 (HSV-1) – HHV-2 (HSV-2) – HHV-3 (Varicela-zoster) – HHV-4 (Epstein-Barr) – HHV-5 (Citomegalovírus) – menos efetivo 31

Acyclovir • Farmacocinética – Baixa absorção oral (15 a 20%) – Excretada na urina – Meia-vida: 2 a 3 horas somente – Valaciclovir e Famciclovir: melhor absorção oral (50 e 70%, respectivamente) 32
Acyclovir • Resistência – Mutações na timidina quinase ou na DNA polimerase viral • Efeitos colaterais – Oral: náusea, diarréia e dor de cabeça 33

Inibidores enzimáticos • São aqueles que interferem com os processos de replicação viral, mas não são análogos de nucleosídeos • Podem inativar as enzimas virais por ligarem-se diretamente a elas ou por serem inibidores da protease • Exemplos: – Fosfato de oseltamivir - Efavirenz – Foscarnet - Indinavir – Nevirapina - Ritonavir – Delavirdine - Saquinavir 34

Hepatite C – novo tratamento • Inclui inibidor de protease: boceprevir ou telaprevir • Chance de cura aumenta para 70% • Limitado ao genótipo 1 • Mais efeitos colaterais: – anemia grave e quadros dermatológiocos severos 35

HCV – Sofosbuvir e Simeprevir • Antiviral de ação direta: inibe a RNA polimerase viral NS 5 B • Menor efeito colateral • Associado a Interf + Ribav: ~90% de cura • Tempo de tratamento diminui: 12 semanas • Daclatasvir: inibe a NS 5 A Fonte: http: //www. blog. saude. gov. br/index. php/34964 -daclatasvir-novo-medicamento-hepatite-c-recebe-registro-da-anvisa 36
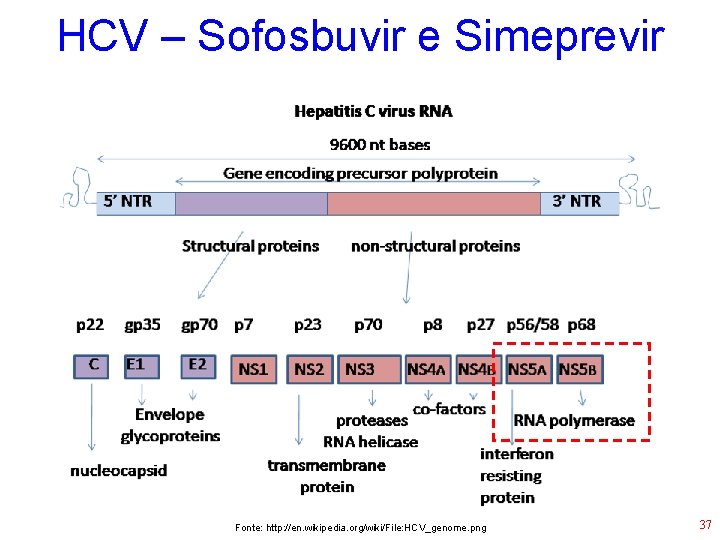
HCV – Sofosbuvir e Simeprevir Fonte: http: //en. wikipedia. org/wiki/File: HCV_genome. png 37

Inibidores de protease • Saquinavir (SQV), Nelfanir (NFV), Indinavir (IDV), Ritonavir (RTV), Lopinavir e Aprenavir (AMP) • Se ligam a poliproteina e impedem a clivagem em proteínas funcionais • Administrado oralmente • Saquivir: meia-vida de 12 horas 38

Nucleosídeos inibidores da transcriptase reversa • Utilizadas contra retrovirus (HIV) • Uso prolonga e melhora a qualidade de vida • Não curam a infecção • Zidovudine (AZT), Abacavir (ABC) • Lamivudine (3 TC), Didanosine (ddl) • Zalcitabine (dd. C), Estavudine (d 4 T) 39
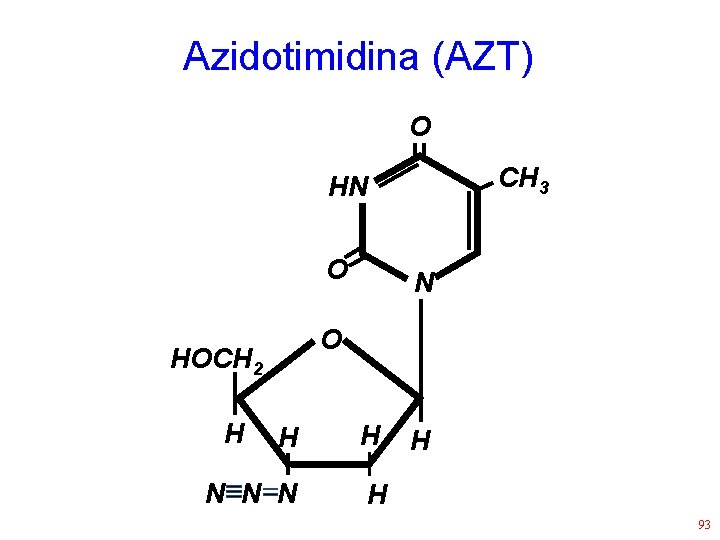
Azidotimidina (AZT) O CH 3 HN O O HOCH 2 H N H H N N N H H 93
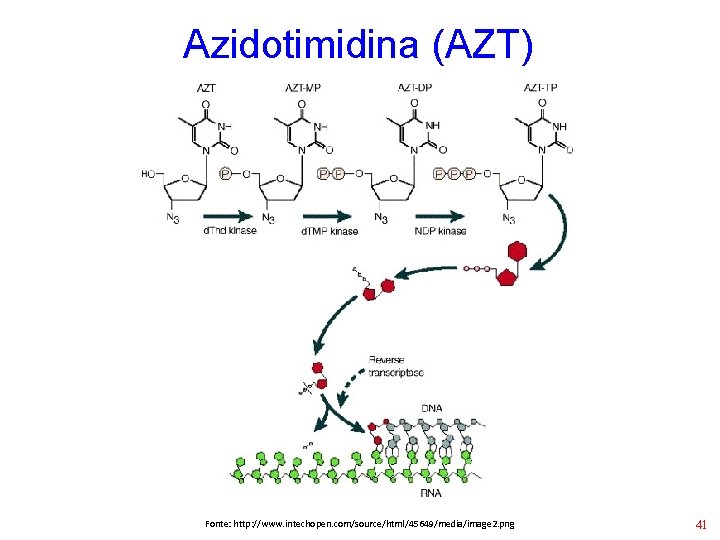
Azidotimidina (AZT) Fonte: http: //www. intechopen. com/source/html/45649/media/image 2. png 41

Azidotimidina (AZT) • Inibe a transcriptase reversa • Previne a infecção de novas células pelo HIV • Resistencia: mutação pontual que altera a transcriptase reversa • Cinética: Biodisponibilidade: 60 a 80% – Meia-vida: 1 hora / intracelular: 3 horas 42

Azidotimidina (AZT) • Efeitos colaterais: – Anemia, náusea, vomito, dor abdominal • Interação: paracetamol (inibe o metabolismo de AZT) • Uso: HIV em combinação com Lamivudine (3 TC) e NVP 43

Duovir-N • Composto contendo: Ø Lamivudine: 150 mg Ø Zidovudine: 300 mg Ø Nevirapine: 200 mg Fonte: http: //www. dropshipmd. com/wp-images/hiv/duovir-n_tablets. jpg 44

Inibidores não-nucleosídicos da transcriptase reversa • Nevirapine (NVP), Delavirdine (DLV), Efavirenz (EFZ), • Inibem diretamente a transcriptase reversa sem fosforilação intracelular • Se liga próximo sitio a catalítico causa e desnaturação • Mais potente que AZT contra HIV-1, mas não contra HIV-2 45

Não-nucleosideos inibidores da transcriptase reversa • Cinética: • Administração oral • Meia vida: 20 min no plasma • Pode prevenir a transmissão de HIV da mãe para o feto se administrado em ambos • Efeito colateral: febre, dor de cabeça, letargia, hepatite 46

Terapia combinada contra o HIV • Objetivos: alcançar eficácia máxima, minimizar a toxicidade pela redução da dosagem individual da droga e diminuir as chances de desenvolvimento de resistência. • Combinação usual: 1 inibidor de protease + 2 inibidores de transcriptase reversa 47

48

HAART • Highly active antiretroviral therapy Fonte: http: //www. amfar. org/uploaded. Images/_amfarorg/Articles/In_The_Lab/2013/HAART. jpg 49

HAART • Highly active antiretroviral therapy • Terapia antiretroviral agressiva com o objetivo de suprimir a carga viral no plasma • Combinações de várias drogas: • 2 NRTIs + 1 NNRTI (Z+L+Efavirenz) • 2 NRTIs + 1 ou 2 inibidor de protease (Z+L+Lopinavir) 50

Terapia combinada contra HIV 2 drogas 3 drogas AZT + ddl AZT + dd. C AZT + DLV AZT + 3 TC ddl + DLV d 4 T + ddl Ritonavir + 1 análogo de nucleotídeo Ritonavir + AZT Indinavir + AZT Norvir + AZT + 3 TC Indinavir + AZT + dd. I 51

Drogas anti-Influenza Fonte: http: //media. syracuse. com/news/photo/2009/12/tamiflu-apjpg-38 ced 3484 b 9517 ba_large. jpg 52

Drogas anti-Influenza • Inibidores de Neuraminidase – Oseltamivir - Tamiflu – Zanamivir - Relenza – Bloqueiam a liberação de partículas virais • Inibidores de canais de íons M 2 – Amantadina – Mantidan – Rimantadina (não comercializado no BR) – Influenza A, B e o H 1 N 1 já são resistentes 53
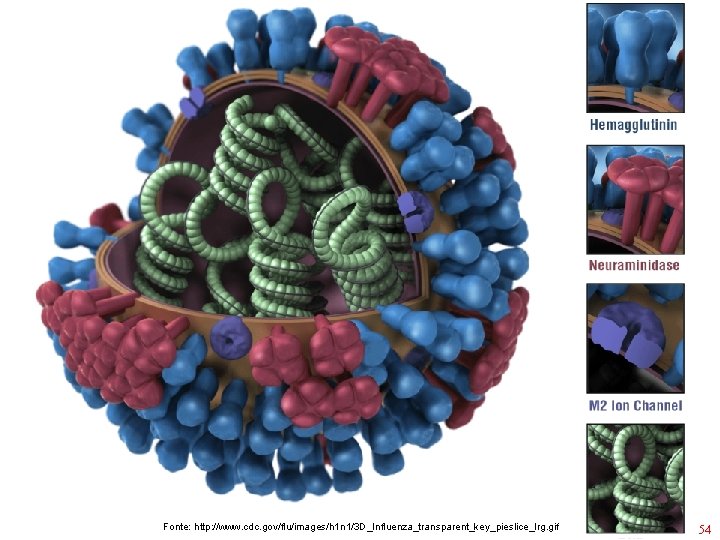
Fonte: http: //www. cdc. gov/flu/images/h 1 n 1/3 D_Influenza_transparent_key_pieslice_lrg. gif 54

Drogas anti-Influenza • Amantadine, Oseltamivir, Rimantadine, Zanamivir Peramivir, • Amantadina: inibe o desnudamento viral • Somente Influenza A • Age especificamente sobre proteina M 2 (Matriz) • Oseltamivir (Tamiflu): Influenza A, B e aviário 55

Drogas anti-Influenza • Oseltamivir (Tamiflu): • Inibidor da neuraminidase • Diminuir a duração dos sintomas em cerca de 24 horas e chance de hospitalização em 30% • Efeito colateral: náusea e vomito 56

Drogas anti-Influenza • Zanamivir (Relenza): • Inibidor da neuraminidase • Inalação oral • Diminuir a duração dos sintomas em cerca de 24 horas 57

Drogas anti-citomegalovírus humano (HCMV) • Ganciclovir (Cymevene)– inibidor de DNApol • Valganciclovir (Valcyte) – pró-droga (convertido em ganciclovir) • Fomivirsen (Vitravene) – inibidor antisense – liga ao m. RNA viral do gene IE 2 • Fosfonoformato ( Foscarnet)- análogo do pirofosfato – retinites por HCMV liga-se ao pirofosfato da DNApol viral. 58

Outros anti-virais • Polímero m-PEG • Age cobrindo as células (receptores) e não permitindo a adsorção viral • Amplo espectro (vírus respiratórios) • Efeito colateral: nulo (segundo os autores) • Kyluik et al. , 2011 59
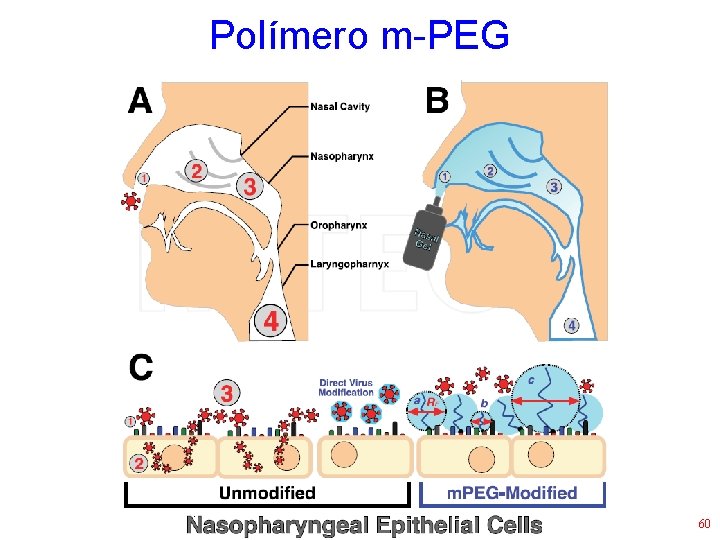
Polímero m-PEG 60
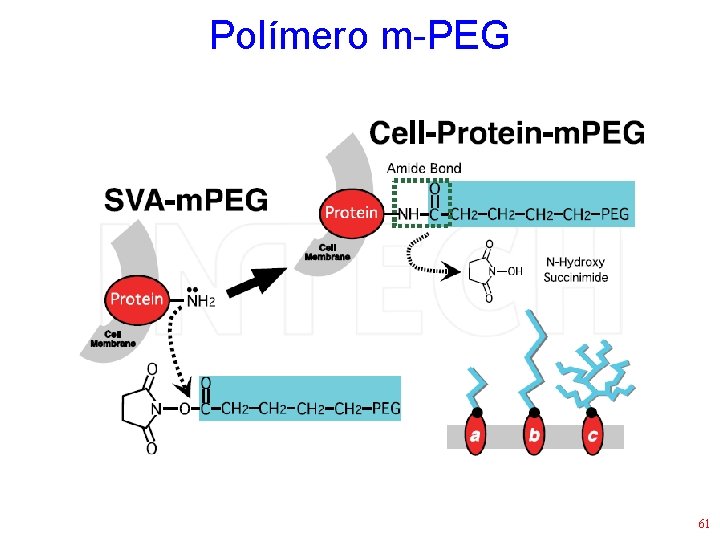
Polímero m-PEG 61
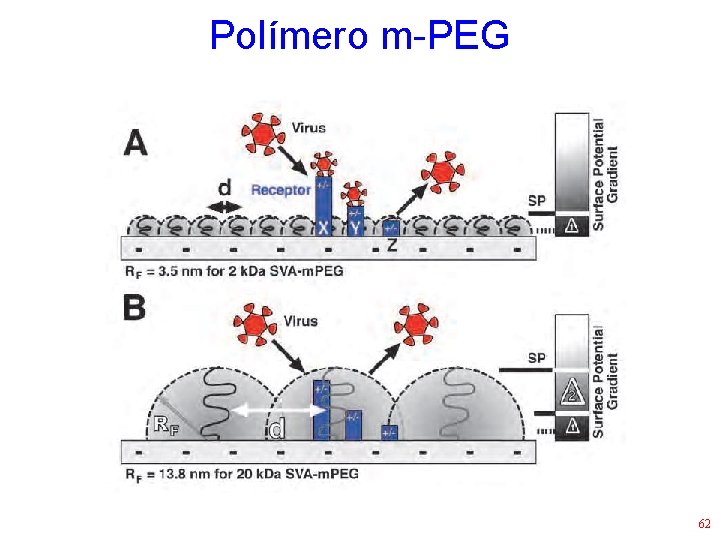
Polímero m-PEG 62

Polímero m-PEG 63

Mascaras antivirais Fonte: http: //www. amazon. com/Curad-Antiviral-Face-Mask-Count/dp/B 009 GGUIK 6 64

Vídeo exemplificando a replicação do HIV 65
Definição Estrutura dos vírus Replicação Viral Antivirais Resistencia viral Mensagem principal Fonte: http: //www. google. com/imghp 66

Por que é tão difícil criar drogas antivirais? • Vírus utilizam a maquinaria celular para a replicação (parasita intracelular) • Se replicam muito rapidamente e aos milhares ou milhões por células • Infectam novas células / hospedeiros • Fazem latência (Herpesvírus) ou promovem infecções persistentes (HIV) 67
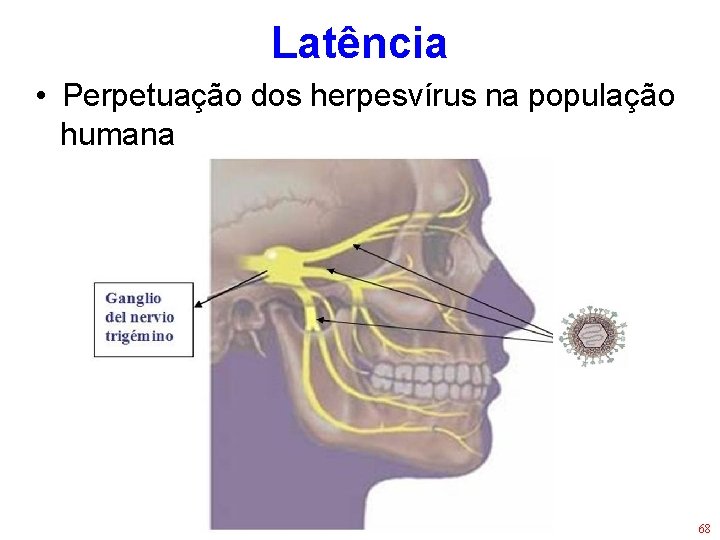
Latência • Perpetuação dos herpesvírus na população humana 68
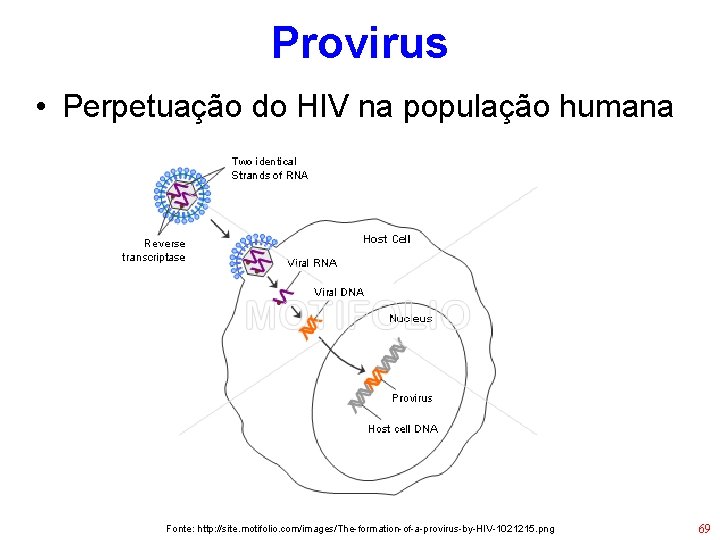
Provirus • Perpetuação do HIV na população humana Fonte: http: //site. motifolio. com/images/The-formation-of-a-provirus-by-HIV-1021215. png 69

Por que é tão difícil criar drogas antivirais? • Possuem mais de um hospedeiro (Influenza) • Possuem reservatórios (vírus da Dengue) • Sofrem mutações (variações antigênicas) • Possuem vários tipos e subtipos 70

Por que é tão difícil criar drogas antivirais? • Falta de conhecimento de detalhes do método de replicação (HPV) • Sem contato prévio (Ebola) • Resistência viral • Não existe um padrão de replicação 71
Definição Estrutura dos vírus Replicação Viral Antivirais Resistencia viral Mensagem principal Fonte: http: //www. google. com/imghp 72

Mensagens principais • Entender os mecanismos da replicação viral é a fonte para a descoberta de novas drogas antivirais 73
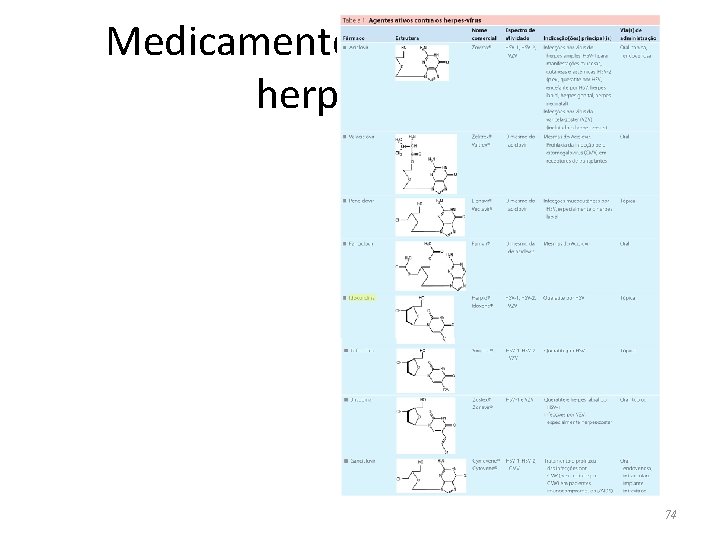
Medicamentos ativos contra herpesvírus 74

Medicamentos ativos contra herpesvírus • • Aciclovir Valaciclovir Penciclovir Fanciclovir Idoxuridina Trifluridina Brivudina Ganciclovir Zovirax Zelitrex, Denavir Famvir Herpesine Viroptic Zostex Cytovene HSV-1 e 2 oral, tópica, IV “ + profilaxia CMV HSV 1 e 2 = aciclovir queratite HSV queratite, VZV CMV trat e prev oral, IV, introcular, Implante intravítreo • • • oral tópica oral, tóp Valganciclovir Foscarnet Valcyte Foscavir CMV trat e prev Retinite CMV na AIDS; Cidofovir Vistide Retinite CMV; Herpes genital Molusco, Adenovírus, poliomavírus • Fomivirseno Vitravene HSV mucocutânea e VZV resist. ao ACV na AIDS IV Retinite CMV na AIDS 75

Antivirais para influenza • • • Amantadina Rimantadina Zanamivir Oseltamivir Ribavirina 76

Antivirais HBV • • • IFN alfa peguilado Lamivudina Adefovir dipivoxil Entricitabina/FTC Entecavir 77

78

Antivirais para picornavírus • Pleconaril entero e rinovírus INasal 79

80

• Existem cerca de 1016 genomas de HIV no planeta atualmente • Com este número de genomas, é altamente provável que os genomas de HIV existentes são resistentes a qualquer uma das drogas antivirais atuais e futuras! 81

Sugestões de leitura Fonte: http: //www. google. com/imghp 82

Sugestões de leitura • Livros: – Kyluik, D. L. , Sutton, T. C. , Le, Y. , Scott, M. D. Polymer-Mediated Broad Spectrum Antiviral Prophylaxis: Utility in High Risk Environments, Progress in Molecular and Environmental Bioengineering - From Analysis and Modeling to Technology Applications, Angelo Carpi (Ed. ), ISBN: 978 -953 -307 -268 -5, In. Tech. 2011. – Principles of Virology. Flint, S. J. ; Enquist, L. W. ; Racaniello, V. R. 3 rd ed. ASM Press, 2009. – S. N J Korsman, G. Van Zyl, L. Nutt, M. I. Andersson, W. Preiser. Virologia Churchill Livingstone/Elsevier. 2014. • Artigos: – He, H. 2013. Vaccines and Antiviral Agents. Current Issues in Molecular Virology - Viral Genetics and Biotechnological Applications (http: //dx. doi. org/10. 5772/56866) • Blog / site: – Virology blog (http: //www. virology. ws/). – Slide Share (http: //pt. slideshare. net/drdhriti/antiviral-drugs-drdhriti) 83

Grato pela atenção!!! camposvet@gmail. com 84
- Slides: 84