Vodk VY32 INOVACECHE118 AUTOR Ing Ladislava Semerdov ANOTACE













- Slides: 14

Vodík VY-32 -INOVACE-CHE-118 AUTOR: Ing. Ladislava Semerádová ANOTACE: Výukový materiál je určen pro studenty 1. ročníku SŠ. Může být použit při výkladu vlastností vodíku. KLÍČOVÁ SLOVA: výskyt vodíku, fyzikální vlastnosti vodíku, příprava, výroba a použití vodíku

Vodík

Vodík ve vesmíru a na Zemi • O vzniku vesmíru nevíme nic s jistotu • teorie velkého třesku – došlo k němu před 10 – 18 miliardami let • Prajádro vesmíru – látka o neuvěřitelně velké hustotě se postupně rozpadla na elementární částice ( protony, elektrony, neutrony) • Z nich vznikla jádra nejlehčích prvků - vodíku a helia

• Dalšími termojadernými reakcemi vznikala jádra těžších prvků • 4 He + 4 He = 8 Be • Vznik chemických prvků není ukončen

Reakce probíhající ve Slunci Každou sekundu se přemění : 600 000 tun vodíku na He a záření, kterým Slunce zásobuje i naši Zemi • Podobných hvězd jako Slunce je ve vesmíru bezpočet

Zastoupení prvků ve vesmíru • 91% vodík • 9% helium • 0, 06 % kyslík

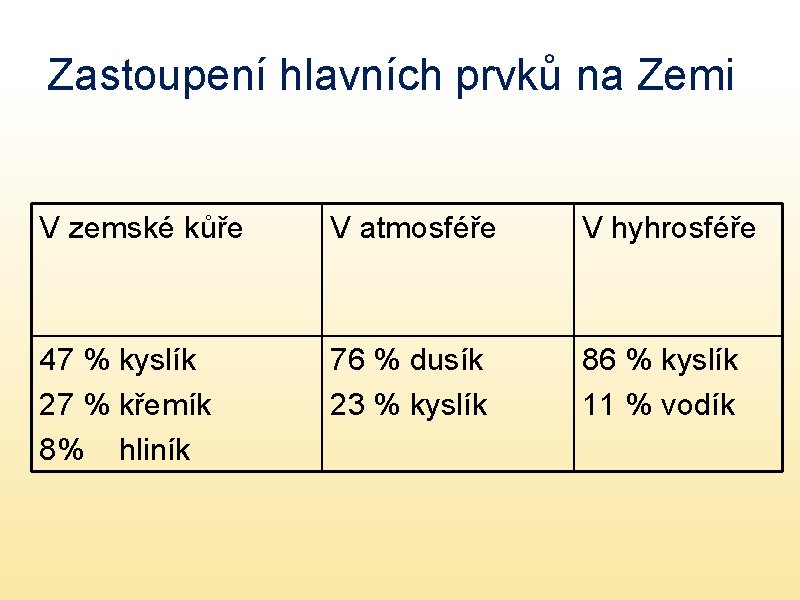
Zastoupení hlavních prvků na Zemi V zemské kůře V atmosféře V hyhrosféře 47 % kyslík 27 % křemík 8% hliník 76 % dusík 23 % kyslík 86 % kyslík 11 % vodík

Vodík – vlastnosti, výroba, použití

Fyzikální vlastnosti • Nejlehčí plyn, hořlavý, hoří namodralým plamenem, ale hoření nepodporuje • Nelze jej detekovat zrakem, čichem ani podle chuti • Vzduch s obsahem 6 % objemu se stává třaskavou směsí • Reakce s kyslíkem je silně exotermická • Vodík je 4 x výhřevnější než hnědé uhlí

Vodík jako nosné médium vzducholodí • Zeppelin LZ-129 Hindenburg • 1937

Příprava a výroba vodíku • Laboratorní příprava: • Reakce kyselin s kovy • Zn (s) + 2 HCl(aq) H 2(g) + Zn. Cl 2 • Průmyslová výroba • CH 4(g) + H 2 O(g) Ni, 900 OC 3 H 2(g) + CO (g) • katalyzovaná reakce methanu s vodní párou

Hlavní použití vodíku • 80% vyrobeného vodíku se používá na výrobu amoniaku: 3 H 2(g) + N 2(g) 2 NH 3(g) • hydrogenace tuků – přeměna rostlinných olejů na tuhé jedlé tuky (Rama) • využívá se jako redukční činidlo při výrobě celé řady látek

Sloučeniny vodíku • Tvoři nejvíce sloučenin ze všech prvků jednak anororganické (hydridy, kyseliny, hydroxidy), ale hlavně velké množství organických sloučenin Hydridy • Binární sloučeniny vodíku, ve kterých je oxidační číslo vodíku –I • Mg. H-I 2

POUŽITÉ ZDROJE: DUŠEK, Bohuslav a Vratislav FLEMR. Obecná a anorganická chemie pro gymnázia. SPN, 2007. ISBN 80 -7235 -369 -1. Klouda P. Obecná a anorganická chemie. třetí. Ostrava: Pavel Klouda, Ostrava, 2004. ISBN 8086369 -10 -2. www. glassschool. cz