Voda alkoholy ethery voda methanol monoalkyl derivt vody




- Slides: 48

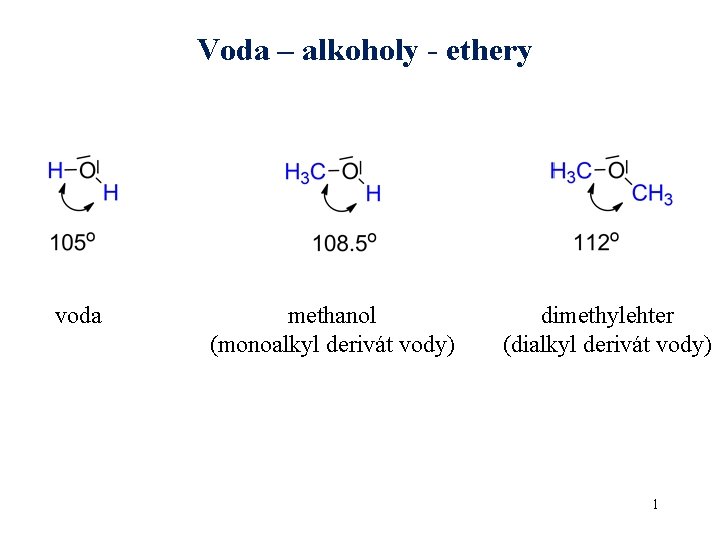
Voda – alkoholy - ethery voda methanol (monoalkyl derivát vody) dimethylehter (dialkyl derivát vody) 1

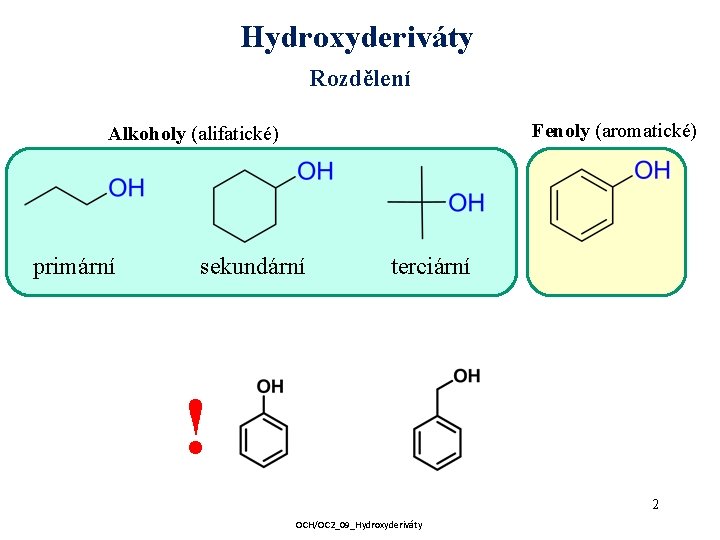
Hydroxyderiváty Rozdělení Fenoly (aromatické) Alkoholy (alifatické) primární sekundární terciární ! 2 OCH/OC 2_09_Hydroxyderiváty

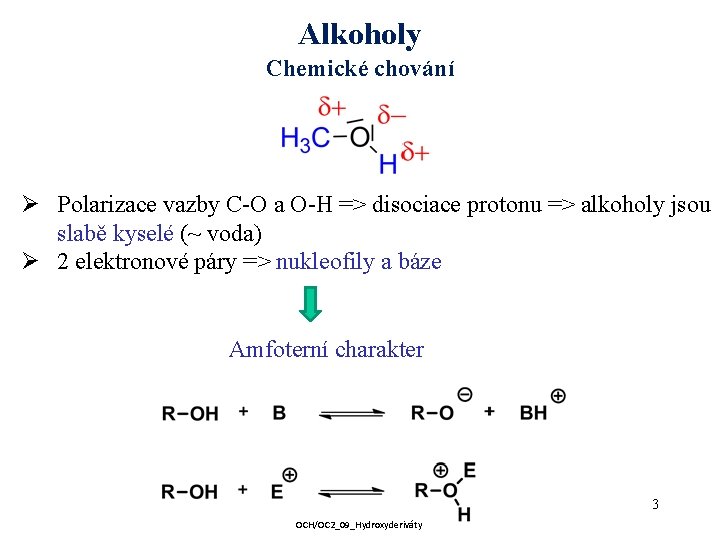
Alkoholy Chemické chování Ø Polarizace vazby C-O a O-H => disociace protonu => alkoholy jsou slabě kyselé (~ voda) Ø 2 elektronové páry => nukleofily a báze Amfoterní charakter 3 OCH/OC 2_09_Hydroxyderiváty

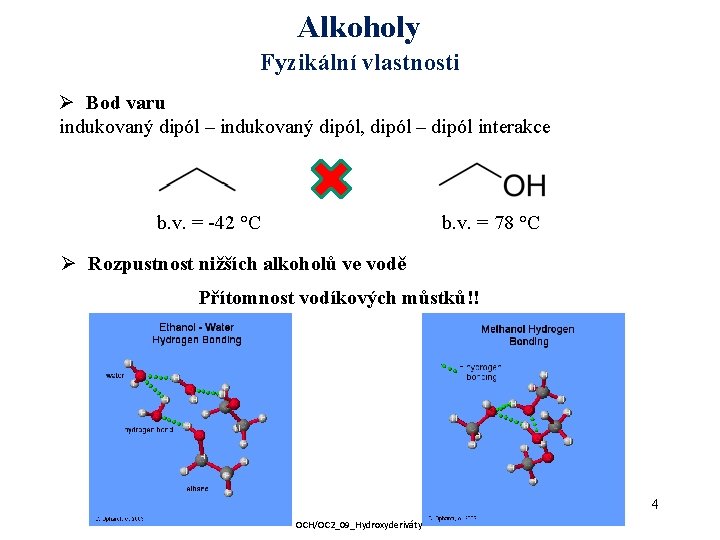
Alkoholy Fyzikální vlastnosti Ø Bod varu indukovaný dipól – indukovaný dipól, dipól – dipól interakce b. v. = -42 °C b. v. = 78 °C Ø Rozpustnost nižších alkoholů ve vodě Přítomnost vodíkových můstků!! 4 OCH/OC 2_09_Hydroxyderiváty

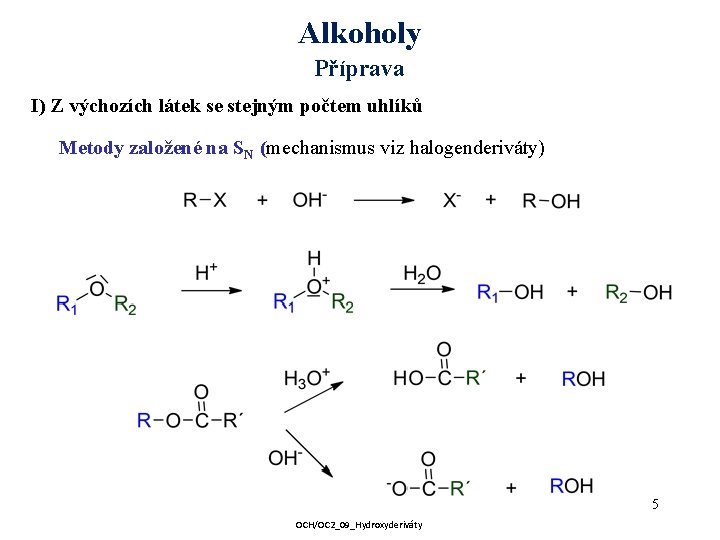
Alkoholy Příprava I) Z výchozích látek se stejným počtem uhlíků Metody založené na SN (mechanismus viz halogenderiváty) 5 OCH/OC 2_09_Hydroxyderiváty

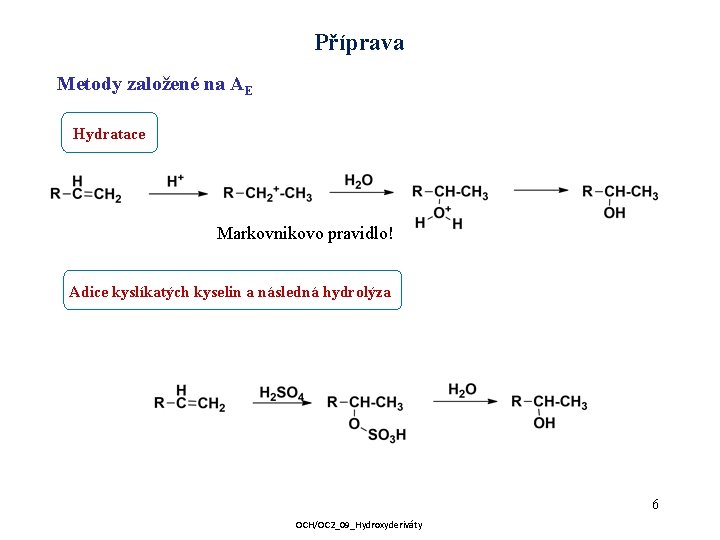
Příprava Metody založené na AE Hydratace Markovnikovo pravidlo! Adice kyslíkatých kyselin a následná hydrolýza 6 OCH/OC 2_09_Hydroxyderiváty

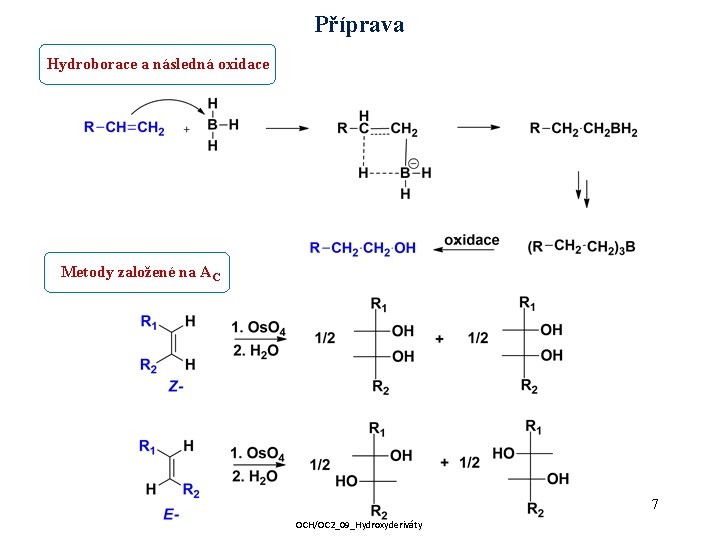
Příprava Hydroborace a následná oxidace Metody založené na AC 7 OCH/OC 2_09_Hydroxyderiváty

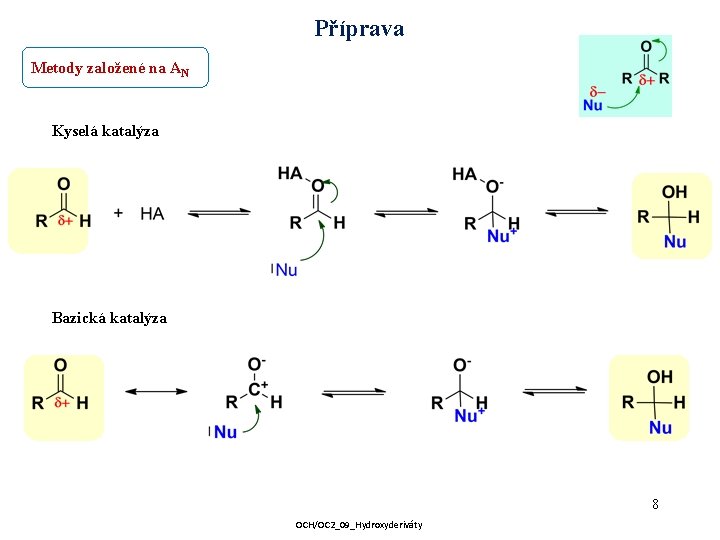
Příprava Metody založené na AN Kyselá katalýza Bazická katalýza 8 OCH/OC 2_09_Hydroxyderiváty

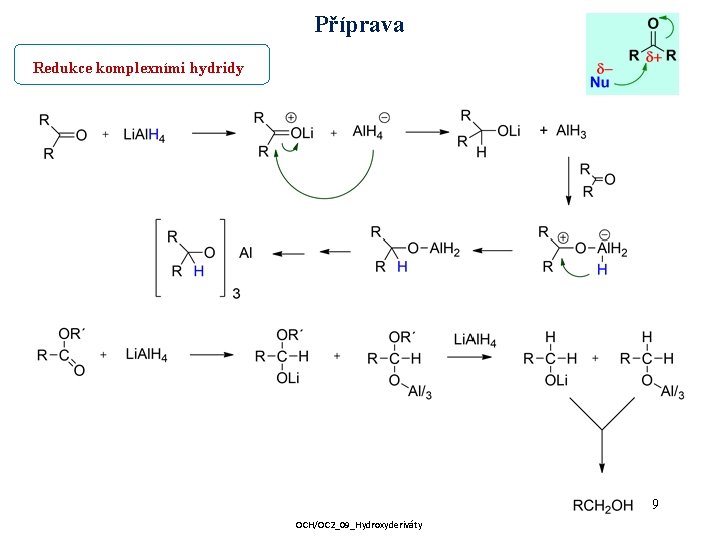
Příprava Redukce komplexními hydridy 9 OCH/OC 2_09_Hydroxyderiváty

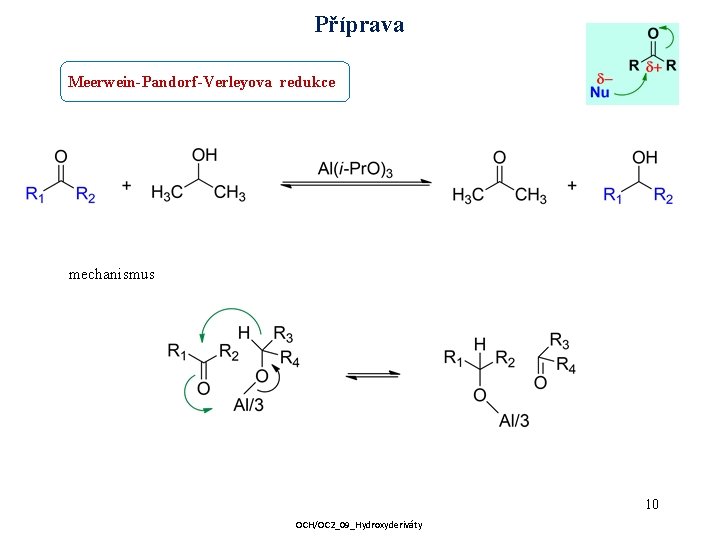
Příprava Meerwein-Pandorf-Verleyova redukce mechanismus 10 OCH/OC 2_09_Hydroxyderiváty

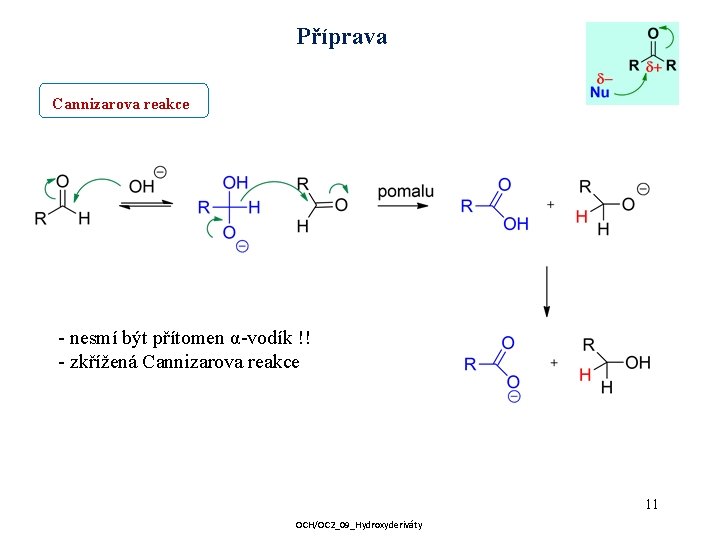
Příprava Cannizarova reakce - nesmí být přítomen α-vodík !! - zkřížená Cannizarova reakce 11 OCH/OC 2_09_Hydroxyderiváty

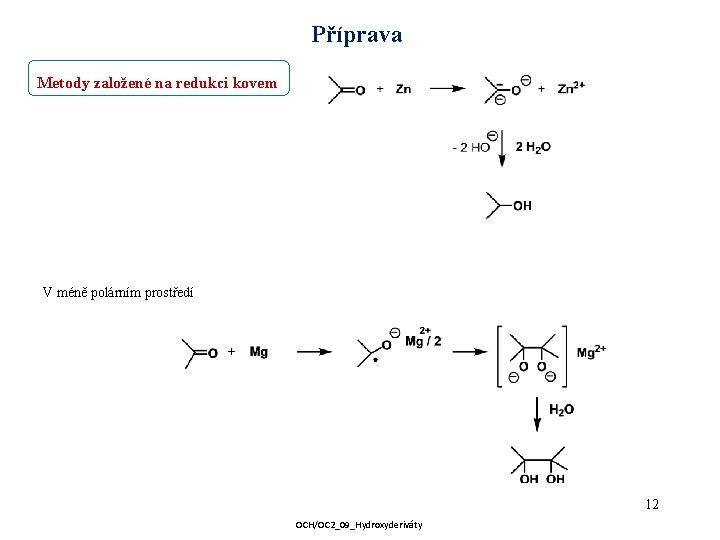
Příprava Metody založené na redukci kovem V méně polárním prostředí 12 OCH/OC 2_09_Hydroxyderiváty

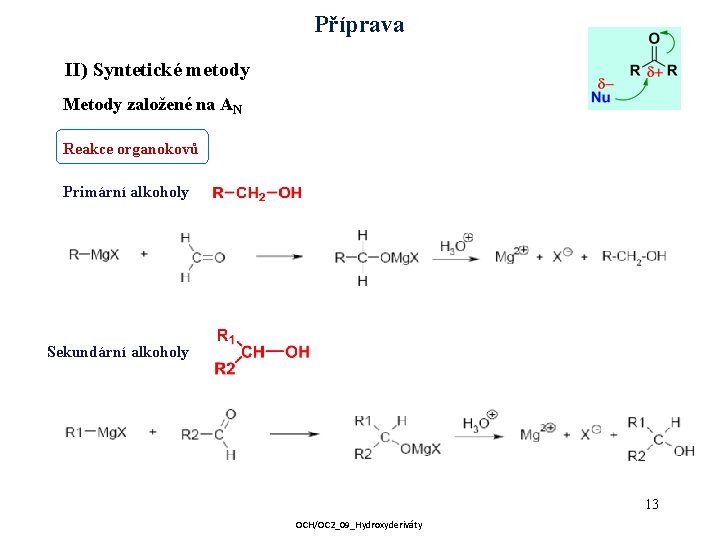
Příprava II) Syntetické metody Metody založené na AN Reakce organokovů Primární alkoholy Sekundární alkoholy 13 OCH/OC 2_09_Hydroxyderiváty

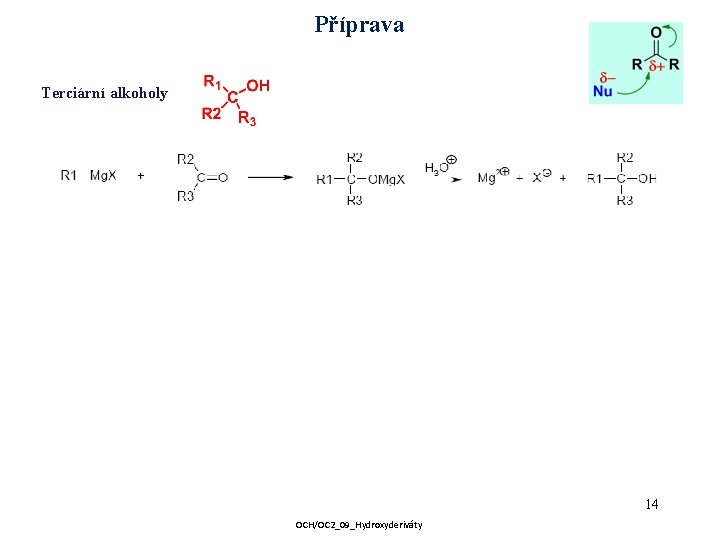
Příprava Terciární alkoholy 14 OCH/OC 2_09_Hydroxyderiváty

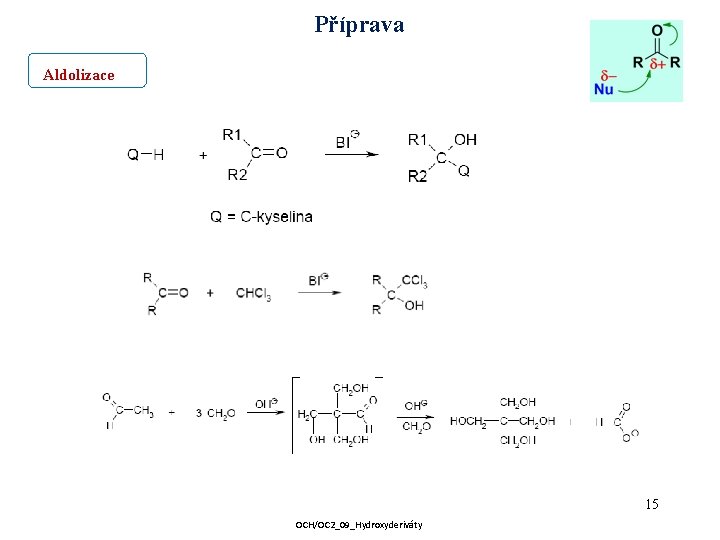
Příprava Aldolizace 15 OCH/OC 2_09_Hydroxyderiváty

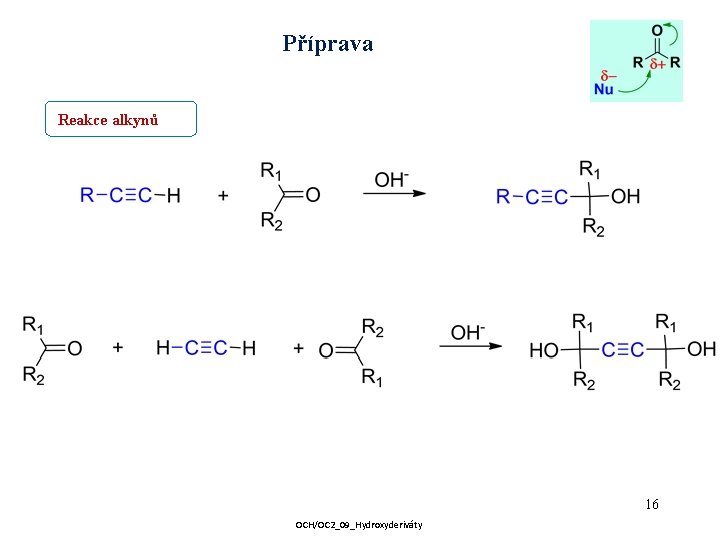
Příprava Reakce alkynů 16 OCH/OC 2_09_Hydroxyderiváty

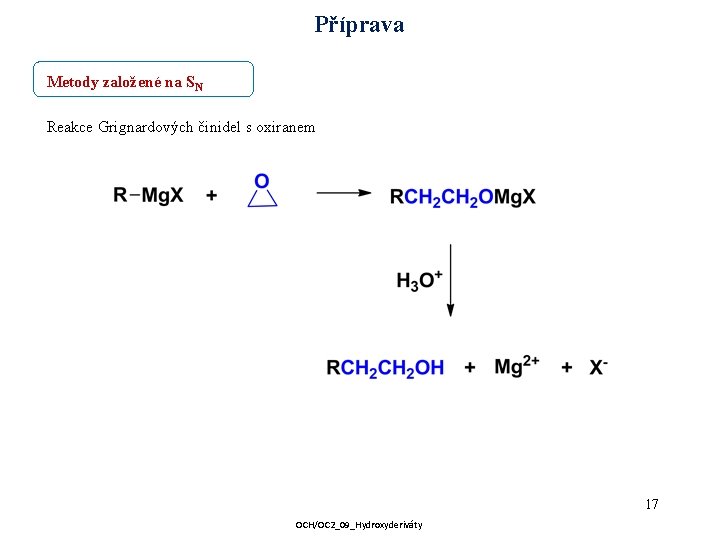
Příprava Metody založené na SN Reakce Grignardových činidel s oxiranem 17 OCH/OC 2_09_Hydroxyderiváty

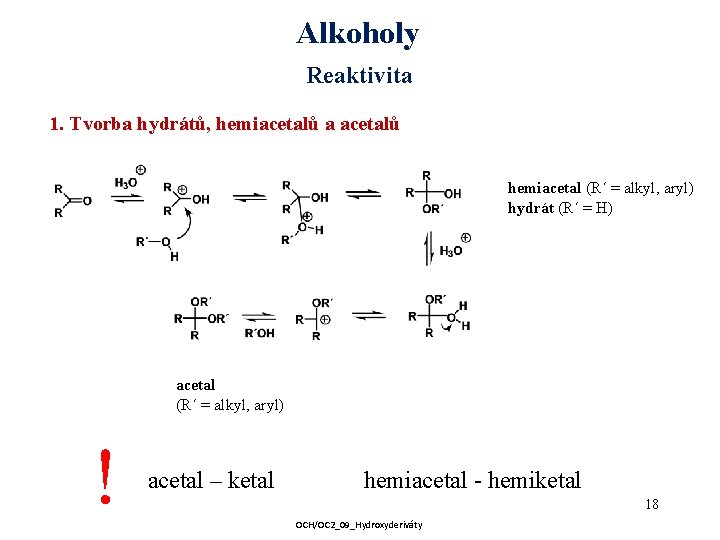
Alkoholy Reaktivita 1. Tvorba hydrátů, hemiacetalů a acetalů hemiacetal (R´ = alkyl, aryl) hydrát (R´ = H) acetal (R´ = alkyl, aryl) ! acetal – ketal hemiacetal - hemiketal 18 OCH/OC 2_09_Hydroxyderiváty

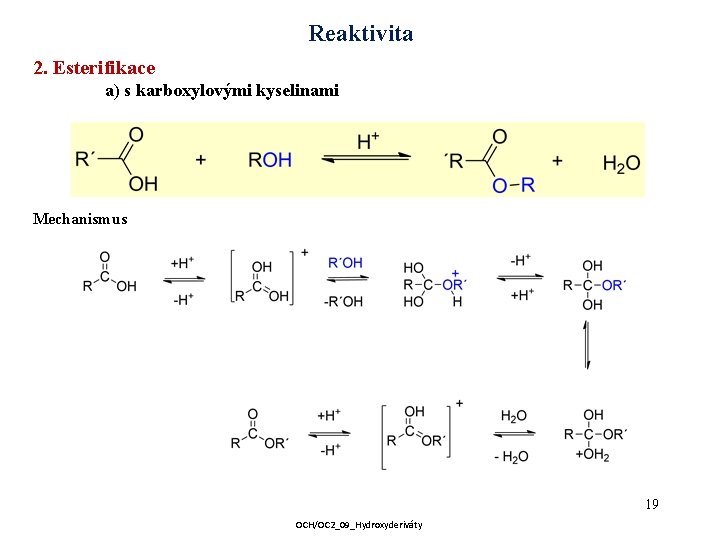
Reaktivita 2. Esterifikace a) s karboxylovými kyselinami Mechanismus 19 OCH/OC 2_09_Hydroxyderiváty

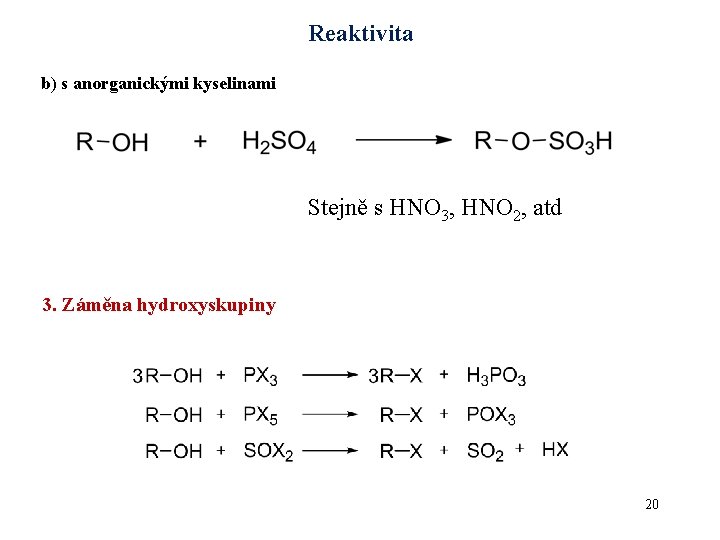
Reaktivita b) s anorganickými kyselinami Stejně s HNO 3, HNO 2, atd 3. Záměna hydroxyskupiny 20

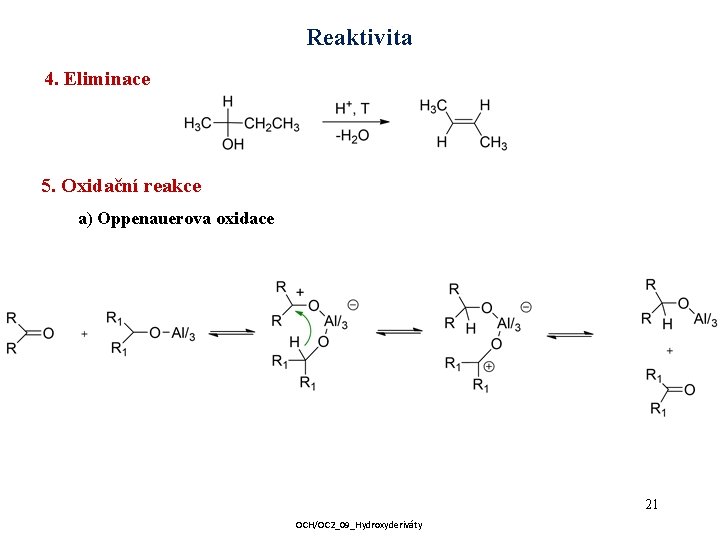
Reaktivita 4. Eliminace 5. Oxidační reakce a) Oppenauerova oxidace 21 OCH/OC 2_09_Hydroxyderiváty

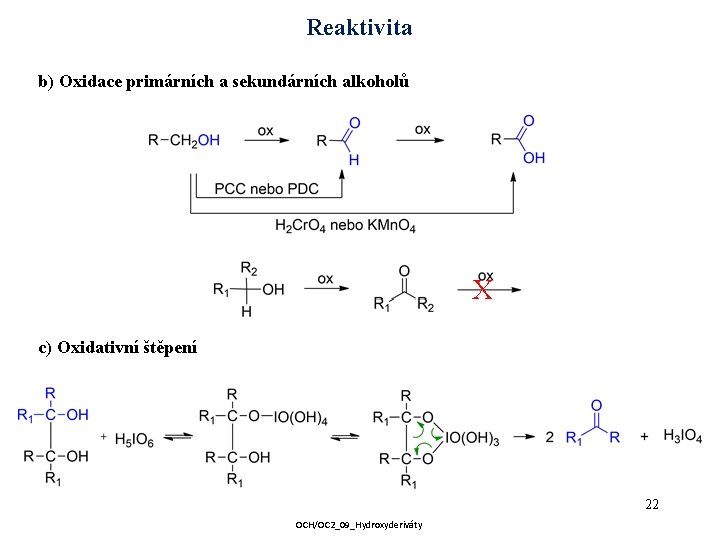
Reaktivita b) Oxidace primárních a sekundárních alkoholů X c) Oxidativní štěpení 22 OCH/OC 2_09_Hydroxyderiváty

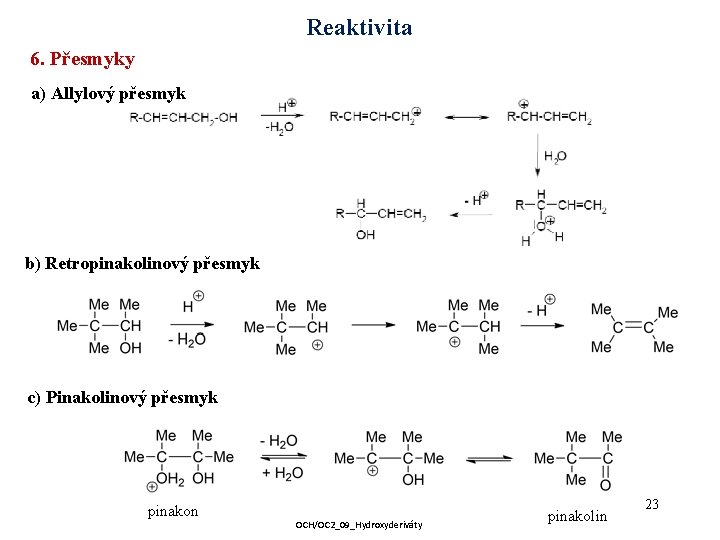
Reaktivita 6. Přesmyky a) Allylový přesmyk b) Retropinakolinový přesmyk c) Pinakolinový přesmyk pinakon OCH/OC 2_09_Hydroxyderiváty pinakolin 23

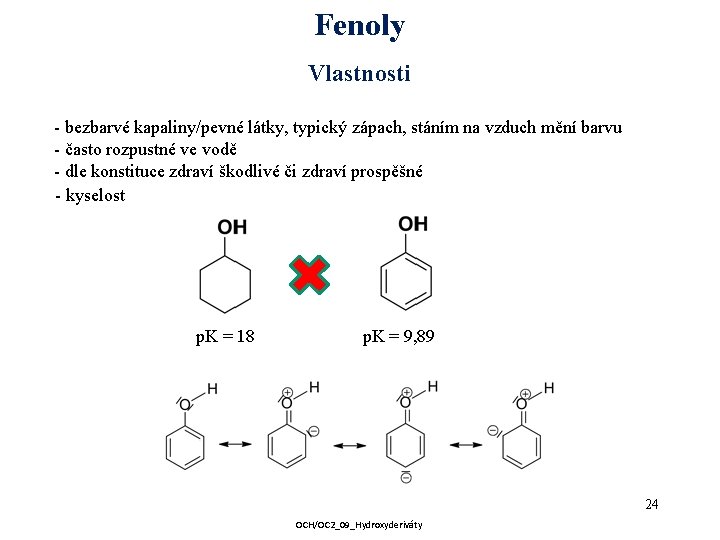
Fenoly Vlastnosti - bezbarvé kapaliny/pevné látky, typický zápach, stáním na vzduch mění barvu - často rozpustné ve vodě - dle konstituce zdraví škodlivé či zdraví prospěšné - kyselost p. K = 18 p. K = 9, 89 24 OCH/OC 2_09_Hydroxyderiváty

Vlastnosti - skupiny s –M, -I efektem zvyšují kyselost - skupiny s +M, +I efektem snižují kyselost Využití: - umělá vlákna, pryskyřice - desinfekce, ochrana dřeva - léčiva OCH/OC 2_09_Hydroxyderiváty 25

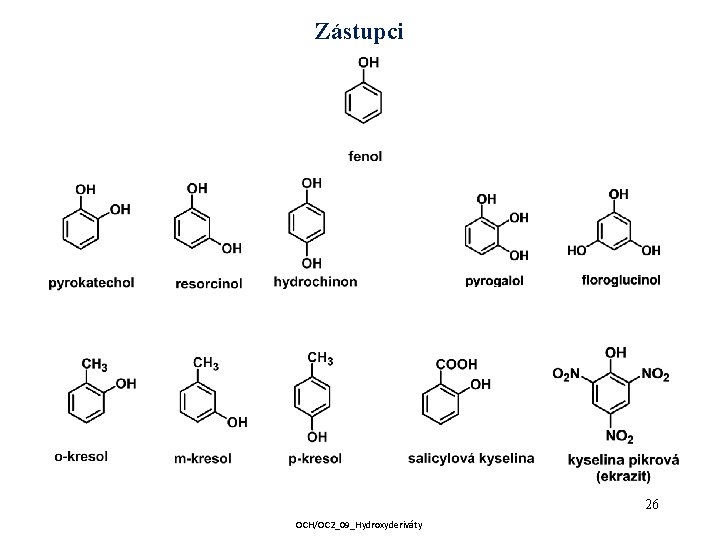
Zástupci 26 OCH/OC 2_09_Hydroxyderiváty

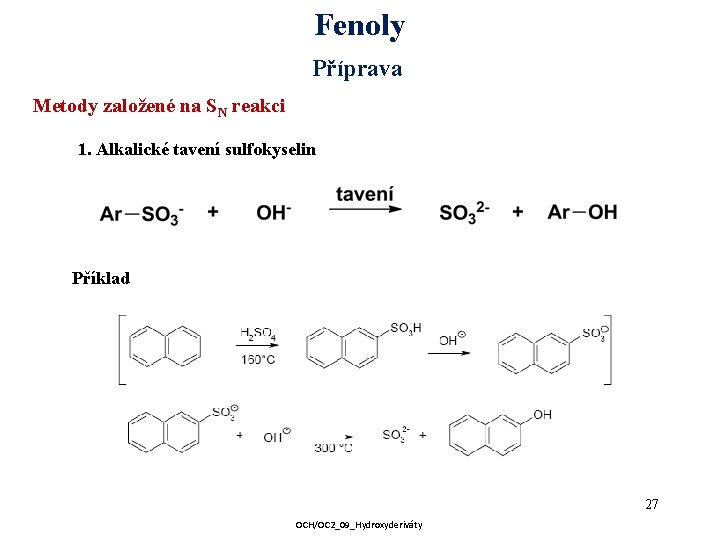
Fenoly Příprava Metody založené na SN reakci 1. Alkalické tavení sulfokyselin Příklad 27 OCH/OC 2_09_Hydroxyderiváty

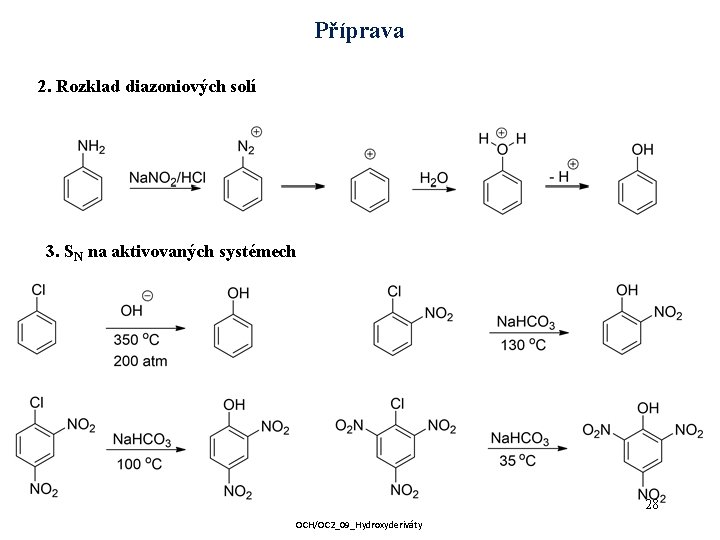
Příprava 2. Rozklad diazoniových solí 3. SN na aktivovaných systémech 28 OCH/OC 2_09_Hydroxyderiváty

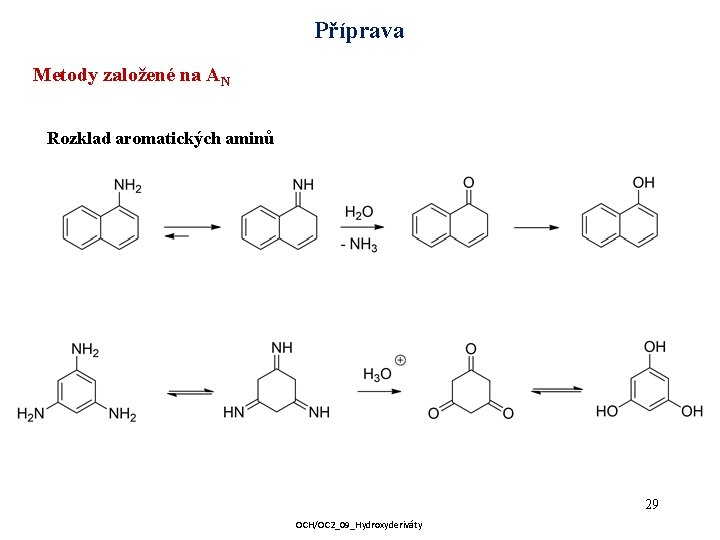
Příprava Metody založené na AN Rozklad aromatických aminů 29 OCH/OC 2_09_Hydroxyderiváty

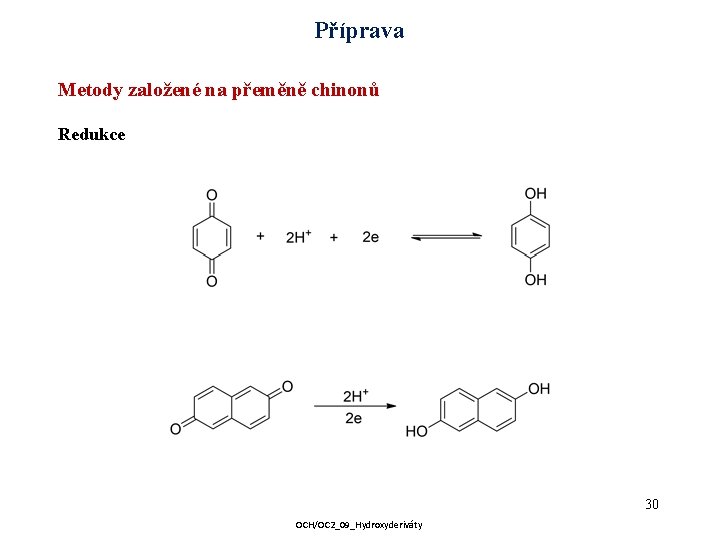
Příprava Metody založené na přeměně chinonů Redukce 30 OCH/OC 2_09_Hydroxyderiváty

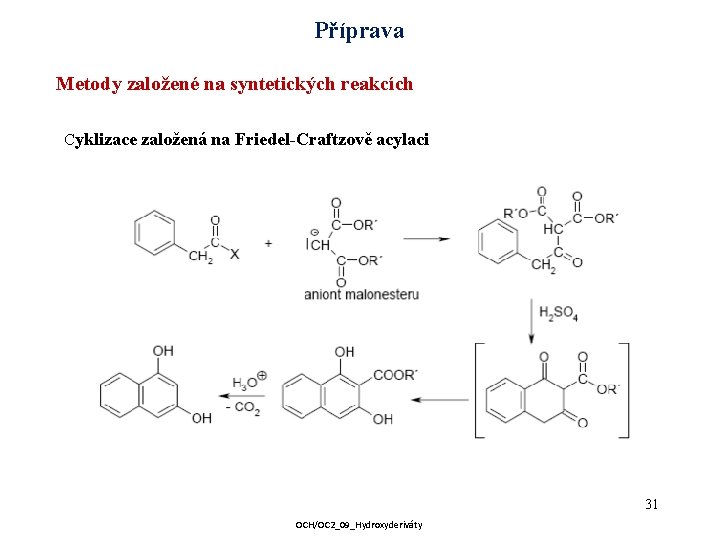
Příprava Metody založené na syntetických reakcích Cyklizace založená na Friedel-Craftzově acylaci 31 OCH/OC 2_09_Hydroxyderiváty

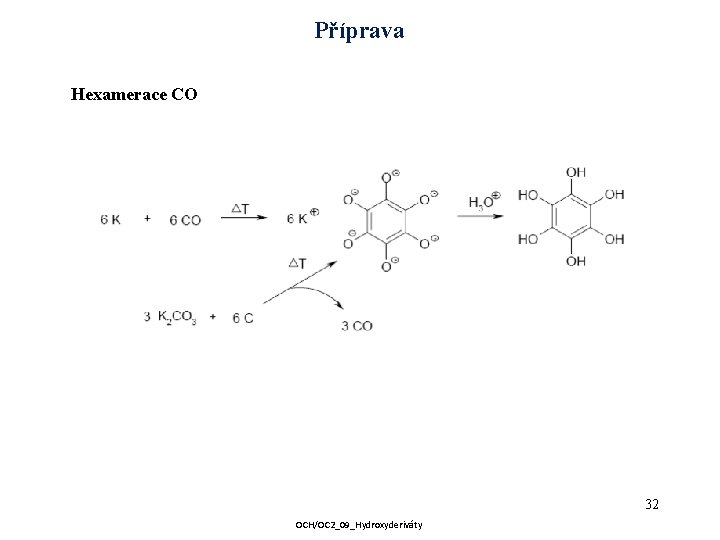
Příprava Hexamerace CO 32 OCH/OC 2_09_Hydroxyderiváty

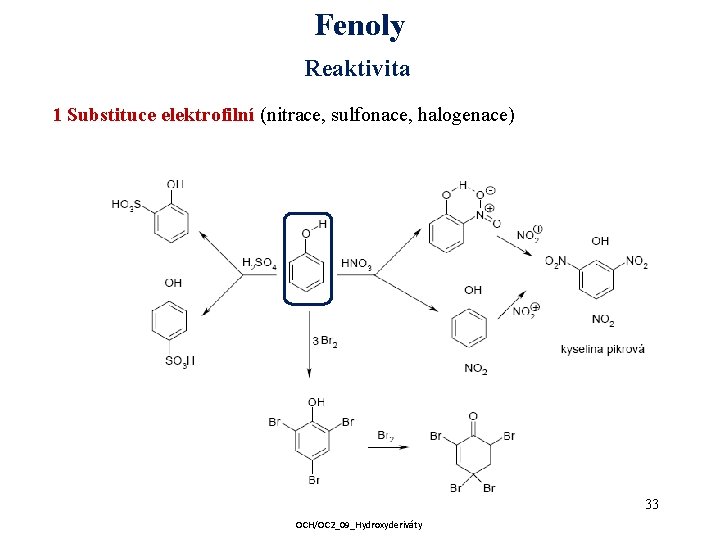
Fenoly Reaktivita 1 Substituce elektrofilní (nitrace, sulfonace, halogenace) 33 OCH/OC 2_09_Hydroxyderiváty

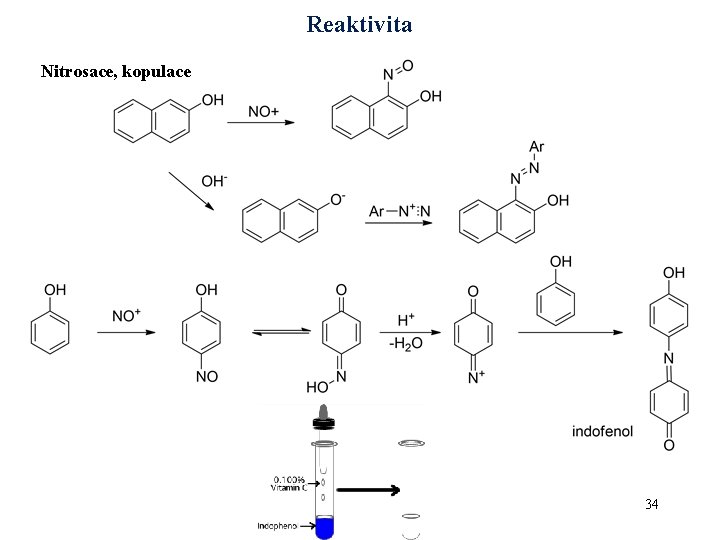
Reaktivita Nitrosace, kopulace 34 OCH/OC 2_09_Hydroxyderiváty

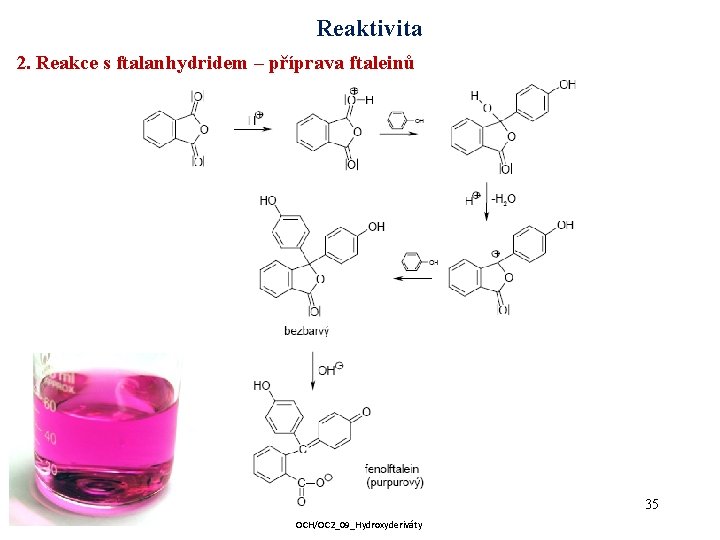
Reaktivita 2. Reakce s ftalanhydridem – příprava ftaleinů 35 OCH/OC 2_09_Hydroxyderiváty

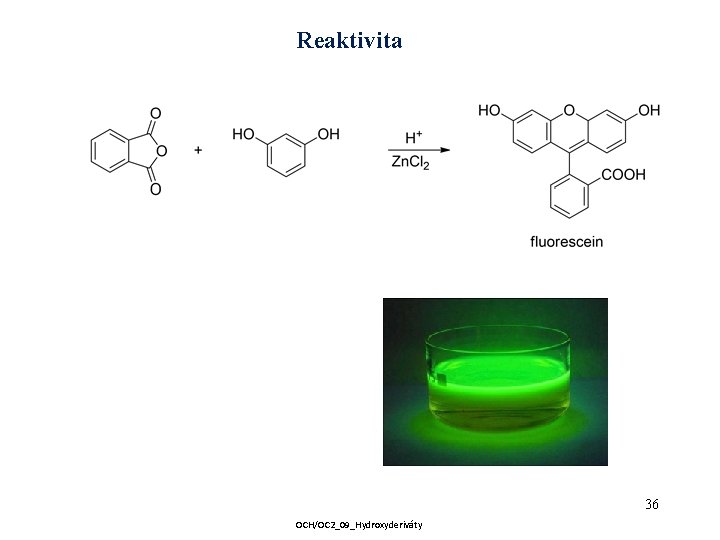
Reaktivita 36 OCH/OC 2_09_Hydroxyderiváty

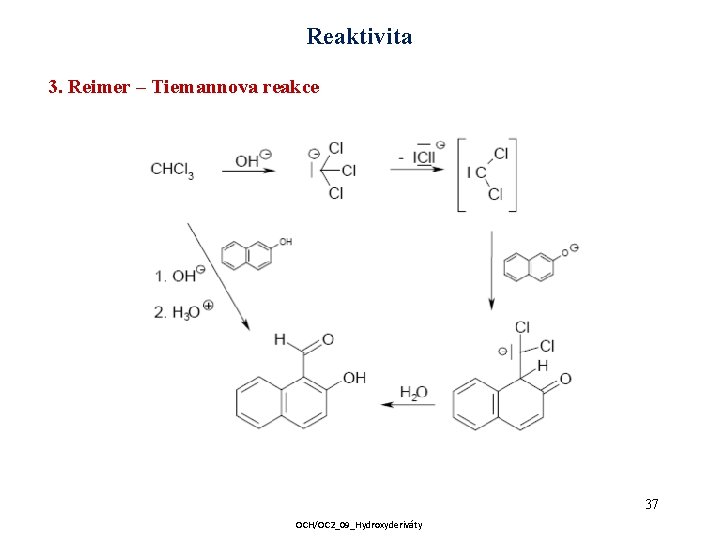
Reaktivita 3. Reimer – Tiemannova reakce 37 OCH/OC 2_09_Hydroxyderiváty

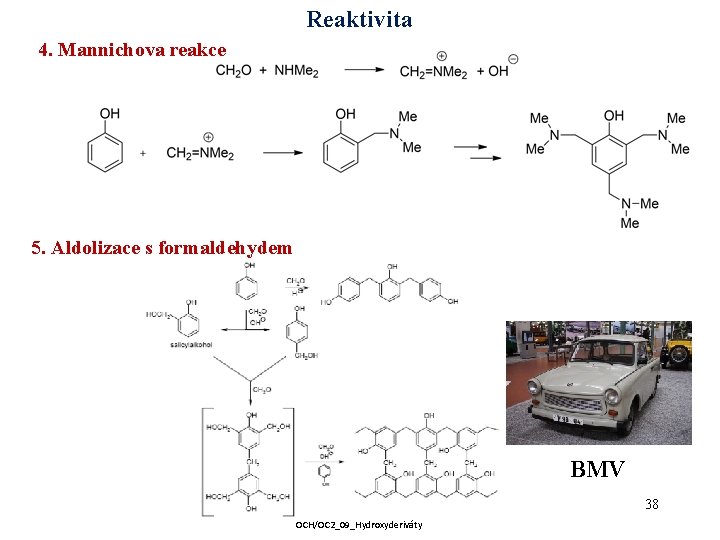
Reaktivita 4. Mannichova reakce 5. Aldolizace s formaldehydem BMV 38 OCH/OC 2_09_Hydroxyderiváty

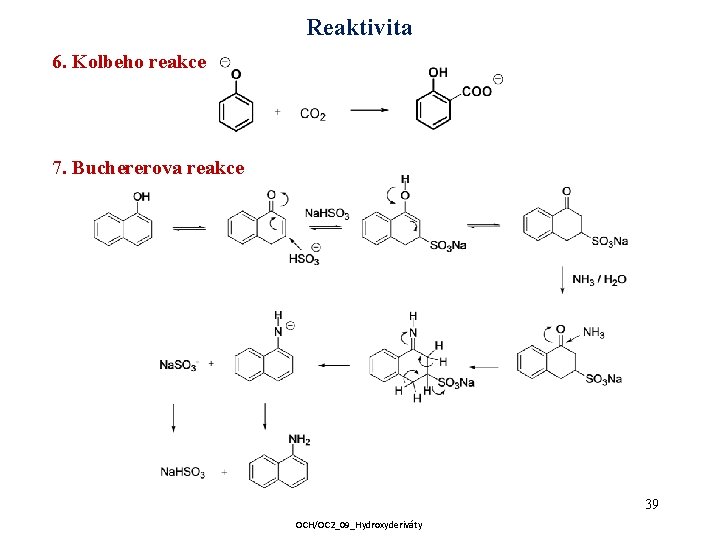
Reaktivita 6. Kolbeho reakce 7. Buchererova reakce 39 OCH/OC 2_09_Hydroxyderiváty

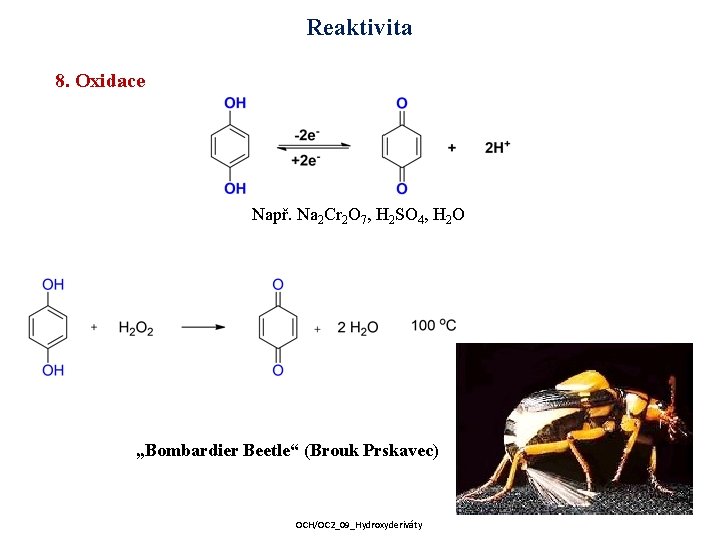
Reaktivita 8. Oxidace Např. Na 2 Cr 2 O 7, H 2 SO 4, H 2 O „Bombardier Beetle“ (Brouk Prskavec) 40 OCH/OC 2_09_Hydroxyderiváty

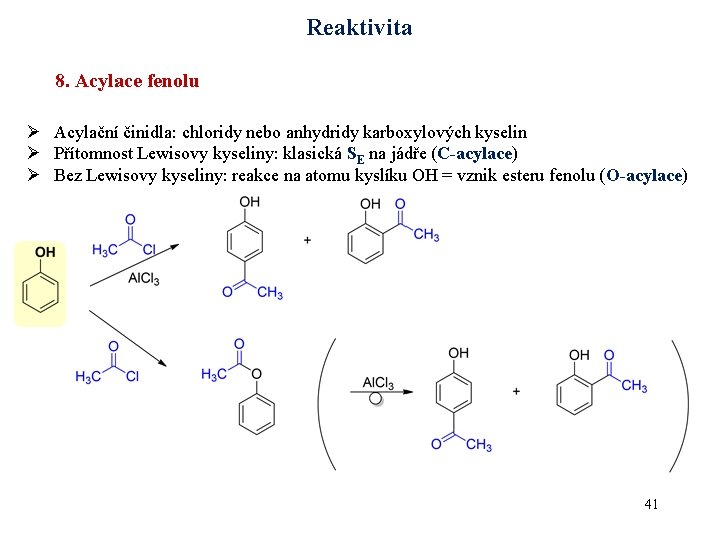
Reaktivita 8. Acylace fenolu Ø Acylační činidla: chloridy nebo anhydridy karboxylových kyselin Ø Přítomnost Lewisovy kyseliny: klasická SE na jádře (C-acylace) Ø Bez Lewisovy kyseliny: reakce na atomu kyslíku OH = vznik esteru fenolu (O-acylace) 41

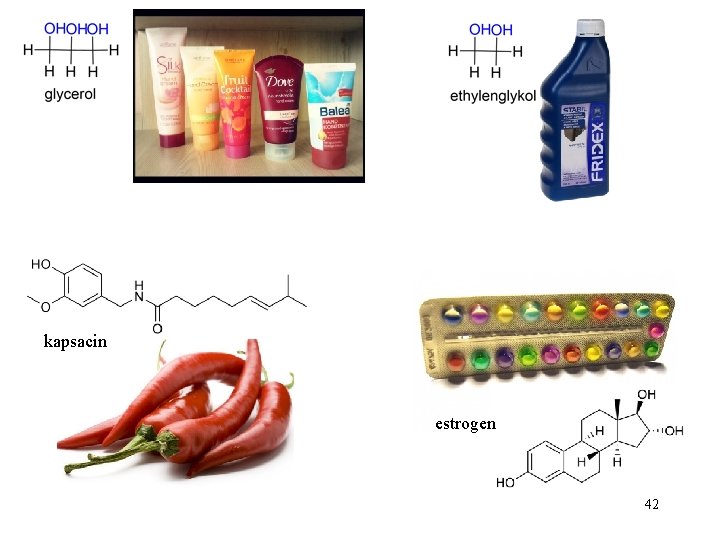
kapsacin estrogen 42

Procvičování 1. Seřaďte uvedené hydroxysloučeniny podle vzrůstající kyselosti: propanol, p-nitrofenol, p-aminofenol, methanol, fenol 2. Napište libovolnou reakci alkoholu, ve které se alkohol chová: a. jako báze b. jako kyselina 3. Napište libovolnou konkrétní reakci, při které dochází v kyselém prostředí ke vzniku alkoholu. 4. Napište průběh reakce, ke které bude docházet, když směs formaldehydu a benzaldehydu podrobíte působení hydroxidu. 5. Navrhněte přípravu: a. 2 -propanolu z libovolného esteru karboxylové kyseliny b. 3, 6 -dimethyl-oktan-3, 6 -diolu z ethynu c. m-nitrofenolu z benzenu d. 4 -hydroxybenzaldehyd z fenolu 43

Procvičování 6. Jaký produkt budete očekávat při reakci: a. 2 -methyl-oxiranu s methylmagnesium bromidem a následným rozkladem vzniklého produktu vodou b. 2 -butanonu s bezvodým ethanolem za kyselé katalýzy c. 1 -naftolu s 4 -methoxybenzendiazonium chloridem d. 3, 3 -diethyl-pentan-2 -olu v kyselém prostředí 7. Napište produkty hydroborace: a. 2 -methyl-cyklopentenu b. methylen-cyklopentanu 8. Napište produkt kysele katalyzované dehydratační reakce následujících derivátů: 44

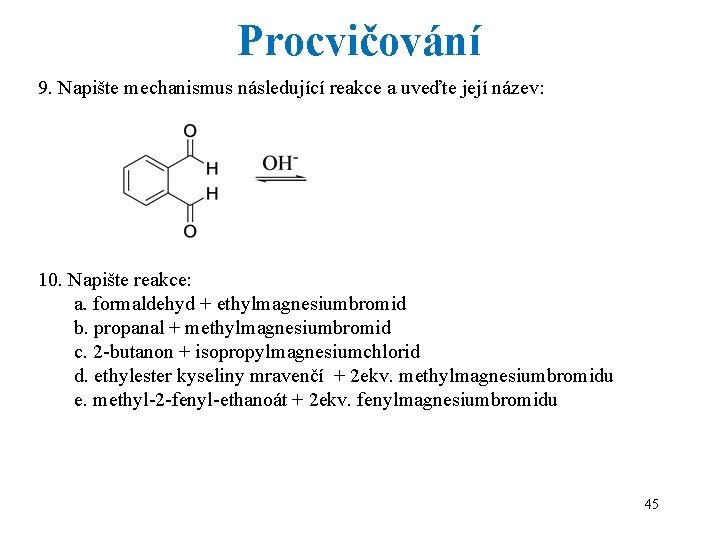
Procvičování 9. Napište mechanismus následující reakce a uveďte její název: 10. Napište reakce: a. formaldehyd + ethylmagnesiumbromid b. propanal + methylmagnesiumbromid c. 2 -butanon + isopropylmagnesiumchlorid d. ethylester kyseliny mravenčí + 2 ekv. methylmagnesiumbromidu e. methyl-2 -fenyl-ethanoát + 2 ekv. fenylmagnesiumbromidu 45

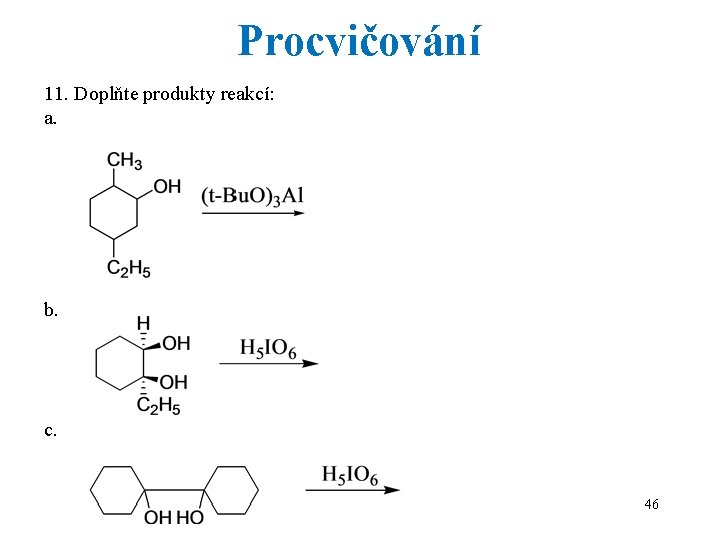
Procvičování 11. Doplňte produkty reakcí: a. b. c. 46

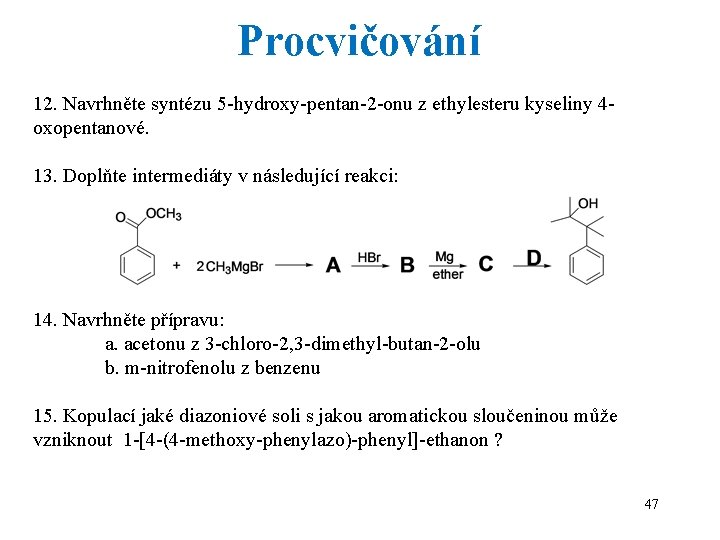
Procvičování 12. Navrhněte syntézu 5 -hydroxy-pentan-2 -onu z ethylesteru kyseliny 4 oxopentanové. 13. Doplňte intermediáty v následující reakci: 14. Navrhněte přípravu: a. acetonu z 3 -chloro-2, 3 -dimethyl-butan-2 -olu b. m-nitrofenolu z benzenu 15. Kopulací jaké diazoniové soli s jakou aromatickou sloučeninou může vzniknout 1 -[4 -(4 -methoxy-phenylazo)-phenyl]-ethanon ? 47

Procvičování 16. Jakou reakcí připravíte z 2 -brombutanu 1 -buten ? 17. Která z uvedených sloučenin nemůže být opticky aktivní ? 2 -brombutan, 2 -brompropan, 2, 3 -dihydroxypropan, methoxyethan 18. Jednostupňovou reakcí připravte z benzaldehydu opticky aktivní sloučeninu. 19. Jaké produkty vzniknou oxidací Z-(1 -bromo-2 -chloro-propenyl)-benzenu manganistanem draselným? Nakreslete jejich prostorové vzorce a vyberte správná tvrzení: a. vzniká pouze jeden derivát, který je opticky aktivní b. vzniká pouze jeden derivát, který není opticky aktivní c. vznikají dva deriváty, přičemž jednoho je výrazně víc d. vznikají dva deriváty ve stejném poměru e. vznikají tři deriváty ve stejném poměru f. vznikají dva enantiomery g. vznikají dva diastereoisomery h. vznikají dva diastereoisomery, které nejsou opticky aktivní 48 i. vznikají tři diastereoisomery