VKUUMTECHNIKA GYAKORLATI ALAPJAI Bohtka Sndor s Langer Gbor

VÁKUUMTECHNIKA GYAKORLATI ALAPJAI Bohátka Sándor és Langer Gábor 5. FELÜLETI JELENSÉGEK, KIGÁZOSODÁS TÁMOP-4. 1. 1. C-12/1/KONV-2012 -0005 projekt „Ágazati felkészítés a hazai ELI projekttel összefüggő képzési és K+F feladatokra"

5. FELÜLETI JELENSÉGEK, KIGÁZOSODÁS Ha megvizsgáljuk egy edény vákuumra történő leszívása során a nyomás időbeli változását, jelentős eltérést kapunk a kinetikus gázelméletből számolhatóhoz képest. A nagy különbséget elsősorban az okozza, hogy a kinetikus gázelmélet nem számol a vákuumteret határoló felületeken lejátszódó jelenségekkel, a falakról felszabaduló, illetve azokon keresztüli gázáramokkal. Ebben a fejezetben a vákuumteret határoló falakon foglalkozunk. lejátszódó jelenségekkel 5. 2. 1. Párolgás A kondenzált anyagok részecskéit az anyagra jellemző erők tartják össze elektronkötés, ill. fémes-kötés, ionos kötés, van der Waals kötés és ezek átmeneteinek formájában. A kondenzált anyagtól végtelen távoli részecskére ható erő, és így a részecske energiája is zérus, az anyaghoz kötött helyen pedig a kötési energiával azonos negatív érték. Azt a küszöbenergiát, amelyet az elpárolgó molekula mozgási energiájának meg kell haladnia ahhoz, hogy elhagyja a felületet, a molekula párolgási munkájának vagy párolgási hőjének ( p) nevezzük. A mólnyi anyag párolgási hője: p, mol = p NA 1 g anyag párolgási hője (specifikus párolgási hő): p, spec = p, mol /Mmol
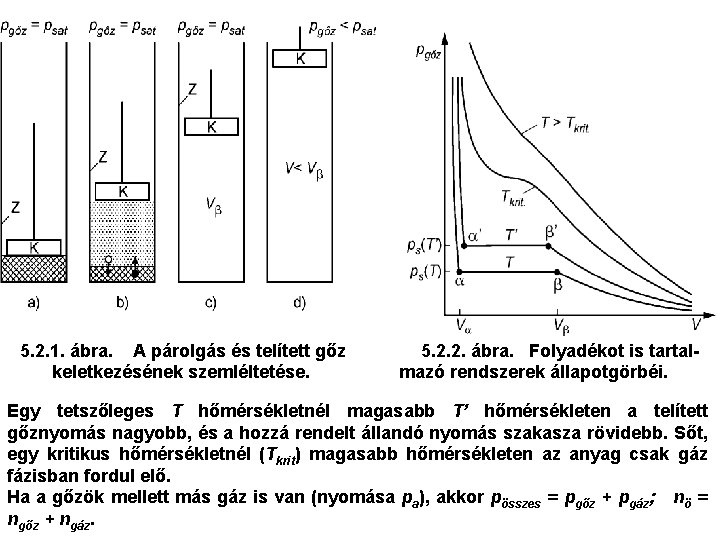
5. 2. 1. ábra. A párolgás és telített gőz keletkezésének szemléltetése. 5. 2. 2. ábra. Folyadékot is tartalmazó rendszerek állapotgörbéi. Egy tetszőleges T hőmérsékletnél magasabb T’ hőmérsékleten a telített gőznyomás nagyobb, és a hozzá rendelt állandó nyomás szakasza rövidebb. Sőt, egy kritikus hőmérsékletnél (Tkrit) magasabb hőmérsékleten az anyag csak gáz fázisban fordul elő. Ha a gőzök mellett más gáz is van (nyomása pa), akkor pösszes = pgőz + pgáz; nö = ngőz + ngáz.

A párolgás és kondenzáció egyszerre végbemenő ellentétes folyamat. Dinamikus egyensúlyban az egységnyi folyadékfelszínről időegység alatt távozó részecskék száma átlagosan azonos a gőztérből a folyadékfelszínre irányuló részecskeáram sűrűségével, ha 100%-os a tapadás valószínűsége: (5. 2. 1. 4. ) A valóságban a folyadékfelszínbe ütköző részecskéknek csak egy része kondenzálódik (kondenzációs valószínűség vagy akkomodációs tényező: k ), a többi pedig reflektálódik a felületről [(1 - k)rész]. Így a gőzrészecskéknek a felületegységre vonatkoztatott kondenzációs áram sűrűsége: (5. 2. 1. 5. ) Egyensúlyban: ahol ngőz a gőz részecskesűrűsége. (5. 2. 1. 6. ) Amikor – adott hőmérsékleten – a folyadékfelszínből kipárolgott részecskék sűrűsége ngőz és így pgőz is állandóvá válik, azt telített gőznek nevezzük (nsat , psat).

Ha a folyadék felszínéről folyamatosan eltávolítjuk a gőzrészecskéket (szivattyúzással v. gáz áramoltatásával), akkor egyrészt a térben a gőznyomás zérusnak tekinthető, másrészt a párolgási áram sűrűsége maximális értéket vesz fel, nagysága azonos a maximális kondenzációs áram sűrűségével. Tehát az előző j. N, pár = j. N, kond megfontolással: a párolgás maximális részecskeáram-sűrűsége (pl. vákuumra szívott felületről): Az ismert Mmol = NA ma és p = nk. T összefüggést és kifejezését felhasználva: (5. 2. 1. 7. ) Az atomi tömeggel szorozva: a párolgás maximális tömegáram-sűrűsége: (5. 2. 1. 8. ) (5. 2. 1. 9. ) [ jm ]=kg m-2 s-1; [ psat ]=mbar; [T ]=K; [Mmol]=kg

A maximális párolgás azonban nem mindig érvényesülhet. Ha a folyadék feletti térből a gőzrészecskék eltávolítása nem tökéletes, akkor a térben a pgőz gőznyomás nem zérus: 0 < pgőz < psat , a molekulák gőztérből történő visszakondenzálása csökkenti a párolgást. Hasonló hatással van, ha a folyadék felszínén helyileg kialakul egy maradék gőzréteg, vagy idegen gázok vannak a folyadékfelszín felett. A kipárolgó részecskék ugyanis ezekbe ütközve reflektálódhatnak, és visszakondenzálnak a felületre: a párolgás hatásfoka romlik. Az eredő párolgási tömegáram, ha a felület felett van gőz/gáz: (5. 2. 1. 11. ) (5. 2. 1. 12. ) ahol = pgőz / psat a telítettség mértéke. Levegőben vízgőz esetén jelentése a jól ismert relatív páratartalom. [jm] = kg m-2 s-1; [psat] = mbar; [T] = K; [Mmol]=kg

Gyakorlati alkalmazás: Izzólámpák wolframszálának párolgását csökkenti, az élettartamát növeli a nemesgáz töltet, mert a kipárolgó atomok az izzószál feletti sűrű gázréteg atomjaiba ütközve nagy valószínűséggel reflektálódnak és visszakondenzálódnak a felületre. A mért pgáz , jm és számított értékek igazolják az idegen gázok párolgást csökkentő hatását. Megfelelő összetételű és nyomású nemesgáz töltettel akár 100 szoros élettartam növekedés is elérhető.

Fagyasztva szárítás (liofilizálás): Mi történik, ha szobahőmérsékleten etilalkoholt tartalmazó edényt szívunk vákuumra? Legyen az edényben az alkohol 10 cm vastag rétegben, 100 cm 2 felülettel. További paraméterek: T = 300 K; psat = 100 mbar = 104 Pa, = 0 -nál K = 0, 024, A párolgás maximális tömegáram-sűrűsége kifejezésből számolva: A tömegáram az adott 100 cm 2 felületen: Im = (jm)pár ∙ 10 -2 m 2 = 4, 1 10 -3 kg∙s-1 A térfogati áram (Iv ): és alapján:

Fagyasztva szárítás (liofilizálás) A számítások eredményeként levonható néhány következtetés. - A szükséges szívóteljesítmény: a = 0 állapot, azaz a felületről elpárolgó alkoholgőzök teljes eltávolítása csak úgy lehetséges, ha van legalább egy 22, 2 ℓ/s szívóteljesítményű szivattyúnk (S 22, 2 ℓ/s). - A párolgás csak akkor egyenletes, ha a párolgási hőt kívülről pótoljuk, különben lehűl a folyadék csökken a párolgás. p, spec (alkohol) = 840 k. J/kg Iw = p, spec Im = 3, 44 k. W teljesítményű hőáram betáplálása szükséges. - Ha nem pótoljuk a hőt, az időegység alatti hőmérsékletcsökkenés és m = 0, 79 kg; c = 2, 43 k. J kg-1 K-1 ismeretében: , azaz a folyadék gyorsan hűl.

5. 2. 2. 1. Adszorpciós sebesség (adszorpciós részecskeáram sűrűség) Az adszorpció sebességét a felületegységen időegység alatt megkötődő gázrészecskék számával mérjük, jele: jad. Langmuir egyszerűsítő feltételezése: - csak monomolekuláris réteg alakul ki, - a részecske csak akkor adszorbeálódik, ha be nem fedett felületre érkezik – ez a felület (1 - f) része. Ekkor a H 0 tapadási valószínűségű részecske felülethez kötődésének valószínűsége: H = H 0 (1 -f) A felületre becsapódó gázrészek áramsűrűségét ismerve adszorpciós sebesség: (5. 2. 2. 6. ) , az

Monomolekuláris réteg adszorpciója, Langmuir-féle adszorpciós izoterma Az adszorpciós és deszorpciós folyamatok dinamikus egyensúlyba kerülnek, ha jad = jdes. Az adszorpció és deszorpció sebességét leíró, ismert egyenletekből a számításokat nem részletezve, a p = nk. T felhasználásával kapjuk a Langmuir-féle izotermát a felület fedettségére (f) : (5. 2. 2. 7. ) ahol (5. 2. 2. 8. ) A kifejezést bonyolítja, hogy 0 (az adszorbeált részecske felületre merőleges rezgésének rezgési ideje, ~ 10 -13 s) és Edes (deszorpciós energia) maga is függ f-től és a felület Tfal hőmérsékletétől. A felületi fedettség nyomásfüggése, a Langmuirféle adszorpciós izoterma a következő ábrán látható. p -nél f = 1, azaz nagy nyomáson a felületet borító monomolekuláris réteg teljes. Langmuir egyszerűsítő feltétele szerint legfeljebb egy monomolekuláris réteg alakulhat ki. Olyan alacsony nyomáson, illetve magas hőmérsékleten, ahol p CL << 1 feltétel teljesül, a fenti kifejezésből egyszerű arányosságot kapunk: f p, amelyet sokszor Henry-féle adszorpciós izotermának neveznek.

Monomolekuláris réteg adszorpciója, Langmuir-féle adszorpciós izoterma 5. 2. 3. ábra. Langmuir-féle adszorpciós izoterma két hőmérsékletre. f : fedettségi tényező, p: az adszorbeálódó gáz nyomása. f p, Henry-féle adszorpciós izoterma A Langmuir modellt olyan adszorpcióra alkalmazva, amelyben a kétatomos molekula atomjaira disszociálva adszorbeálódik a felületen, disszociatív Langmuir izotermának nevezzük. Ez megőrzi az eredeti Langmuir izoterma jellegét, csak a fenti ábra görbéjénél hosszabban elnyúló telítési szakaszt mutat.

Monomolekuláris adszorbeált réteg kialakulásának ideje („monoréteg-idő”) A monoréteg-időt (tmono ) csak közelítéssel számoljuk ki, mégpedig azzal a nem nyilvánvaló feltételezéssel, hogy a felületbe ütköző gázmolekulák tartósan ott maradnak (tökéletes tapadás, H = 1). jad tmono = na, mono Innen kifejezve a tmono –t, felhasználva (5. 2. 2. 6. ) kifejezést, további nem részletezett behelyettesítésekkel: (5. 2. 2. 9. ) Numerikusan: (5. 2. 2. 10. ) [tmono] = s; [na, mono] = m-2; [p] = mbar; [T] = K. Levegőre (Mr = 29), T = 300 K, na, mono 1019 m-2 feltételezéssel: (5. 2. 2. 11. )
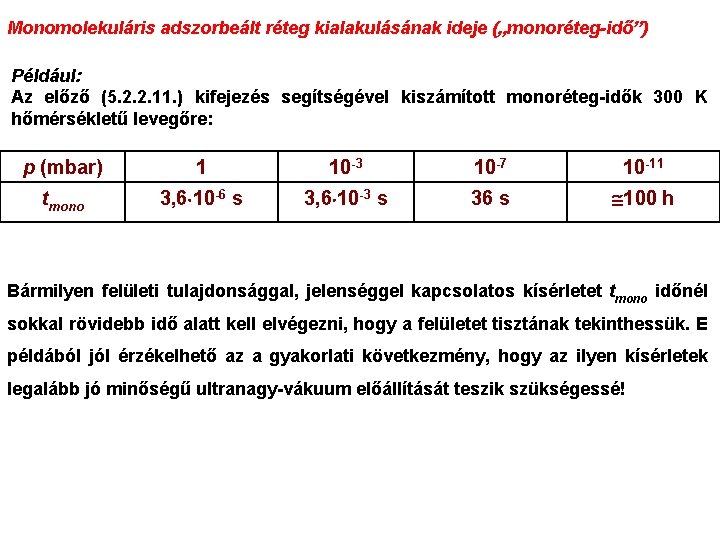
Monomolekuláris adszorbeált réteg kialakulásának ideje („monoréteg-idő”) Például: Az előző (5. 2. 2. 11. ) kifejezés segítségével kiszámított monoréteg-idők 300 K hőmérsékletű levegőre: p (mbar) 1 10 -3 10 -7 10 -11 tmono 3, 6 10 -6 s 3, 6 10 -3 s 36 s 100 h Bármilyen felületi tulajdonsággal, jelenséggel kapcsolatos kísérletet tmono időnél sokkal rövidebb idő alatt kell elvégezni, hogy a felületet tisztának tekinthessük. E példából jól érzékelhető az a gyakorlati következmény, hogy az ilyen kísérletek legalább jó minőségű ultranagy-vákuum előállítását teszik szükségessé!

Többrétegű adszorpció: Brunauer-Emmelt-Teller (BET) izoterma A Langmuir modell jól leírja az erős kemiszorpcióval járó folyamatokat. Nem ad elég jó megoldást azokra a rendszerekre, amelyekben gyengébb adszorpciós erők hatnak (fiziszorpció), mert itt már nem elhanyagolhatóak az adszorbeált részecskék közötti oldalirányú kölcsönhatások, a részecskék mozgékonysága a felszínen, a felszín heterogén természete, és az egy rétegnél vastagabb adszorbeált szerkezet kialakulása. Ezen hatásokat igyekszik figyelembe venni a Brunauer, Emmelt és Teller által megalkotott formula. A BET-formula a mérési eredményekkel jól egyezően írja le a többrétegű adszorpciót. Egyetlen feltétele, hogy a gáz nyomása kisebb legyen telített gőzének nyomásnál (p ps). A valóságban az egyszeres rétegnél nagyobb telítettség (1 < f ) következik be a nyomás növekedésével. Ezt úgy képzelhetjük el, hogy a fizikai vagy kémiai adszorpcióval felülethez kötött monorétegre fiziszorpcióval további rétegek tapadnak: a gáz fázisból a már kialakult saját anyagú rétegre kondenzálódik a gáz. Az első réteg fedettségének kialakulását a korábbi Langmuir egyenlet írja le. A többi réteg kialakulásánál az első rétegre jellemző Edes moláris deszorpciós energia és 0 időállandó helyett a kondenzációs rétegre jellemző p, moláris párolgási hőt és ’ időállandót kell behelyettesíteni. Az összegzés és az itt nem részletezhető számítások után a BET-izotermát leíró függvény egyik jól értelmezhető alakja:

Többrétegű adszorpció: Brunauer-Emmelt-Teller (BET) izoterma (5. 2. 2. 12) ahol (5. 2. 2. 13. ) A telítési gőznyomásnál a gáz folyamatosan, korlátlan rétegvastagságban kondenzálódik (f. BET ), nagyon kis nyomásnál f. BET p (Henry-izoterma), míg a kettő között a Langmuir-féle telítési tartományhoz hasonló viselkedést kapunk, csak itt a nyomással növekvő kondenzáció megy végbe a kialakult monorétegre rakódva, tehát a görbének van egy pozitív meredeksége. A p psat nyomáson végbemenő folyamatos kondenzációt hasznosítjuk a krioszivattyúkban.
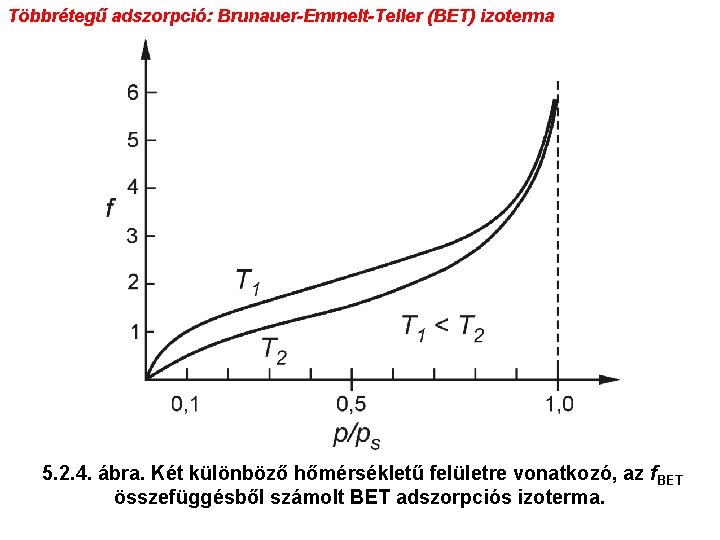
Többrétegű adszorpció: Brunauer-Emmelt-Teller (BET) izoterma 5. 2. 4. ábra. Két különböző hőmérsékletű felületre vonatkozó, az f. BET összefüggésből számolt BET adszorpciós izoterma.

5. 2. 2. 2. Abszorpció Gumik, műanyagok gázabszorpciója sokkal nagyobb, mint a fémeké. A fémek és tömör kerámiák a legjobb vákuumtechnikai anyagok A műanyagok vákuumtechnikai szempontból rossz tulajdonságát hasznosítani is lehet. Erre példa a membrán mintavevős tömegspektrometria. Itt az egyik oldalával atmoszférikus nyomású gázba vagy folyadékba merülő műanyag membrán tulajdonképpen nyomáscsökkentőként és – szelektív gázáteresztése révén – egyes komponensek bedúsítójaként működik. A közegből egy kis mennyiség permeációval (lásd még az 5. 4. fejezetet) halad át a membránon, annak másik, vákuumozott oldalán távozik, és ezt a mintát elemzi a tömegspektrométer. 5. 2. 2. 2. 1. ábra. Membrános gázmintavétel elvi elrendezése.

5. 2. 2. 3. Deszorpció Példa: A CO 2 deszorpciós energiája szén felületen: Edes=34 k. J/mol. Az átlagos tartózkodási idő (5. 2. 2. 2. ) kifejezéséből ( 0 = 10 -13 s) ismeretében a CO 2 molekula átlagos tartózkodási ideje Tfal = 300 K hőmérsékleten: = 10 -7 s; Tfal = 90 K hőmérsékleten = 67 nap! A bemutatott példa mellett megjegyzendő, hogy a ténylegesen mért érték az anyagfajtától függően óriási szórást mutat: 10 -4 s 0 10 -15 s: Edes(cseppf. He) 0, 08 k. J/mol = 0, 8 me. V/atom, Edes(O 2 titánon) = 980 k. J/mol = 9, 8 e. V/molekula. Néhány gáz átlagos tartózkodási ideje a felületen 300 K hőmérsékleten: He: 1, 2 10 -13 s; H 2: fiziszorpcióval 1, 3 10 -12 s, kemiszorpcióval 100 s; CO kemiszorpcióval Ni felületen: 102 – 1017 év! A nem kifűtött vákuumrendszerek maradékgázainak legnagyobb komponense a víz, mert a falakat zömmel H 2 O molekulák fedik akár több rétegben a H 2 O nagy deszorpciós energiája miatt. Ultranagy-vákuum rendszereket ezért száraz nitrogénnel (esetleg argonnal) érdemes fellevegőzni, hogy a legközelebbi leszívás ideje rövidebb legyen.
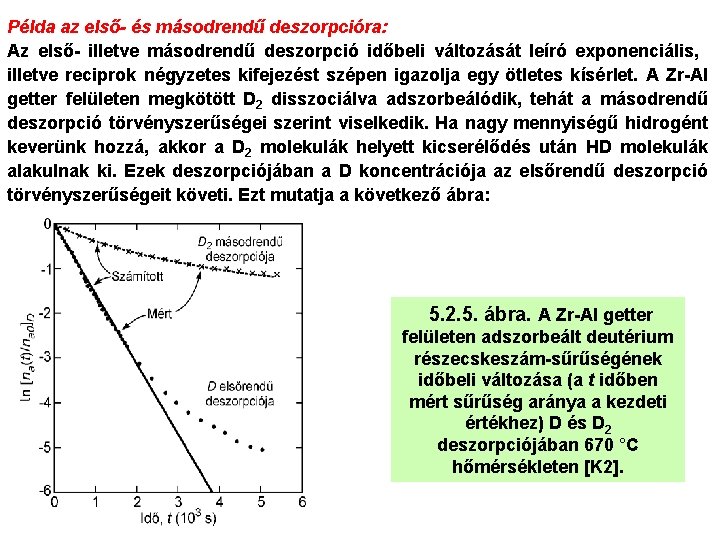
Példa az első- és másodrendű deszorpcióra: Az első- illetve másodrendű deszorpció időbeli változását leíró exponenciális, illetve reciprok négyzetes kifejezést szépen igazolja egy ötletes kísérlet. A Zr-Al getter felületen megkötött D 2 disszociálva adszorbeálódik, tehát a másodrendű deszorpció törvényszerűségei szerint viselkedik. Ha nagy mennyiségű hidrogént keverünk hozzá, akkor a D 2 molekulák helyett kicserélődés után HD molekulák alakulnak ki. Ezek deszorpciójában a D koncentrációja az elsőrendű deszorpció törvényszerűségeit követi. Ezt mutatja a következő ábra: 5. 2. 5. ábra. A Zr-Al getter felületen adszorbeált deutérium részecskeszám-sűrűségének időbeli változása (a t időben mért sűrűség aránya a kezdeti értékhez) D és D 2 deszorpciójában 670 °C hőmérsékleten [K 2].
- Slides: 20