Vitamine generalit Vitamine liposolubili A D E K

Vitamine: generalità Vitamine liposolubili A, D, E, K Meccanismo della visione Calcio Coagulazione del sangue

VITAMINE Micronutrienti organici, richiesti in quantità pari a milligrammi o microgrammi Per la maggior parte dovono essere introdotte con la dieta (non sintetizzate o sintetizzate in parte dall’organismo) Non vengono usate per produrre energia né per usi strutturali • • fanno parte di coenzimi, sono precursori di ormoni, agiscono da antiossidanti, partecipano come substrati a reazioni specifiche

Le VITAMINE sono classificate in LIPOSOLUBILI ed IDROSOLUBILI sulla base della loro insolubilità o solubilità in acqua La denominazione con le lettere dell’alfabeto ha origini storiche Ø 1910 -20 - isolate sostanze che in piccola quantità erano necessarie per prevenire malattie e denominate sostanza liposolubile - fattore A sostanza idrosolubile - fattore B Ø fattore A suddiviso in A - fattore della crescita - visione notturna 1915 D - antirachitica 1916 fattore B suddiviso in 1917 B - fattore anti beri 1918 C - fattore antiscorbuto Ø fattore B ulteriormente suddiviso in B 1 - fattore anti beri B 2 - altre vitamine del complesso B

13 vitamine sono essenziali per l’uomo LIPOSOLUBILI Vitamina A - retinolo Vitamina D - colecalciferolo (malattia da carenza: rachitismo) Vitamina E - tocoferolo Vitamina K - fillochinone IDROSOLUBILI Vitamina C - acido ascorbico (malattia da carenza: scorbuto) Vitamina B 1 - tiamina (malattia da carenza: beri-beri) Vitamina B 2 - riboflavina Vitamina B 3 - niacina (acido nicotinico ed ammide) (carenza: pellagra) Vitamina B 5 - acido pantotenico Vitamina B 6 - piridossina, piridossale, piridossammina Vitamina B 7 - biotina Folati Vitamina B 12 - cobalammina (malattia da carenza: anemia perniciosa) Vitamine del complesso B: sintetizzate dai vegetali tranne la B 12 sintetizzata solo da batteri

Vitamina A
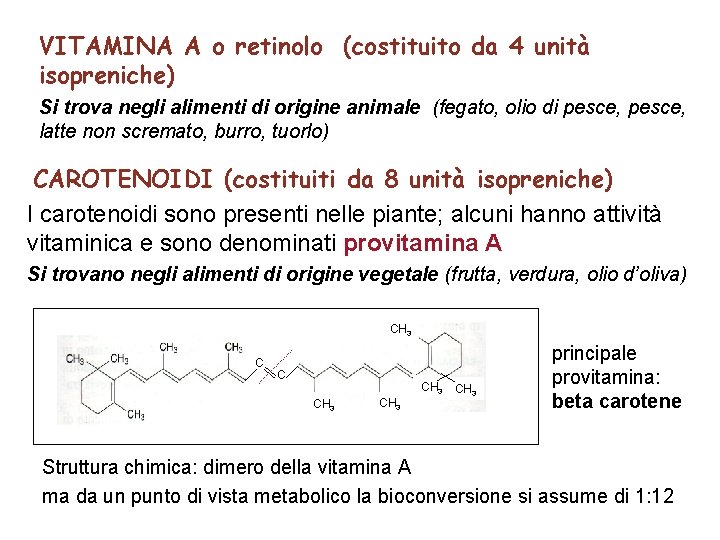
VITAMINA A o retinolo (costituito da 4 unità isopreniche) Si trova negli alimenti di origine animale (fegato, olio di pesce, latte non scremato, burro, tuorlo) CAROTENOIDI (costituiti da 8 unità isopreniche) I carotenoidi sono presenti nelle piante; alcuni hanno attività vitaminica e sono denominati provitamina A Si trovano negli alimenti di origine vegetale (frutta, verdura, olio d’oliva) CH 3 C C CH 3 principale provitamina: beta carotene Struttura chimica: dimero della vitamina A ma da un punto di vista metabolico la bioconversione si assume di 1: 12
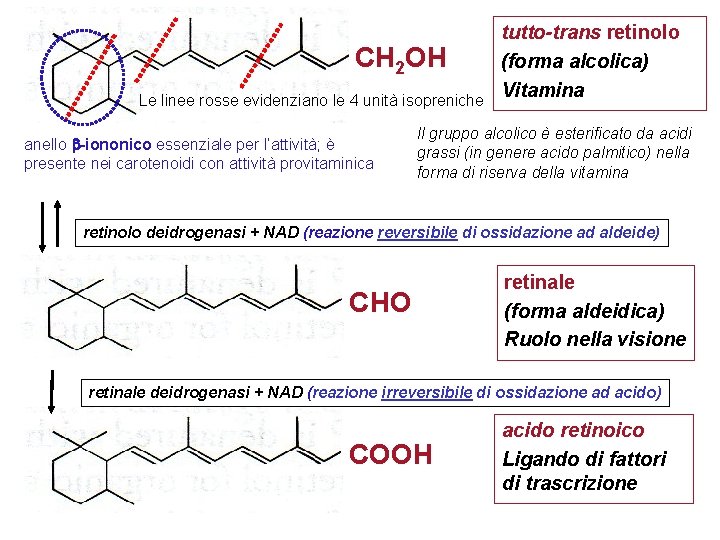
CH 2 OH Le linee rosse evidenziano le 4 unità isopreniche anello -iononico essenziale per l’attività; è presente nei carotenoidi con attività provitaminica tutto-trans retinolo (forma alcolica) Vitamina Il gruppo alcolico è esterificato da acidi grassi (in genere acido palmitico) nella forma di riserva della vitamina retinolo deidrogenasi + NAD (reazione reversibile di ossidazione ad aldeide) CHO retinale (forma aldeidica) Ruolo nella visione retinale deidrogenasi + NAD (reazione irreversibile di ossidazione ad acido) COOH acido retinoico Ligando di fattori di trascrizione
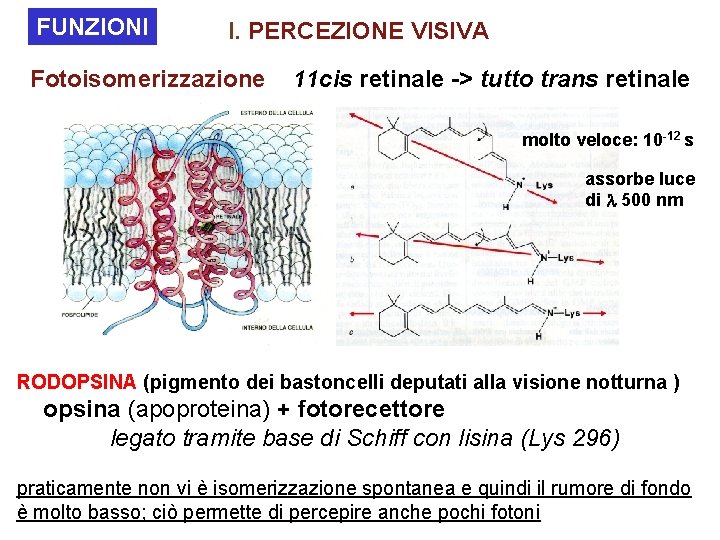
FUNZIONI I. PERCEZIONE VISIVA Fotoisomerizzazione 11 cis retinale -> tutto trans retinale molto veloce: 10 -12 s assorbe luce di 500 nm RODOPSINA (pigmento dei bastoncelli deputati alla visione notturna ) opsina (apoproteina) + fotorecettore legato tramite base di Schiff con lisina (Lys 296) praticamente non vi è isomerizzazione spontanea e quindi il rumore di fondo è molto basso; ciò permette di percepire anche pochi fotoni
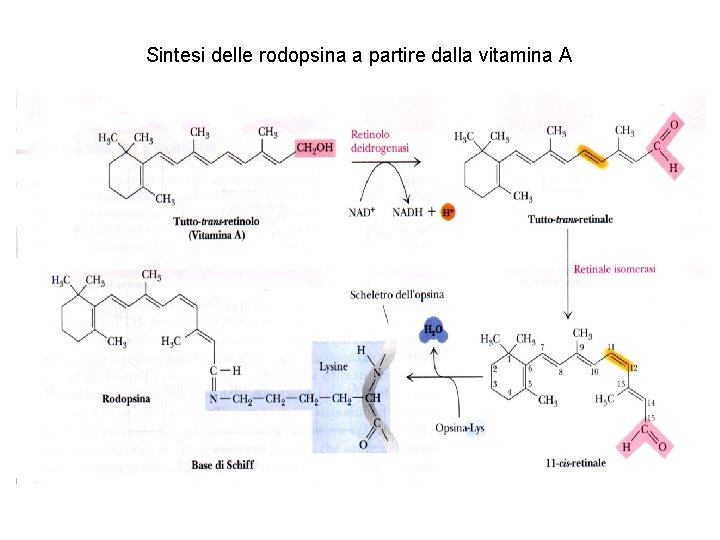
Sintesi delle rodopsina a partire dalla vitamina A
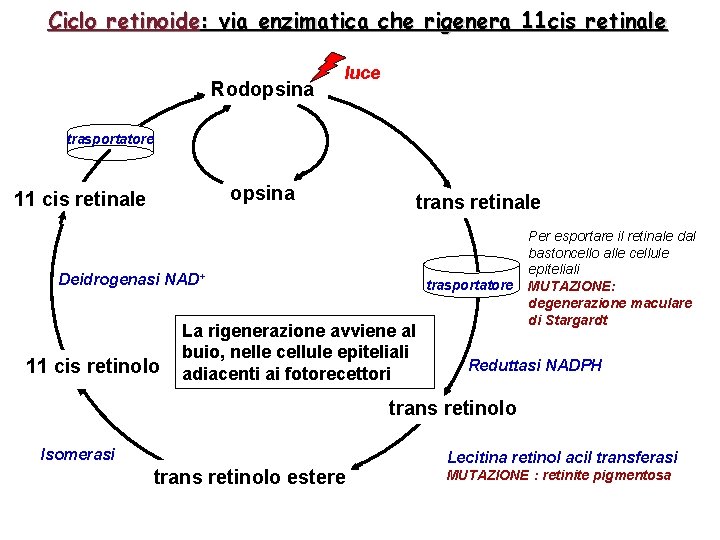
Ciclo retinoide: via enzimatica che rigenera 11 cis retinale Rodopsina luce trasportatore opsina 11 cis retinale trans retinale Deidrogenasi NAD+ 11 cis retinolo trasportatore La rigenerazione avviene al buio, nelle cellule epiteliali adiacenti ai fotorecettori Per esportare il retinale dal bastoncello alle cellule epiteliali MUTAZIONE: degenerazione maculare di Stargardt Reduttasi NADPH trans retinolo Isomerasi trans retinolo estere Lecitina retinol acil transferasi MUTAZIONE : retinite pigmentosa

II. FUNZIONE TRASCRIZIONALE Lega fattori di trascrizione: Recettori dell’ Acido Retinoico (RXR) RXR forma eterodimeri con i recettori per - ormoni steroidei - Vit D - ormoni tiroidei. Anche questi recettori sono fattori trascrizionali attivati dal legame con l’ormone e dalla dimerizzazione con RXR, conseguente inibizione o attivazione di specifici geni Questo spiega i numerosi fenomeni biologici in cui è coinvolta la vitamina A Base molecolare per il ruolo fisiologico nel differenziamento, proliferazione, sviluppo embrionale.

vitamina D

VITAMINA D FONTI - sintesi endogena: esposizione alla luce solare - dieta (necessita di lipidi e sali biliari per l’assorbimento) PRECURSORE dell’ormone steroideo 1, 25 -diidrossi colecalciferolo FUNZIONI dell’ormone: agisce a livello trascrizionale • omeostasi del calcio, in particolare assorbimento a livello intestinale: geni codificanti per il trasportatore del calcio e per la “proteina legante il calcio“ • mineralizzazione ossea • secrezione dell’insulina • crescita, differenziamento • sistema immunitario
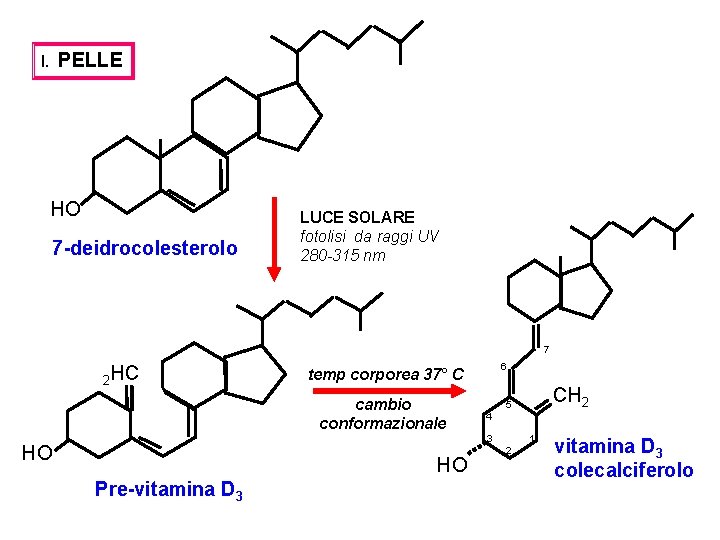
PELLE I. HO 7 -deidrocolesterolo LUCE SOLARE fotolisi da raggi UV 280 -315 nm 7 2 HC 6 temp corporea 37° C cambio conformazionale 4 1 3 HO HO Pre-vitamina D 3 CH 2 5 2 vitamina D 3 colecalciferolo
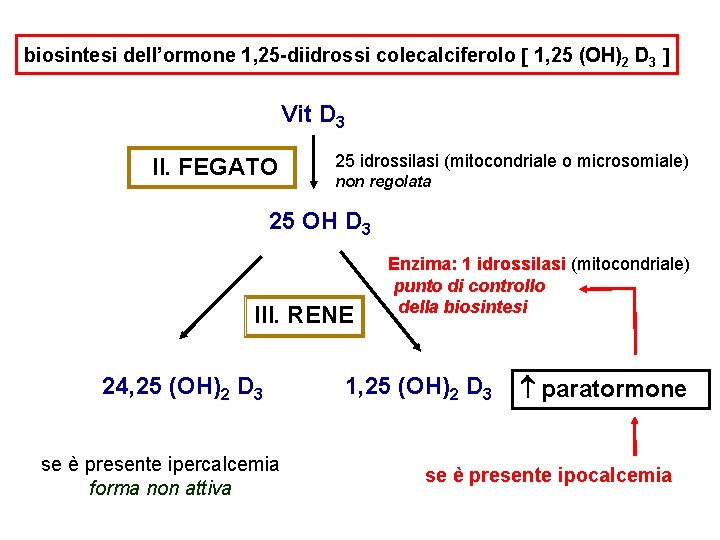
biosintesi dell’ormone 1, 25 -diidrossi colecalciferolo 1, 25 (OH)2 D 3 Vit D 3 II. FEGATO 25 idrossilasi (mitocondriale o microsomiale) non regolata 25 OH D 3 III. RENE 24, 25 (OH)2 D 3 se è presente ipercalcemia forma non attiva Enzima: 1 idrossilasi (mitocondriale) punto di controllo della biosintesi 1, 25 (OH)2 D 3 paratormone se è presente ipocalcemia

Alcune funzioni del CALCIO Struttura (osso e denti) v Coagulazione del sangue (vedi vitamina K) v Contrazione muscolare v Attivazione di enzimi -amilasi pancreatica, protein chinasi C, fosfofruttochinasi v Rilascio di ormoni e neurotrasmettitori v Le funzioni regolatorie prevalgono sulle funzioni scheletriche perturbazioni nell’omeostasi sono tamponate da tessuto osseo

Adulto: Calcio corporeo (1000 - 1200 g ) Livello plasmatico = 10 (9 -11) mg/d. L (2, 4 m. M) 50% ione non complessato - fisiologicamente attivo 40% legato a proteine (albumina) 10% sale fosfato, citrato, bicarbonato Scarsa tolleranza alle deviazioni di [Ca++]: Ø Ipocalcemia: ipereccitabilità, convulsioni tetaniche Ø Ipercalcemia: paralisi muscolare, coma Ormoni di controllo di [Ca++]: Ø Ormone paratiroideo (PTH) Ø Vitamina D
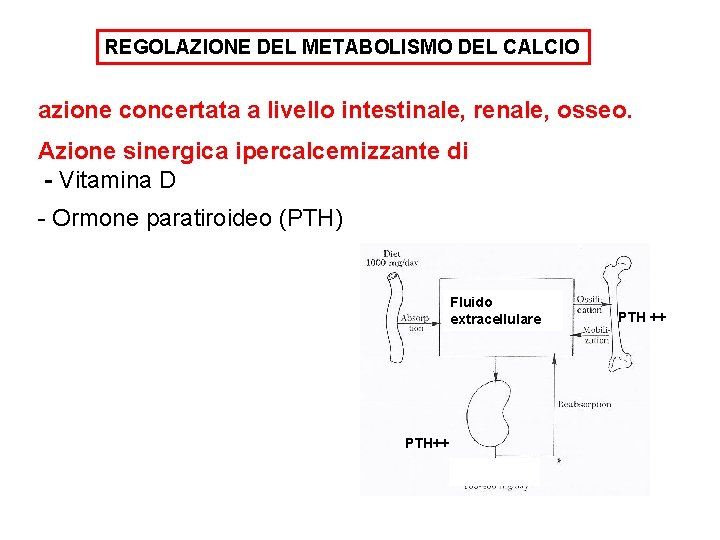
REGOLAZIONE DEL METABOLISMO DEL CALCIO azione concertata a livello intestinale, renale, osseo. Azione sinergica ipercalcemizzante di - Vitamina D - Ormone paratiroideo (PTH) Vita D ++ Fluido extracellulare PTH++ PTH ++
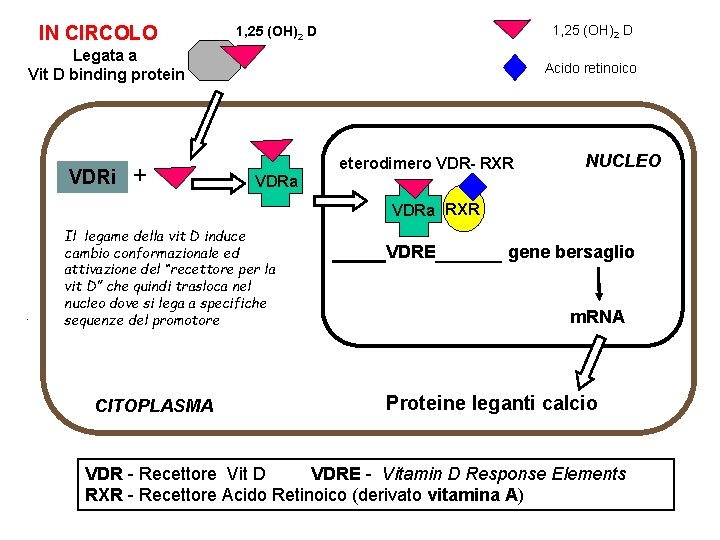
IN CIRCOLO 1, 25 (OH)2 D Legata a Vit D binding protein VDRi + Acido retinoico eterodimero VDR- RXR NUCLEO VDRa RXR Il legame della vit D induce cambio conformazionale ed attivazione del “recettore per la vit D” che quindi trasloca nel nucleo dove si lega a specifiche sequenze del promotore CITOPLASMA ____VDRE_____ gene bersaglio m. RNA Proteine leganti calcio VDR - Recettore Vit D VDRE - Vitamin D Response Elements RXR - Recettore Acido Retinoico (derivato vitamina A)

ASSORBIMENTO DEL CALCIO A livello del duodeno, digiuno, ileo, colon (4%) Assorbito il 20 -30% del calcio assunto - nei bambini fino al 70% trasporto dal lume intestinale all’eneterocita ATTIVO transcellulare, saturabile (sotto il controllo di 1, 25(OH)2 D). transito nell’enterocita (è la tappa limitante). tramite Calcium Binding Protein (CBP) (sotto il controllo di 1, 25(OH)2 D) • estrusione dalla cellula intestinale tramite Ca ATPasi e scambio Ca/Na

CARENZA di Vit D RACHITISMO: bambino Deficiente mineralizzazione con deformità delle ossa sconosciuto nei paesi tropicali, scandinavi, esquimesi nell’ 800 trattato con olio di fegato di pesce e esposizione al sole, nel 1930 identificata la vitamina OSTEOMALACIA: adulto osteopenia con aumentato rischio di frattura ed un diffuso dolore osseo anche per mancata sintesi dell’ormone o mancata risposta ormonale -

Vitamina E
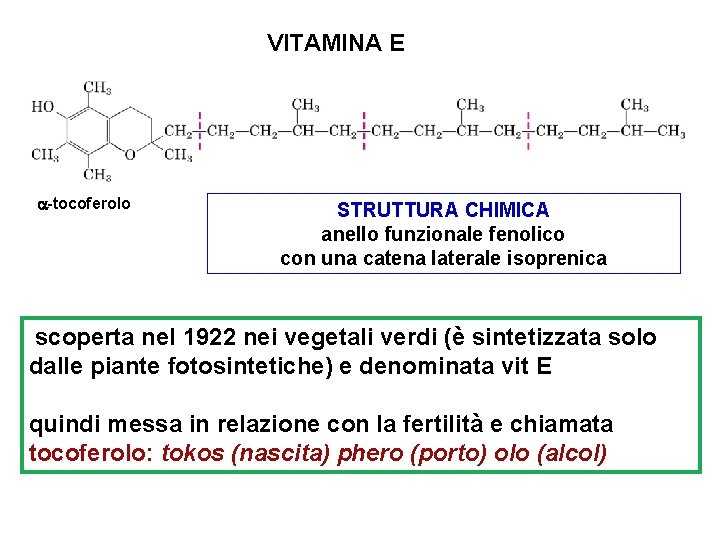
VITAMINA E -tocoferolo STRUTTURA CHIMICA anello funzionale fenolico con una catena laterale isoprenica scoperta nel 1922 nei vegetali verdi (è sintetizzata solo dalle piante fotosintetiche) e denominata vit E quindi messa in relazione con la fertilità e chiamata tocoferolo: tokos (nascita) phero (porto) olo (alcol)

FONTI: soprattutto in alimenti di origine vegetale, olio di oliva, noci, mandorle, vegetali verdi LOCALIZZAZIONE: zone ricche in lipidi quali membrane cellulari, lipoproteine, depositi di grasso FUNZIONE v protezione da auto-ossidazione degli acidi grassi polinsaturi. v previene ossidazione lipoproteine (LDL) MECCANISMO: antiossidante che interrompe la catena di radicali che reagiscono più velocemente con la vi t. E che con acidi grassi ROO • + Vit E-OH Vit E-O • + ROOH Vi E-O • reagisce con vitamina C o altro donatore di di idrogeno e ridiventa Vit E-OH

Vitamina K
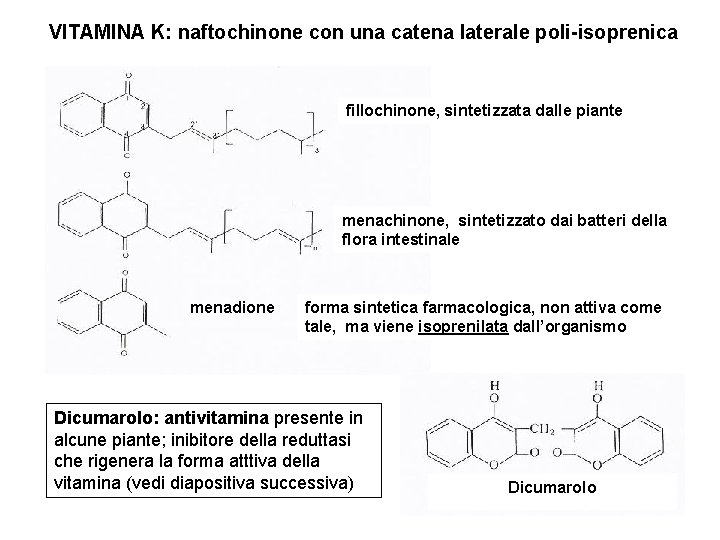
VITAMINA K: naftochinone con una catena laterale poli-isoprenica fillochinone, sintetizzata dalle piante menachinone, sintetizzato dai batteri della flora intestinale 6 -11 menadione forma sintetica farmacologica, non attiva come tale, ma viene isoprenilata dall’organismo Dicumarolo: antivitamina presente in alcune piante; inibitore della reduttasi che rigenera la forma atttiva della vitamina (vedi diapositiva successiva) Dicumarolo
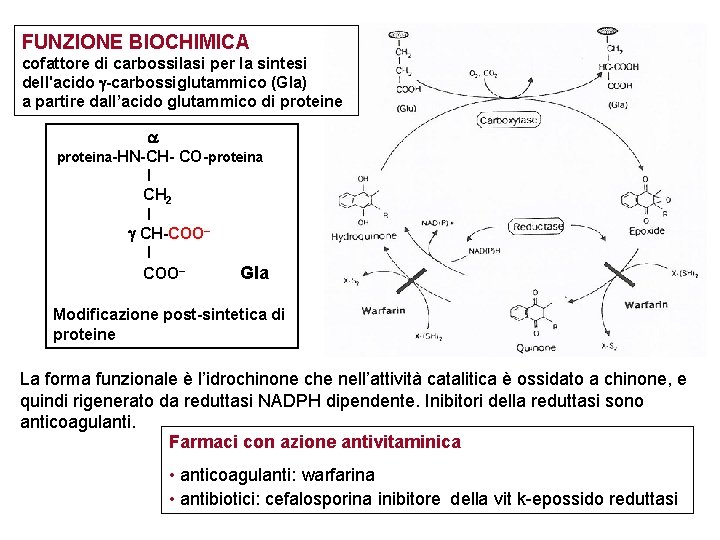
FUNZIONE BIOCHIMICA cofattore di carbossilasi per la sintesi dell'acido -carbossiglutammico (Gla) a partire dall’acido glutammico di proteine proteina-HN-CH- CO-proteina I CH 2 I CH-COO– I COO– Gla Modificazione post-sintetica di proteine La forma funzionale è l’idrochinone che nell’attività catalitica è ossidato a chinone, e quindi rigenerato da reduttasi NADPH dipendente. Inibitori della reduttasi sono anticoagulanti. Farmaci con azione antivitaminica • anticoagulanti: warfarina • antibiotici: cefalosporina inibitore della vit k-epossido reduttasi

L’amminoacido Gla, avendo due cariche negative, lega bene il calcio ionizzato (Ca 2+) con 2 cariche positive La vitamina K interviene come fattore antiemorragico nella coagulazione del sangue. La coagulazione implica una attivazione a cascata di enzimi proteolitici già presenti nel plasma come precursori inattivi: la specifica proteolisi rende attivo il fattore (reazione finale: fibrinogeno fibrina) In tale processo le proteine che hanno Gla legano il Ca 2+ che si lega anche ai fosfolipidi negativi della superficie delle piastrine attivate; tale legame è indispensabile per subire l’attivazione I fattori della coagulazione vit K-dipendenti sono: Protrombina Fattore VII Fattore IX Fattore X In assenza di Ca 2+ non si legano alle piastrine attive e non vengono trasformati nella forma attiva dall’enzima proteolitico di cui sono substrato
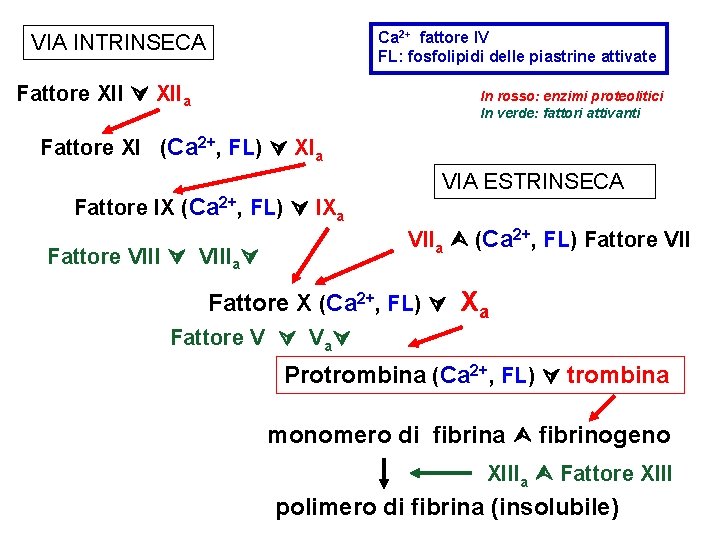
Ca 2+ fattore IV FL: fosfolipidi delle piastrine attivate VIA INTRINSECA Fattore XIIa In rosso: enzimi proteolitici In verde: fattori attivanti Fattore XI (Ca 2+, FL) XIa Fattore IX (Ca 2+, FL) IXa VIA ESTRINSECA VIIa (Ca 2+, FL) Fattore VIIIa Fattore X (Ca 2+, FL) Xa Fattore V Va Protrombina (Ca 2+, FL) trombina monomero di fibrina fibrinogeno XIIIa Fattore XIII polimero di fibrina (insolubile)
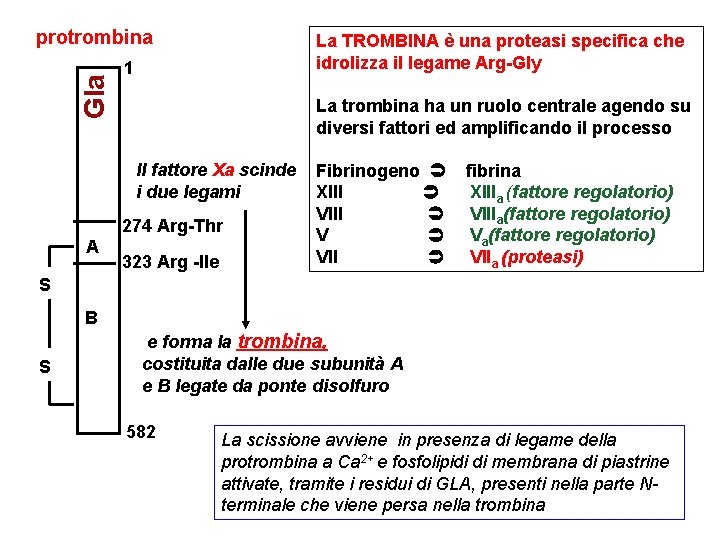
Gla protrombina La TROMBINA è una proteasi specifica che idrolizza il legame Arg-Gly 1 La trombina ha un ruolo centrale agendo su diversi fattori ed amplificando il processo Il fattore Xa scinde i due legami 274 Arg-Thr A 323 Arg -Ile Fibrinogeno XIII V VII fibrina XIIIa (fattore regolatorio) VIIIa(fattore regolatorio) VIIa (proteasi) S B S e forma la trombina, costituita dalle due subunità A e B legate da ponte disolfuro 582 La scissione avviene in presenza di legame della protrombina a Ca 2+ e fosfolipidi di membrana di piastrine attivate, tramite i residui di GLA, presenti nella parte Nterminale che viene persa nella trombina
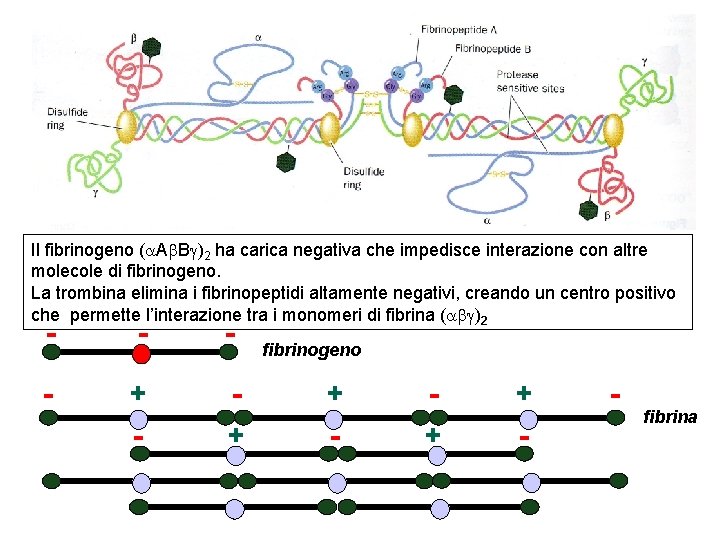
Il fibrinogeno ( A B )2 ha carica negativa che impedisce interazione con altre molecole di fibrinogeno. La trombina elimina i fibrinopeptidi altamente negativi, creando un centro positivo che permette l’interazione tra i monomeri di fibrina ( )2 - - + - + - + - fibrinogeno - fibrina

Il legame ionico viene quindi stabilizzato dalla formazione di legami covalenti fra le catene laterali per azione del fattore XIIIa ANTITROMBINA Proteina plasmatica: inibisce la trombina legandosi con un complesso 1: 1 EPARINA: si lega alla antitrombina e ne aumenta l’attività di centinaia di volte
- Slides: 32