Virus de la Diarrea Viral Bovina Desarrollo de

Virus de la Diarrea Viral Bovina Desarrollo de una vacuna de nueva generación Dr Andrés Wigdorovitz Instituto de Virología, INTA Castelar.

VDVB üPerteneciente al complejo respiratorio, reproductivo y diarreas neonatales üProduce desde una enfermedad respiratoria o gastroentérica leve a síndromes hemorrágicos, abortos y enfermedad de las mucosas. üDistribución Mundial. Diversos planes de erradicación en Europa ü Endémico üReservorio en otras especies üCausante de importantes pérdidas económicas (industria ganadera y de productos biológicos).
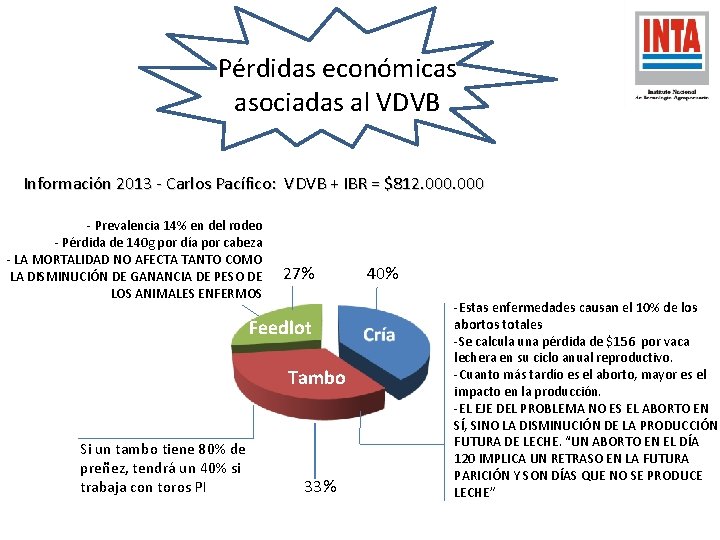
Pérdidas económicas asociadas al VDVB Información 2013 - Carlos Pacífico: VDVB + IBR = $812. 000 - Prevalencia 14% en del rodeo - Pérdida de 140 g por día por cabeza - LA MORTALIDAD NO AFECTA TANTO COMO LA DISMINUCIÓN DE GANANCIA DE PESO DE LOS ANIMALES ENFERMOS 27% Feedlot Tambo Si un tambo tiene 80% de preñez, tendrá un 40% si trabaja con toros PI 33% 40% -Estas enfermedades causan el 10% de los abortos totales -Se calcula una pérdida de $156 por vaca lechera en su ciclo anual reproductivo. -Cuanto más tardío es el aborto, mayor es el impacto en la producción. -EL EJE DEL PROBLEMA NO ES EL ABORTO EN SÍ, SINO LA DISMINUCIÓN DE LA PRODUCCIÓN FUTURA DE LECHE. “UN ABORTO EN EL DÍA 120 IMPLICA UN RETRASO EN LA FUTURA PARICIÓN Y SON DÍAS QUE NO SE PRODUCE LECHE”
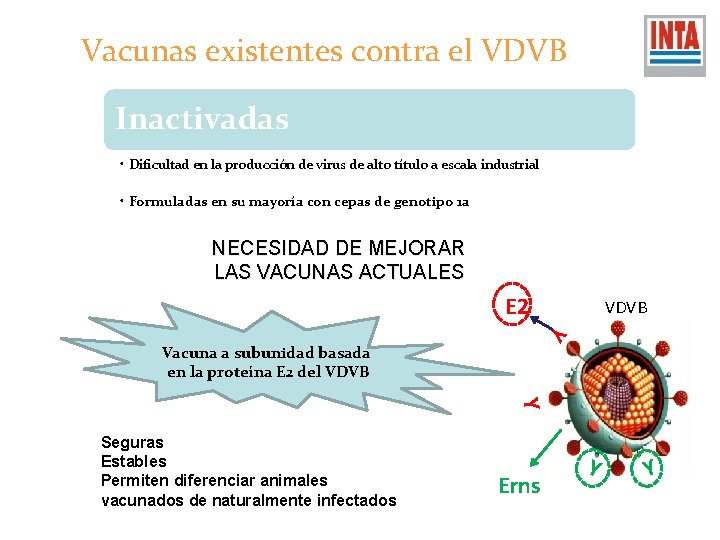
Vacunas existentes contra el VDVB Inactivadas • Dificultad en la producción de virus de alto título a escala industrial • Formuladas en su mayoría con cepas de genotipo 1 a NECESIDAD DE MEJORAR LAS VACUNAS ACTUALES E 2 VDVB Y Vacuna a subunidad basada en la proteína E 2 del VDVB Y Seguras Estables Permiten diferenciar animales vacunados de naturalmente infectados Erns Y Y
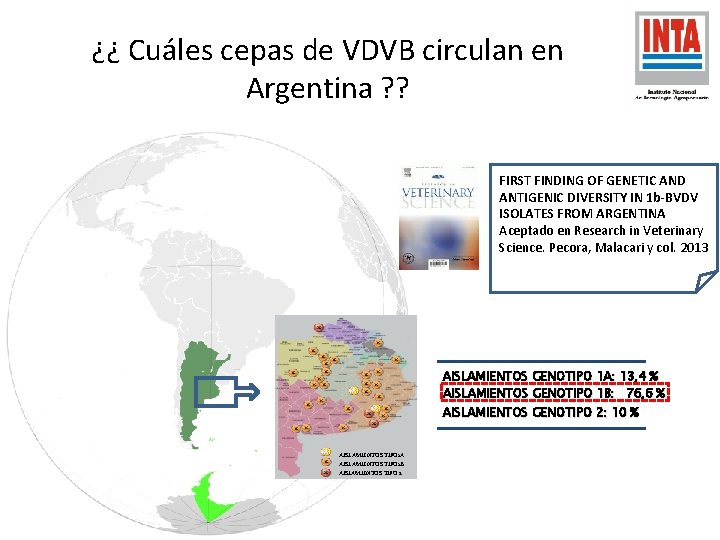
¿¿ Cuáles cepas de VDVB circulan en Argentina ? ? FIRST FINDING OF GENETIC AND ANTIGENIC DIVERSITY IN 1 b-BVDV ISOLATES FROM ARGENTINA Aceptado en Research in Veterinary Science. Pecora, Malacari y col. 2013 AISLAMIENTOS GENOTIPO 1 A: 13, 4 % AISLAMIENTOS GENOTIPO 1 B: 76, 6 % AISLAMIENTOS GENOTIPO 2: 10 % AISLAMIENTOS TIPO 1 A AISLAMIENTOS TIPO 1 B AISLAMIENTOS TIPO 2

Vacunas inteligentes Anticuerpo simple cadena (APCH 1) Proteínas de fusión con direccionamiento de antígenos vacunales a células presentadoras de antígeno. PREMIO 8 th INTERNATIONAL VETERINARY IMMUNOLOGY SYMPOSIUM OURO PRETO –BRASIL 2007 PCT/ES 2008/070053. P 080101073 Incuinta – Start up Algenex
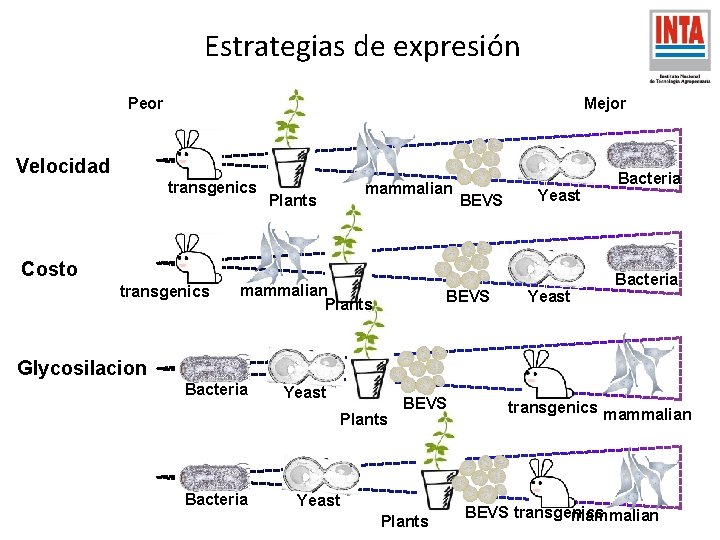
Estrategias de expresión Peor Mejor Velocidad transgenics Plants mammalian BEVS Yeast Costo transgenics mammalian Plants BEVS Yeast Bacteria Glycosilacion Bacteria Yeast Plants Bacteria BEVS Yeast Plants transgenics mammalian BEVS transgenics mammalian

Niveles de expresión de la proteína E 2 en tres sistemas eucariotas E 2 t en baculovirus Larvas de insectos 30 mg/1 L E 2 t en baculovirus células en suspensión E 2 t en células de mamífero 3 mg/1 L 0. 3 mg /1 L E 2 t en alfalfa 0. 4 mg /1 L P 040102842 P 090100556. Vet Res Commun. 2012 Sep; 36(3): 157 -64. doi: 10. 1007/s 11259 -012 -9526 -x. Epub 2012 May 26. Veterinary Immunology and Immunopathology Volume 151, Issues 3– 4, 15 February 2013, Pages 315– 324
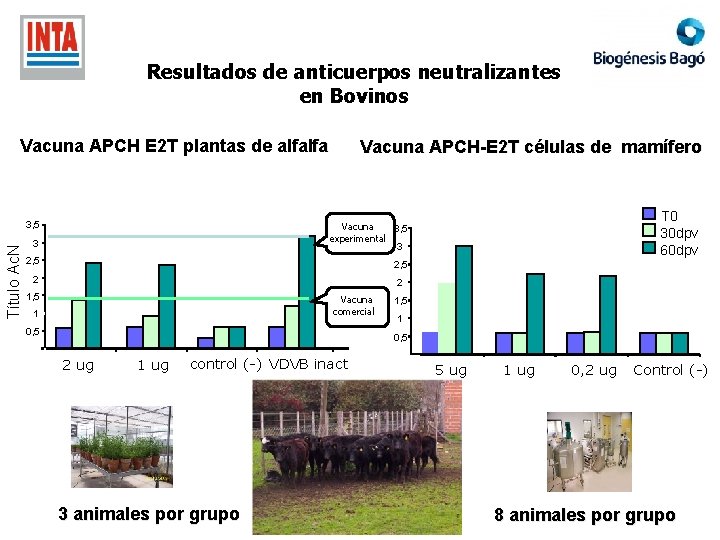
Resultados de anticuerpos neutralizantes en Bovinos Vacuna APCH E 2 T plantas de alfalfa Título Ac. N 3, 5 Vacuna APCH-E 2 T células de mamífero 3 Vacuna 3, 5 experimental 3 2, 5 2 T 0 30 dpv 60 dpv 2 1, 5 Vacuna comercial 1 0, 5 2 ug 1 ug control (-) VDVB inact 3 animales por grupo 5 ug 1 ug 0, 2 ug Control (-) 8 animales por grupo
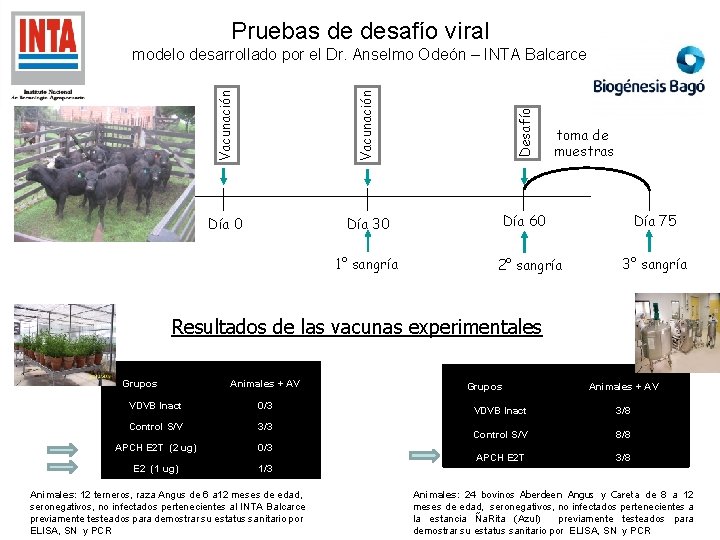
Pruebas de desafío viral Vacunación Desafío modelo desarrollado por el Dr. Anselmo Odeón – INTA Balcarce Día 0 Día 30 Día 60 1° sangría toma de muestras 2° sangría Día 75 3° sangría Resultados de las vacunas experimentales Grupos Animales + AV VDVB Inact 0/3 Control S/V 3/3 APCH E 2 T (2 ug) 0/3 E 2 (1 ug) 1/3 Animales: 12 terneros, raza Angus de 6 a 12 meses de edad, seronegativos, no infectados pertenecientes al INTA Balcarce previamente testeados para demostrar su estatus sanitario por ELISA, SN y PCR Grupos Animales + AV VDVB Inact 3/8 Control S/V 8/8 APCH E 2 T 3/8 Animales: 24 bovinos Aberdeen Angus y Careta de 8 a 12 meses de edad, seronegativos, no infectados pertenecientes a la estancia Ña. Rita (Azul) previamente testeados para demostrar su estatus sanitario por ELISA, SN y PCR
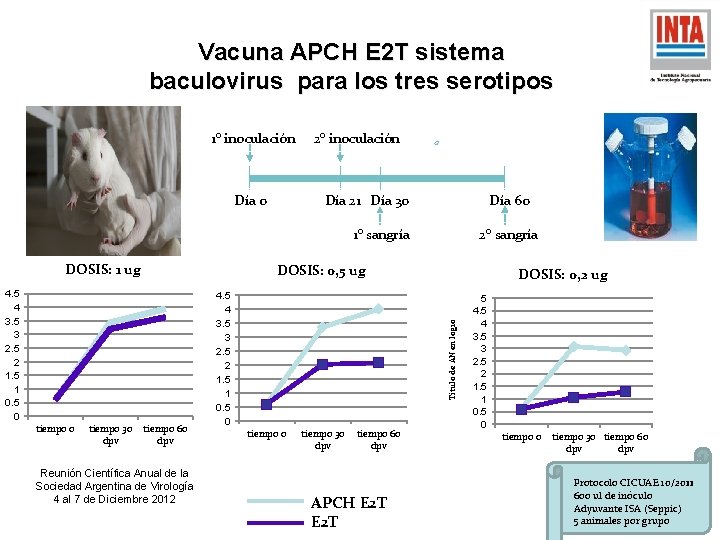
Vacuna APCH E 2 T sistema baculovirus para los tres serotipos 1° inoculación Día 0 2° inoculación Día 21 Día 30 Día 60 1° sangría DOSIS: 1 ug DOSIS: 0, 5 ug tiempo 30 dpv tiempo 60 dpv Reunión Científica Anual de la Sociedad Argentina de Virología 4 al 7 de Diciembre 2012 4. 5 4 3. 5 3 2. 5 2 1. 5 1 0. 5 0 DOSIS: 0, 2 ug Título de AN en log 10 4. 5 4 3. 5 3 2. 5 2 1. 5 1 0. 5 0 tiempo 0 2° sangría tiempo 0 tiempo 30 dpv tiempo 60 dpv APCH E 2 T 5 4 3. 5 3 2. 5 2 1. 5 1 0. 5 0 tiempo 30 tiempo 60 dpv Protocolo CICUAE 10/2011 600 ul de inóculo Adyuvante ISA (Seppic) 5 animales por grupo
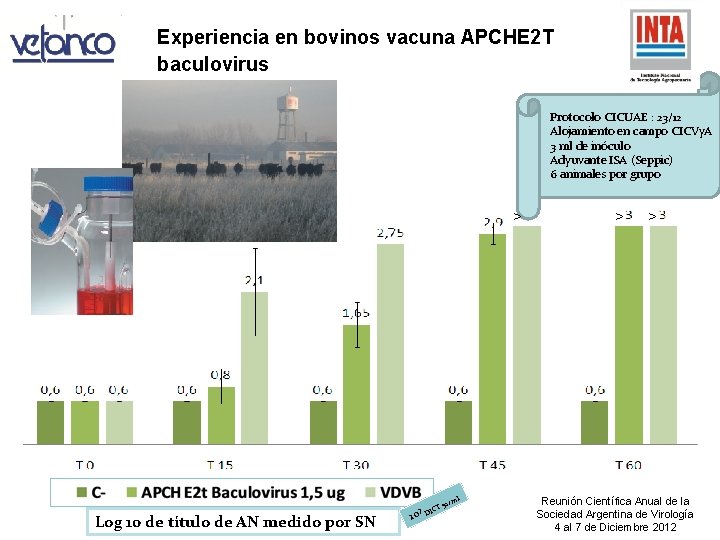
Experiencia en bovinos vacuna APCHE 2 T baculovirus Protocolo CICUAE : 23/12 Alojamiento en campo CICVy. A 3 ml de inóculo Adyuvante ISA (Seppic) 6 animales por grupo > Log 10 de título de AN medido por SN 1 CT 7 0 DI ml 50/ > > Reunión Científica Anual de la Sociedad Argentina de Virología 4 al 7 de Diciembre 2012
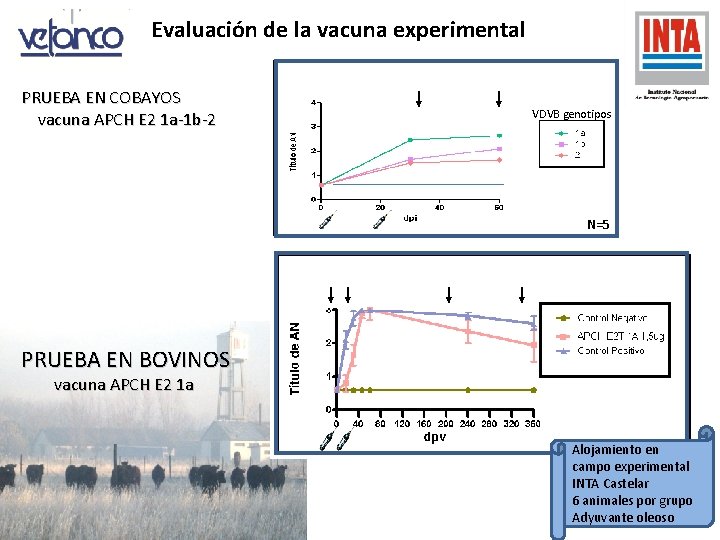
Evaluación de la vacuna experimental PRUEBA EN COBAYOS vacuna APCH E 2 1 a-1 b-2 VDVB genotipos N=5 PRUEBA EN BOVINOS vacuna APCH E 2 1 a Alojamiento en campo experimental INTA Castelar 6 animales por grupo Adyuvante oleoso
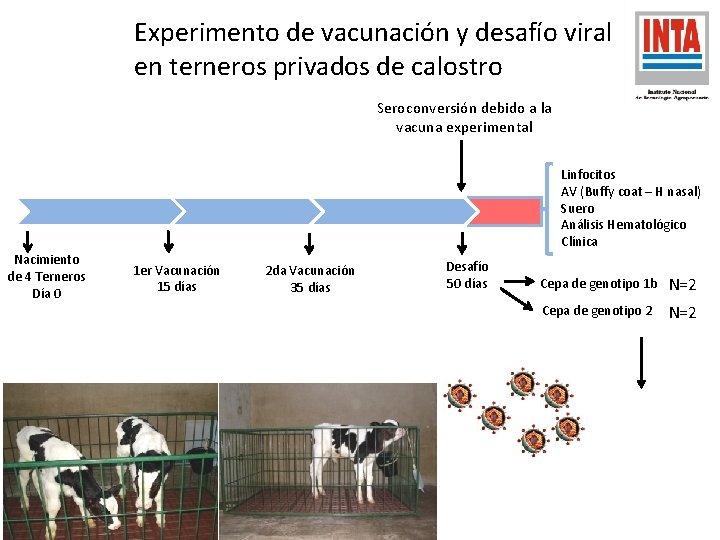
Experimento de vacunación y desafío viral en terneros privados de calostro Seroconversión debido a la vacuna experimental Linfocitos AV (Buffy coat – H nasal) Suero Análisis Hematológico Clínica Nacimiento de 4 Terneros Día 0 1 er Vacunación 15 días 2 da Vacunación 35 días Desafío 50 días Cepa de genotipo 1 b N=2 Cepa de genotipo 2 N=2
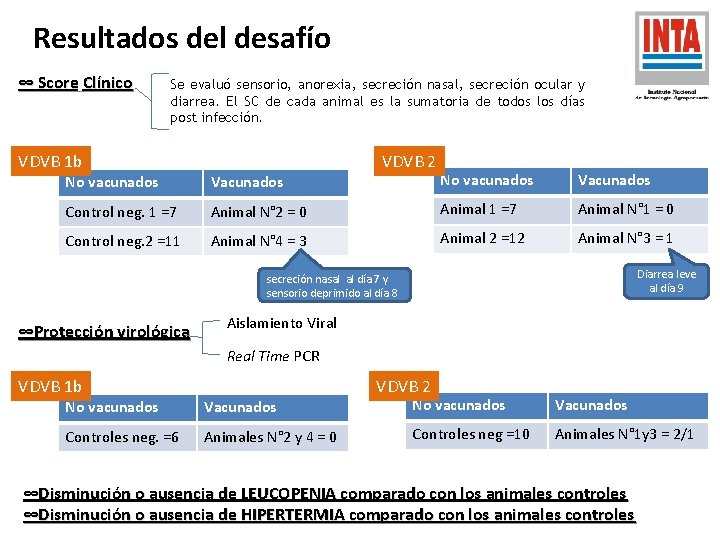
Resultados del desafío ∞ Score Clínico Se evaluó sensorio, anorexia, secreción nasal, secreción ocular y diarrea. El SC de cada animal es la sumatoria de todos los días post infección. VDVB 1 b VDVB 2 No vacunados Vacunados Control neg. 1 =7 Animal N° 2 = 0 Animal 1 =7 Animal N° 1 = 0 Control neg. 2 =11 Animal N° 4 = 3 Animal 2 =12 Animal N° 3 = 1 Diarrea leve al día 9 secreción nasal al día 7 y sensorio deprimido al día 8 ∞Protección virológica Aislamiento Viral Real Time PCR VDVB 1 b VDVB 2 No vacunados Vacunados Controles neg. =6 Animales N° 2 y 4 = 0 Controles neg =10 Animales N° 1 y 3 = 2/1 ∞Disminución o ausencia de LEUCOPENIA comparado con los animales controles ∞Disminución o ausencia de HIPERTERMIA comparado con los animales controles

Conclusiones • Se logro obtener vacunas eficientes contra el VDVB mediante la expresión de la proteina APCH-E 2 T en distintos sistemas de expresión • Se determinaron las proteinas E 2 de los distintos serotipos cirulantes del país • Se logró la expresión de las proteínas APCH-E 2 T de los genotipos 1 a, 1 b y 2 y las mismas proteínas fusionadas a APCH en el sistema baculovirus • La vacuna APCH E 2 T 1 a en una dosis de 1. 5 ugr fue capaz de inducir una respuesta de AN superior a 3 utilizando el protocolo de inmunizacion y booster Se desarrollo una vacuna con los tres serotipos y se demostró su efecto protectivo para los serotipos 1 y 2 •

Actividades en curso y Futuras • • : Generación de todos los registros Optimizar el Rendimiento Proteínas Secretadas al Medio Celular Probar Distintos Medios Probar Distintos Adyuvantes Fermentador Evaluación de Costos a Escala Industrial

Pecora, A; Bellido, D; Perez Aguirreburualde, MS; Dus Santos, MJ Wigdorovitz, A. Instituto de Virología, INTA Castelar. • CONTACTO: awigdorovitz@cnia. inta. gov. ar
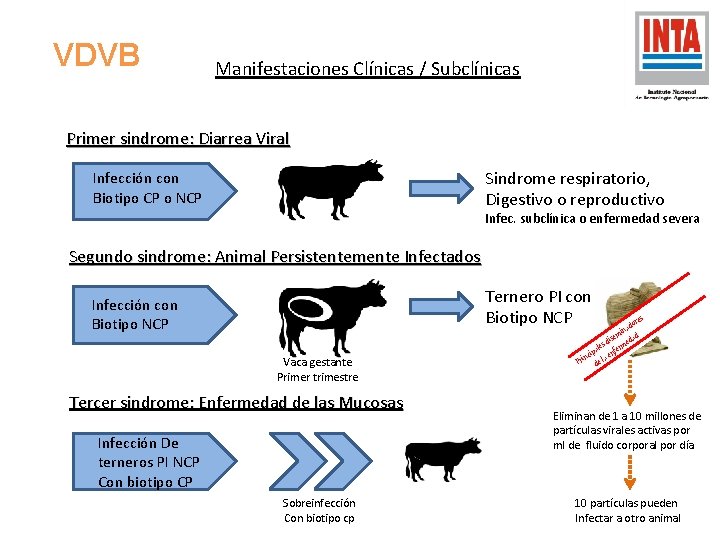
VDVB Manifestaciones Clínicas / Subclínicas Primer sindrome: Diarrea Viral Sindrome respiratorio, Digestivo o reproductivo Infección con Biotipo CP o NCP Infec. subclínica o enfermedad severa Segundo sindrome: Animal Persistentemente Infectados Ternero PI con Biotipo NCP Infección con Biotipo NCP Vaca gestante Primer trimestre Tercer sindrome: Enfermedad de las Mucosas Infección De terneros PI NCP Con biotipo CP Sobreinfección Con biotipo cp s re ado n i em d dis meda s e l fer pa nci e la en i r P d Eliminan de 1 a 10 millones de partículas virales activas por ml de fluido corporal por día 10 partículas pueden Infectar a otro animal
- Slides: 19