VIRUS A DNA Replicazione nucleare 1 2 DNA












- Slides: 29

VIRUS A DNA Replicazione nucleare 1. 2. DNA lineare DNAss = Parvovirus DNAds = Adenovirus - Herpesvirus DNAds circolare = Poliomavirus e Papillomavirus Replicazione citoplasmatica POXVIRUS Replicazione nucleare e citoplasmatica HEPADNAVIRUS 1

TRASCRIZIONE DEI VIRUS A DNA Nucleare utilizzano la RNA pol II cellulare (ecc. POXVIRUS) Adenovirus POXVIRUS: Utilizzano enzimi presenti nel core del virus. Trascritti senza introni. Assenza di splicing 2

TRASCRIZIONE DEI VIRUS A DNA Proteine virali regolano l’interazione di fattori trascrizionali cellulari con sequenze promoter o enhancer al 5’ dei geni virali (es: HSV-1= VP 16) ØTrascrizione di geni su filamenti diversi di DNA (es: SV 40 = early e late su filamenti opposti) ØPossibilità di m. RNA policistronici con introni Splicing intranucleare Aggiunta di catene di poli A (100 -200 residui di adenina) al 3’ e cap metilato al 5’ 3

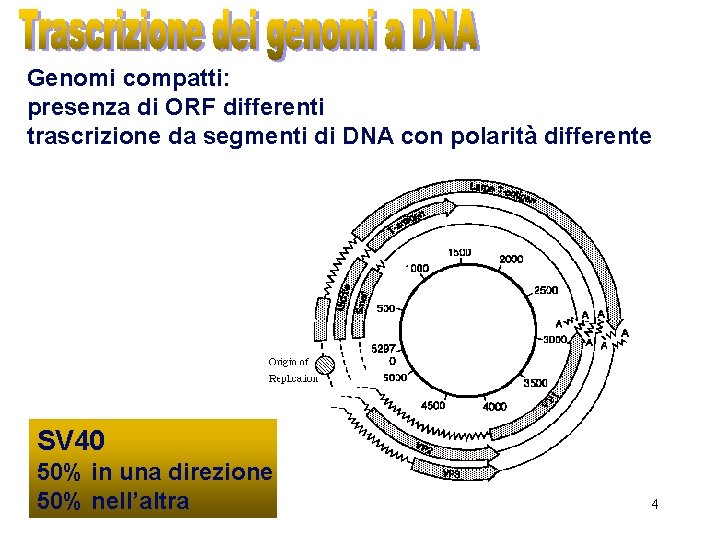
Genomi compatti: presenza di ORF differenti trascrizione da segmenti di DNA con polarità differente Es schema genoma papova SV 40 50% in una direzione 50% nell’altra 4

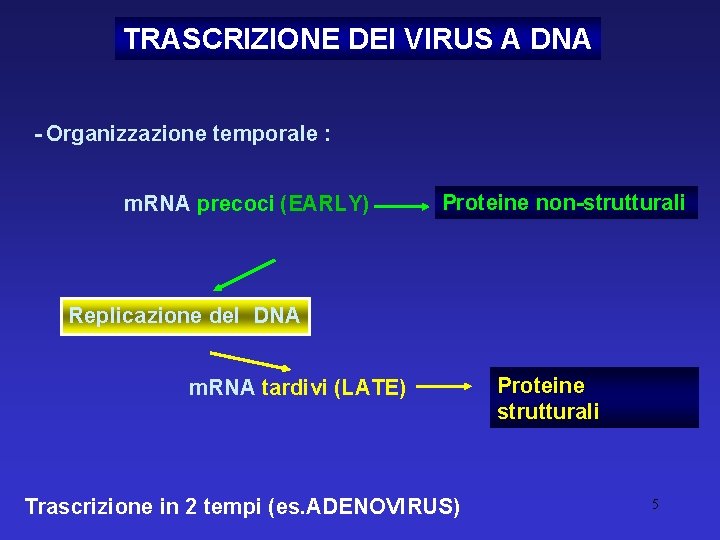
TRASCRIZIONE DEI VIRUS A DNA - Organizzazione temporale : m. RNA precoci (EARLY) Proteine non-strutturali Replicazione del DNA m. RNA tardivi (LATE) Trascrizione in 2 tempi (es. ADENOVIRUS) Proteine strutturali 5

TRASCRIZIONE NEI VIRUS A DNA HERPESVIRUS - Organizzazione temporale (in 3 tempi) : Precoci immediati* (CHX insensibili) m. RNA precoci Precoci ritardati (CHX sensibili) Replicazione del DNA m. RNA tardivi * Utilizzano fattori di trascrizione virali (a-TIF, nel virione) e cellulari (NF-k. B) 6

REPLICAZIONE del DNA VIRALE SEMICONSERVATIVA con vari intermedi di replicazione Parvovirus - Papillomavirus-Poliomavirus: DNA pol cellulare Adenovirus - Herpesvirus: DNA pol virale > velocità > errori Target per antivirali (acyclovir) 7

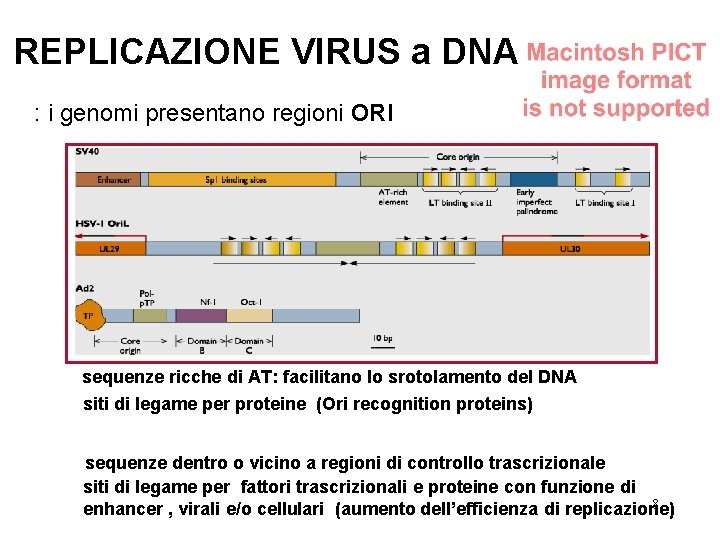
REPLICAZIONE VIRUS a DNA : i genomi presentano regioni ORI sequenze ricche di AT: facilitano lo srotolamento del DNA siti di legame per proteine (Ori recognition proteins) sequenze dentro o vicino a regioni di controllo trascrizionale siti di legame per fattori trascrizionali e proteine con funzione di 8 enhancer , virali e/o cellulari (aumento dell’efficienza di replicazione)

Replicazione del genoma dei virus a DNA : le proteine di riconoscimento della regione ORI Tutti i virus a DNA codificanore almeno una proteina per iniziare la replicazione del genoma lega la regione ORI del genoma virale. il legame della/e proteine tende a distorcere la regione ORI La distorzione della regione ORI facilita il reclutamento di proteine (virali o celluleri) ad attività di elicasi ATP-dipendente che permette lo srotolamento del DNA virale I virus più grandi codificano la DNA polimerasi ed altre proteine necessarie per la replicazione del genoma 9

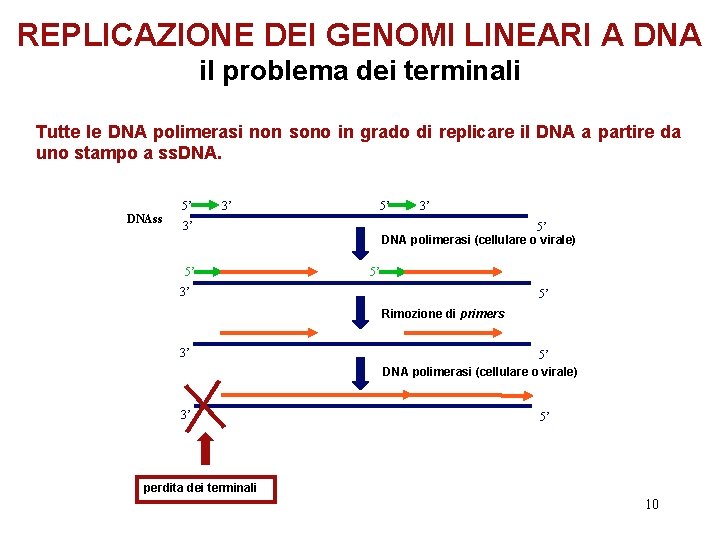
REPLICAZIONE DEI GENOMI LINEARI A DNA il problema dei terminali Tutte le DNA polimerasi non sono in grado di replicare il DNA a partire da uno stampo a ss. DNAss 5’ 5’ 3’ 3’ 5’ DNA polimerasi (cellulare o virale) 5’ 3’ 5’ Rimozione di primers 3’ 3’ 5’ DNA polimerasi (cellulare o virale) 5’ perdita dei terminali 10

Ridondanza terminale: presenza di “terminal repeats” (TR) (genoma di Adenovirus) Sequenze identiche ……. . . e di “inverted terminal repeats” (ITR) (genoma di Poxvirus, Parvovir ed Herpesvirus). 5’ 3’ a b c c’ b’ a’ a’ b’ c’ c b a 3’ 5’ La lunghezza dei ITR varia da 20 a 150 residui nucleotidici. Nei Poxvirus è di oltre 10. 000 basi (> 5% del genoma) 11

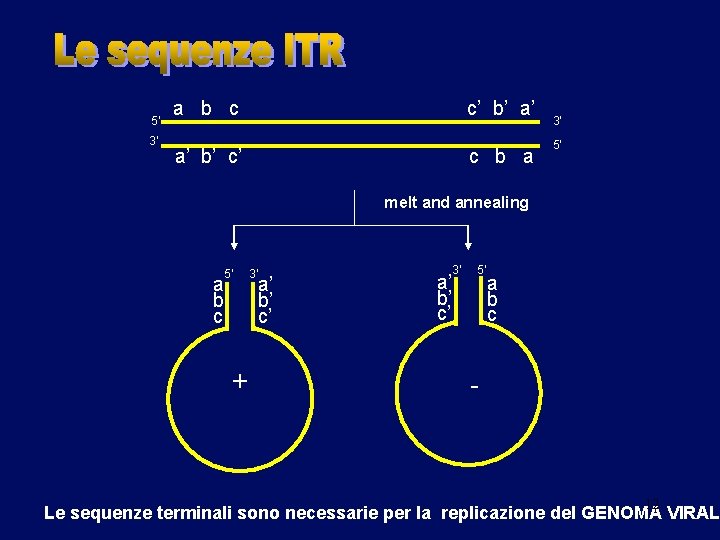
5’ 3’ a b c c’ b’ a’ a’ b’ c’ c b a 3’ 5’ melt and annealing a b c 5’ + 3’ a’ b’ c’ 5’ a b c - 12 Le sequenze terminali sono necessarie per la replicazione del GENOMA VIRAL

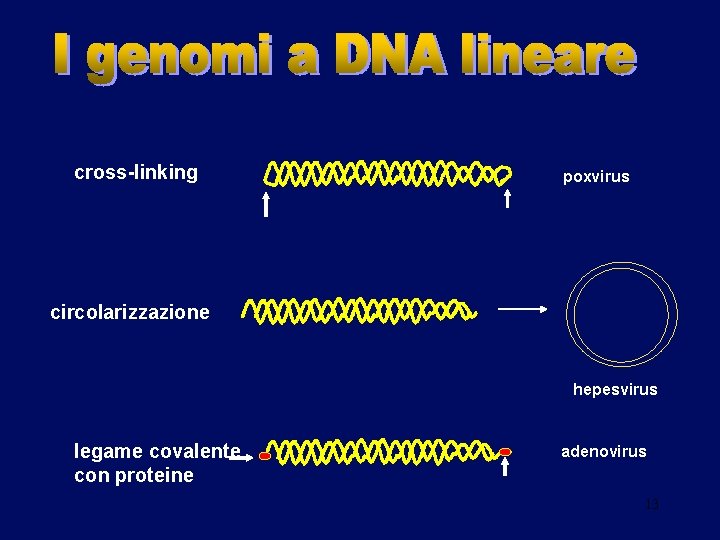
cross-linking poxvirus circolarizzazione hepesvirus legame covalente con proteine adenovirus 13

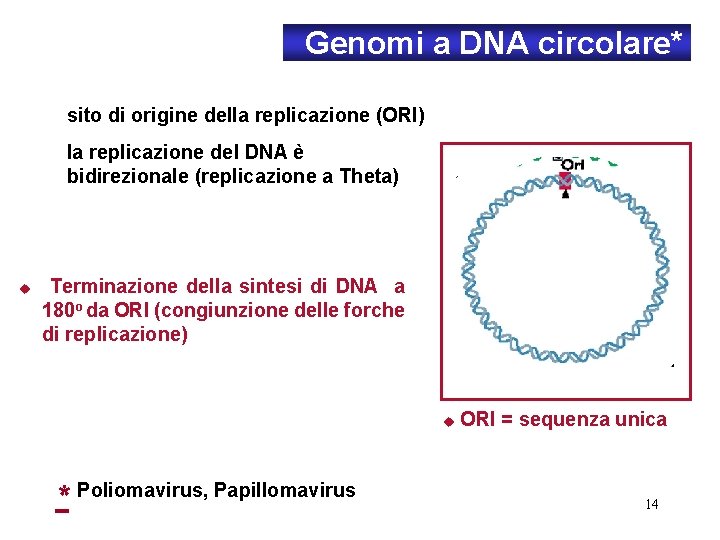
Genomi a DNA circolare* sito di origine della replicazione (ORI) la replicazione del DNA è bidirezionale (replicazione a Theta) u Terminazione della sintesi di DNA a 180 o da ORI (congiunzione delle forche di replicazione) u * Poliomavirus, Papillomavirus ORI = sequenza unica 14

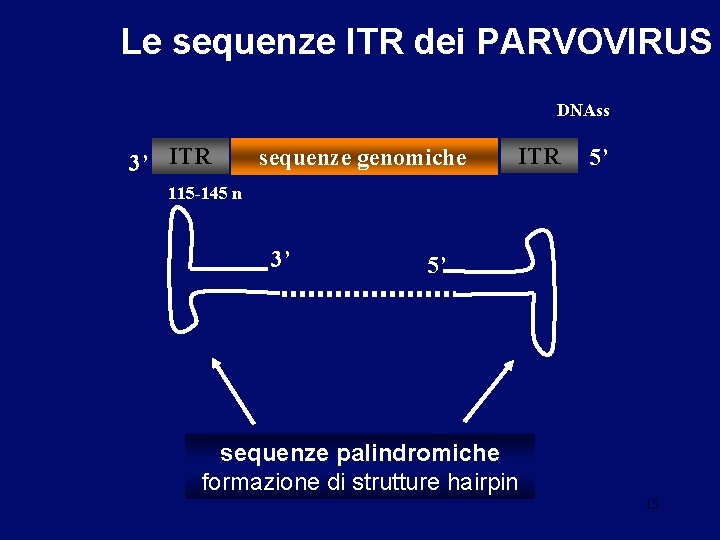
Le sequenze ITR dei PARVOVIRUS DNAss 3’ ITR sequenze genomiche ITR 5’ 115 -145 n 3’ 5’ sequenze palindromiche formazione di strutture hairpin 15

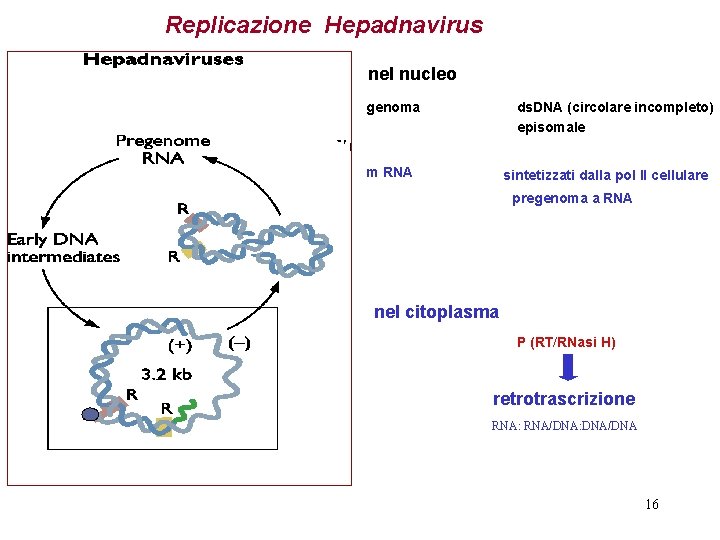
Replicazione Hepadnavirus nel nucleo genoma ds. DNA (circolare incompleto) episomale m RNA sintetizzati dalla pol II cellulare pregenoma a RNA nel citoplasma P (RT/RNasi H) retrotrascrizione RNA: RNA/DNA: DNA/DNA 16

VIRUS A RNA Replicazione citoplasmatica 1. RNA lineare ss -polarità positiva -polarita negativa 2. RNAds = Reovirus Replicazione nucleare ORTHMYXOVIRUS e RETROVIRUS 17

REPLICAZIONE dei virus a RNA polimerasi RNA-dipendenti (Rp. Rd) non utilizzano PRIMERS (la trascrizione e/o replicazione dell’ RNA inizia all’estremità della molecola lineare) > velocità assenza di proof-reading èCaratteristica delle RNA polimerasi RNA dipendenti Resistenti a sostanze che inibiscono le RNA polimerasi DNAdipendenti (Actinomicina D) 18

TRASCRIZIONE di VIRUS a RNA i virus ad RNA non hanno elementi di controllo dell’espressione genica simili a quelli dei virus a DNA meccanismi differenti per regolare l’espressione dei geni virali gli m. RNA virali devono essere organizzati e tradotti come gli m. RNA cellulari i virus a RNA eucariotici devono avere una struttura genomica che genera m. RNA monocistronici 19

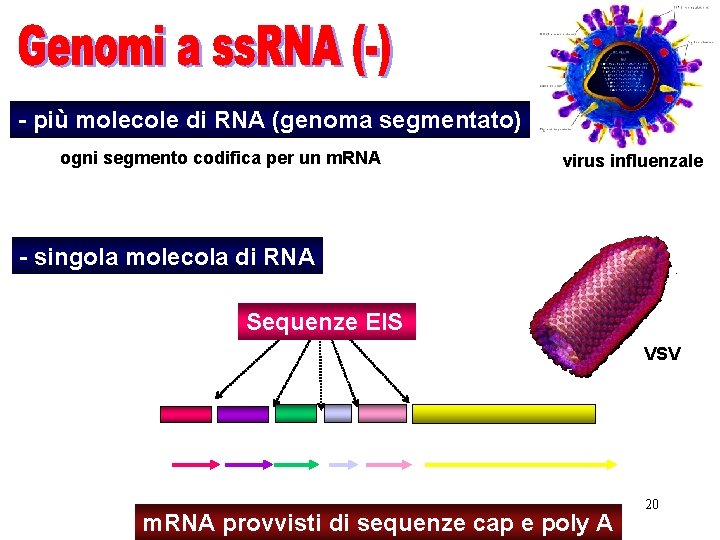
- più molecole di RNA (genoma segmentato) ogni segmento codifica per un m. RNA virus influenzale - singola molecola di RNA Sequenze EIS VSV 3’ m. RNA provvisti di sequenze cap e poly A 5’ 20

Struttura secondaria della sequenza IRES (Internal Ribosome Entry Site) presente al 5’ del RNA genomico. Necessaria per la funzione del genoma come m. RNA. IRES di POLIOVIRUS 21

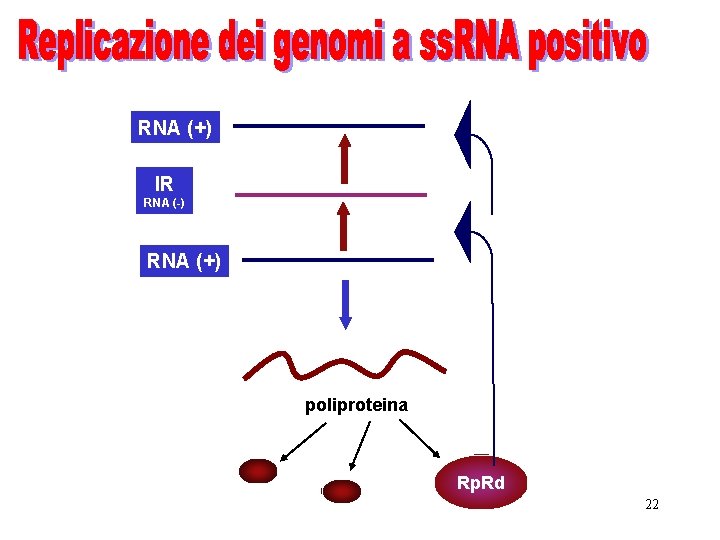
RNA (+) IR RNA (-) RNA (+) poliproteina Rp. Rd 22

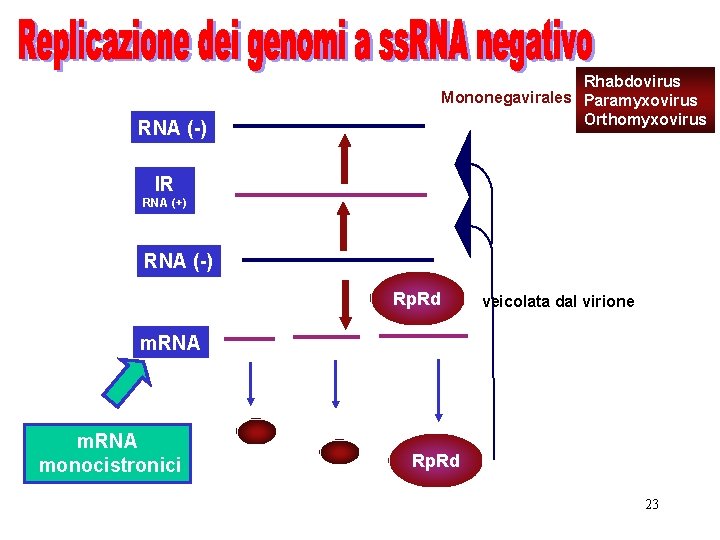
Rhabdovirus Mononegavirales Paramyxovirus Orthomyxovirus RNA (-) IR RNA (+) RNA (-) Rp. Rd veicolata dal virione m. RNA monocistronici Rp. Rd 23

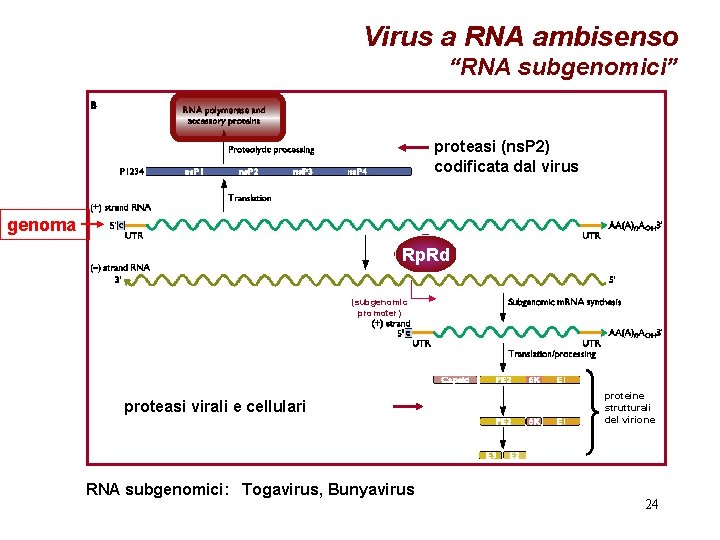
Virus a RNA ambisenso “RNA subgenomici” proteasi (ns. P 2) codificata dal virus genoma Rp. Rd (subgenomic promoter) proteasi virali e cellulari RNA subgenomici: Togavirus, Bunyavirus proteine strutturali del virione 24

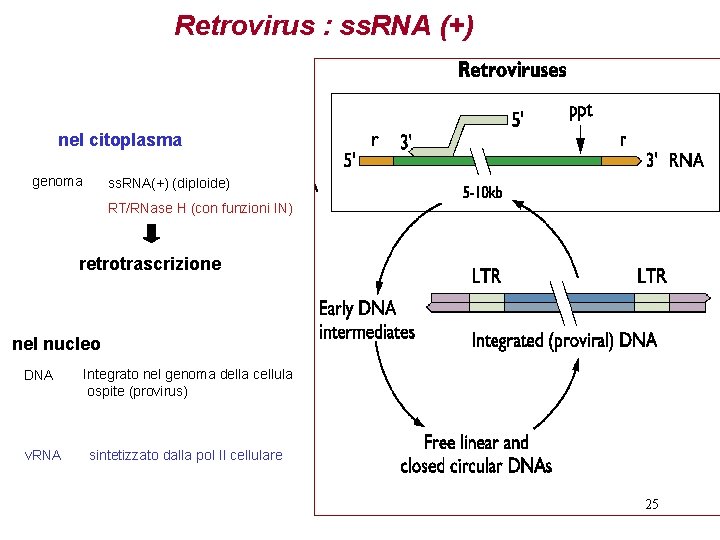
Retrovirus : ss. RNA (+) nel citoplasma genoma ss. RNA(+) (diploide) RT/RNase H (con funzioni IN) retrotrascrizione nel nucleo DNA v. RNA Integrato nel genoma della cellula ospite (provirus) sintetizzato dalla pol II cellulare 25

MATURAZIONE E LIBERAZIONE DEI VIRUS ANIMALI 1. Assemblaggio del capside (procapside) 2. Formazione del nucleocapside Virus a DNA nel NUCLEO (ecc. POXVIRUS - HEPADNAVIRUS) Virus a RNA nel CITOPLASMA (ecc. ORTHOMYXOVIRUS)) LISI 3. LIBERAZIONE GEMMAZIONE ESOCITOSI 26

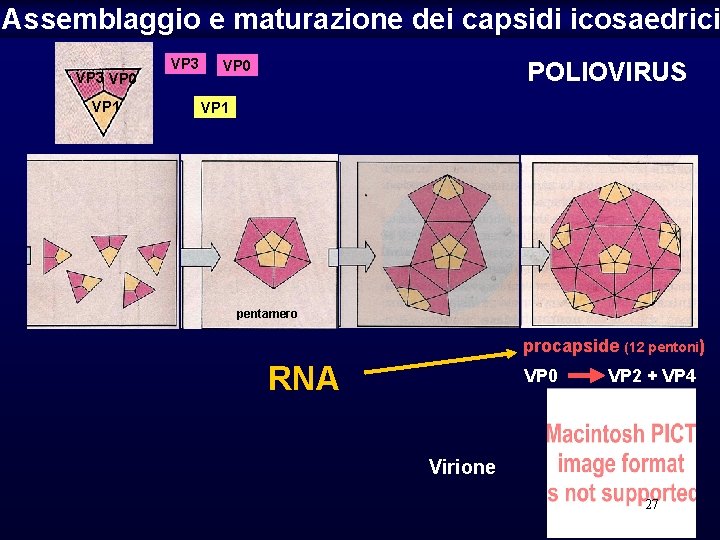
Assemblaggio e maturazione dei capsidi icosaedrici VP 3 VP 0 VP 1 VP 3 VP 0 POLIOVIRUS VP 1 pentamero procapside (12 pentoni) RNA VP 0 VP 2 + VP 4 Virione 27

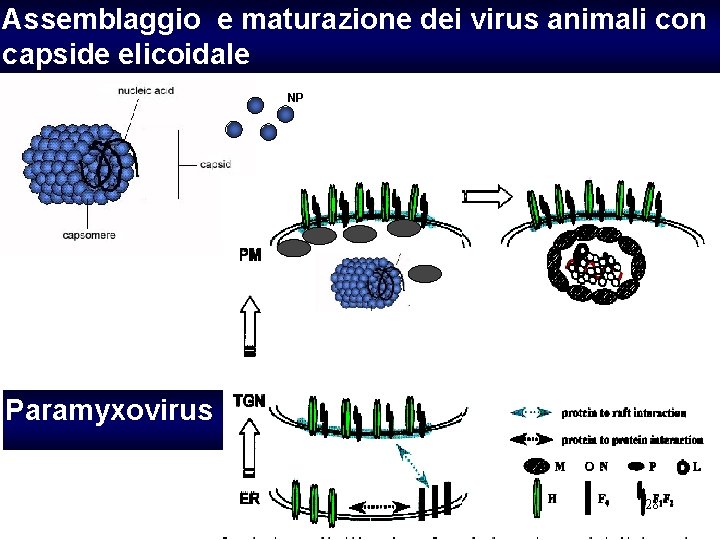
Assemblaggio e maturazione dei virus animali con capside elicoidale NP Paramyxovirus 28

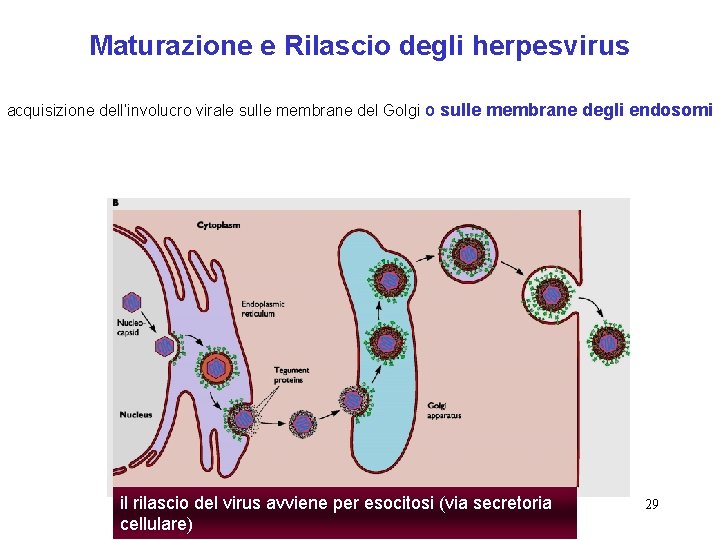
Maturazione e Rilascio degli herpesvirus acquisizione dell’involucro virale sulle membrane del Golgi o sulle membrane degli endosomi ? il rilascio del virus avviene per esocitosi (via secretoria cellulare) 29