Virologie physiopathologie histoire naturelle du VIH classification OMS


























- Slides: 47

Virologie, physiopathologie, histoire naturelle du VIH classification OMS promotion 8 session 1 médecins juin 2013

objectifs connaître la diversité virologique du VIH et son implication pratique l connaître les éléments utiles du cycle viral l connaître la relation CD 4 et CV dans l’évolution de la maladie l connaître la classification OMS et son implication dans la pratique l

Virologie virus à ARN

Deux types HIV-1 Global HIV-2 Afrique de l’ouest

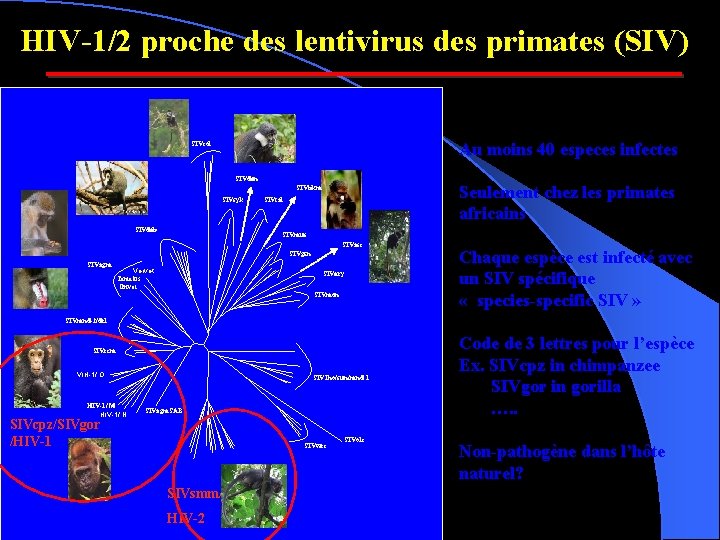
HIV-1/2 proche des lentivirus des primates (SIV) Au moins 40 especes infectes SIVcol SIVden Seulement chez les primates africains SIVbkm SIVsyk SIVdeb SIVtal SIVmus SIVasc SIVgsn SIVagm Vervet Tantalus Grivet SIVery SIVmon Chaque espèce est infecté avec un SIV spécifique « species-specific SIV » SIVmnd-2/drl SIVrcm VIH-1/ O HIV-1/ M HIV-1/ N SIV lho/sun/mnd-1 SIVagm. SAB SIVcpz/SIVgor /HIV-1 SIVwrc SIVsmm/ HIV-2 SIVolc Code de 3 lettres pour l’espèce Ex. SIVcpz in chimpanzee SIVgor in gorilla …. . Non-pathogène dans l’hôte naturel?

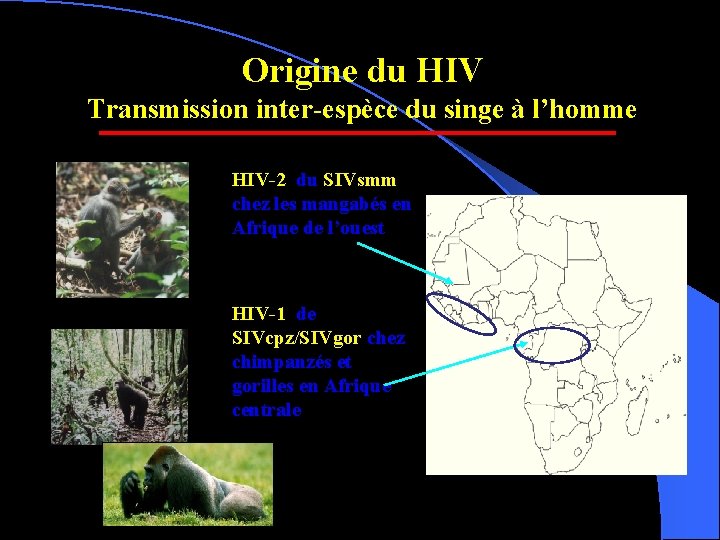
Origine du HIV Transmission inter-espèce du singe à l’homme HIV-2 du SIVsmm chez les mangabés en Afrique de l’ouest HIV-1 de SIVcpz/SIVgor chez chimpanzés et gorilles en Afrique centrale

Characteristiques de l‘évolution du virus HIV • Taux de réplication élevé: 1010 virions par jour • Reverse transcriptase taux de mutation: 1 substitution par genome par cycle • Recombinaison : 7 -30 cross-overs par genome per cycle • double infection: recombinants gag pol env recombination A A B B gag C A B pol C C A B env C

Characteristiques de l‘évolution du virus HIV chez le patient: multiple quasi-espèces F. Mc. Cutchan Transmission singe-homme l’homme Transmission de different quasi-espèces chez Effect foundateurs, evolution

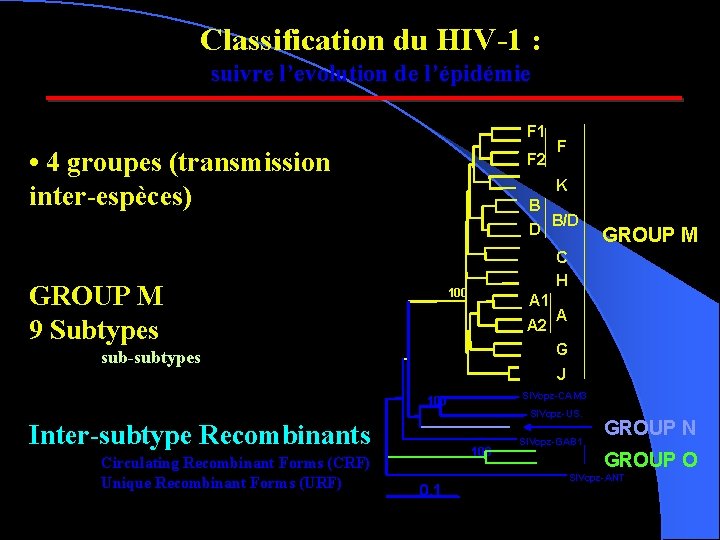
Classification du HIV-1 : suivre l’evolution de l’épidémie F 1 • 4 groupes (transmission inter-espèces) F 2 K B B/D D GROUP M 9 Subtypes GROUP M C H 100 A 1 A 2 A G sub-subtypes J SIVcpz-CAM 3 100 SIVcpz-US. Inter-subtype Recombinants Circulating Recombinant Forms (CRF) Unique Recombinant Forms (URF) F 100 0. 1 SIVcpz-GAB 1 GROUP N GROUP O SIVcpz-ANT

Nouveau groupe du VIH-1 !!! VIH-1 groupe P 2 Aout 2009 10

CRF: Circulating Recombinant Forms Meme structure recombinant identifié chez au moins 4 patients jouant un role dans l’epidemie >40 CRFS:

prevalence globale et distribution des différents soustypes/CRFs (Hemelaar et al, AIDS 2006) l l l Subtype C Subtype A Subtype B Subtype G CRF 01 -AE CRF 02 -AG 50% 12% 10% 6% 5% 100 5% SIVcpz-CAM 3 SIVcpz-US. 100 Other CRFS l Subtypes F+H+J+K l 18% 0. 94% 100 0. 1 F F 2 K B D B/D C H A 1 A A 2 G J GROUP M GROUP N GROUP O SIVcpz-ANT SIVcpz-GAB 1

Global distibution of HIV-1 M variants CRF 03 -AB B B CRF 14_BG G A, B, C, F 1 , B, C CRF 09 -CPX CRF 06 -cpx B, CRF 07 -BC CRF 08 -BC CRF 02 -AG A, D, CC, B, A CRF 01_AE O, N F 1 CRF 12_BF CRF 01 -AE, B CRF 11 -cpx A, C, D, F, CRF 10 -CD G, H, J, K CRF 05 -DF C, B B

Distribution geographique des soustypes/CRF dynamique et évolutive

Pourquoi étudier l ’évolution de la diversité génétique du HIV? l Differences de pathogenicité, transmissibilité resistance aux ARVs ? l Implications pour developpement d’un vaccin? l Efficacité des tests diagnostques l l l Serologie Moleculaire Charge virale pour le suivi de l’efficacité des traitements

physiopathologie

Système immunitaire normal • Protège l’organisme des agressions externes et internes notamment infectieuses • Organes lymphoïdes : moelle osseuse, rate, ganglions, thymus, sites lymphoïdes (TD), … • 2 mécanismes principaux/complémentaires – Cellulaire = : lymphocyte T, macrophages destruction des cellules malades/infectées récepteur de surface sur lymphocyte T: CD 4 ++, CD 8 (lymphocyte T killer), CD 3 – Humorale = lymphocyte B production des Ac de « reconnaissance » ultérieure après premier contact avec Ag facilite la destruction cellulaire • lymphocyte T CD 4 : rôle majeur de « coordination » entre les acteurs => CIBLE PRINCIPALE DU VIH

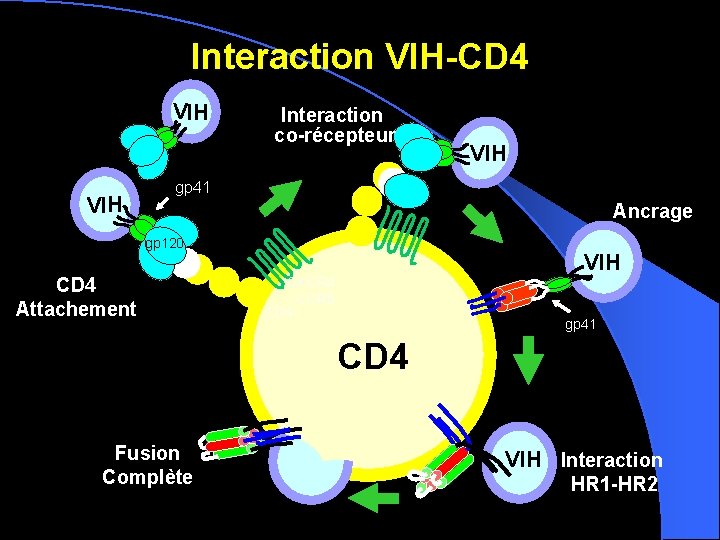
Interaction VIH-CD 4 VIH Interaction co-récepteur VIH gp 41 Ancrage gp 120 CD 4 Attachement VIH CXCR 4 CCR 5 CD 4 gp 41 CD 4 Fusion Complète VIH Interaction HR 1 -HR 2

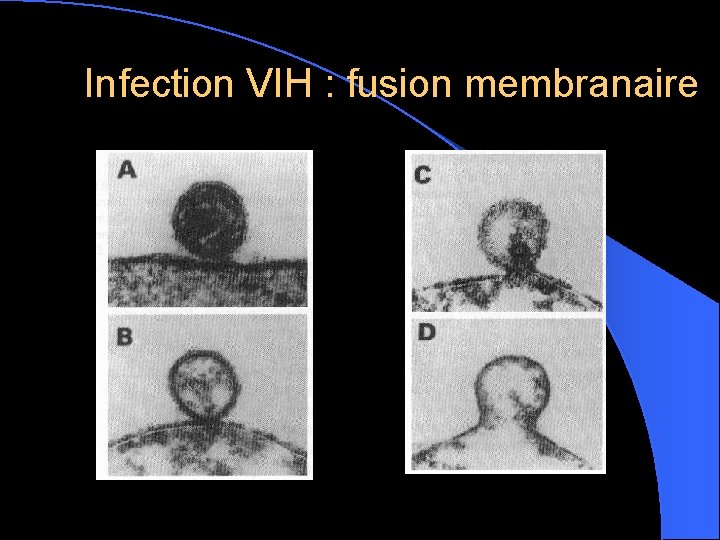
Infection VIH : fusion membranaire


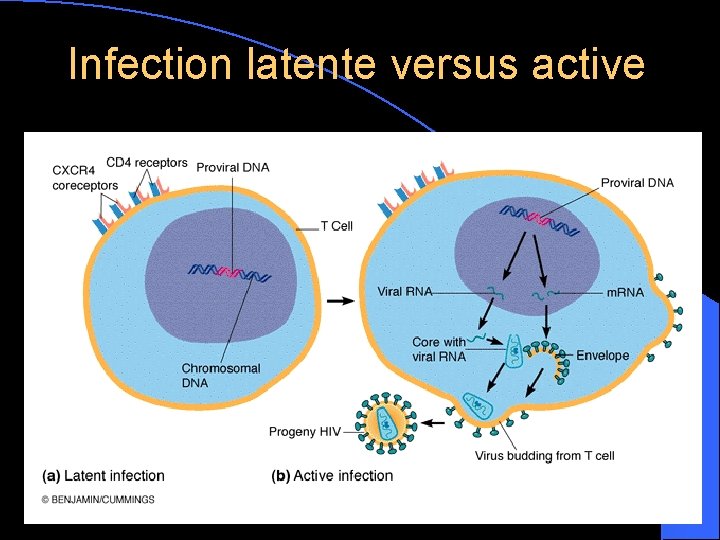
Infection latente versus active

Réplication continue du VIH dans les cellules CD 4 + au sein des tissus lymphoides ganglions rate Circulation sanguine tissus lymphoides muqueuses digestive et génitale

Etapes initiales de l’infection VIH

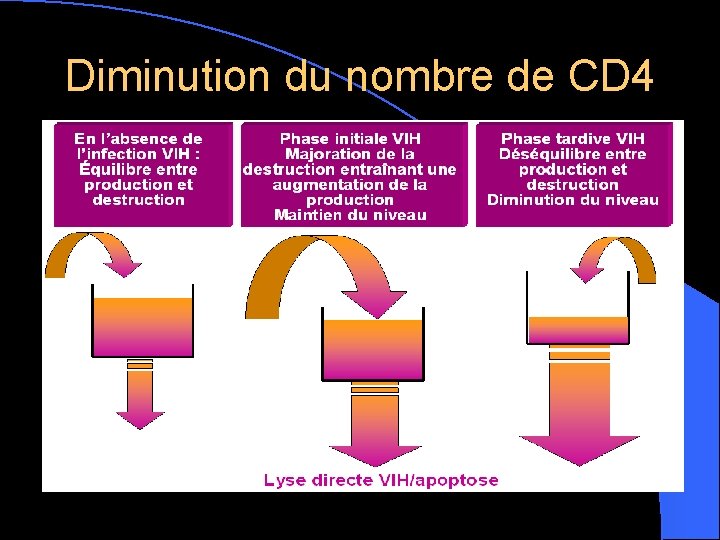
Diminution du nombre de CD 4

Mécanisme du déficit immunitaire lié au VIH

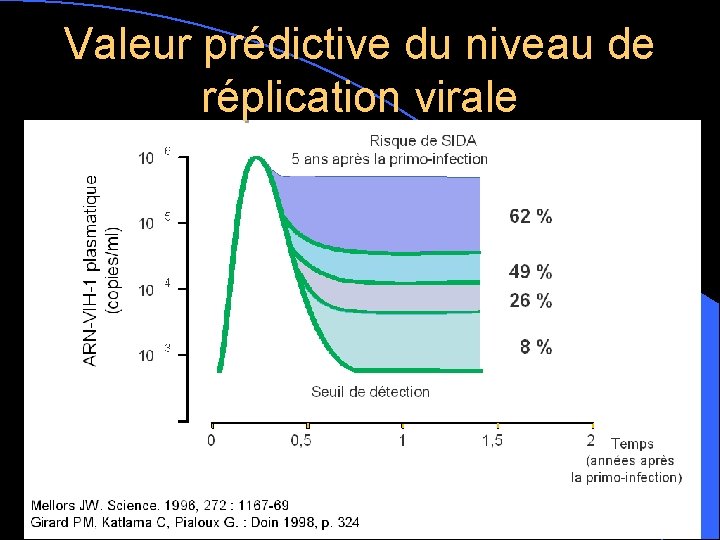
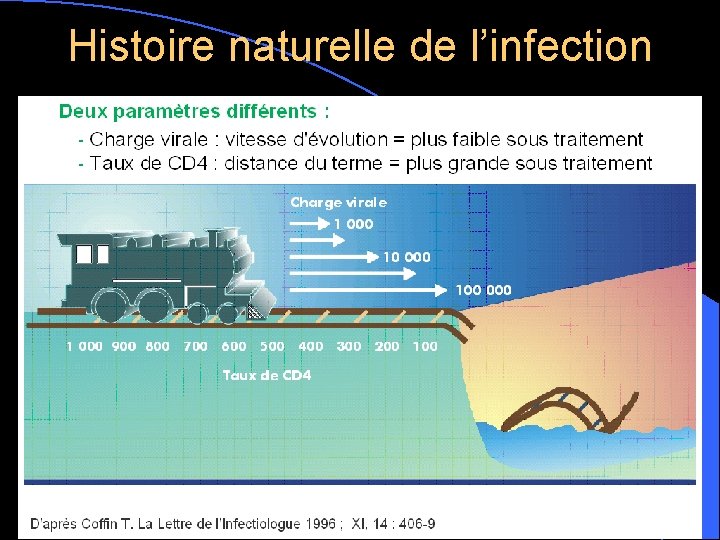
Valeur prédictive du niveau de réplication virale

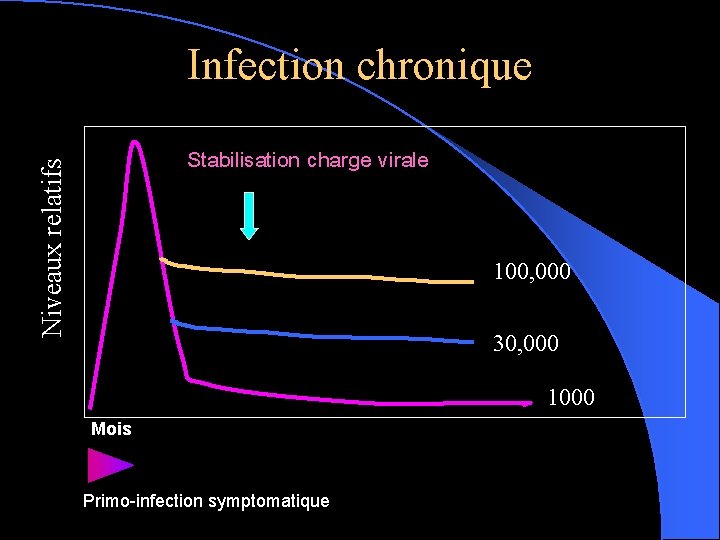
Infection chronique Niveaux relatifs Stabilisation charge virale 100, 000 30, 000 1000 Mois Primo-infection symptomatique

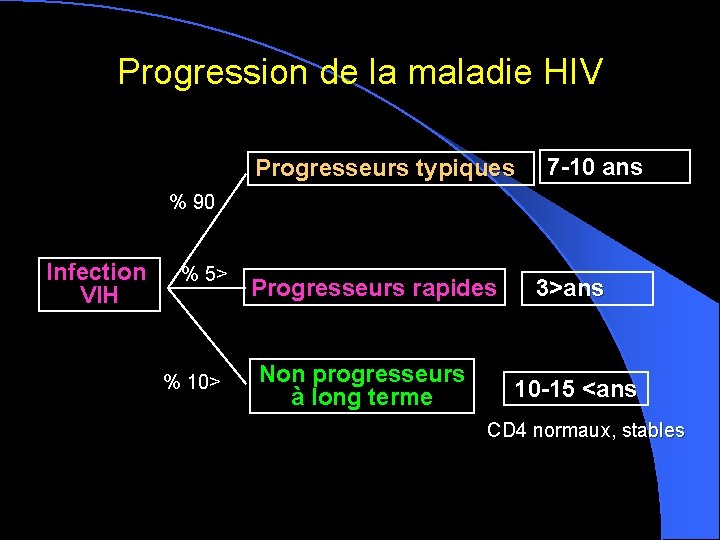
Progression de la maladie HIV Progresseurs typiques 7 -10 ans % 90 Infection VIH % 5> % 10> Progresseurs rapides Non progresseurs à long terme 3>ans 10 -15 <ans CD 4 normaux, stables

Charge virale et CD 4 sont des marqueurs de progression de la maladie Le niveau de stabilisation de la charge virale prédit la vitesse de progression de la maladie VIH

Histoire naturelle

Histoire naturelle de l’infection

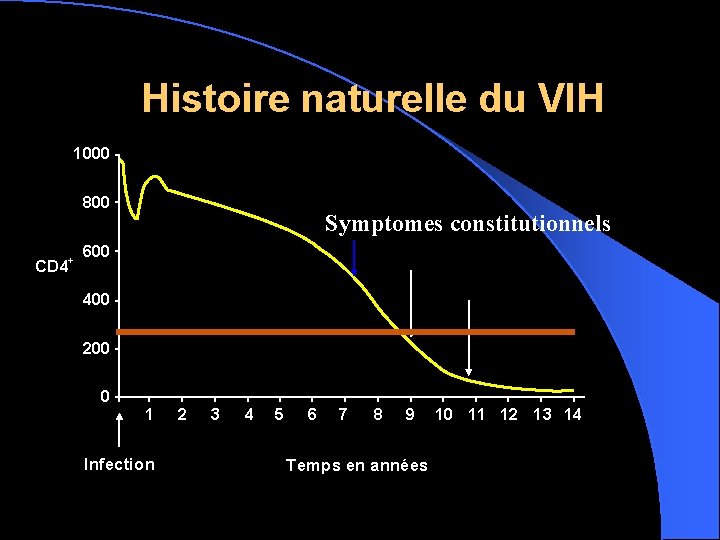
Histoire naturelle du VIH 1000 800 CD 4+ Symptomes constitutionnels 600 400 200 0 1 Infection 2 3 4 5 6 7 8 9 Temps en années 10 11 12 13 14

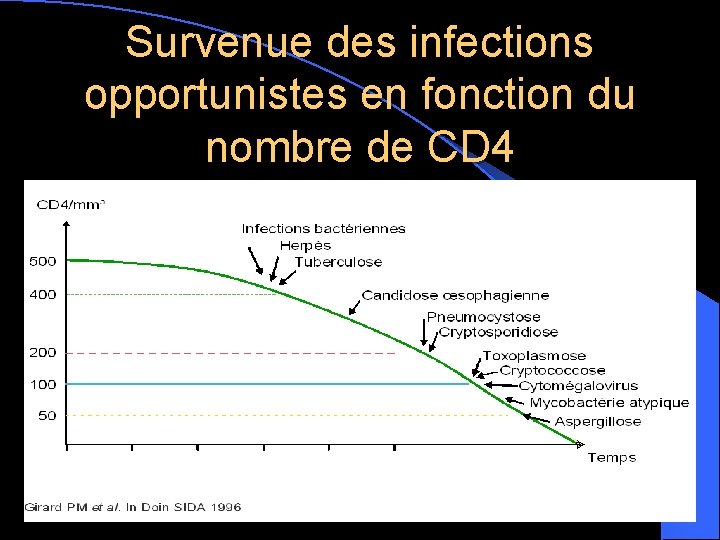
Survenue des infections opportunistes en fonction du nombre de CD 4

Pathogène opportuniste Hôte Agent pathogène Statut immunitaire de l’hôte Maladie

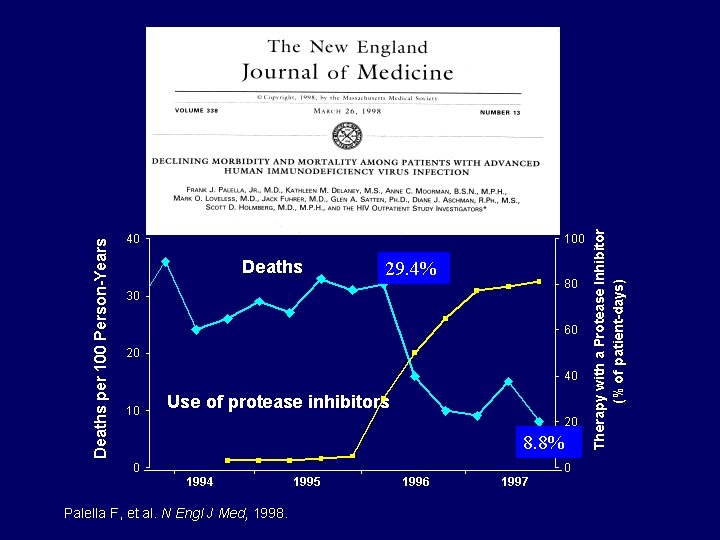
Effet des trithérapies antirétrovirales (HAART) sur l’histoire naturelle du VIH

29. 4% 8. 8%

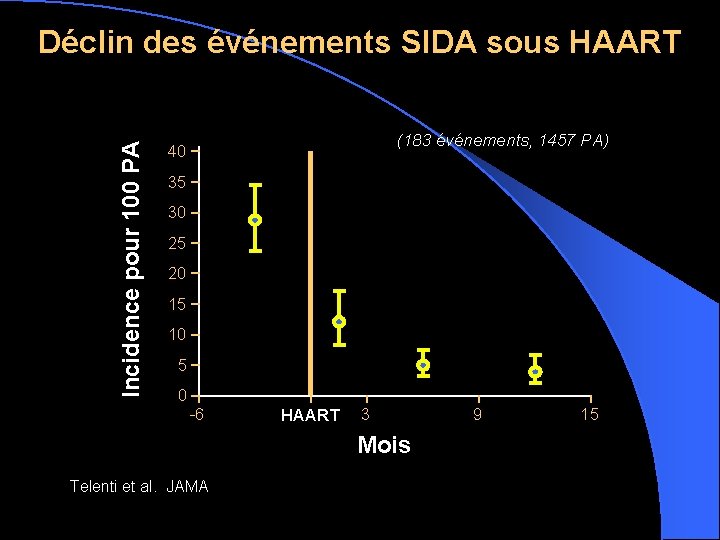
Incidence pour 100 PA Déclin des événements SIDA sous HAART (183 événements, 1457 PA) 40 35 30 25 20 15 10 5 0 -6 HAART 3 Mois Telenti et al. JAMA 9 15

Raison l Déficit immunitaire = responsable de la mortalité et de la morbidité dans l’infection VIH l HAART restaure l’immunité

Classification OMS

Intérêts d’une classification l Prise en charge – Rationalisation des stratégies Prophylaxies l ARV l l Collectif : données épidémiologiques – Évaluation / validation des stratégies – Comparaisons / partage d’expérience

l Stade I : 1. Asymptomatique 2. Lymphadénopathies généralisées l Stade II: 3. Perte de poids, < 10% du poids corporel 4. Manifestations cutanéo-muqueuses mineures (dermatose séborrhéique, prurigo, mycoses unguéales, ulcérations buccales récurrentes, chéilite angulaire) 5. Zona dans les cinq dernières années 6. Sinusite bactérienne récurrentes Et/ou échelle de performance 2 : symptomatique, activité normale

l Stade III : 7. Perte de poids, > 10 % du poids corporel 8. Diarrhée chronique inexpliquée, > 1 mois 9. Fièvre prolongée non expliquée (intermittente ou constante) , > 1 mois 10. Candidose buccale (muguet) 11. Leucoplasie chevelue de la cavité buccale 12. Tuberculose pulmonaire 13. Infections bactériennes graves (c’est-à-dire pneumonie, pyomyositis) Et/ou échelle de performance 3 : alité < 50% du jour durant le dernier mois.

l Stade IV: 14. Syndrome cachectique dû au VIH 15. Pneumopathie pneumocystis jirovecii 16. Toxoplasmose cérébrale 17. Cryptosporidiose avec diarrhée > 1 mois 18. Cryptococcose extrapulmonaire 19. Maladie cytomégalovirus d’un organe autre que foie, rate ou nodule lymphatique (ex: rétinite) 20. Infection au virus Herpes simplex, mucocutanée (> 1 mois) ou viscérale 21. Leucoencéphalopathie multifocale progressive 22. Toute mycose endémique disséminée 23. Candidose de l’œsophage, de la trachée, des bronches

Suite stade IV: 24. Mycobactériose atypique, disséminée ou pulmonaire 25. Septicémie à salmonelle non-typhoïdique 26. Tuberculose extrapulmonaire 27. Lymphome 28. Sarcome de Kaposi 29. Encéphalopathie VIH Et/ou échelle de performance 4 : alité > 50% de la journée durant le dernier mois.

Classification OMS selon manifestations cliniques EXERCICE

Exercice: classification OMS 1 OMS 2 OMS 3 OMS 4

Effet du HAART sur les manifestations cliniques HAART