VIII Chemick reakce KINETIKA Chemick kinetika se zabv

VIII. Chemické reakce : KINETIKA Chemická kinetika se zabývá rychlostí reakce.

CHEMICKÉ REAKCE - obecně: Při chemické reakci se přeskupují částice, zanikají staré chemické vazby, vznikají nové. Příčinou je srážka částic; při ní někdy chemická reakce proběhne, někdy ne. KDY reakce proběhne ? ?
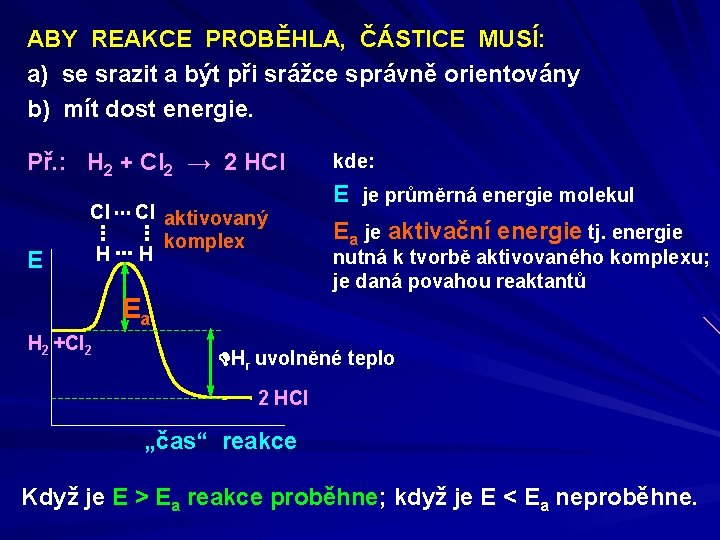
ABY REAKCE PROBĚHLA, ČÁSTICE MUSÍ: a) se srazit a být při srážce správně orientovány b) mít dost energie. Př. : H 2 + Cl 2 → 2 HCl Cl E H Cl aktivovaný komplex H kde: E je průměrná energie molekul Ea je aktivační energie tj. energie nutná k tvorbě aktivovaného komplexu; je daná povahou reaktantů Ea H 2 +Cl 2 Hr uvolněné teplo 2 HCl „čas“ reakce Když je E > Ea reakce proběhne; když je E < Ea neproběhne.

ZAJÍMÁ NÁS: Ø Za jakou dobu dostaneme produkt ? (chem. kinetika) Ø Kolik produktu vznikne ? (chemická rovnováha) Ø Jaké bude tepelné zbarvení reakce ? (chem. thermodynamika) Ø Co chemickou reakcí vznikne ? Na to není obecně jednoznačná odpověď. Pro určité typy chem. reakcí známe přesnou odpověď a ty se dále naučíme. V ostatních případech lze produkty odhadnout pomocí: • zkušenosti či • znalosti podobné reakce (podobné chemicky, tj např. polohou prvků ve stejné skupině PSP)
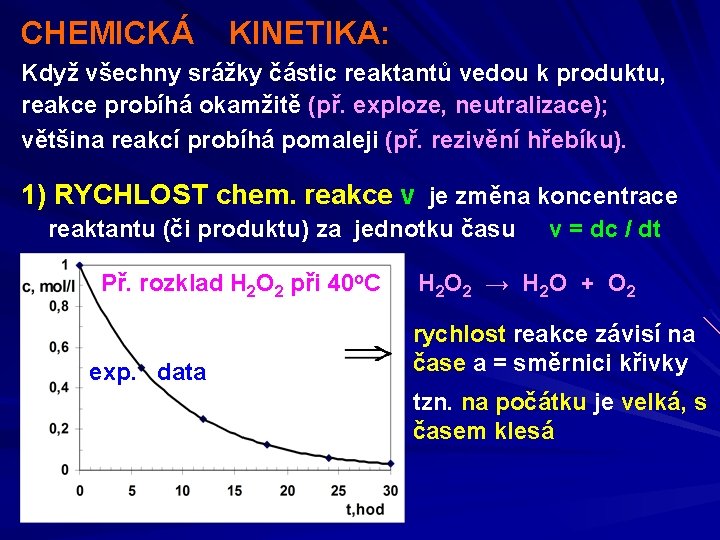
CHEMICKÁ KINETIKA: Když všechny srážky částic reaktantů vedou k produktu, reakce probíhá okamžitě (př. exploze, neutralizace); většina reakcí probíhá pomaleji (př. rezivění hřebíku). 1) RYCHLOST chem. reakce v je změna koncentrace reaktantu (či produktu) za jednotku času Př. rozklad H 2 O 2 při 40 o. C exp. data v = dc / dt H 2 O 2 → H 2 O + O 2 rychlost reakce závisí na čase a = směrnici křivky tzn. na počátku je velká, s časem klesá

2) CO OVLIVŇUJE RYCHLOST a JAK ? Rychlost je tím větší, čím je : • větší četnost srážek • • větší energie částic menší Ea (aktivační energie) Rychlost ovlivňuje : a) Koncentrace reaktantů (čím je větší, tím je četnost srážek větší, tím je rychlost větší) pro obecnou reakci : a. A + b. B → c. C + d. D (a, b, c, d jsou stech. koeficienty) je rychlost : v = k * c. Ai * c. Bj , kde k je rychlostní konstanta a i, j určíme z experimentů

b)Teplota –vliv velký (čím větší T, tím je větší rychlost i energie částic a četnost srážek a tím větší je rychlost reakce) Př. : ještěrka, vaření, lednice Platí : k = A * e( - Ea / R T ) , kde k je rychlostní konstanta, A je konstanta Ea je aktivační energie Jen FBI : Velká Ea znamená velkou závislost k na T a obráceně : Př. : Hoření vodíku: Hoření fosforu: 2 H 2 + O 2 → 2 H 2 O P 4 + 5 O 2 → 2 P 2 O 5 Ea je velká Ea je malá K zapálení H 2 nutná větší iniciace. Pak hoření explozivní, rychlost obrovská. K zapálení P 4 stačí malá iniciace (třením). Pak hoření klidné, rychlost „malá“.

SAMOVZNÍCENÍ látek: (u reakcí uvolňujících teplo a kde je zároveň pomalý odvod tepla do okolí) Zpočátku : reakce pomalá, uvolní se málo tepla, látka teplo částečně pohltí, její teplota T roste. S rostoucí T: roste rychlost reakce, uvolňuje se více tepla až dojde k samovznícení příp. k explozi. Pozn. : K samovznícení je obvykle nutné větší množství látky a delší čas. Př. : samovznícení hader napuštěných fermeží v uzavřeném malém prostoru Dále : VŠICHNI

c) Velikost plochy reaktantů (např. pro reakce, kde jedním reaktantem je plyn, druhým je pevná látka) Čím větší je plocha, tím větší je rychlost reakce. Př. : Zatápění – třísky, exploze v silech (snadné vznícení mouky, cukru ve vznosu ve vzduchu) d) Katalyzátor Snižuje aktivační energii, tím zvyšuje rychlost reakce. Reakcí se nespotřebovává. Většina průmyslových reakcí probíhá s katalyzátorem. Pozn. : Opačnou funkci má INHIBITOR. Zmenšuje rychlost reakce.
- Slides: 9