Vieelektronski atomi Spektar Izborna pravila Shrdingerova jednadba Aproksimacija
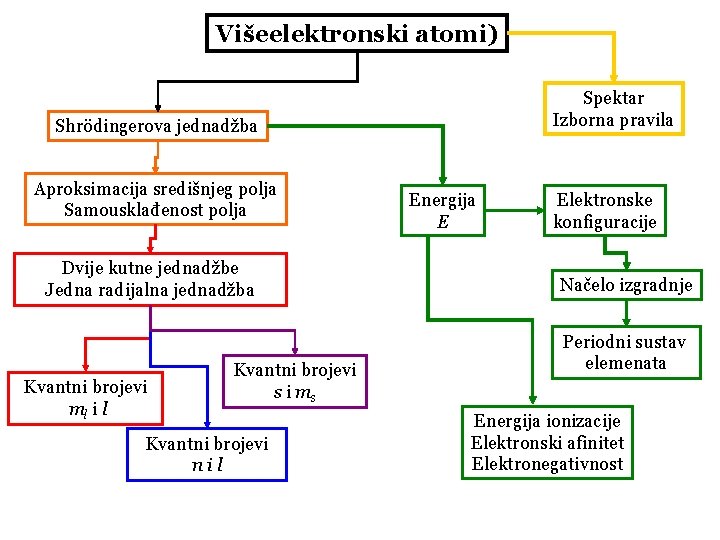
Višeelektronski atomi) Spektar Izborna pravila Shrödingerova jednadžba Aproksimacija središnjeg polja Samousklađenost polja Dvije kutne jednadžbe Jedna radijalna jednadžba Kvantni brojevi ml i l Kvantni brojevi s i ms Kvantni brojevi nil Energija E Elektronske konfiguracije Načelo izgradnje Periodni sustav elemenata Energija ionizacije Elektronski afinitet Elektronegativnost

He Prva aproksimacija: Druga aproksimacija:
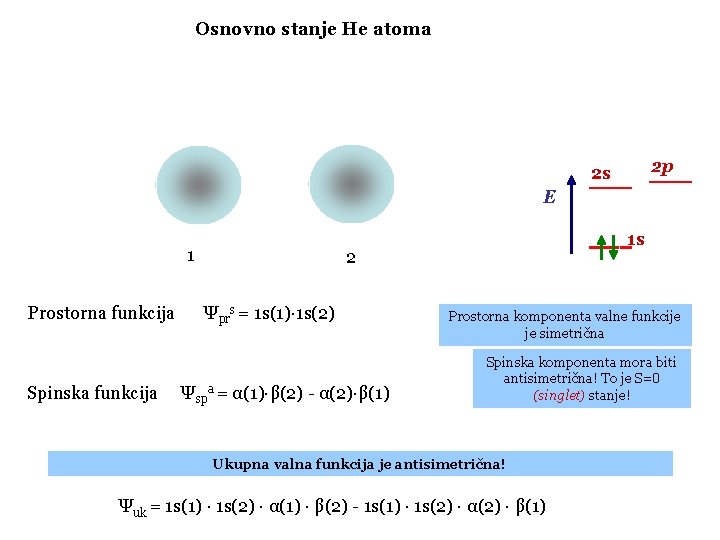
Osnovno stanje He atoma 2 p 2 s E 1 Prostorna funkcija Spinska funkcija 1 s 2 Ψprs = 1 s(1)· 1 s(2) Ψspa = α(1)·β(2) - α(2)·β(1) Prostorna komponenta valne funkcije je simetrična Spinska komponenta mora biti antisimetrična! To je S=0 (singlet) stanje! Ukupna valna funkcija je antisimetrična! Ψuk = 1 s(1) · 1 s(2) · α(1) · β(2) - 1 s(1) · 1 s(2) · α(2) · β(1)
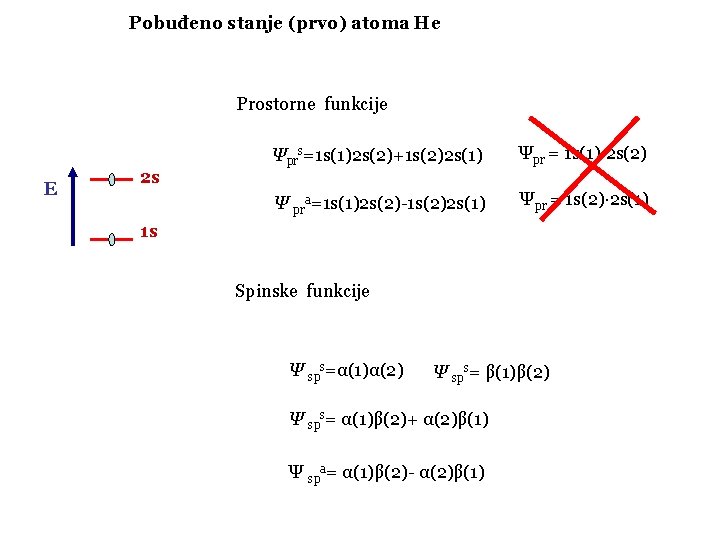
Pobuđeno stanje (prvo) atoma He Prostorne funkcije E 2 s Ψprs=1 s(1)2 s(2)+1 s(2)2 s(1) Ψpr = 1 s(1)· 2 s(2) Ψ pra=1 s(1)2 s(2)-1 s(2)2 s(1) Ψpr = 1 s(2)· 2 s(1) 1 s Spinske funkcije Ψ sps=α(1)α(2) Ψ sps= β(1)β(2) Ψ sps= α(1)β(2)+ α(2)β(1) Ψ spa= α(1)β(2)- α(2)β(1)

Pobuđeno stanje (prvo) atoma He 2 s E Y s=Yprs. Yspa Singletno stanje. Simetrična prostorna i antisimetrična spinska funkcija! 1 s Singlet (1 S 0) Ukupni spin je nula (S=0) Jedna spinska funkcija. Spinski multiplicitet je 1! Spinski multiplicitet je 2 S+1! 2 s 1 s Y t=Ypra. Ysps Tripletno stanje. Antisimetrična prostorna i simetrična spinska funkcija! Ukupni spin je 1 (S=1) Triplet (3 S 1) Tri spinske funkcije. Spinski multiplicitet je 3!
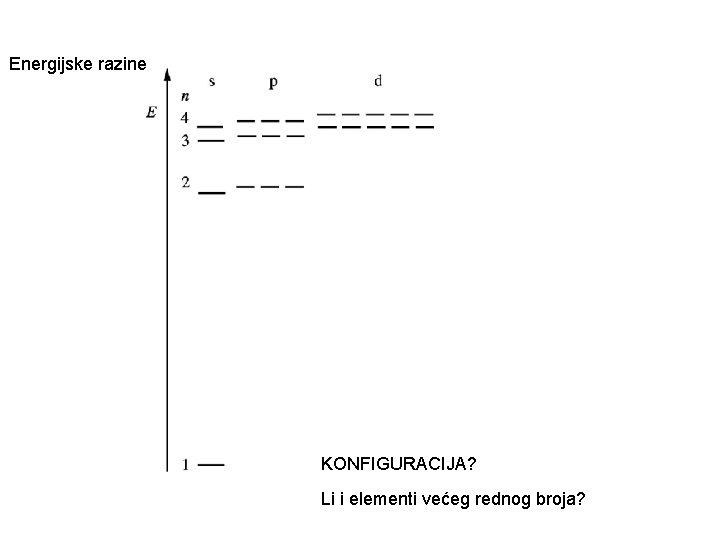
Energijske razine KONFIGURACIJA? Li i elementi većeg rednog broja?
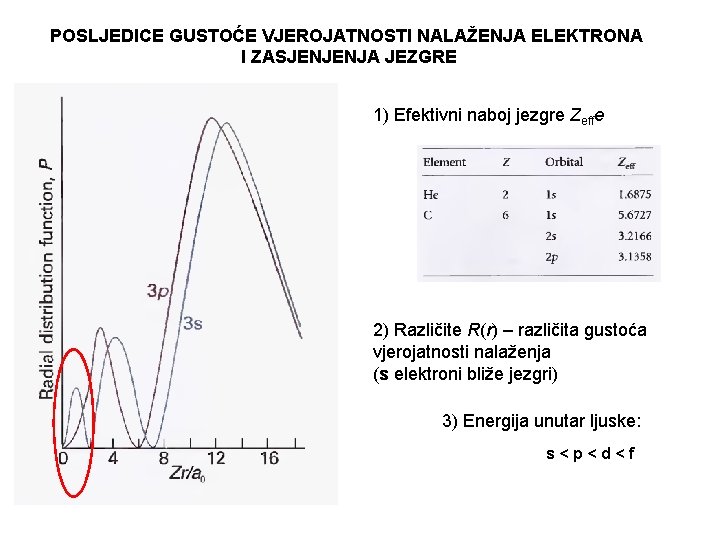
POSLJEDICE GUSTOĆE VJEROJATNOSTI NALAŽENJA ELEKTRONA I ZASJENJENJA JEZGRE 1) Efektivni naboj jezgre Zeffe 2) Različite R(r) – različita gustoća vjerojatnosti nalaženja (s elektroni bliže jezgri) 3) Energija unutar ljuske: s<p<d<f
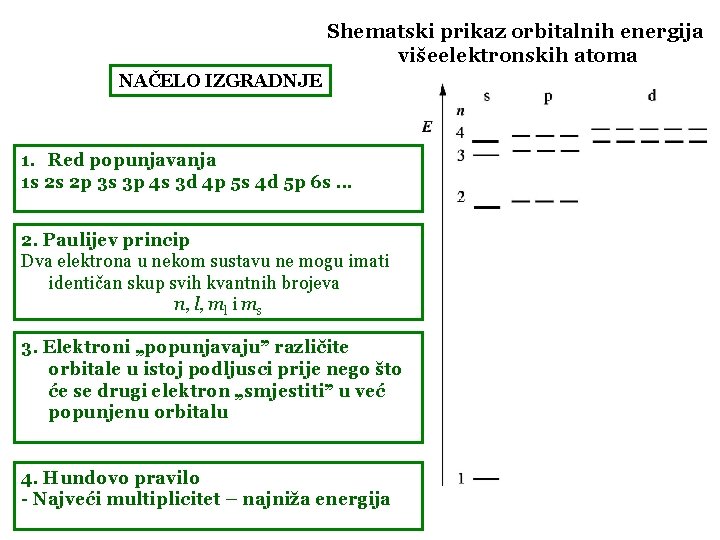
Shematski prikaz orbitalnih energija višeelektronskih atoma NAČELO IZGRADNJE 1. Red popunjavanja 1 s 2 s 2 p 3 s 3 p 4 s 3 d 4 p 5 s 4 d 5 p 6 s. . . 2. Paulijev princip Dva elektrona u nekom sustavu ne mogu imati identičan skup svih kvantnih brojeva n, l, ml i ms 3. Elektroni „popunjavaju” različite orbitale u istoj podljusci prije nego što će se drugi elektron „smjestiti” u već popunjenu orbitalu 4. Hundovo pravilo - Najveći multiplicitet – najniža energija

Poboljšanje valnih funkcija Aproksimacija središnjeg polja 1. i-ti elektron osjeća usrednjen potencijal ostalih elektrona 2. Potencijal je sferno simetričan Efektivni potencijal privlačenje jezgre (stabilizirajuće) Odbijanje između elektrona. Ovisi o svim elektronima! Taj potencijal je pozitivan (destabilizirajući)!

APROKSIMACIJA SREDIŠNJEG POLJA Svaki elektron osjeća uprosječeni potencijal svih ostalih elektrona. Takav potencijal ovisi o koordinatama elektrona ri. Schrödingerova jednadžba za Z elektrona može se rastaviti na Z jednadžbi za po jedan elektron! Valna funkcija opisuje stanje i-tog elektrona. Valna funkcija atoma (koji sadrži Z elektrona) je produkt Z takvih funkcija!

METODA SAMOUSKLAĐENOG POLJA Douglas Hartee & Vladimir Fock Metoda iteracije Rješenje Schrödingerove jednadžbe -dvije kutne funkcije – jednake kao i za jednoelektronski atom - jedna radijalna funkcija – drugačija zbog efektivnog potencijala Odstupanja od eksperimentalnih vrijednosti 2 ppm

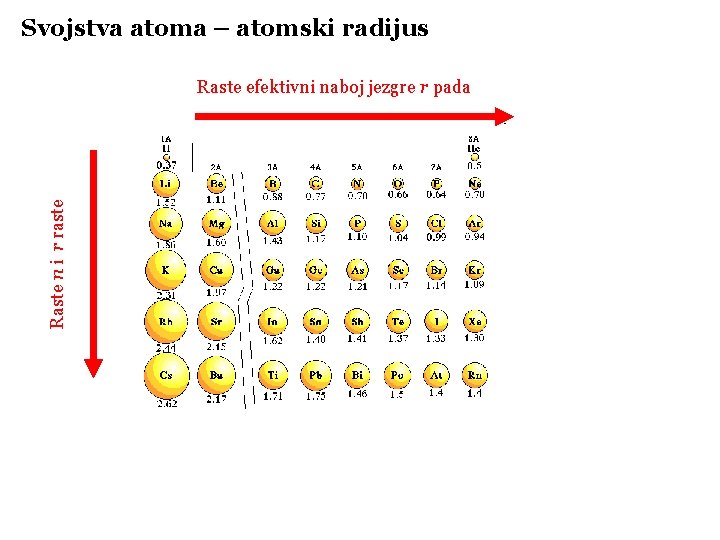
Svojstva atoma – atomski radijus Raste n i r raste Raste efektivni naboj jezgre r pada

Promjena energije ionizacije (Ei) s porastom atomskog broja Z
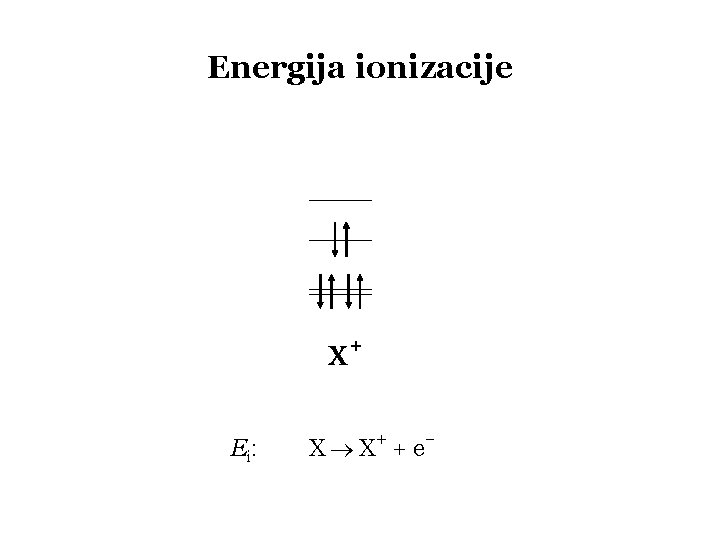
Energija ionizacije x+ Ei : X X+ + e –

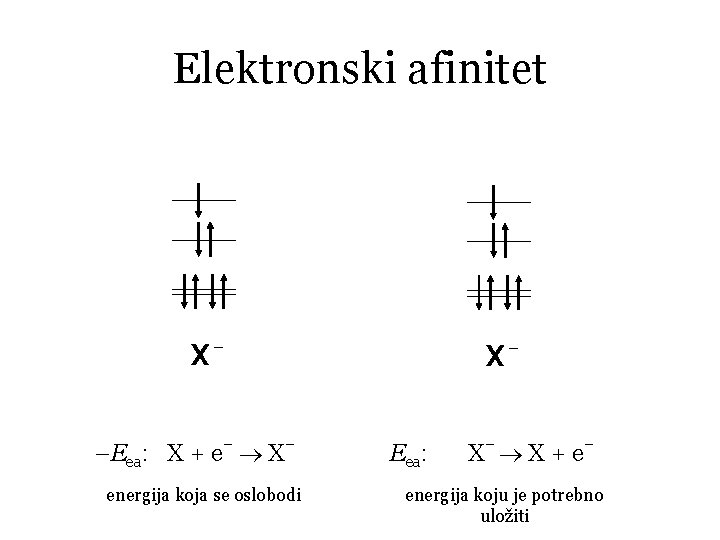
Elektronski afinitet x–Eea: X + e– X– energija koja se oslobodi x. Eea: X– X + e – energija koju je potrebno uložiti

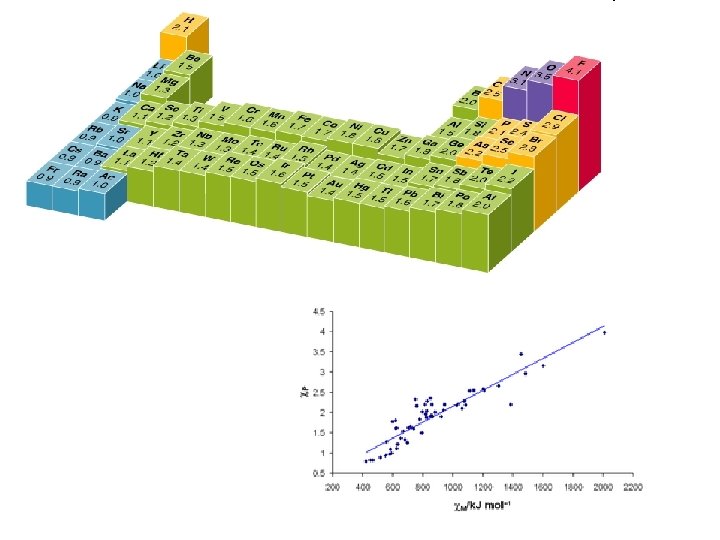
Elektronegativnost R. S. Mulliken L. Pauling
Višeelektronski atomi) Spektar Izborna pravila Shrödingerova jednadžba Aproksimacija središnjeg polja Samousklađenost polja Dvije kutne jednadžbe Jedna radijalna jednadžba Kvantni brojevi ml i l Kvantni brojevi s i ms Kvantni brojevi nil Energija E Elektronske konfiguracije Načelo izgradnje Periodni sustav elemenata Energija ionizacije Elektronski afinitet Elektronegativnost

Višeelektronski atomi 1. Po čemu se razlikuju energije višeelektronskih atoma od onih jednoelektronskih? 2. O koliko kvantnih brojeva ovisi energija elektrona u atomu? 3. Zbog čega su energijske razine višeelektronskih atoma u kvalitativnome smislu različite od onih kod atoma vodika? 4. Što je aproksimacija središnjeg polja? Periodičnost 1. 2. 3. 4. Kako se mijenja atomski radius unutar periodnog sustava elemenata? Objasnite linearnu ovisnost korijena prvih energija ionizacije o protonskom broju? Što je elektronski afinitet? Što je elektronegativnost? Simetrija valne funkcije 1. Zašto valna funkcija mora biti simetriča ili antisimetrična s obzirom na izmjenu para čestica? 2. Što su bosoni? 3. Što su fermioni? 4. U kakve čestice ubrajamo elektrone? 5. Kako glasi Paulijev princip?
- Slides: 21