vidences disponibles pour lutilisation de la dite ctogne

Évidences disponibles pour l’utilisation de la diète cétogène dans le traitement du diabète de type 2. Noémie Tremblay R 1 UMF Verdun

Qu’est-ce que c’est? Guide alimentaire canadien 2019 45 à 65% de glucides Terminologie de la diète faible en glucides Modérée 25 à 45% Faible < 25% Cétogène < 10% (20 à 50 g) **Méditerranéenne glucides 40% lipides 35% Sir William Osler 1900 Tx du diabète avant l’insuline 20 s Dr Atkin’s Diet Revolution 1972 Épilepsie, Alzheimer

Mécanismes d’action proposés 1. Augmentation de la satiété, la tendance à ingérer intuitivement moins de calories et diminution des hypoglycémies rebonds(7, 8) Effet annulé par comparatifs iso caloriques 2. “L’avantage métabolique” Perte de poids plus importante et une amélioration des facteurs de risque cardiovasculaires plus significative qu’une diète high carb isocalorique. (9, 10, 11) oxydation des graisses corporelles comme source d’énergie effet thermogénique diminution de la lipogenèse induite par les taux d’insuline élevés perte de calories via l’excrétion de cétones dans l’urine et la sudation
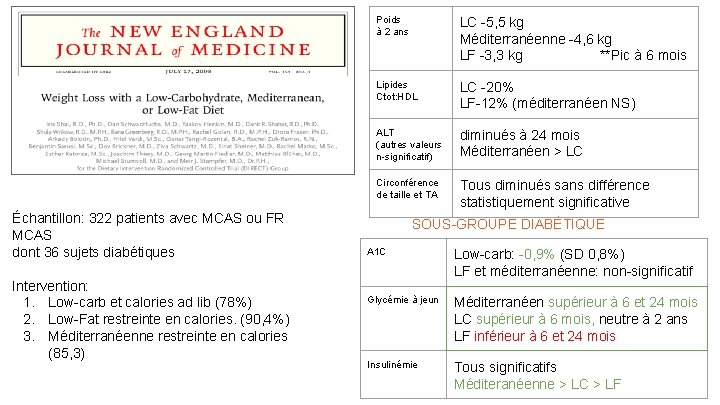
Échantillon: 322 patients avec MCAS ou FR MCAS dont 36 sujets diabétiques Intervention: 1. Low carb et calories ad lib (78%) 2. Low Fat restreinte en calories. (90, 4%) 3. Méditerranéenne restreinte en calories (85, 3) Poids à 2 ans LC 5, 5 kg Méditerranéenne 4, 6 kg LF 3, 3 kg **Pic à 6 mois Lipides Ctot: HDL LC 20% LF 12% (méditerranéen NS) ALT (autres valeurs n significatif) diminués à 24 mois Méditerranéen > LC Circonférence de taille et TA Tous diminués sans différence statistiquement significative SOUS GROUPE DIABÉTIQUE A 1 C Low carb: 0, 9% (SD 0, 8%) LF et méditerranéenne: non significatif Glycémie à jeun Méditerranéen supérieur à 6 et 24 mois LC supérieur à 6 mois, neutre à 2 ans LF inférieur à 6 et 24 mois Insulinémie Tous significatifs Méditeranéenne > LC > LF
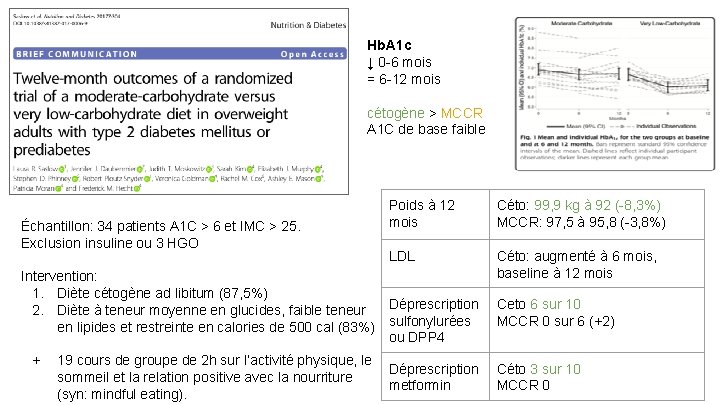
Hb. A 1 c ↓ 0 6 mois = 6 12 mois cétogène > MCCR A 1 C de base faible Échantillon: 34 patients A 1 C > 6 et IMC > 25. Exclusion insuline ou 3 HGO Poids à 12 mois Céto: 99, 9 kg à 92 ( 8, 3%) MCCR: 97, 5 à 95, 8 ( 3, 8%) LDL Céto: augmenté à 6 mois, baseline à 12 mois Intervention: 1. Diète cétogène ad libitum (87, 5%) Déprescription 2. Diète à teneur moyenne en glucides, faible teneur en lipides et restreinte en calories de 500 cal (83%) sulfonylurées ou DPP 4 + 19 cours de groupe de 2 h sur l’activité physique, le sommeil et la relation positive avec la nourriture (syn: mindful eating). Déprescription metformin Ceto 6 sur 10 MCCR 0 sur 6 (+2) Céto 3 sur 10 MCCR 0

Hb. A 1 C Céto 0, 8% ( 1, 1 à 0, 6) Plate non significatif Poids Céto 12, 7 kg ( 16, 1 à 9, 2) Plate non significatif Triglycérides Céto 60, 1 mg/d. L( 91, 3 à 28, 9) Plate 6, 2 mg/dl ( 46, 0 à 33, 6) aucun effet HDL et LDL Modification Rx aucune statistiquement significative Échantillon: 25 patients diabétique Hb. A 1 C > 6, 5 et IMC >25 SEULEMENT sous metformin Intervention Programme de 32 semaines en ligne a. diète cétogène ad libitum (n=12) + capsules vidéo sur le concept du “mindful eating”, le sommeil et l’activité physique pas de capsules vidéo sur les autres aspects que la diète a. “plate method” (n=13) Expérience subjective; “moins difficile à suivre et donnait une plus grande impression de santé”. Adhérence Céto: 11 sur 12 Plate: 7 sur 13
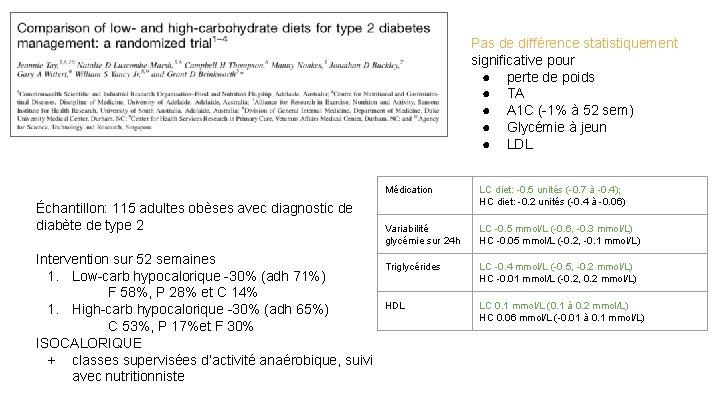
Pas de différence statistiquement significative pour ● perte de poids ● TA ● A 1 C ( 1% à 52 sem) ● Glycémie à jeun ● LDL Échantillon: 115 adultes obèses avec diagnostic de diabète de type 2 Intervention sur 52 semaines 1. Low carb hypocalorique 30% (adh 71%) F 58%, P 28% et C 14% 1. High carb hypocalorique 30% (adh 65%) C 53%, P 17%et F 30% ISOCALORIQUE + classes supervisées d’activité anaérobique, suivi avec nutritionniste Médication LC diet: 0. 5 unités ( 0. 7 à 0. 4); HC diet: 0. 2 unités ( 0. 4 à 0. 06) Variabilité glycémie sur 24 h LC 0. 5 mmol/L ( 0. 6, 0. 3 mmol/L) HC 0. 05 mmol/L ( 0. 2, 0. 1 mmol/L) Triglycérides LC 0. 4 mmol/L ( 0. 5, 0. 2 mmol/L) HC 0. 01 mmol/L ( 0. 2, 0. 2 mmol/L) HDL LC 0. 1 mmol/L (0. 1 à 0. 2 mmol/L) HC 0. 06 mmol/L ( 0. 01 à 0. 1 mmol/L)
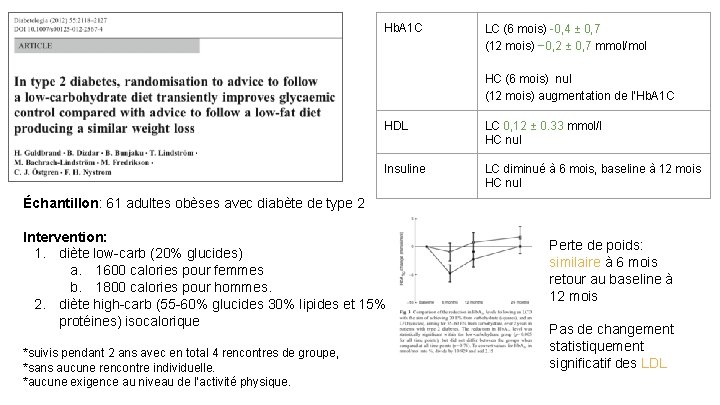
Hb. A 1 C LC (6 mois) 0, 4 ± 0, 7 (12 mois) − 0, 2 ± 0, 7 mmol/mol HC (6 mois) nul (12 mois) augmentation de l’Hb. A 1 C HDL LC 0, 12 ± 0. 33 mmol/l HC nul Insuline LC diminué à 6 mois, baseline à 12 mois HC nul Échantillon: 61 adultes obèses avec diabète de type 2 Intervention: 1. diète low carb (20% glucides) a. 1600 calories pour femmes b. 1800 calories pour hommes. 2. diète high carb (55 60% glucides 30% lipides et 15% protéines) isocalorique *suivis pendant 2 ans avec en total 4 rencontres de groupe, *sans aucune rencontre individuelle. *aucune exigence au niveau de l’activité physique. Perte de poids: similaire à 6 mois retour au baseline à 12 mois Pas de changement statistiquement significatif des LDL

Discussion ● Amélioration significative poids et le contrôle glycémique à 6 mois ● Amélioration variable des FR de MCAS ○ ● l’augmentation des HDL, diminution des triglycérides(13, 16, 17) Études isocaloriques (16, 17) ○ perte de poids comparable avec la diète faible en gras ○ besoins en hypoglycémiants, la variabilité glycémique et le bilan lipidique (HDL et triglycérides) améliorés sous diète cétogène (l’avantage métabolique) **études sont de faible envergure. ● Perte de poids est associée à un meilleur contrôle glycémique ○ Amélioration de ll’hémoglobine glyquée, du taux de HDL et de l’insulinémie après la période critique de 6 mois de perte de poids ● La diète cétogène est donc non inférieure à la diète faible en gras ○ vs. méditeranéenne? une question d’adhérence ● Dé prescription de médication comme issue secondaire ● Efficacité évidente des méthodes comportementale, du support, du suivi rapproché par différents professionnels ● Sécurité à long terme?

Conclusion La diète cétogène est non inférieure à la diète à faible teneur en gras pour la perte de poids et le contrôle glycémique. supériorité? données de qualité sub optimale. L’utilisation de la diète cétogène pourrait être recommandée par le clinicien dans le contrôle du diabète de type 2, en association avec des méthodes comportementales rigoureuses + un suivi étroit soit fait avec un médecin qualifié + études de sécurité à long terme soient publiées.

Bibliographie 1. 2. 3. Atkins RC. “Dr Atkins diet revolution. ” 1ère Édition. New York: David Mc. Kay Company, 1972: 1– 310. Osler W. The principles and practice of medicine. New York: D. Appleton and Company, 1978: 2– 1079. Allen FM, Stillman E, Fitz R. Total dietary regulation in the treatment of diabetes. No. 11. New York: The Rockerfeller Institute for Medical Research, 1919: 1– 650. 4. Baranano KW, Hartman ALThe Ketogenic Diet: Uses in Epilepsy and Other Neurologic Illnesses, Curr Treat Options Neurol. 2008 Nov; 10(6): 410– 419. 5. Gouvernement du Canada, Guide Alimentaire Canadien, Publication janvier 2019 < https: //guide alimentaire. canada. ca/fr/recommandations en matiere dalimentation saine/prenez habitude de manger legumes fruits grains entiers proteines/ > 6. Feinman RD, Pogozelski WK, Astrup A, et al. Dietary carbohydrate restriction as the first approach in diabetes management: critical review and evidence base. Nutrition 2015; 31: 1– 13. 7. Nickols Richardson SM, Coleman MD, Volpe JJ, et al. Perceived hunger is lower and weight loss is greater in overweight premenopausal women consuming a low carbohydrate/high protein vs high carbohydrate/low fat diet. J Am Diet Assoc 2005; 105: 1433– 7. 8. Melanson KJ, Westerterp Plantenga MS, Saris WH, et al. Blood glucose patterns and appetite in time blinded humans: carbohydrate versus fat. Am J Physiol 1999; 277: R 337 – 45. 9. Feinman RD, Fine EJ. Thermodynamics and metabolic advantage of weight loss diets. Metab Syndr Relat Disord 2003; 1: 209– 19. 10. Feinman RD, Fine EJ. ‘A calorie is a calorie’ violates the second law of thermodynamics. Nutr J 2004; 3: 9. 11. Volek JS, Freidenreich DJ, Saenz C, et al. Metabolic characteristics of keto adapted ultra endurance runners. Metab Clin Exp 2016; 65: 100– 10. 12. Fabbrini E, Higgins PB, Magkos F, et al. Metabolic response to high carbohydrate and low carbohydrate meals in a nonhuman primate model. Am J Physiol Endocrinol Metab 2013; 304: E 444– 51. 13. Shai et al, Weight Loss with a Low Carbohydrate, Mediterranean, or Low Fat diet, New England Journal of Medicine, juillet 2008 14. Saslow et al, Twelve month outcomes of a randomized trial of a moderate carbohydrate versus very low carbohydrate diet in overweight adults with type 2 diabetes mellitus or prediabetes, Journal Nutrition and Diabetes, 2017 15. Saslow et al, An Online Intervention Comparing a Very Low Carbohydrate Ketogenic Diet and Lifestyle Recommendations Versus a Plate Method Diet in Overweight Individuals With Type 2 Diabetes: A Randomized Controlled Trial, Journal of Internet Medical Research, Février 2017 16. Tay et Al. “Comparison of low and high carbohydrate diets for type 2 diabetes management: a randomized tria”l, American Society for Nutrition 2015 17. Guldbrand et al, “In type 2 diabetes, randomisation to advice to follow a low carbohydrate diet transiently improves glycaemic control compared with advice to follow a low fat diet producing a similar weight loss”, Diabetologia, avril 2012 18. Gannon MC, Nuttall FQ. Control of blood glucose in type 2 diabetes without weight loss by modification of diet composition. Nutr Metab (Lond) 2006; 3: 16 19. Zhang Q. , Xu L. Treatment of Diabetic Mice with a Combination of Ketogenic Diet and Aerobic Exercise via Modulations of PPARs Gene Programs, PPAR research Aout 2017
- Slides: 11