VI DERIVAI FUNCIONALI AI ACIZILOR CARBOXILICI Conf Dr

VI. DERIVAŢI FUNCŢIONALI AI ACIZILOR CARBOXILICI Conf. Dr. Anca Peter

• Majoritatea derivaţilor funcţionali ai acizilor carboxilici, pot fi derivaţi formal prin înlocuirea grupei hidroxil sau a oxigenului carbonilic (în unii, a ambelor grupe) cu grupe nucleofile. VI. 1. HALOGENURI ACIDE VI. 1. 1. Nomenclatură • Halogenurile acide se denumesc ca halogenuri de acil (de exemplu, formulele (VI. 1), (VI. 2) şi (VI. 3)). • În cazul moleculelor mai complicate (VI. 4), gruparea -CO-Cl de acetil clorură de benzoil clorură de fenil-acetil se clorură consideră ca substituent, numit cloroformil. (VI. 1) (VI. 2) (VI. 3)

acid 3 -cloroformil-benzoic (VI. 4) VI. 1. 2. Metode de sinteză 1. Tratarea acizilor cu clorură de tionil (SOCl 2) sau cu halogenuri de fosfor (PX 3 sau PX 5), la temperatura camerei sau la slabă încălzire. • Utilizarea clorurii de tionil prezintă avantajul că duce la formarea clorurii acide în stare practic pură, produşii secundari ai reacţiei şi excesul de reactant fiind volatili.

2. Fluorurile şi iodurile acide se obţin din cloruri acide prin tratare cu HF, respectiv cu HI (r. VI. 2) sau cu ioduri alcalino-pământoase. (VI. 2) X = F, I • Fluorura de acetil se obţine din anhidridă acetică şi acid fluorhidric anhidru, conform r. VI. 3. (VI. 3) • Dintre toate aceste categorii de halogenuri acide, cele mai multe utilizări practice le au clorurile. VI. 1. 3. Proprietăţi fizice • Halogenurile acizilor inferiori sunt lichide lacrimogene incolore, cu miros înţepător şi care fumegă la aer. Cele acizilor superiori sunt substanţe solide. Au puncte de fierbere inferioare acizilor din care provin. Sunt substanţe stabile şi se pot distila fără descompunere.

• Clorurile acide turnate în apă, cad întâi la fundul vasului fiind insolubile, apoi reacţionează cu aceasta. Reacţia cu apa este cu atât mai energică, cu cât acidul corespunzător clorurii este mai solubil în apă (de exemplu, clorura de acetil reacţionează violent cu apa, iar cea de benzoil mult mai lent). VI. 1. 4. Proprietăţi chimice 1. Reacţii de substituţie a halogenului prin tratare cu: § apa, când se formează acizi (VI. 4 a), § alcoolii, când se obţin esteri (VI. 4 b), § amoniacul, când rezultă amide (VI. 4 c), § amine primare (VI. 4 d) şi secundare, când se obţin amine acilate (amide substituite), § fenolii (VI. 4 e) sau fenoxizii metalelor alcaline, când se formează esterii fenolilor.

(VI. 4 a) (VI. 4 b) (VI. 4 c) (VI. 4 d) (VI. 4 e) 2. Reducerea catalitică. Utilizând catalizatori cu acţiune atenuantă (Pd “otrăvit” cu o soluţie de sulf în chinolină), reducerea clorurilor acide, în special a celor aromatice, poate fi oprită la stadiu de aldehide (VI. 5). Reducerea cu hidrură de aluminiu (Li. Al. H 4) conduce la alcooli, foarte probabil prin intermediul unei aldehide. (VI. 5) 3. Reacţia cu compuşi organo-metalici conduce la alcooli terţiari (r. VI. 6). Intermediar se formează o cetonă care reacţionează mai departe cu excesul de compus organo-magnezian (a se vedea cap. IV. 3).

(VI. 6) 4. Reacţii ale ionului acil (Friedel - Crafts). În prezenţa Al. Cl 3, clorurile acide reacţionează cu hidrocarburile aromatice, formând cetone mixte (r. VI. 7) sau aromatice. (VI. 7) VI. 1. 5. Reprezentanţi 1. Clorura de formil (HCOCl) este instabilă şi nu se formează prin reacţia directă a acidului, ci din CO şi HCl uscat, la 60 C. 2. Fluorura de formil (HCOF) se obţine prin reacţia fluorurii de benzoil cu HCOOH, la 100 C (r. VI. 8). Este stabilă la temperaturi joase, la cea ambiantă descompunându-se lent. (VI. 8)

3. Clorura de acetil (CH 3 -CO-Cl) se obţine: • Industrial, din acid acetic sau anhidridă acetică şi fosgen (COCl 2), la temperatură ridicată (r. VI. 9 a şi VI. 9 b). (VI. 9 a) (VI. 9 b) • din reacţia acetatului de sodiu anhidru cu halogenuri acide anorganice (SO 2 Cl 2, SOCl 2, PX 3, etc. ), conform r. VI. 10. (VI. 10) • prin adiţia HCl la cetenă (CH 2=C=O), conform r. VI. 11. (VI. 11) • Se utilizează pentru introducerea grupării acetil în fenoli sau amine şi la obţinerea acetofenonei. 4. Clorura de benzoil (C 6 H 5 -CO-Cl) se obţine industrial prin hidroliza parţială a fenil-tricloro-metanului (r. VI. 12). (VI. 12)

• Se utilizează la benzoilarea aminelor, alcoolilor, fenolilor şi la obţinerea peroxidului de benzoil. 5. Clorura de oxalil (Cl. OC-COCl) se formează prin reacţia acidului oxalic cu PCl 5, conform r. VI. 13. (VI. 13) • Lucrând cu clorura de oxalil, în anumite condiţii, aceasta poate reacţiona ca CO datorită transformării VI. 14, fiind posibilă sinteza unor cetone. De asemenea, se utilizează la obţinerea de -dicetone prin sinteza Friedel-Crafts. (VI. 14) 6. Clorura de ftalil (VI. 5) se obţine din anhidridă ftalică şi PCl 5 (r. VI. 15). (VI. 15)

• În prezenţă de Al. Cl 3 se izomerizează, conform r. VI. 16, la un derivat ciclic (dicloro-ftalida). În această formă participă la reacţii Friedel-Crafts. (VI. 16) VI. 2. ANHIDRIDE ALE ACIZILOR CARBOXILICI • Rezultă prin eliminarea 1 molecule de apă între 2 grupări carboxil (r. VI. 17). (VI. 17) VI. 2. 1. Nomenclatură • Anhidridele formate din acelaşi acid se denumesc prin adăugarea termenului „anhidridă” la numele acidului, ((VI. 6), (VI. 7) şi (VI. 8)). La anhidridele formate din acizi diferiţi, se face precizarea de „anhidridă mixtă” (VI. 9).

anhidridă acetică (VI. 6) 1. anhidridă succinică (VI. 7) anhidridă maleică (VI. 8) anhidridă mixtă acetică-benzoică (VI. 9) VI. 2. 2. Metode de sinteză Metoda generală de sinteză constă în tratarea sărurilor de Na ale acizilor cu clorurile acide respective (VI. 18) • La termenii superiori este posibilă reacţia directă dintre (VI. 19) acidul carboxilic şi clorura sa acidă (r. VI. 19). • Se mai pot obţine din acizi carboxilici şi cantităţi mici (sub cele stoechiometrice) de SOCl 2, când se formează clorura acidă (a se vedea r. VI. 1 a), care reacţionează cu

2. Anhidridele mixte se obţin prin adiţia carboxilici la cetenă, conform r. VI. 20. acizilor (VI. 20) • Acestea disproporţionează, în amestecul format, în 2 anhidride simetrice (r. VI. 21). (VI. 21) • Anhidrida acetică se îndepărtează din amestec prin distilare, având p. f. scăzut. 3. Anhidridele cu cicluri de cinci atomi, se formează prin simpla încălzire a acizilor 1, 4 -dicarboxilici respectivi. În acest mod, din acidul ftalic se obţine anhidrida ftalică (r. VI. 22), iar din acidul maleic cea maleică (VI. 8). (VI. 22)

• • • 1. VI. 2. 3. Proprietăţi fizice Anhidridele acizilor inferiori sunt lichide stabile, distilabile, cu miros înţepător asemănător acizilor respectivi. Cele superioare sunt substanţe solide, cristaline, inodore. Au p. f. superioare celor ale acizilor corespunzători. VI. 2. 4. Proprietăţi chimice Reacţii de acilare. Anhidridele sunt agenţi de acilare, reacţionând cu apa (lent), cu alcoolii şi cu aminele (VI. 23 a, b şi c). (VI. 23 a) (VI. 23 b) (VI. 23 c)

2. Reacţia Friedel-Crafts. Anhidridele reacţionează cu arenele, în prezenţă de Al. Cl 3, formând cetone (r. VI. 24). (VI. 24) Cetonele formate reţin 1 moleculă Al. Cl 3, motiv pentru care cantitatea de catalizator necesară este aparent necatalitică. 3. Reacţia de condensare. Anhidridele funcţionează ca şi componentă metilenică (r. VI. 26) în reacţii de condensare de tip aldoolic (a se vedea sinteza Perkin, cap. IV. 5. 3. 5). (VI. 26)

4. Reacţia de reducere cu Na(Hg) formează alcooli cu mic, deoarece concomitent cu reducerea are loc şi hidroliza. Un agent de reducere mai eficient este Li. Al. H 4. VI. 2. 5. Reprezentanţi 1. Anhidrida acidului formic (H-CO-O-CO-H) nu există. 2. Anhidrida mixtă acetică-formică (CH 3 -CO-O-CO-H) se obţine prin reacţia CH 3 COCl cu HCOONa (r. VI. 27). (VI. 27) 3. Anhidrida acetică (CH 3 -CO-O-CO-CH 3) se obţine industrial, alături de acetaldehidă, prin descompunerea termică a diacetatului de etiliden, format din acetatul de vinil, rezultat prin adiţia CH 3 COOH la C 2 H 2 (r. VI. 28). (VI. 28)

• • Cantităţi mari de anhidridă acetică se obţin prin oxidarea cu aer sau O 2 a CH 3 CHO, în prezenţă de catalizatori (acetat de cobalt şi de cupru), formându-se şi CH 3 COOH Cel mai avantajos se fabrică anhidrida acetică prin piroliza acidului acetic, r. VI. 29. (VI. 29) • Anhidrida acetică este utilizată în industria farmaceutică şi cea a parfumurilor, la obţinerea acetatului de celuloză (mătase), ca agent de acetilare, etc. 4. Anhidrida succinică (VI. 7) se obţine direct din acidul succinic prin încălzire, în prezenţă de anhidridă acetică sau clorură de acetil (r. VI. 30). (VI. 30)

• Reacţionează cu H 2 O, alcoolii şi NH 3 la fel ca anhidridele acizilor inferiori. De asemenea, reacţionează cu C 6 H 6 în prezenţă de Al. Cl 3 (reacţie Friedel-Crafts), conform r. VI. 31. (VI. 31)

5. Anhidrida maleică (VI. 8) se obţine industrial prin oxidarea catalitică a benzenului (VI. 32 a) sau prin oxidarea cu aer a furfurolului (VI. 32 b). (VI. 32 a) (VI. 32 b) • Fiind o filodienă, participă la sinteze dien. Este utilizată în industria materialelor plastice, la obţinerea de agenţi de dispersie şi udare. 6. Anhidrida ftalică (VI. 10) se obţine prin încălzirea acidului ftalic, cu câteva grade peste p. t. , (a se vedea r. VI. 22). anhidrida ftalică (VI. 10)

• Prin dizolvarea anhidridei ftalice în alcooli se obţin monoesteri(r. VI. 33 a), reacţie folosită ca metodă de dozare (VI. 33 a) • Esterii ftalici neutri se obţin în condiţii mai drastice, prin fierberea cu exces de alcool şi adaus de H 2 SO 4 (r. VI. 33 b). (VI. 33 b) • Anhidrida ftalică participă la r. Friedel-Crafts formând chinone. Reacţia serveşte la obţinerea industrială a antrachinonei (r. VI. 34). (VI. 34) • Grupele carbonilice din anhidrida ftalică au o reactivitate asemănătoare cu aldehidele şi cetonele (reacţiile VI. 35).

(VI. 35) • Prin încălzire cu CH 3 -CO-O-CO-CH 3, în prezenţa CH 3 COONa, are loc o condensare similară cu condensarea Perkin (r. VI. 36). (VI. 36) • Anhidrida ftalică se condensează cu fenolul, în prezenţa Zn. Cl 2 anhidră sau a altor agenţi de deshidratare, obţinându-se fenolftaleină (r. VI. 37). (VI. 37)

• În mod asemănător, prin condensare cu alţi fenoli se formează coloranţi ftaleinici, rodaminici, etc. • Anhidrida ftalică se utilizează la fabricarea antrachinonei, a răşinilor aldehidice, a esterilor ftalici care sunt la rândul lor plastifianţi. VI. 3. ESTERI AI ACIZILOR CARBOXILICI • Esterii sunt derivaţi funcţionali ai acizilor carboxilici în care grupa -OH din carboxil este înlocuită cu gruparea -OR. • Sunt produşi de eliminare de apă dintr-o moleculă de acid şi una de alcool, conform r. VI. 38. (VI. 38) VI. 3. 1. Nomenclatură • Numele esterilor se formează în mod analog cu numele sărurilor (de exemplu, formulele (VI. 11), (VI. 12) şi (VI. 13)).

etil acetat de etil (VI. 11) dietil malonat de etil (VI. 12) metil acrilat de metil (VI. 13) • Monoesterii acizilor dicarboxilici se denumesc analog cu sărurile acide (de exemplu, ftalat acid de etil (VI. 14)). ftalat acid de etil (VI. 14) • În compuşii cu structuri mai complexe, carboxilul esterificat se notează cu prefixul carboalcoxi (de exemplu, carbometoxi -COOCH 3, carbetoxi –COOC 2 H 5, etc. ) sau alcoxicarbonil. De exemplu, acid 1 -carbetoxi-ciclobutan-3 carboxilic sau acid 1 -etoxicarbonil-ciclobutan-3 -carboxilic (VI. 15)

VI. 3. 2. Metode de sinteză 1. Din derivaţi funcţionali ai acizilor şi alcooli sau fenoli. a) Din cloruri acide şi alcooli sau fenoli, conform r. VI. 39. (VI. 39) • R. are aplicaţii largi, decurgând practic cantitativ de la stânga la dreapta. Se obţin pe această cale, esteri ai acizilor şi alcoolilor care nu pot fi esterificaţi direct (r. VI. 40). (VI. 40) b) Din anhidride şi alcooli sau fenoli, conform r. VI. 41. (VI. 41) • Anhidridele au reactivitate puţin mai redusă decât clorurile acide, din cauza unei conjugări interne mai pronunţate, motiv pentru care, fără catalizator (H+), reacţionează lent dar incomparabil mai repede decât un acid. 2. Din cetenă şi alcooli sau fenoli, conform r. VI. 42.

(VI. 42) 3. Din sărurile de Ag sau K ale acizilor carboxilici şi compuşi halogenaţi alifatici primari, r. VI. 43. (VI. 43) • Metoda este utilizată la preparare de esteri ai alcoolilor instabili în prezenţă de acizi minerali (r. VI. 44). (VI. 44) 4. Din acizi liberi şi diazo-derivaţi alifatici, în special diazometan, se obţin esteri metilici, conform r. VI. 45. (VI. 45) 5. Adiţia acizilor organici la alchene (în special superioare), sub acţiunea catalitică a H 2 SO 4 sau a fluorurii de bor (BF 3), decurge conform r. VI. 46. (VI. 46) 6. Din aldehide alifatice, sub influenţa catalitică a etoxidului de aluminiu, se obţin esteri conform r. VI. 47 (r. Tiscenko).

(VI. 47) 7. Esterificarea directă (cea mai des utilizată metodă), prin încălzirea acidului cu alcool, în prezentă de cantităţi catalitice de acid mineral (H 2 SO 4, HCl uscat), cand se stabileşte un echilibru între reactanţi şi produşi (VI. 48) • Mărirea randamentului în ester se face prin: § § folosirea unei componente în exces (alcoolul sau acidul); îndepărtarea din reacţie a unuia din produşi (apa sau esterul) prin distilare, cu condiţia să fie mai volatili decât acidul şi alcoolul luat în lucru. VI. 3. 3. Proprietăţi fizice • Esterii alcoolilor monohidroxilici inferiori sunt lichide insolubile în apă, miscibile cu solvenţi organici, având miros plăcut.

• P. f. ale esterilor sunt mai joase decât ale acizilor şi alcoolilor din care provin, deoarece moleculele esterilor nu se asociază prin punţi de hidrogen. • Esterii metilici au uneori p. t. mai ridicate decât esterii alcoolilor superiori, datorită uniformităţii reţelei. VI. 3. 4. Proprietăţi chimice 1. Reacţia de hidroliză. Esterii suferă hidroliză când sunt încălziţi cu apa, formând acidul şi alcoolul de provenienţă. Reacţia este catalizată de acizi şi este reversibilă (echilibrul VI. 49). (VI. 49) • Dacă eterii şi acetalii hidrolizează doar în cataliză acidă (cum se şi formează), esterii hidrolizează şi în cataliză bazică, într-o reacţie ireversibilă (VI. 50)

a) Hidroliza acidă decurge prin 2 tipuri de mecanism: rupere acil-O (ruperea legăturii RCO-OR’) sau rupere alchil-O (ruperea legăturii RCOO-R’). • Hidroliza prin rupere acil-O (mecanism curent pentru R’ = alchil primar sau secundar) este SN 2 (VI. 51)

• Hidroliza prin rupere alchil-O are loc la unii esteri care conţin un rest de alcool capabil să formeze cationi stabili (terţ-butil, benzil) şi decurge prin mecanism SN 1 (VI. 52) • Cu hidracizii concentraţi tari, are loc o reacţie de acidoliză (VI. 53) în care se formează acid carboxilic şi halogenură de alchil. Reacţia se utilizează la dozarea grupărilor metoxi, etc. (VI. 53) b) Mecanismul hidrolizei bazice sau saponificării (r. VI. 54) implică atacul ionului hidroxil (nucleofil) la carbonilul esterului. În anionul format prin adiţia nucleofilă a bazei, are loc eliminarea grupei alcoxid, RO-.

• Deoarece RO- este o bază tare, are loc un transfer de H+ cu formarea unei molecule de alcool. Alcoolul fiind un acid mai slab decât acidul carboxilic, ultima etapă a reacţiei este ireversibilă. Prin aceasta, hidroliza bazică se deosebeşte de hidroliza în mediu acid. (VI. 54) • La hidroliza bazică ruperea acil-O a fost demonstrată prin izolarea alcoolului marcat izotopic (r. VI. 55). (VI. 55) 2. Reacţia de transesterificare, prin încălzirea unui ester cu un alcool, în mediu acid (VI. 56).

(VI. 56) • Transesterificarea se poate produce şi sub influenţa catalitică a alcoolaţilor. Reacţia este reversibilă atât în mediu acid cât şi în mediu bazic deoarece, în acest caz, în reacţie nu se formează acid (grupă carboxilică liberă) ca şi în cazul reacţiei de hidroliză în mediu bazic. 3. Amonoliza esterilor conduce la formare de amide, conform r. VI. 57. (VI. 57) • Esterii formează amide substituite (R-CONH-R’ sau R-CON(R’)(R’’)) în r. cu aminele primare sau secundare. • Similar, reacţionează cu hidrazina (NH 2 -NH 2) şi hidroxilamina (NH 2 -OH), formând hidrazide (R-CONH-NH 2) şi acizi hidroxamici (R-CONH-OH). Reacţiile au valoare preparativă în sinteza derivaţilor funcţionali ai acizilor, mai ales când utilizarea clorurilor acide este neindicată.

4. Reacţia esterilor cu compuşi organo-metalici (VI. 58) conduce la obţinerea de alcooli terţiari, cu excepţia formiaţilor care, în aceste condiţii, formează alcooli secundari (r. VI. 59). (VI. 58) (VI. 59) 5. Reducerea catalitică a esterilor conduce la alcooli primari (a se vedea cap. II. 1. 3, r. II. 8 -II. 10). 6. Rezistenţa esterilor faţă de agenţi oxidanţi este folosită pentru protejarea grupărilor OH alcoolice şi fenolice, prin esterificare, în r. de oxidare sau de nitrare.

VI. 3. 5. Reprezentanţi 1. Formiatul de metil (HCOOCH 3) şi formiatul de etil (HCOOC 2 H 5) se obţin industrial din CO şi alcool, în prezenţă de cantităţi catalitice de alcoxid de Na (r. VI. 60) (VI. 60) • Datorită mirosului plăcut sunt utilizaţi în industria alimentară. 2. Acetatul de etil (CH 3 COOC 2 H 5) se obţine prin esterificare directă, din cetenă şi alcool, prin r. Tiscenko sau prin hidrogenarea acetatului de vinil (r. VI. 61). (VI. 61) • Acetatul de etil se utilizează ca dizolvant şi ca intermediar în numeroase sinteze organice.

3. Butiratul de etil (CH 3 -(CH 2)2 -COOC 2 H 5) şi butiratul de izoamil (CH 3 -(CH 2)2 -COO(CH 2)2 -CH(CH 3)2) se utilizează în industria alimentară la prepararea esenţelor aromate. De asememea, datorită mirosului lor plăcut, acetatul de benzil (CH 3 COOCH 2 -C 6 H 5) şi propionatul de benzil (CH 3 -CH 2 -COOCH 2 -C 6 H 5) se folosesc în parfumeriei. 4. Diesterii acidului malonic (ROOC-CH 2 -COOR) prezintă importanţă datorită metilenului activ. Sub acţiunea Na, formează diesterul malonic sodat (r. VI. 62), a cărui anion este stabilizat prin conjugare ((VI. 16), (VI. 17) şi (VI. 18)). (VI. 16) (VI. 17) (VI. 18)

• • În r. se exercită un efect de conjugare dinamic sub influenţa reactantului, astfel că, diesterul malonic sodat reacţionează în forma (VI. 16), în care sarcina (-) este localizată la C. În reacţia diesterului malonic cu derivaţi halogenaţi reactivi, se obţin derivaţi ai diesterului malonic substituiţi la C (r. VI. 63 a şi VI. 63 b). (VI. 63 a) (VI. 63 b) • Aceşti diesteri mai conţin un H mobil, ce poate fi înlocuit cu Na. Compuşii sodaţi astfel obţinuţi pot reacţiona cu derivaţi halogenaţi formând diesteri disubstituiţi ai acidului malonic (r. VI. 64). (VI. 64)

• Diesterii substituiţi formează prin hidroliză acizi malonici care, fiind acizi -dicarboxilici, se decarboxilează uşor la încălzire cu formare de acizi monocarboxilici(VI. 65 a şi b) (VI. 65 a) (VI. 65 b) • Diesterul malonic sodat reacţionează şi cu derivaţii dihalogenaţi. În funcţie de proporţia dintre acesta şi derivatul dihalogenat, se obţin produşi diferiţi. Astfel, prin reacţia dintre 1 mol derivat dihalogenat şi 2 moli de diester malonic sodat, se obţine, după hidroliză urmată de decarboxilare parţială, acidul glutaric (VI. 66)

• Când reacţionează 1 mol diester malonic cu 1 mol compus dihalogenat (de preferinţă cu X cu reactivitate diferită), se formează un derivat cu structură ciclică (VI. 67). Reacţia este catalizată de alcoxizi (RO-Na+) şi mai este cunoscută sub numele de sinteza Perkin jr. (VI. 67) • Dacă diesterul malonic sodat este supus acţiunii I 2, are loc eliminarea Na şi formarea unei noi legături C-C (r. VI. 68). (VI. 68) • Metilenul activ reacţionează în anumite condiţii cu aldehidele şi cetonele. Se formează iniţial un produs de

(VI. 69) • R. decurge în cataliză bazică (amine secundare) şi mai este cunoscută sub numele de reacţia Knoevenagel. • Diesterul sodat al acidului malonic se adiţionează, prin adiţie 1, 4 conjugată, la sistemele carbonilice , nesaturate (reacţia Michael), formând compuşi carbonilici saturaţi. Mecanismul unei astfel de adiţii este r. VI. 70. (VI. 70)

5. Esterii glicerinei cu acidul acetic servesc ca dizolvanţi pentru taninuri sau anumiţi coloranţi. Prin reacţia glicerinei cu CH 3 COOH se pot obţine 2 monoacetaţi izomeri ((VI. 19) şi (VI. 20)), numiţi şi acetine, 2 diacetaţi ((VI. 21) şi (VI. 22)) sau 1 triacetat (VI. 23). (VI. 19) (VI. 20) (VI. 21) (VI. 22) VI. 4. AMIDE (VI. 23) VI. 4. 1. Clasificare. Nomenclatură. • Sunt derivaţi funcţionali ai acizilor carboxilici, în care grupa hidroxil (-OH) este înlocuită cu grupa amino (-NH 2). • Se mai pot considera acil-derivaţi ai NH 3. • După nr. grupărilor acil şi/sau alchil, ce înlocuiesc H într-o ipotetică moleculă de NH 3, amidele se clasifică în: primare (VI. 26), secundare(VI. 27 a)-(VI. 27 b)), terţiare(VI. 28 a)- (VI. 28 b)
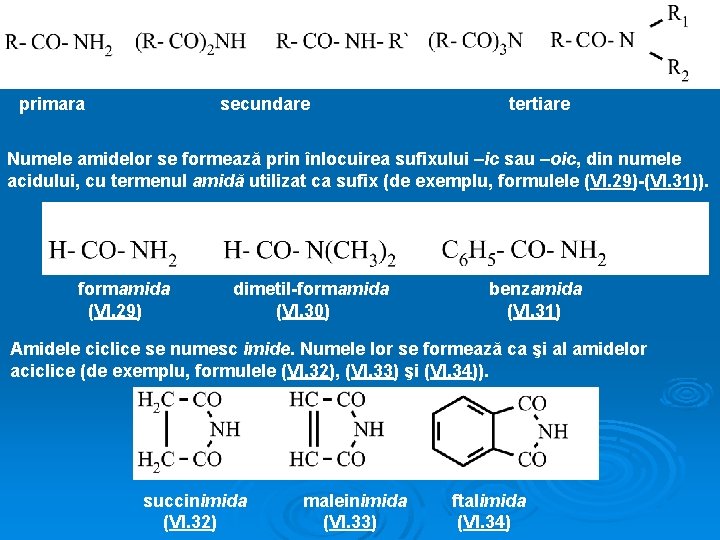
primara secundare tertiare Numele amidelor se formează prin înlocuirea sufixului –ic sau –oic, din numele acidului, cu termenul amidă utilizat ca sufix (de exemplu, formulele (VI. 29)-(VI. 31)). formamida (VI. 29) dimetil-formamida (VI. 30) benzamida (VI. 31) Amidele ciclice se numesc imide. Numele lor se formează ca şi al amidelor aciclice (de exemplu, formulele (VI. 32), (VI. 33) şi (VI. 34)). succinimida (VI. 32) maleinimida (VI. 33) ftalimida (VI. 34)

VI. 4. 2. Metode de sinteză 1. Din NH 3 şi derivaţi ai acizilor carboxilici (cloruri acide, 2. anhidride sau esteri), se obţin amide conform reacţiilor VI. 73 a, b şi c. 2. Din NH 3 şi acizi carboxilici stabili termic, se obţin, conform reacţiei VI. 74, amide. Acizii carboxilici formează la tratare cu NH 3 săruri de amoniu. Prin încălzirea acestora peste 200ºC, în prezenţă de NH 3 în exces, se obţin amide şi se elimină apa Reacţia se aplică numai la moleculele stabile termic la această temperatură. Se obţin pe această cale amide ale acizilor carboxilici saturaţi (de exemplu, din acid acetic şi NH 3 se obţine acetamida). Dacă în locul amoniacului se utilizează amine, se obţin amide substituite.

3. Hidroliza parţială a nitrililor conduce la formare ce amide, conform reacţiei VI. 75. Reacţia are loc fie prin dizolvarea nitrilului în H 2 SO 4 concentrat, urmată de diluare cu apă, fie prin încălzirea uşoară a nitrilului cu H 2 O 2 în Na. OH. VI. 4. 3. Proprietăţi fizice - Amidele primare, cu excepţia formamidei, sunt substanţe solide, frumos cristalizat Cele inferioare sunt solubile în apă Termenii superiori sunt solubili în dizolvanţi organici polari (de exemplu, cloroform) Punctele de fierbere ridicate ale amidelor se explică pe baza asociaţiilor moleculare prin legături de hidrogen (VI. 35), între grupe NH şi grupe C=O.
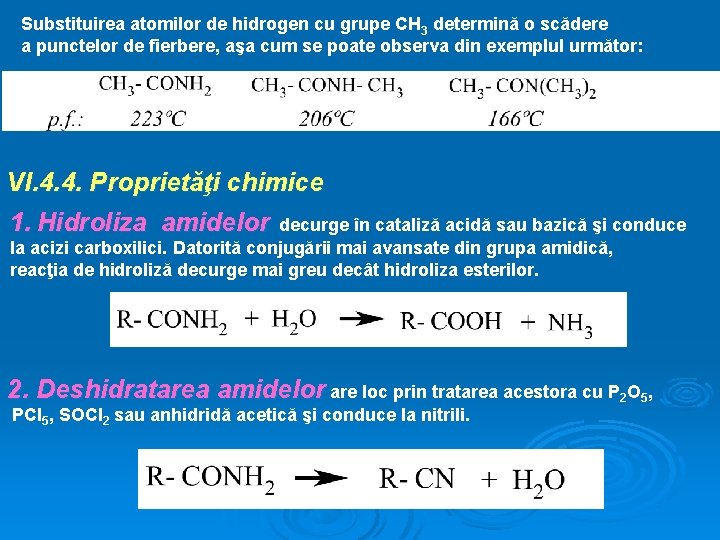
Substituirea atomilor de hidrogen cu grupe CH 3 determină o scădere a punctelor de fierbere, aşa cum se poate observa din exemplul următor: VI. 4. 4. Proprietăţi chimice 1. Hidroliza amidelor decurge în cataliză acidă sau bazică şi conduce la acizi carboxilici. Datorită conjugării mai avansate din grupa amidică, reacţia de hidroliză decurge mai greu decât hidroliza esterilor. 2. Deshidratarea amidelor are loc prin tratarea acestora cu P 2 O 5, PCl 5, SOCl 2 sau anhidridă acetică şi conduce la nitrili.
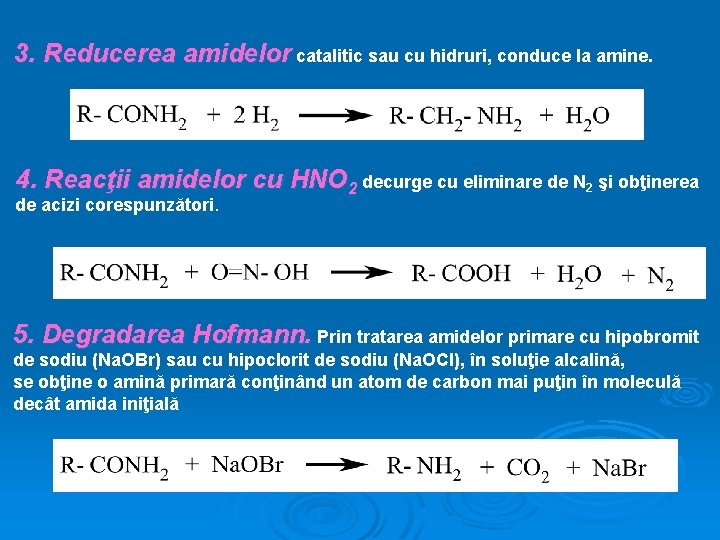
3. Reducerea amidelor catalitic sau cu hidruri, conduce la amine. 4. Reacţii amidelor cu HNO 2 decurge cu eliminare de N 2 şi obţinerea de acizi corespunzători. 5. Degradarea Hofmann. Prin tratarea amidelor primare cu hipobromit de sodiu (Na. OBr) sau cu hipoclorit de sodiu (Na. OCl), în soluţie alcalină, se obţine o amină primară conţinând un atom de carbon mai puţin în moleculă decât amida iniţială
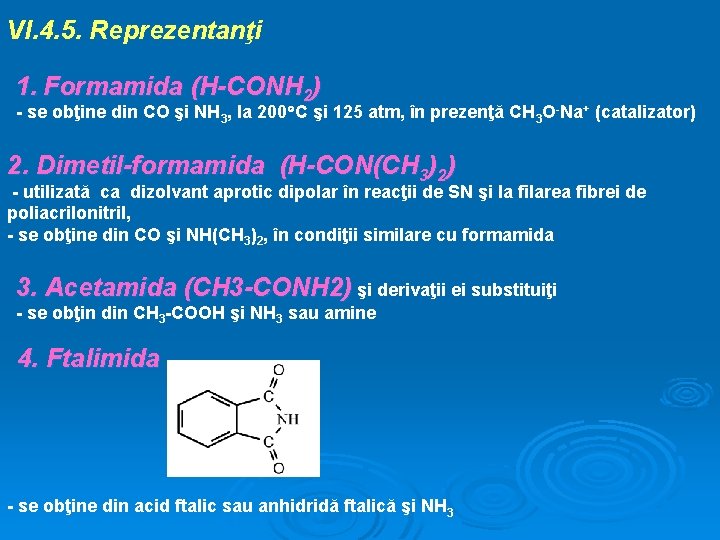
VI. 4. 5. Reprezentanţi 1. Formamida (H-CONH 2) - se obţine din CO şi NH 3, la 200 C şi 125 atm, în prezenţă CH 3 O-Na+ (catalizator) 2. Dimetil-formamida (H-CON(CH 3)2) - utilizată ca dizolvant aprotic dipolar în reacţii de SN şi la filarea fibrei de poliacrilonitril, - se obţine din CO şi NH(CH 3)2, în condiţii similare cu formamida 3. Acetamida (CH 3 -CONH 2) şi derivaţii ei substituiţi - se obţin din CH 3 -COOH şi NH 3 sau amine 4. Ftalimida - se obţine din acid ftalic sau anhidridă ftalică şi NH 3
- Slides: 44