Vestibular UFRGS 2007 Prova de Qumica correo comentada

Vestibular UFRGS, 2007 Prova de Química: correção comentada Química, turma 301 Professor Luiz Antônio Tomaz

Nosso público A presente correção comentada da Prova de Química do Vestibular da UFRGS, ano 2007, é dirigida aos alunos da 3. ª série do Ensino Médio do Colégio Inedi de Cachoeirinha – RS.

Nosso objetivo O objetivo desta correção comentada é esclarecer dúvidas e revisar conteúdos programáticos de Química para o Concurso Vestibularda UFRGS.


Resposta correta: B Assunto: Sistemas Materiais, Propriedades da Matéria. Há um único componente: elemento fósforo (P); Mas há três fases: sólido, líquido e gasoso.


Resposta correta: D Assunto: Separação ou Fracionamento de Misturas. Lembremo-nos que dissolução está relacionada à solubilidade das substâncias e há dissolução de um componente pelo menos para haver separação.


Resposta correta: A Assunto: Tabela Periódica. I – Não pode ser o flúor; II - Não pode ser magnésio, alumínio ou enxofre; III – por eliminação, é o carbono.


Resposta correta: C Assunto: Tabela Periódica e Estrutura Atômica. O fato de apresentar massa fracionada significa que há isótopos (média ponderada).


Resposta correta: C Assunto: Leis Ponderais. 10 g. . . 100% 2, 2 g. . . . . x x = 22% *Massa que reagiu: 10 g – 7, 8 g = 2, 2 g


Resposta correta: D Assunto: Conceito de MOL e Acerto de Coeficientes. N 2 + 3 H 2 2 NH 3 3 mols de H 2 2 x 6, 02. 1023 = 1, 2. 1024


Resposta correta: E Assunto: Oxidação-redução. NOx do H: 0 para +1 H 2 + 1/2 O 2 H 2 O NOx do O: 0 para -2 Há transferência de elétrons (corrente elétrica).


Resposta correta: A Assunto: Equilíbrio Químico. A constante de equilíbrio (Kc) depende apenas da temperatura.


Resposta correta: B Assunto: Oxidação-redução. B 4 O 7 -2 4. X + 7. (-2) = -2 X = +3


Resposta correta: A Assunto: Oxidação-redução. O NOx dminui de +2 para zero(redução). Cu+2(aq)+ Mg(s) Cu(s)+ Mg+2(aq)
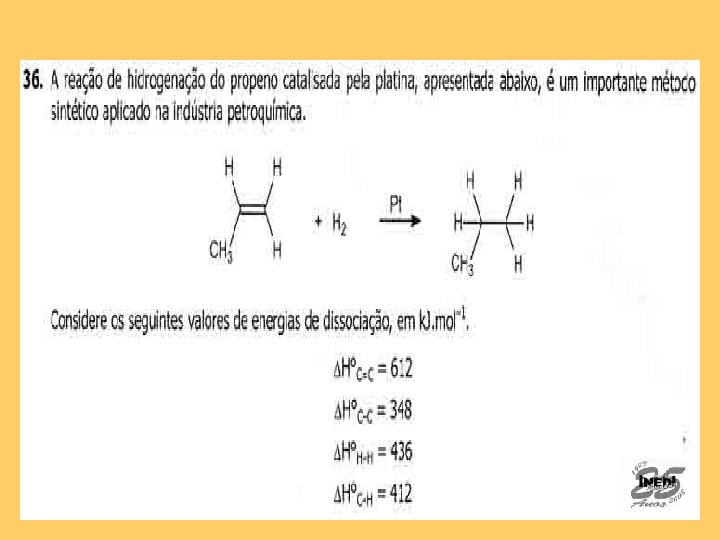


Resposta correta: B Assunto: Termoquímica. ΔH = (612 + 436) – (348 + 412) = -124 k. J
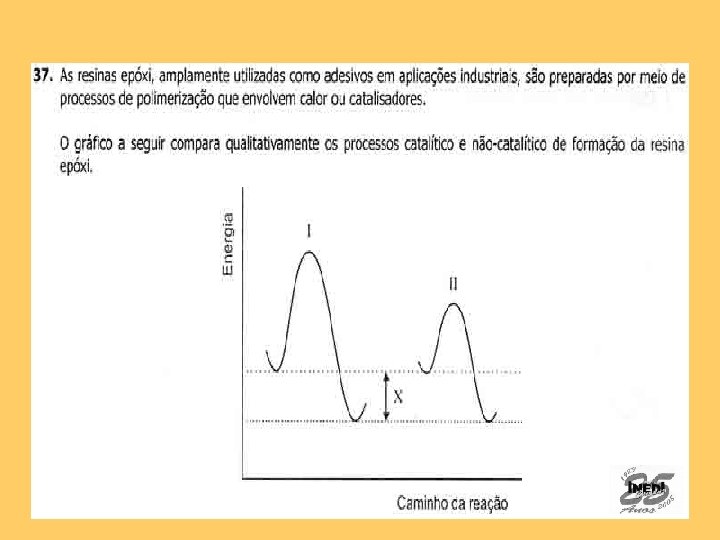


Resposta correta: D Assunto: Cinética Química. Quanto menor a energia de ativação, mais rápida a reação. Isso é conseguido com uso de catalisador.
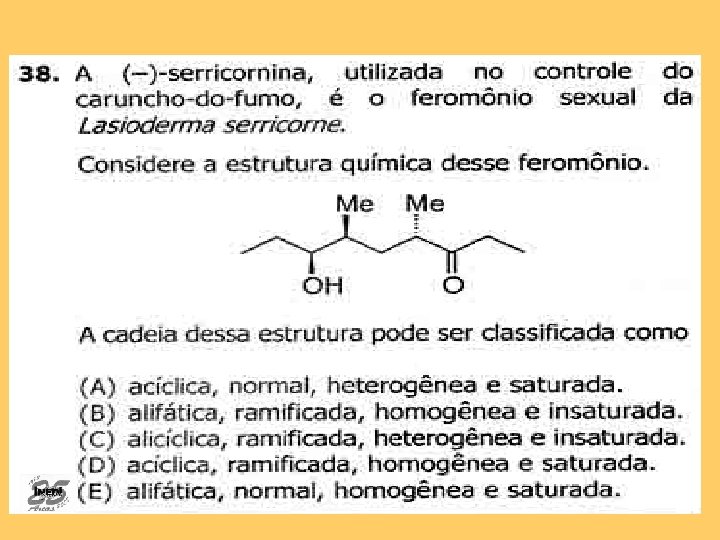

Resposta correta: D Assunto: Cadeias Carbônicas. Acíclica = aberta. Ramificada = Me (metilas). Homogênea = não há heteroátomos. Saturada = só há ligações simples.
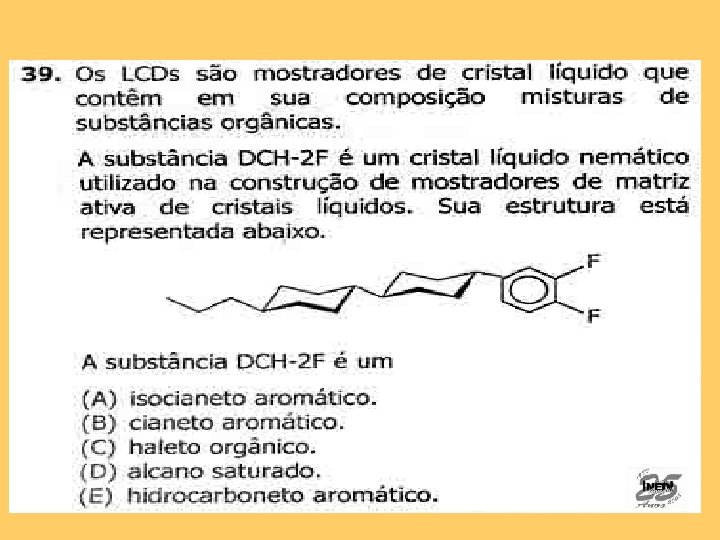

Resposta correta: C Assunto: Funções Químicas Orgânicas. A presença de Flúor (halogênio) ligado diretamente a átomo de carbono, indica Haleto.
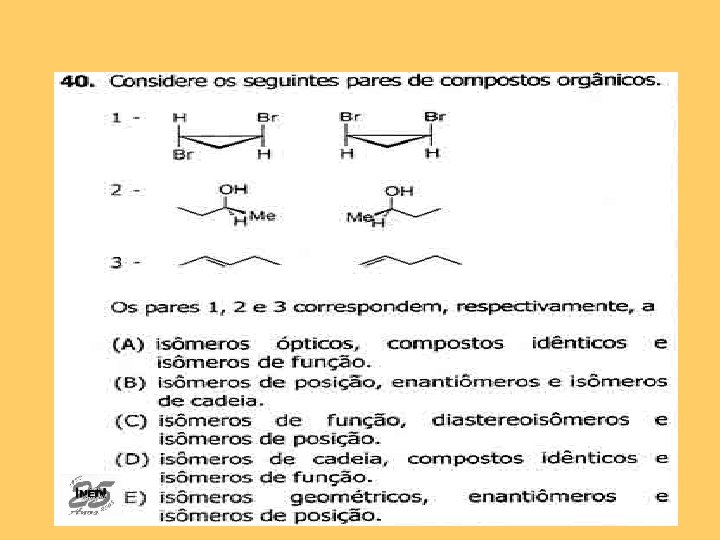

Resposta correta: E Assunto: Isomeria. I – Isomeria geométrica (cis/trans) em cadeia cíclica. II – Isomeria óptica (quiralidade). III – Isomeria de posição (localização da insaturação).




Resposta correta: D Assunto: Nomenclatura de Compostos Orgânicos. Observar que alguns apresentam nomes usuais (não seguem IUPAC).

![Resposta correta: C Assunto: p. H. Para p. H = 9, [H+] = 10 Resposta correta: C Assunto: p. H. Para p. H = 9, [H+] = 10](http://slidetodoc.com/presentation_image_h/02c405f2ae8046e3141a9fbe2cdbf2cd/image-41.jpg)
Resposta correta: C Assunto: p. H. Para p. H = 9, [H+] = 10 -9. Diluindo 10 vezes, [H+] = 10 -8. Daí, p. H = 8.
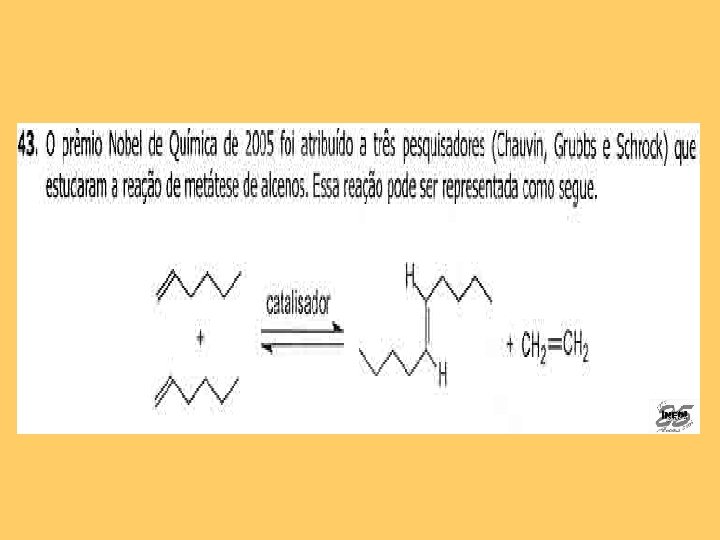


Resposta correta: A Assunto: Deslocamento de Equilíbrio Químico. Aumento na concentração de reagente, desloca o equilíbrio no sentido 1 (direita).


Resposta correta: C Assunto: Propriedades Coligativas. Tonoscopia ou Tonometria está relacionada à pressão de vapor.


Resposta correta: A Assunto: Ligações Químicas. CO 2 e C, não-metal + não-metal (covalente). Ca. O e Cs. F, metal + não-metal (iônica).


Resposta correta: B Assunto: Termoquímica e Estequiometria. 2. 27 g. . . . . 1670 k. J 1 g. . . xk. J x = 321 k. J
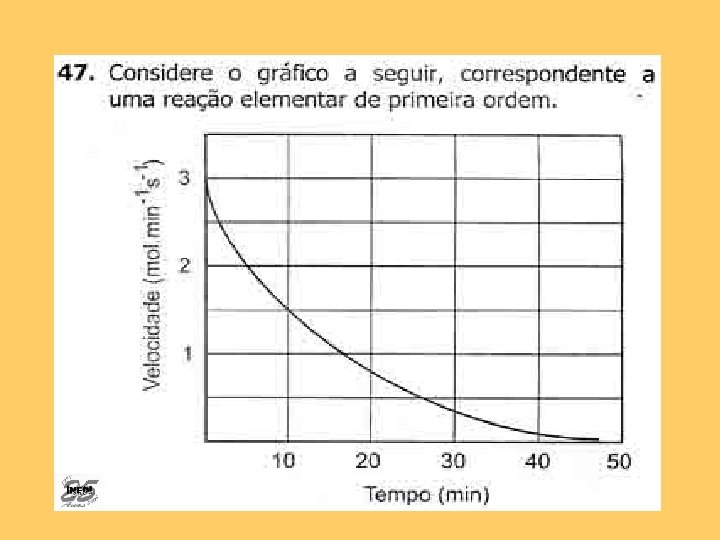


Resposta correta: C Assunto: Cinética Química e Conceito de Meia-vida. A meia-vida significa que a concentração do reagente se reduz pela metade. Como a reação elementar de primeira ordem, faz-se a correspondência direta entre velocidade (3 para 1, 5 em 10 min) e concentração.

![Resposta correta: E Assunto: Cinética Química. Vi = k[NO]1[O 3] 1 Vf = k[2 Resposta correta: E Assunto: Cinética Química. Vi = k[NO]1[O 3] 1 Vf = k[2](http://slidetodoc.com/presentation_image_h/02c405f2ae8046e3141a9fbe2cdbf2cd/image-55.jpg)
Resposta correta: E Assunto: Cinética Química. Vi = k[NO]1[O 3] 1 Vf = k[2 NO]1[2 O 3] 1 Vf = 4 k[NO]1[O 3] 1 Vf = 4 V i
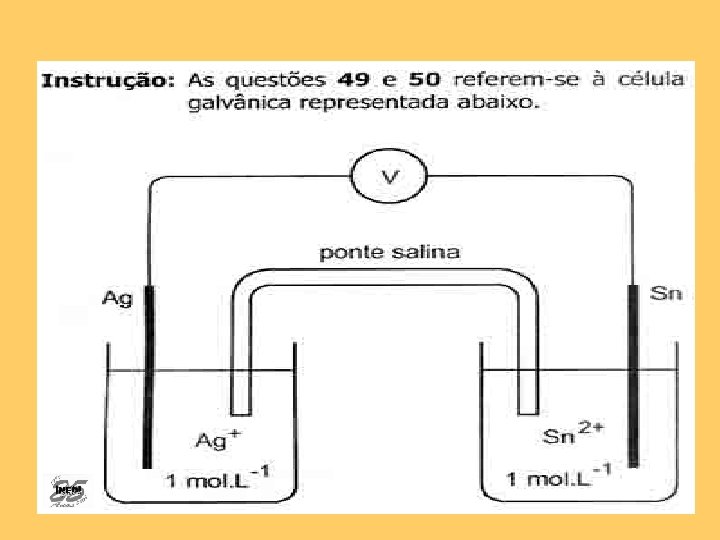



Resposta correta: B Assunto: Eletroquímica. Redução da Ag no cátodo (pólo positivo). Oxidação do Sn no ânodo (pólo negativo). As massas não são iguais, pois as massas molares são diferentes.


Resposta correta: D Assunto: Eletroquímica. f. e. m = +0, 80 V –(– 0, 14 V) f. e. m. = +0, 94 V

Boa Prova ! Prof. Luiz
- Slides: 62