Verbindingen Klas 4 Roosters Kristalrooster regelmatig patroon van

Verbindingen Klas 4

Roosters �Kristalrooster: regelmatig patroon van deeltjes in een vaste stof �Metalen – Alleen metalen �Zouten – Metaal met een niet metaal �Moleculaire stoffen – Alleen niet-metalen

Metalen �Metaalbinding: Binding waarbij de positieve metaalionen bij elkaar gehouden worden door de vrije, negatieve, elektronen behoorlijk sterk �Door de vrije elektronen geleiden metalen stroom �Metaalrooster: regelmatige rangschikking van metaalatomen. Kunnen over elkaar schuiven zonder te breken vervormbaarheid

Ionen �Ionrooster: regelmatige rangschikking van positieve (metaal) ionen en negatieve (niet metaal) ionen. �Kristalrooster van een zout �In vaste vorm geen vrije elektronen geen geleiding �+ en – trekt elkaar aan zeer sterke binding �Hoog smeltpunt

Moleculaire stoffen �Molecuulbinding (vanderwaals krachten): Binding TUSSEN moleculen. �Zeer zwak laag smeltpunt �Ontstaat door aantrekkingskracht �Hoe groter het molecuul, hoe hoger de massa, hoe hoger de aantrekkingskracht, hoe hoger het smeltpunt �Molecuulrooster: regelmatige rangschikking van nietmetalen. Zeer zwakke bindingen, dus smelten snel.
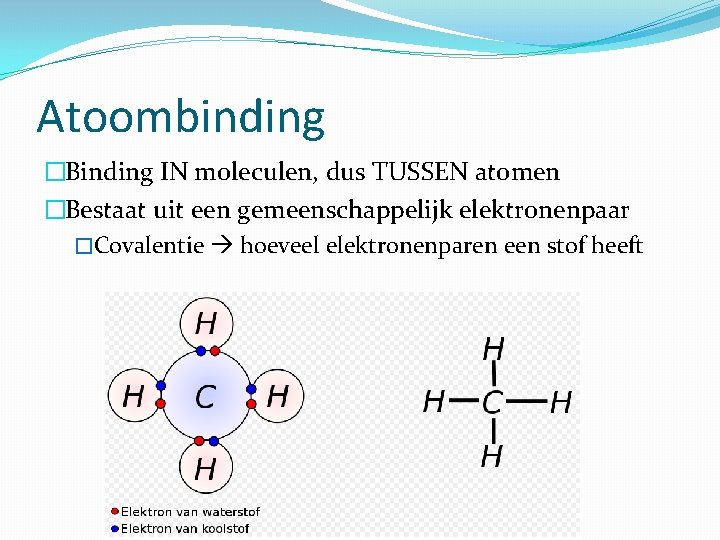
Atoombinding �Binding IN moleculen, dus TUSSEN atomen �Bestaat uit een gemeenschappelijk elektronenpaar �Covalentie hoeveel elektronenparen een stof heeft

Delta min en Delta plus �δ- en δ+ �Als de ene stof harder aan de elektronen trekt dan de andere stof �Verschillende elektronegativiteit Binas 40 A �Polaire binding = binding waarbij er een verschil is in elektronegativiteit sterkere binding hoger smeltpunt �Dipoolmolecuul: Molecuul met een δ- en δ+ kant
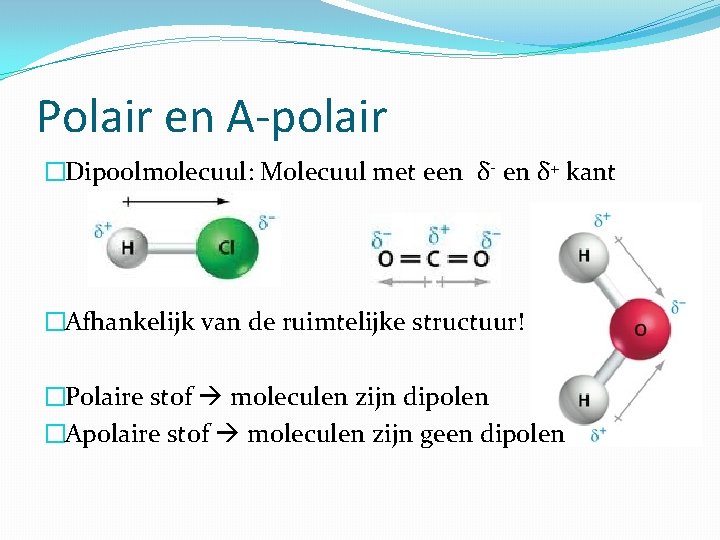
Polair en A-polair �Dipoolmolecuul: Molecuul met een δ- en δ+ kant �Afhankelijk van de ruimtelijke structuur! �Polaire stof moleculen zijn dipolen �Apolaire stof moleculen zijn geen dipolen
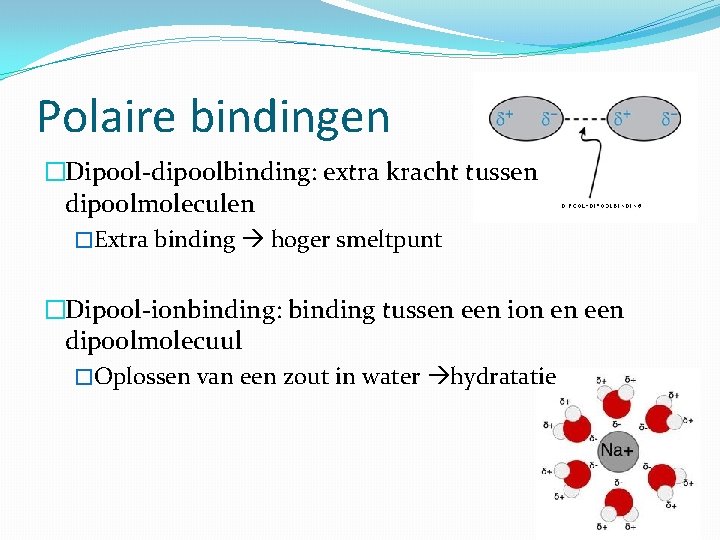
Polaire bindingen �Dipool-dipoolbinding: extra kracht tussen dipoolmoleculen �Extra binding hoger smeltpunt �Dipool-ionbinding: binding tussen een ion en een dipoolmolecuul �Oplossen van een zout in water hydratatie

Invloed op het kook/smeltpunt �Ionbinding = zeer sterk, hoogste smeltpunt �Metaalbinding = redelijk sterk, hoog smeltpunt �Vanderwaalsbinding = zwak, laag smeltpunt �Grotere massa hoger smeltpunt �Dipool extra binding hoger smeltpunt �Atoombinding = redelijk sterk �Polarie atoombinding= sterker hoger smeltpunt
- Slides: 10