Vedov nemoc aludku a duodena Pednka z patologick















- Slides: 41

Vředová nemoc žaludku a duodena Přednáška z patologické fyziologie pro bakaláře 7. 3. 2005 Doc. MUDr. Lydie Izakovičová Hollá, Ph. D.

Patofyziologie žaludku Žaludek plní 2 základní funkce: 1) motorickou: - žaludeční relaxace – adaptace žaludku na příjem potravy (parasympatikus, gastrin, cholecystokinin) - kontrakce žaludečního těla a antra – k promísení potravy - vlastní peristaltika – posunující chymus do duodena Vyprazdňování žaludku je ovlivněno: - fyzikálními a chemickými vlastnostmi potravy - energetickým obsahem potravy - regulačními peptidy

2) sekreční: Objem vylučované žaludeční šťávy může být: zvýšen krátkodobě x dlouhodobě snížen Pokud se jedná o změnu stupně produkce HCL - hypacidita, anacidita (hypochlorhydrie, achlorhydrie) hyperacidita (hyperchlorhydrie) Když není produkována ani HCl ani žaludeční enzymy - achylie



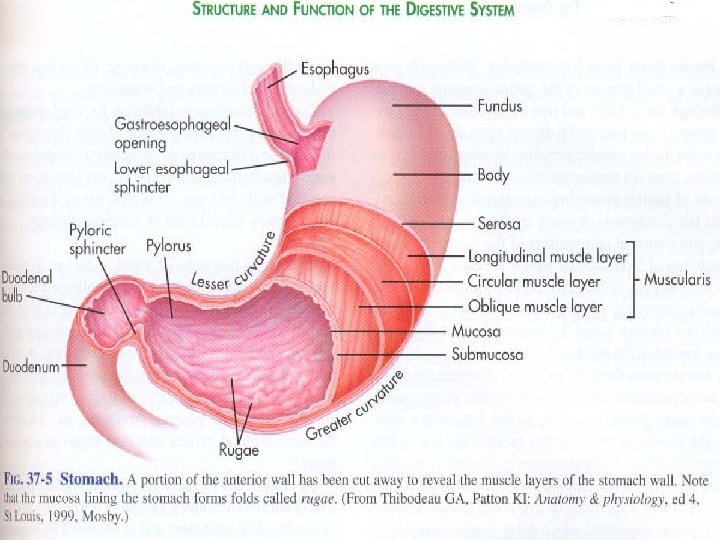
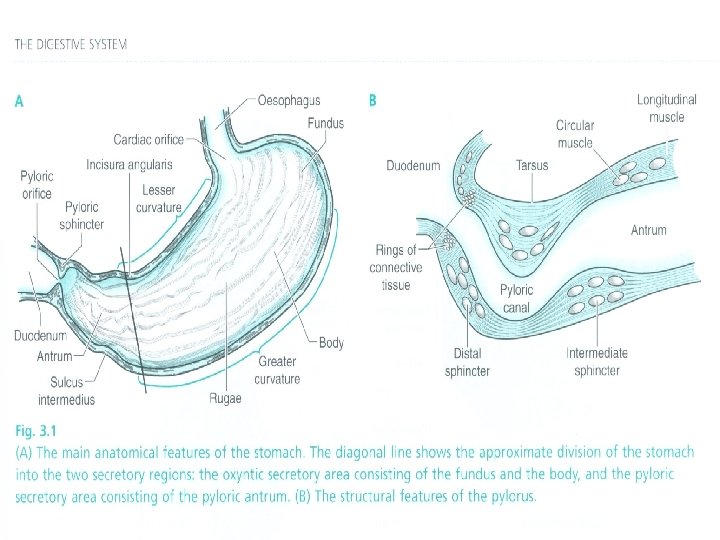
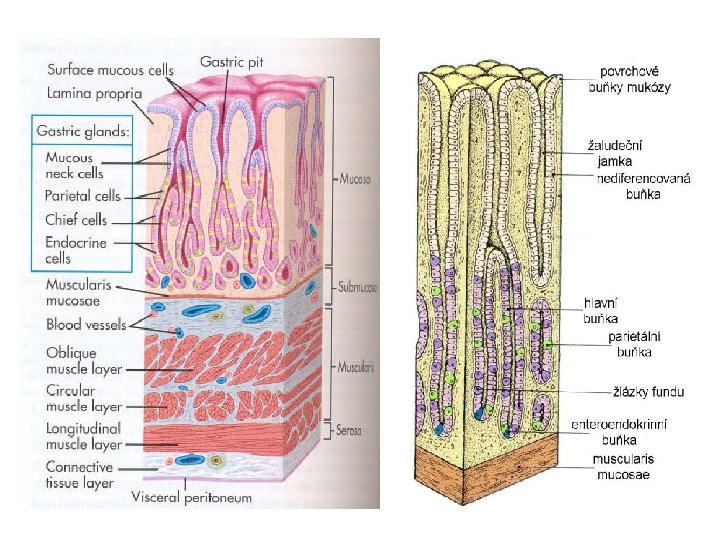
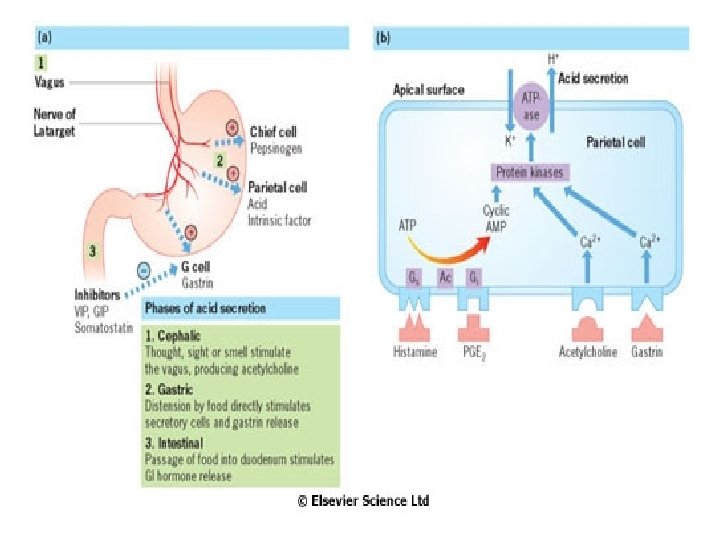
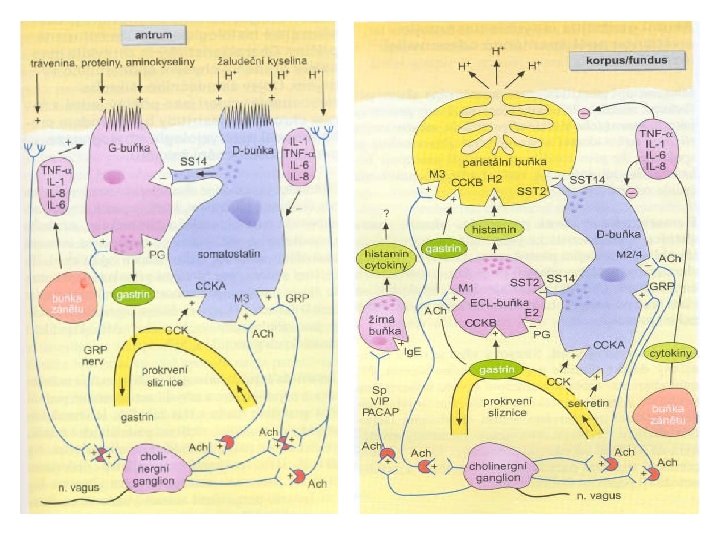
Slizniční bariéra • Sliznice žaludku, zejména podél velké kurvatury, se skládá do tenkých záhybů. • Horní dvě třetiny žaludku obsahují parietální buňky (sekrece HCl) a hlavní buňky, které sekretují pepsinogen (který zahajuje proteolýzu). • Antrum obsahuje buňky sekretující mucin a G buňky, které vylučují gastrin (G 17 a G 34 podle počtu aminokyselin). • Buňky sekretující mucin produkují hlen a bikarbonáty, které jsou vázány v mukózovém gelu. Ten se skládá z mucinů (glykoproteiny). Specializované antrální buňky (D buňky) produkují somatostatin. Slizniční bariéra, tvořená povrchovými membránami slizničních buněk a hlenem chrání vnitřní povrch žaludku před poškozením alkoholem, NSAID a žlučovými solemi. • Prostaglandiny stimulují sekreci hlenu. Jejich syntéza je inhibována NSAID (inhibitory cyklooxygenázy) a kortizolem (inhibitor PLA 2).

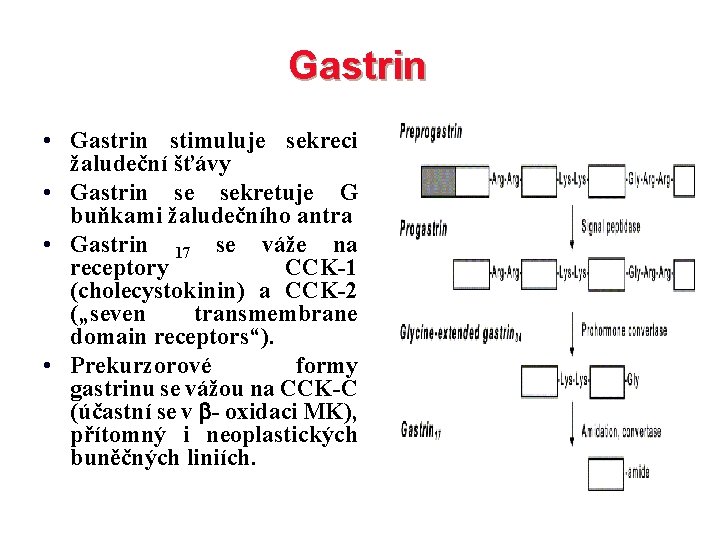
Gastrin • Gastrin stimuluje sekreci žaludeční šťávy • Gastrin se sekretuje G buňkami žaludečního antra • Gastrin 17 se váže na receptory CCK-1 (cholecystokinin) a CCK-2 („seven transmembrane domain receptors“). • Prekurzorové formy gastrinu se vážou na CCK-C (účastní se v - oxidaci MK), přítomný i neoplastických buněčných liniích.





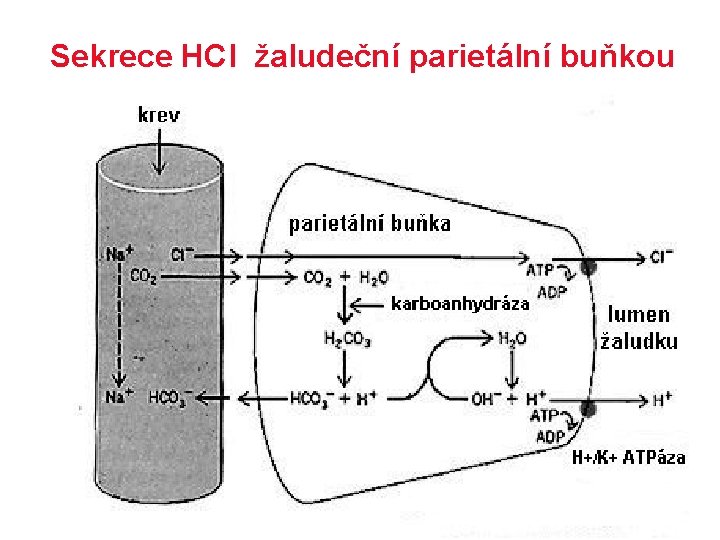
Sekrece HCl žaludeční parietální buňkou

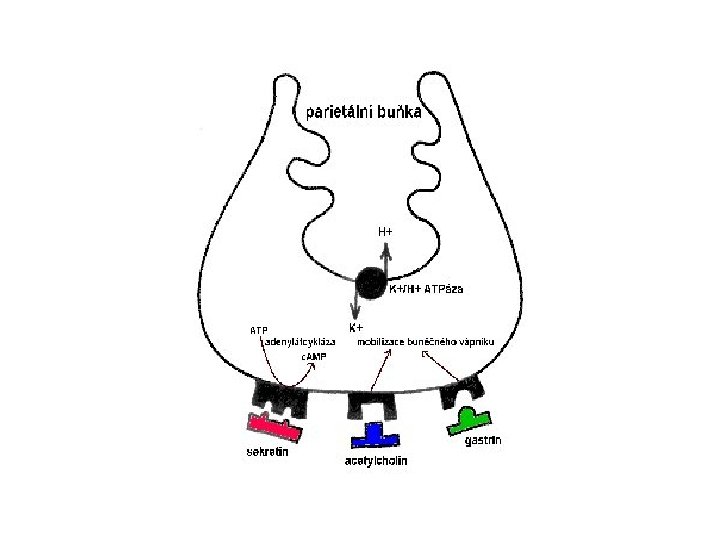
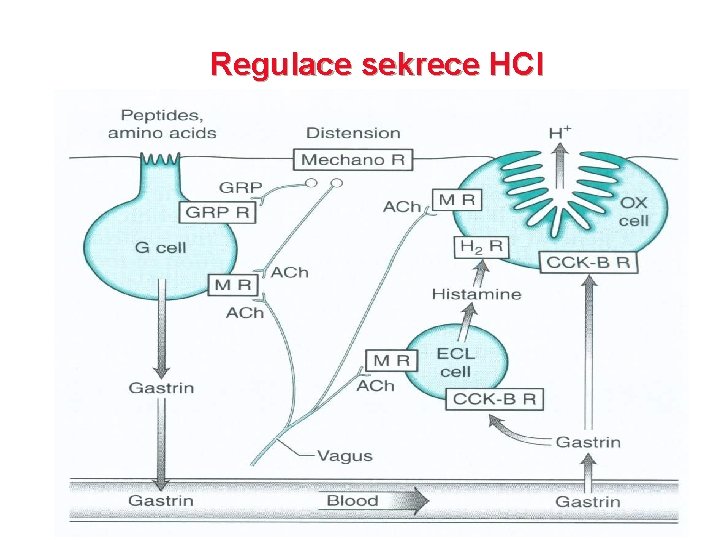
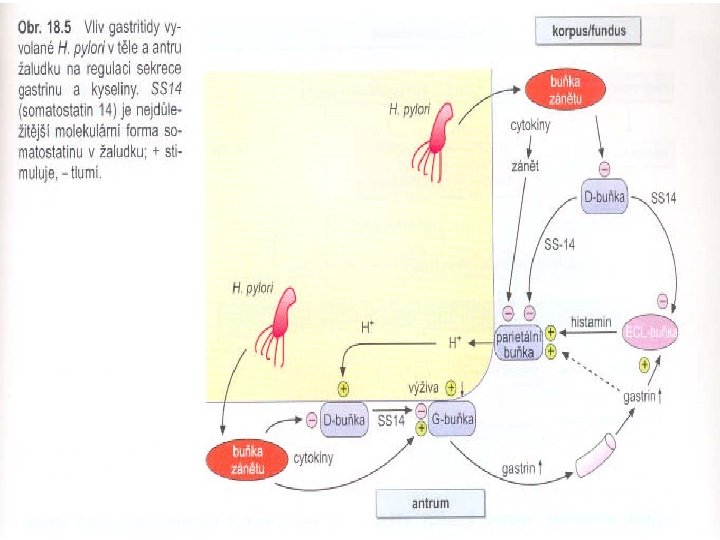
Regulace sekrece HCl

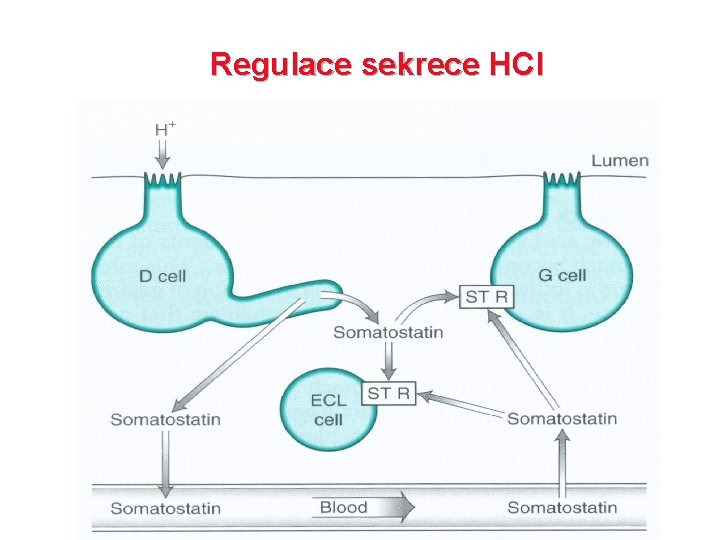
Regulace sekrece HCl

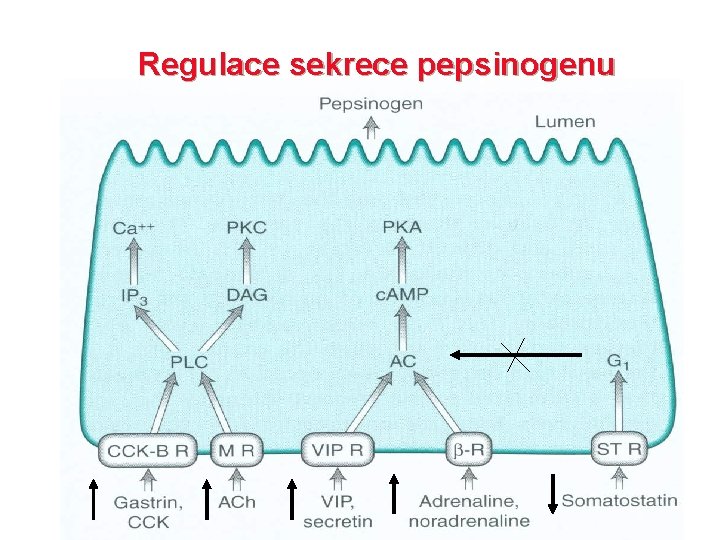
Regulace sekrece pepsinogenu

Účast duodenální sliznice při neutralizaci kyselého obsahu žaludku • Sliznice duodena obsahuje Brunnerovy žlázky, které sekretují alkalický produkt- mucus (hlen). • Ten společně s pankreatickými a biliárními sekrety neutralizuje kyselou žaludeční sekreci ze žaludku.

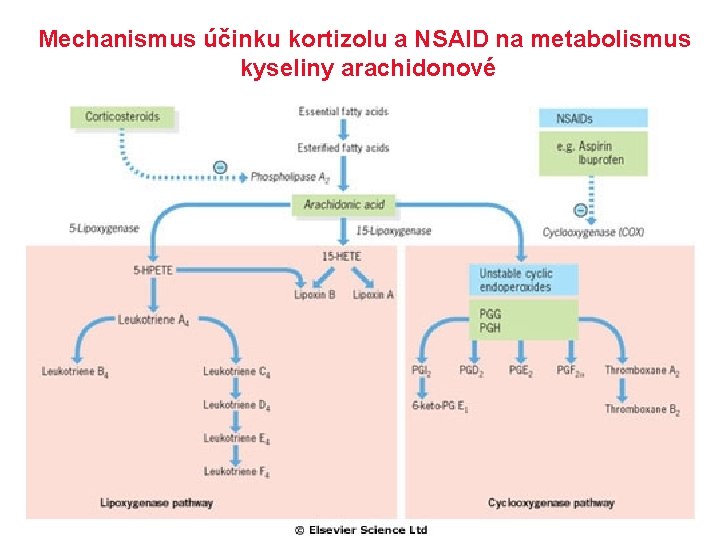
Mechanismus účinku kortizolu a NSAID na metabolismus kyseliny arachidonové

Gastrinom = Zollingerův-Ellisonův syndrom Tumor vycházející z D-buněk Langerhansových ostrůvků pankreatu významná nadprodukce gastrinu Klinické projevy: * stálá vysoká sekrece žaludeční šťávy se zvýšeným množstvím HCl a proteináz * atypicky lokalizované vředy (duodenum, jejunum…) Někdy jako součást MEN I (syndrom mnohočetné endokrinní neoplazie)

Gastritidy • Poruchy sekrece kyseliny jsou nejčastěji vyvolány gastritidou (x maximální hypersekrece HCl – u gastrinomu) Akutní gastritidy Zánětlivý proces s hyperémií, erozemi až vředy Formy: * hemoragicko-erozivní gastritida * akutní stresový vřed Etiologie: infekce, alkohol, závadné jídlo, kouření, radiace, šokové stavy, NSAID….

Chronické gastritidy Etiopatogeneticky rozlišujeme 3 typy: Gastritida typu A - autoimunitně podmíněná gastritida fundu a těla žaludku se ztrátou parietálních buněk, končí atrofií sliznice • perniciózní anémie • achlorhydrie – často vznik tzv. mikrokarcinoidózy event. žaludečních karcinoidů (ECL-nádory)

Gastritida typu C - Označována jako chemicky (toxicky) vyvolaná - Obvykle pruhovitá, cirkulárně uspořádaná zarudnutí (zejm. v antru a pyloru) - Histologicky: edém sliznice, rozšířené slizniční cévky a malá ložiska krvácení (chybí zánětlivá infiltrace) - Příčiny: - nefyziologický reflux žluči z duodena - požití léků poškozujících sliznici (NSAID)

Gastritida typu B - v 95% vyvolaná Helicobacter pylori - nejvýraznější v antru – poškozuje zejména D-buňky ( somatostatinu) gastrinu a sekrece HCl ( riziko duodenálního vředu) - po dlouhodobém průběhu – šíří se až na kardii (pangastritida) – ztráta parietálních buněk hypoacidita ( riziko žaludečního vředu) intestinální metaplazie (dysplazie) – riziko adenoca žaludku - Častěji i vznik MALT-lymfomu (z B – buněk)

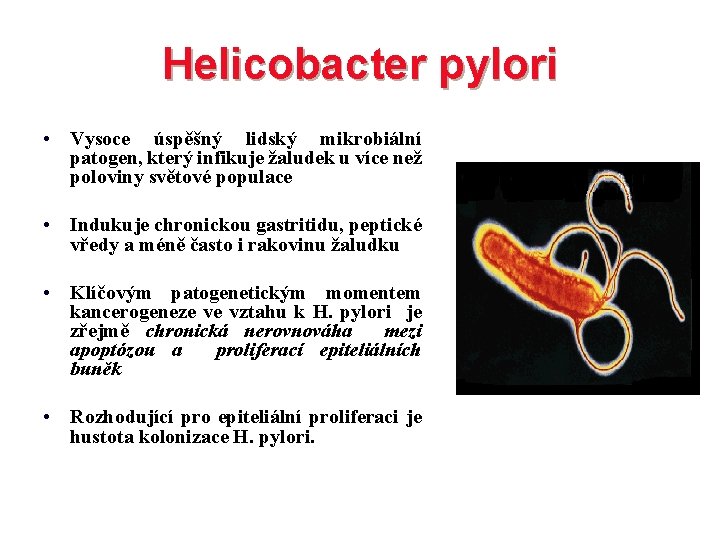
Helicobacter pylori • Vysoce úspěšný lidský mikrobiální patogen, který infikuje žaludek u více než poloviny světové populace • Indukuje chronickou gastritidu, peptické vředy a méně často i rakovinu žaludku • Klíčovým patogenetickým momentem kancerogeneze ve vztahu k H. pylori je zřejmě chronická nerovnováha mezi apoptózou a proliferací epiteliálních buněk • Rozhodující pro epiteliální proliferaci je hustota kolonizace H. pylori.

Helicobacter pylori • Bakterie G - typu, spirálního tvaru, produkující ureázu. • Známa kompletní genomická sekvence. • Nachází se v oblasti antra a v oblastech gastrické metaplazie v duodénu. • H. pylori se nachází nejčastěji pod slizniční vrstvou, kde specificky adheruje k epiteliálním buňkám. • Ke kolonizaci v kyselém prostředí žaludeční sliznice dochází, protože: • Opouzdřený bičík umožňuje H. pylori pohybovat se rychle z kyselého povrchu přes slizniční vrstvu, kde je p. H vyšší (mutované organismy nejsou tak rychlé a nejsou schopny kolonizace). • Akutní infekci provází přechodná hypochlorhydrie. • H. pylori produkuje ureázu. Vznikající amoniak neutralizuje HCl. • H. pylori ovlivňuje protonovou pumpu.

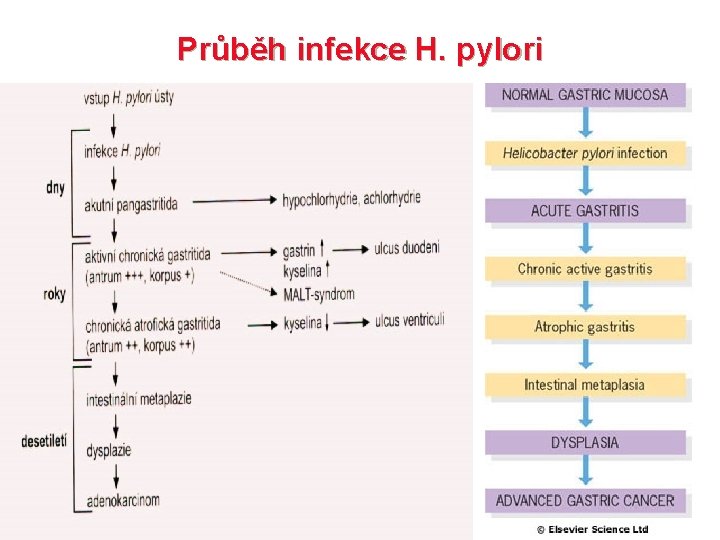
Průběh infekce H. pylori

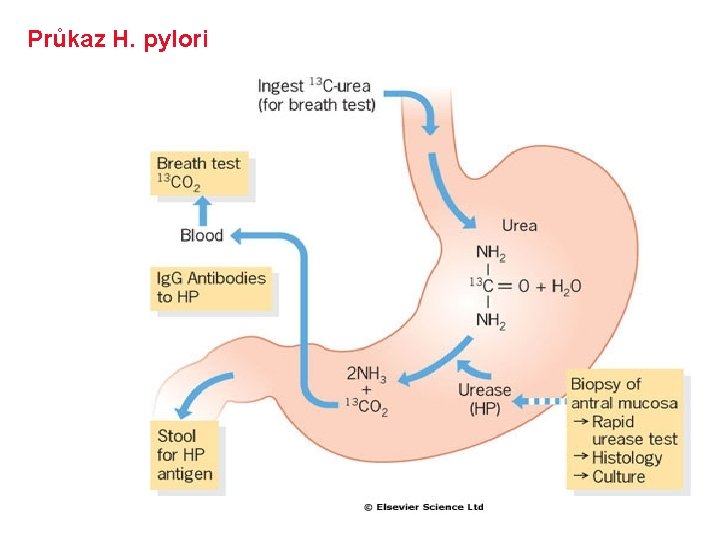
Průkaz H. pylori

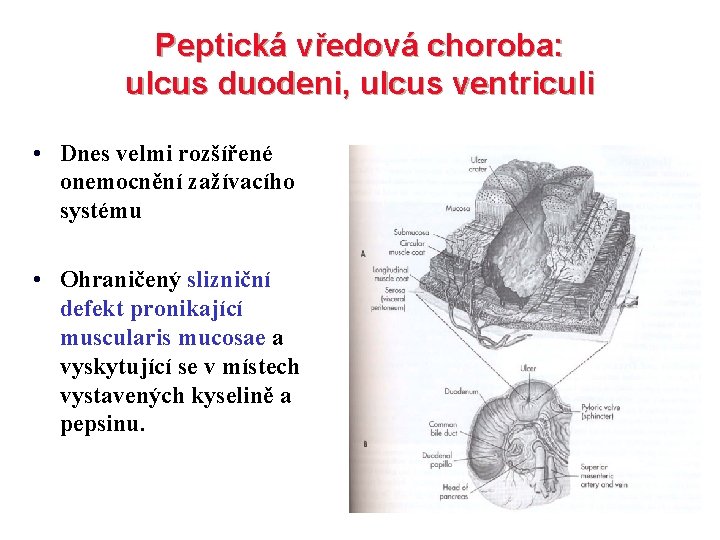
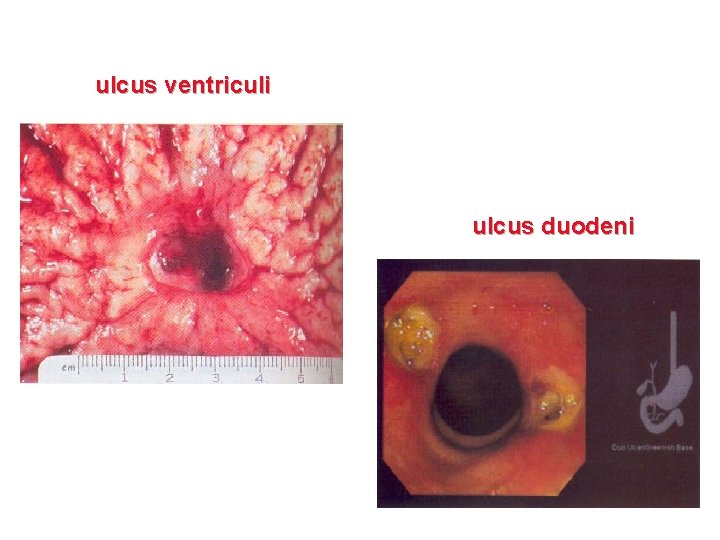
Peptická vředová choroba: ulcus duodeni, ulcus ventriculi • Dnes velmi rozšířené onemocnění zažívacího systému • Ohraničený slizniční defekt pronikající muscularis mucosae a vyskytující se v místech vystavených kyselině a pepsinu.

ulcus ventriculi ulcus duodeni

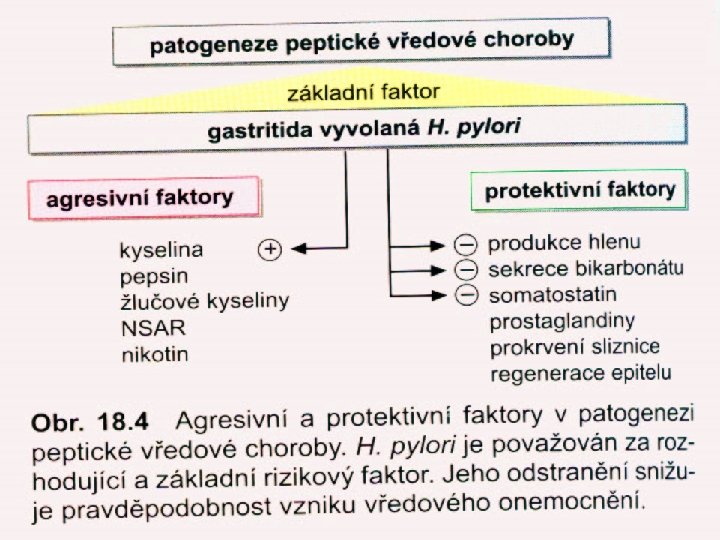
Hypotézy vzniku dříve: „žádná kyselina = žádný vřed“ dnes: výsledek nerovnováhy agresivních a ochranných faktorů

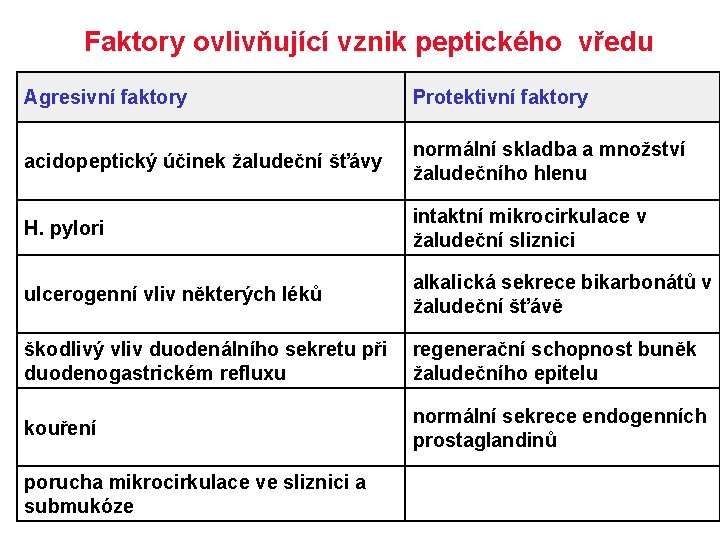
Faktory ovlivňující vznik peptického vředu Agresivní faktory Protektivní faktory acidopeptický účinek žaludeční šťávy normální skladba a množství žaludečního hlenu H. pylori intaktní mikrocirkulace v žaludeční sliznici ulcerogenní vliv některých léků alkalická sekrece bikarbonátů v žaludeční šťávě škodlivý vliv duodenálního sekretu při regenerační schopnost buněk duodenogastrickém refluxu žaludečního epitelu kouření normální sekrece endogenních prostaglandinů porucha mikrocirkulace ve sliznici a submukóze



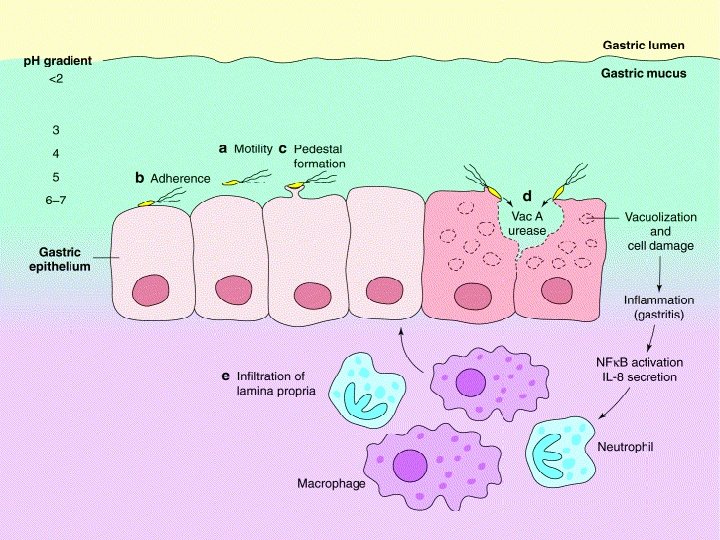
Důležité kroky v patogeneze nemocí žaludku, které jsou spojeny s H. pylori Pro kolonizaci žaludeční sliznice H. pylori je podstatná přítomnost ureázy a motilita. a) Motilitu H. pylori je možno řídit chemotaktickými gradienty, vytvářenými ureou, bikarbonáty nebo hladinami p. H. b) Některé bakterie adherují na epitel a ovlivňují signální transdukci, což vede c) k cytoskeletální přestavbě a tvorbě „patky“. Ta má za následek pohlcení bakterií, polymerizace aktinu a tyrosinovou fosforylaci buněčných proteinů hostitele. d) Toxin Vas. A a ureáza způsobují cytotoxické poškození žaludečního epitelu a bakterie (cag. A+ kmeny) stimulují NF B a uvolnění zánětlivých mediátorů (IL-8), což vede k atrakci makrofágů a neutrofilů. e) Tento buněčný infiltrát v l. propria způsobuje zánětlivou reakci (chronickou aktivní gastritidu), což je podklad celé patologie podmíněné H. pylori


Helicobacter pylori • Předpokládá se , že H. pylori má ve své ekologické nice limitovanou dodávku živin. • Růst H. pylori může proto favorizovat destrukce tkání indukovaná ROS. • H. pylori indukuje neutrofilní infiltraci a inhibuje fagocytózu. • Prerekvizitou pro bakteriální přežití je schopnost uniknout destrukci neutrofily, čili schopnost uniknout fagocytóze.

Mechanizmy působení H. pylori Vede k indukci prozánětlivých cytokinových a chemokinových genů, aktivaci transkripčních faktorů časné odpovědi (NF- B a AP-1), GTPáz a na stres odpovídajících kináz (JNK a p 38). Nezávisle na tomto sekrečním systému Helicobacter pylori reguluje promotory genů, které se účastní • v sekreci HCl (histidin dekarboxyláza) • v syntéze prostaglandinů (COX-2) • v syntéze transkripčních faktorů (BP ( -protein)-1, BP-2, USF (upstream stimulatory factor) -1, USF-2 a CREB (c-AMP responsive element binding protein) • proliferačních GTPáz • MAP (mitogen activating) kináz

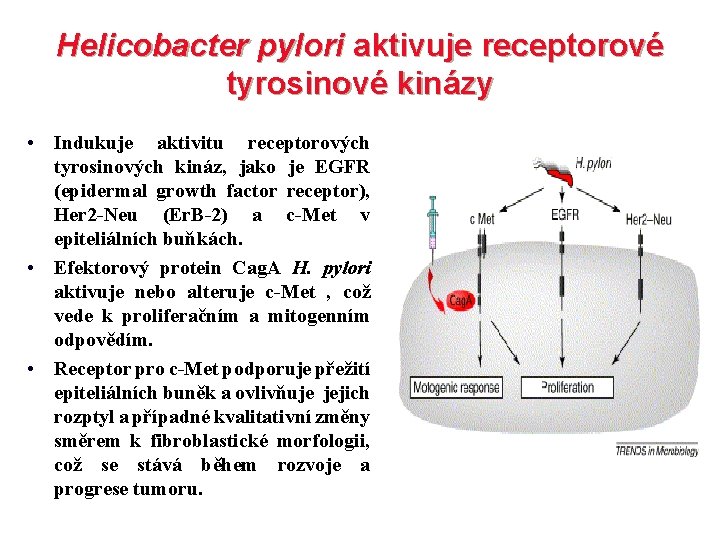
Helicobacter pylori aktivuje receptorové tyrosinové kinázy • Indukuje aktivitu receptorových tyrosinových kináz, jako je EGFR (epidermal growth factor receptor), Her 2 -Neu (Er. B-2) a c-Met v epiteliálních buňkách. • Efektorový protein Cag. A H. pylori aktivuje nebo alteruje c-Met , což vede k proliferačním a mitogenním odpovědím. • Receptor pro c-Met podporuje přežití epiteliálních buněk a ovlivňuje jejich rozptyl a případné kvalitativní změny směrem k fibroblastické morfologii, což se stává během rozvoje a progrese tumoru.

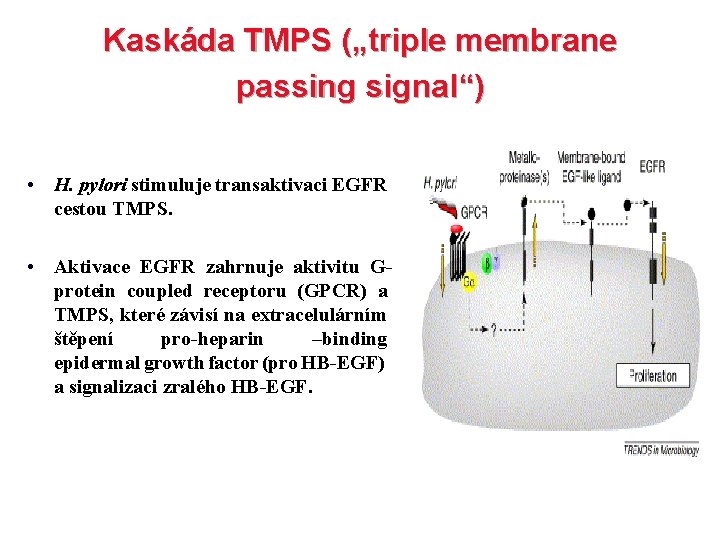
Kaskáda TMPS („triple membrane passing signal“) • H. pylori stimuluje transaktivaci EGFR cestou TMPS. • Aktivace EGFR zahrnuje aktivitu Gprotein coupled receptoru (GPCR) a TMPS, které závisí na extracelulárním štěpení pro-heparin –binding epidermal growth factor (pro HB-EGF) a signalizaci zralého HB-EGF.

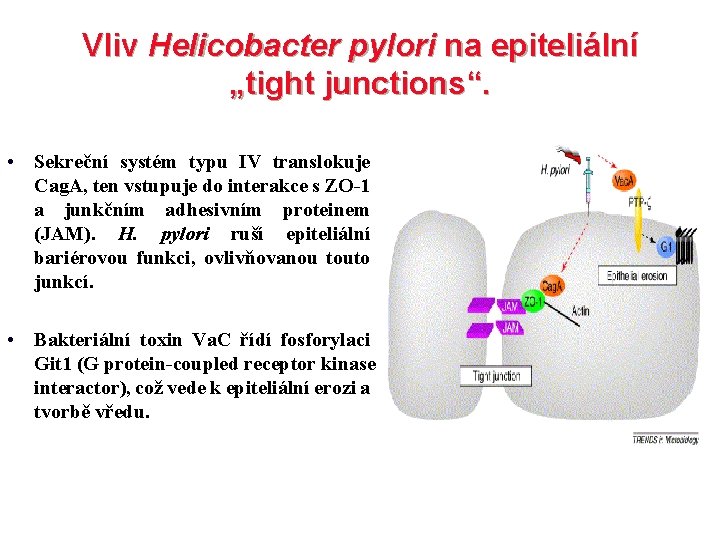
Vliv Helicobacter pylori na epiteliální „tight junctions“. • Sekreční systém typu IV translokuje Cag. A, ten vstupuje do interakce s ZO-1 a junkčním adhesivním proteinem (JAM). H. pylori ruší epiteliální bariérovou funkci, ovlivňovanou touto junkcí. • Bakteriální toxin Va. C řídí fosforylaci Git 1 (G protein-coupled receptor kinase interactor), což vede k epiteliální erozi a tvorbě vředu.

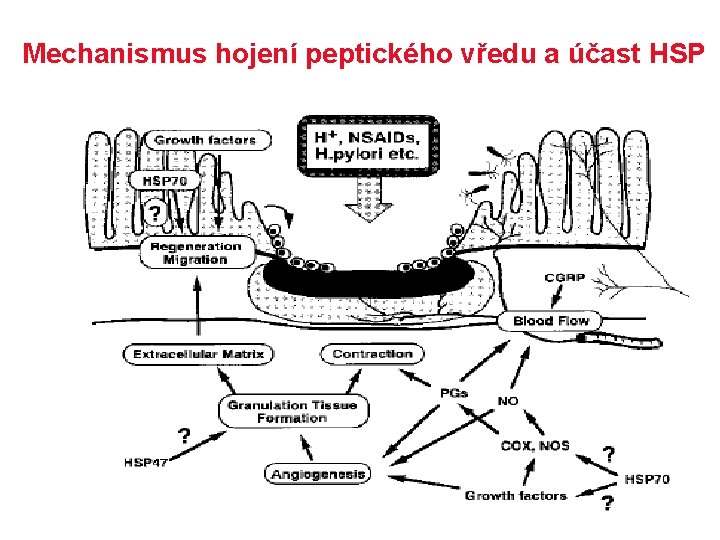
Mechanismus hojení peptického vředu a účast HSP

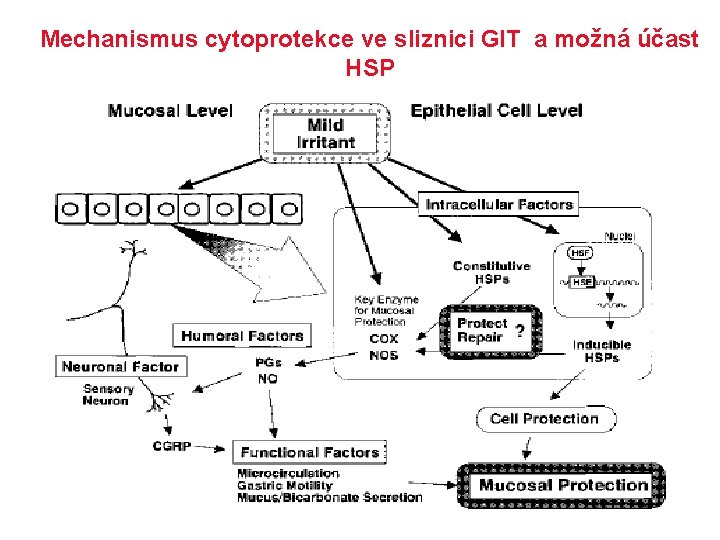
Mechanismus cytoprotekce ve sliznici GIT a možná účast HSP