VARIABILIDADE GENTICA SEQUENCIA CODIFICANTE Droga neurobloqueadora adrenrgica MICROSSATLITE

VARIABILIDADE GENÉTICA
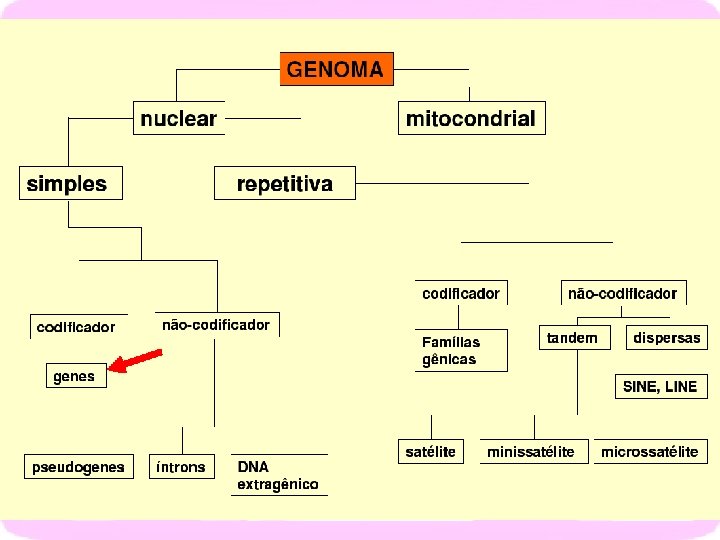
SEQUENCIA CODIFICANTE

Droga neurobloqueadora adrenérgica


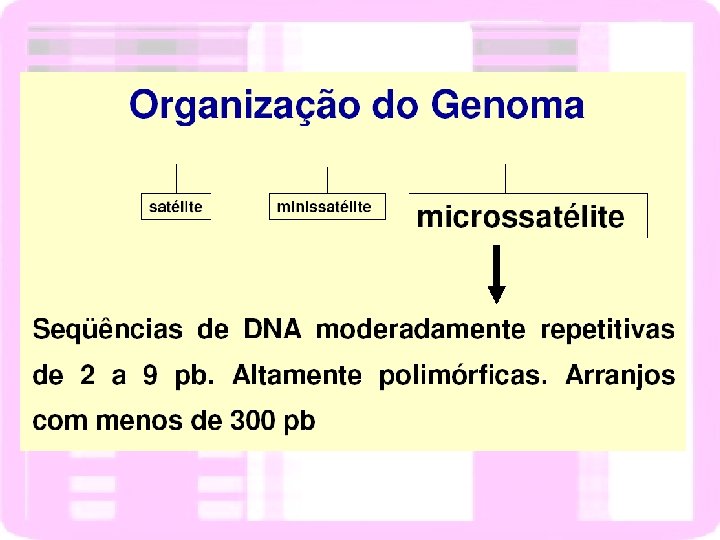
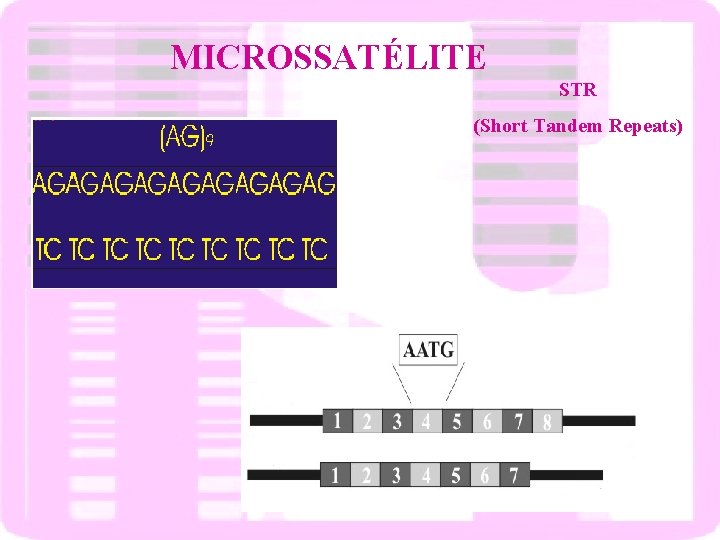
MICROSSATÉLITE STR (Short Tandem Repeats)
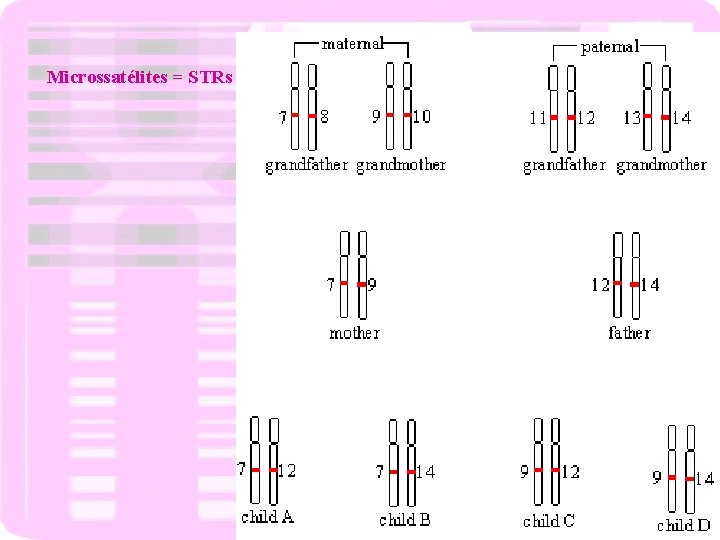
Microssatélites = STRs
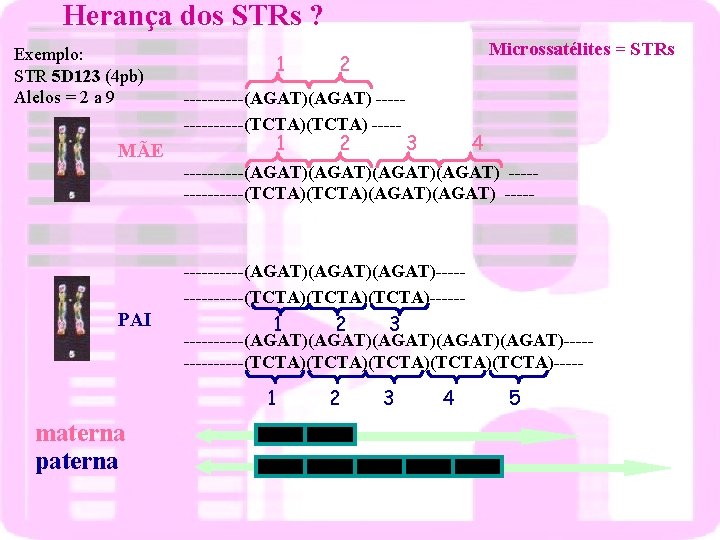
Herança dos STRs ? Exemplo: STR 5 D 123 (4 pb) Alelos = 2 a 9 1 Microssatélites = STRs 2 -----(AGAT) -------(TCTA) ----- 1 MÃE 2 3 4 -----(AGAT)(AGAT) -------(TCTA)(AGAT) ----------(AGAT)(AGAT)-------(TCTA)(TCTA)------ PAI materna paterna 1 2 3 -----(AGAT)(AGAT)(AGAT)-------(TCTA)(TCTA)(TCTA)----- 4 5
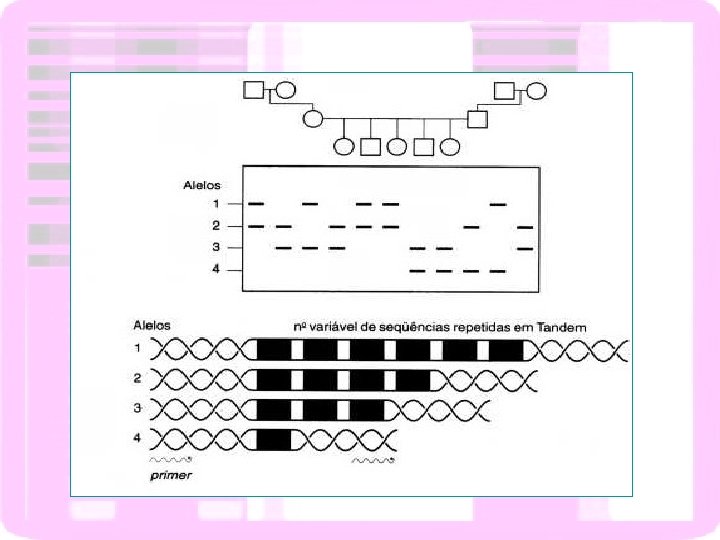

Variabilidade do DNA

MUTAÇÃO E REPARO DO DNA

MUTAÇÃO: Alteração do material genético Processo de alteração da sequência de DNA Alteração na sequência de nucleotídeos Espontânea: decorrentes do funcionamento celular normal Induzida: exposição do organismo à agentes mutagênicos ALTERAÇÕES DO GENÓTIPO: Euploidias e aneuploidias Rearranjos cromossômicos Alterações em genes individuais FONTE DE VARIABILIDADE GENÉTICA Somática - Germinal MATERIAL PARA EVOLUÇÃO MUTANTE: organismo que apresenta um novo fenótipo resultante da presença da mutação POSSIBILITA ADAPTAÇÃO À NOVOS AMBIENTES

TIPOS DE MUTAÇÃO SEQÜÊNCIA ORIGINAL AAGGCAAACCTACTGGTCTTATGT TRANSIÇÃO AAGGCAAATCTACTGGTCTTATGT TRANSVERSÃO AAGGCAAACCTACTGCTCTTATGT DELEÇÃO INSERÇÃO INVERSÃO ACCTA AAGGCAACTGGTCTTATGT AAGGCAAACCTACTAAAGCGGTCTTATGT AAGGTTTGCCTACTGGTCTTATGT
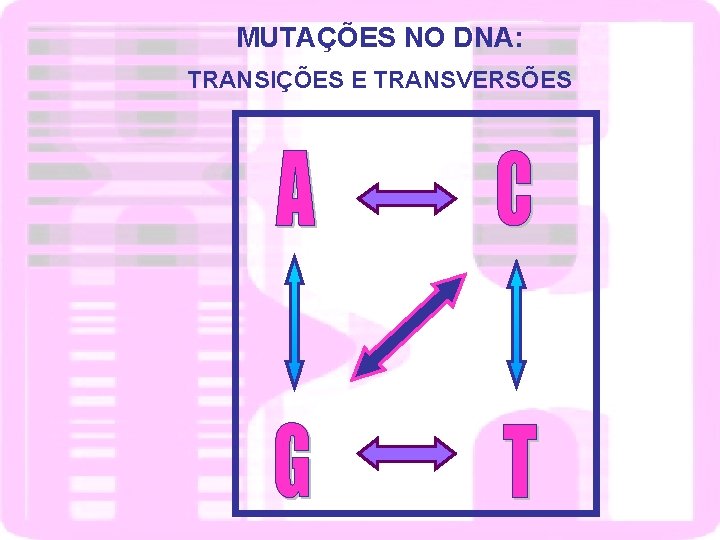
MUTAÇÕES NO DNA: TRANSIÇÕES E TRANSVERSÕES

MUTAÇÕES GÊNICA - regiões codificantes Mutação silenciosa- código degenerado Mutação com sentido alterado- altera aminoácido Mutação neutra- troca de aminoácidos sem alteração da função do polipeptídeo Mutação de janela de leitura- deleção ou inserção de nucleotídeos em número diferente de 3
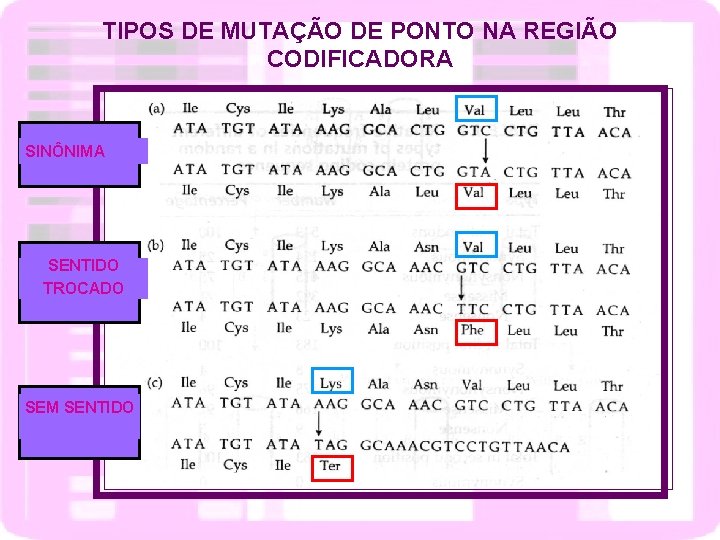
TIPOS DE MUTAÇÃO DE PONTO NA REGIÃO CODIFICADORA SINÔNIMA SENTIDO TROCADO SEM SENTIDO

INSERÇÃO E DELEÇÃO CAUSAM ALTERAÇÕES NO QUADRO DE LEITURA (frameshift) DELEÇÃO INSERÇÃO UMA DELEÇÃO DE G CAUSA O TÉRMINO PREMATURO DA CADEIA E UMA INSERÇÃO DE G OBLITERA O CÓDON DE FINALIZAÇÃO.

NOMENCLATURA PARA DESCRIÇÃO DAS MUTAÇÕES ( Antonarakis et al. (1998) SUBSTITUIÇÃO DE AMINOÁCIDOS Código de uma letra: A, alanine; C, cisteine; D, acido aspartico; E, acido glutamico; F, phenilalanina; G, glicina; H, histidina; I, isoleucina; K, lisina; M, metionina; N, asparagina; P, prolina; Q, glutamina; R, arginina; S, serina; T, treonina; V, valina; W, triptofano; Y, tirosina; X fim. O código de 3 letras também é aceito. R 117 H ou Arg 117 His - substitui arginina 117 pela histidina (o codon iniciador- metionina é o codon 1). G 542 X or Gly 542 Stop - glicina 542 substituida pelo codon de terminação SUBSTITUIÇÃO DE NUCLEOTÍDEO O A do codon de iniciação ATG é +1; a base imediatamente precedente é -1. Não há zero. Número do nucleotídeo seguido pela alteração. Se necessário usar g ou c para designar sequências genomicas e de c. DNA. Para sequencias intronicas, quando apenas a sequência de c. DNA é conhecida, especificar o número do intronpor IVSn ou pelo número da posição no exon mais próxima 1162 G>A - substitui guanina na posição 1162 pela adenina. 621+1 G>T ou IVS 4+1 G>T - substitui G por T na primeira base do intron 4; exon 4 termina no nt 621. DELEÇÕES E INSERÇÕES Use del para deleções e ins para inserções. Como acima, para alterações no DNA , alterações na posição do nucleotídeo ou intervalo vem primeiro, para alterações nos aminoácidos, o símbolo vêm primeiro F 508 del - deleção fenilalanina 508 6232 -6236 del ou 6232 -6236 del. ATAAG - deleção 5 nucleotideos (os quais podem ser específicados) começando com nt 6232. 409 -410 ins. C - inserção C entre nt 409 e 410

Frequência de mutação: Bactéria: 1 mutação / 108 humano: 1 mutação/109 -acuracidade da maquinária de replicação do DNA -Eficiência do sistema de reparo -Exposição à agentes mutagênicos -Proporcional ao tamanho do gene HOTSPOTS – regiões preferenciais de mutação

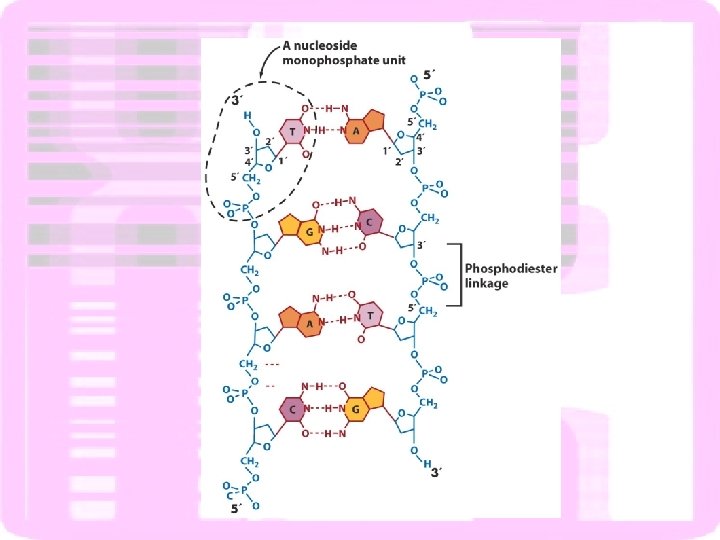
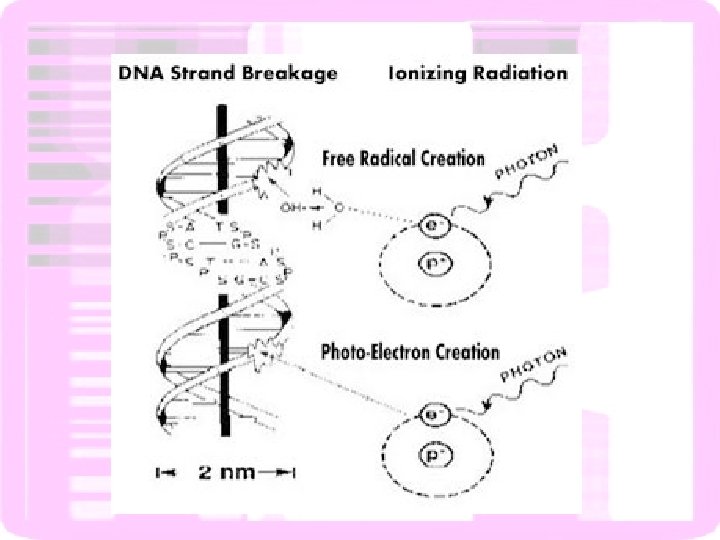
Lesão no DNA- alteração na estrutura da dupla hélice - Alteram a capacidade de replicação e transcrição - Disparam os mecanismos de reparo do DNA INADMISSÍVEIS PARA A CÉLULA
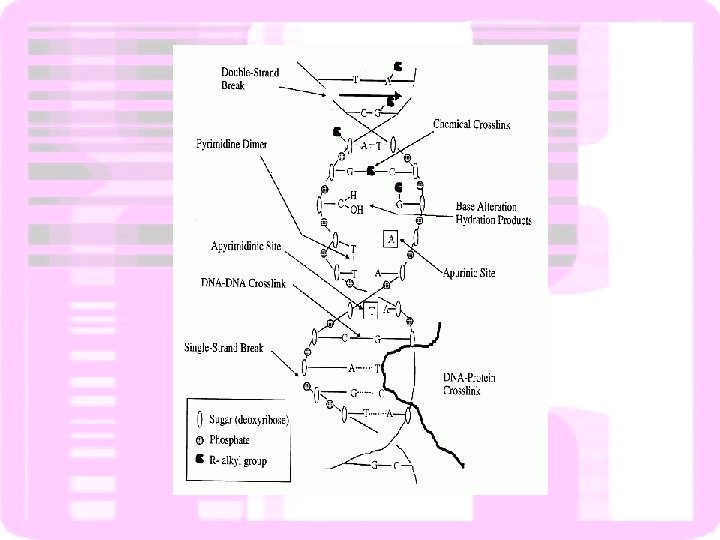
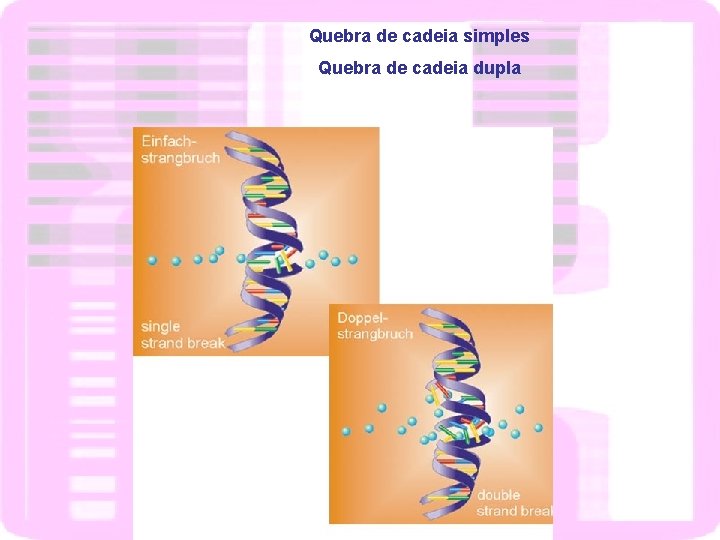
Quebra de cadeia simples Quebra de cadeia dupla
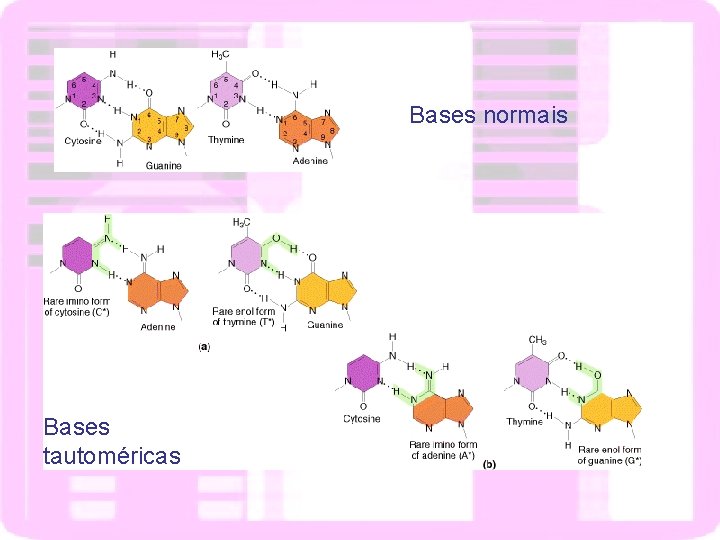
Bases normais Bases tautoméricas
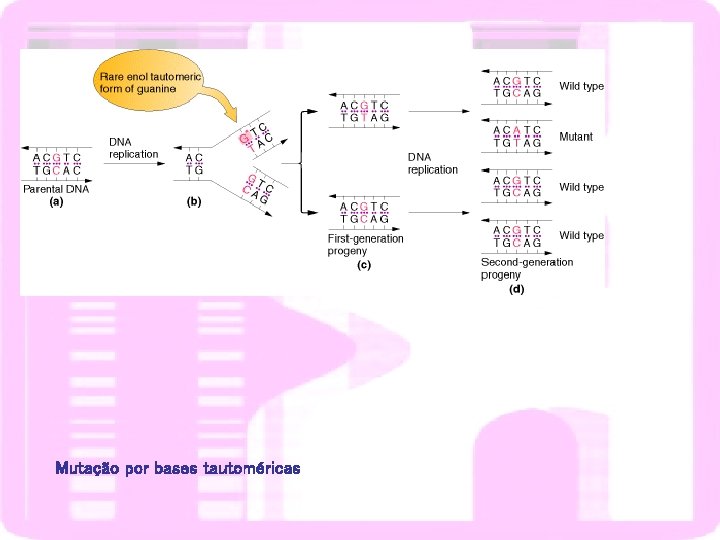
Mutação por bases tautoméricas

Modelo de Streisinger – mudança de matriz de leitura

Deleções em lac I

Sequências de DNA mitocondrial tipo selvagem e de DNA deletado de um paciente com síndrome de Kearns-Sayre

Expansão de uma trinca CGG no gene FMR-1 observada na síndrome do X-frágil

ALTERAÇÕES DE BASES
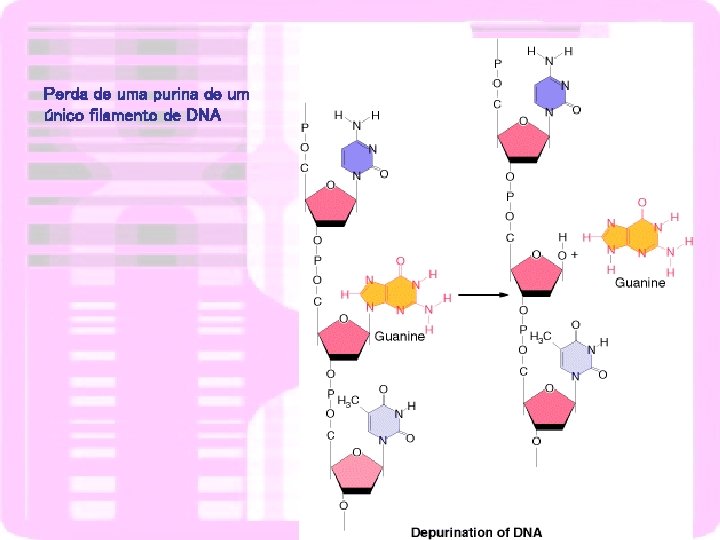
Perda de uma purina de um único filamento de DNA
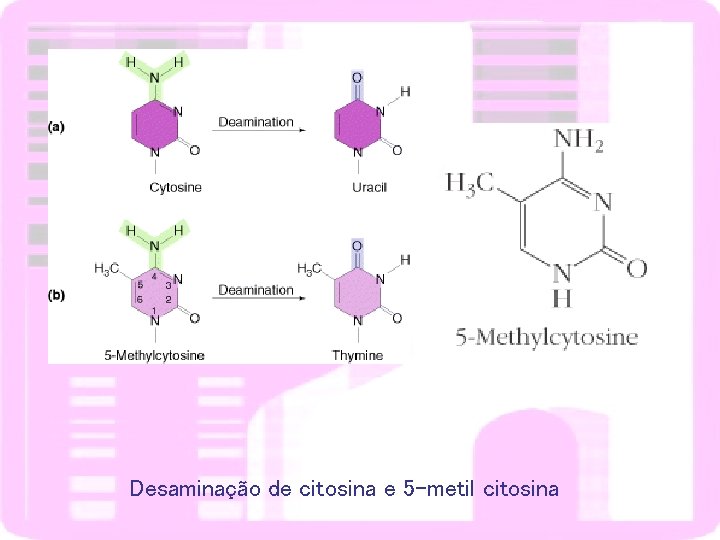
Desaminação de citosina e 5 -metil citosina
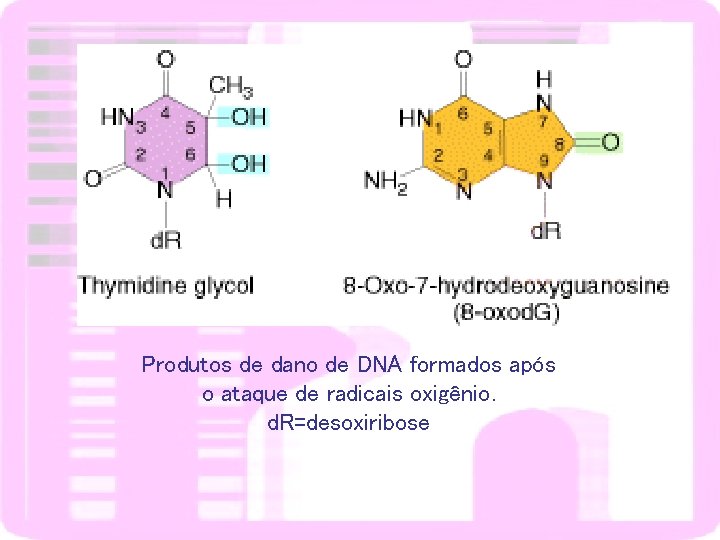
Produtos de dano de DNA formados após o ataque de radicais oxigênio. d. R=desoxiribose
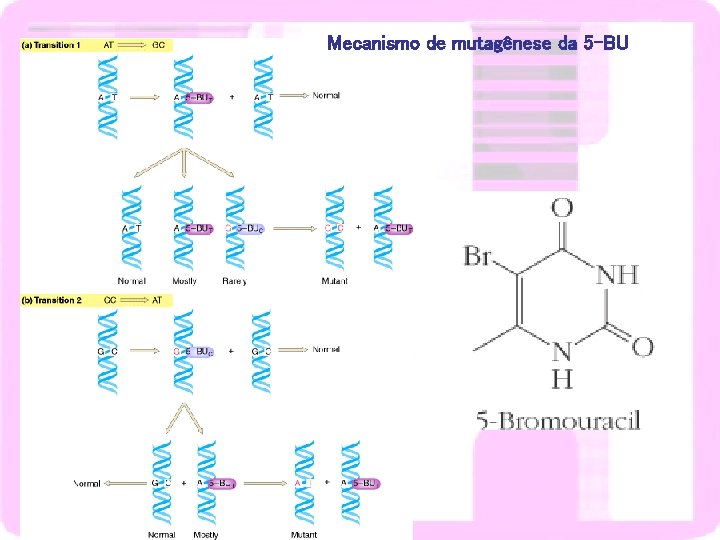
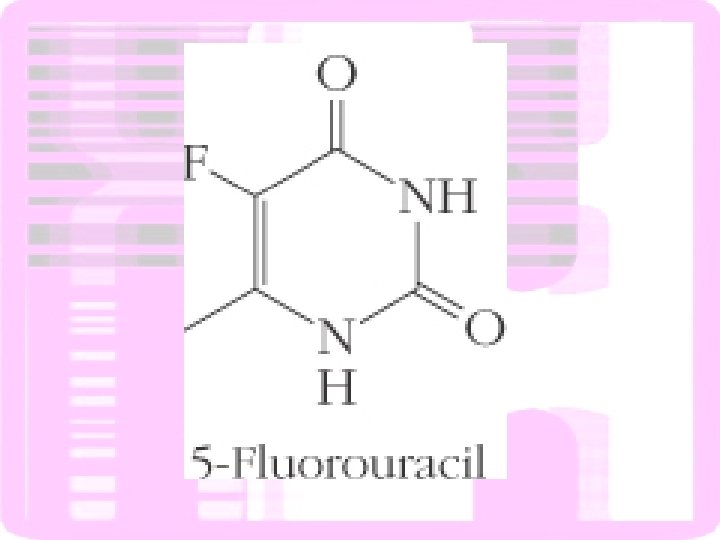
Mecanismo de mutagênese da 5 -BU
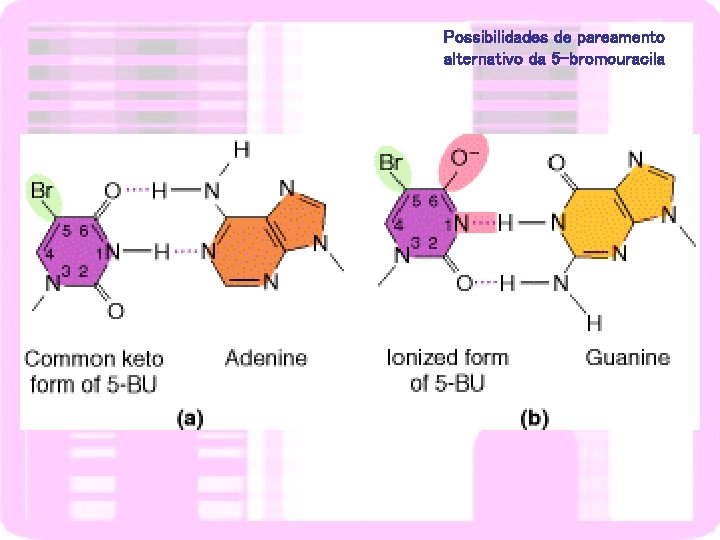
Possibilidades de pareamento alternativo da 5 -bromouracila
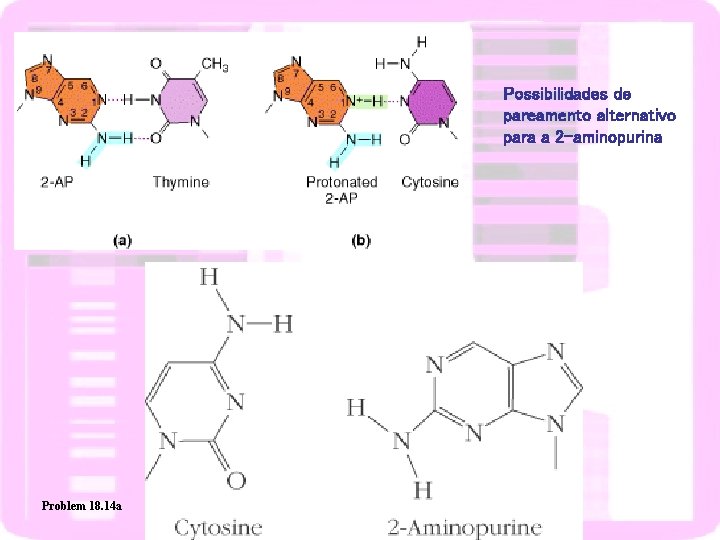
Possibilidades de pareamento alternativo para a 2 -aminopurina Problem 18. 14 a
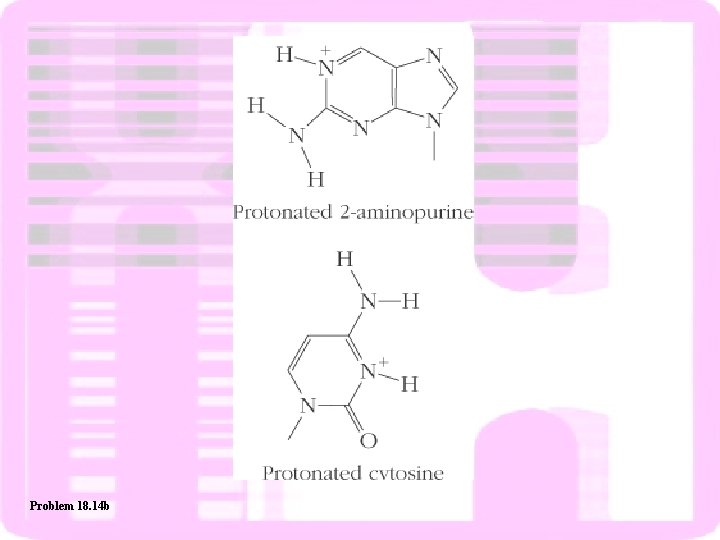
Problem 18. 14 b
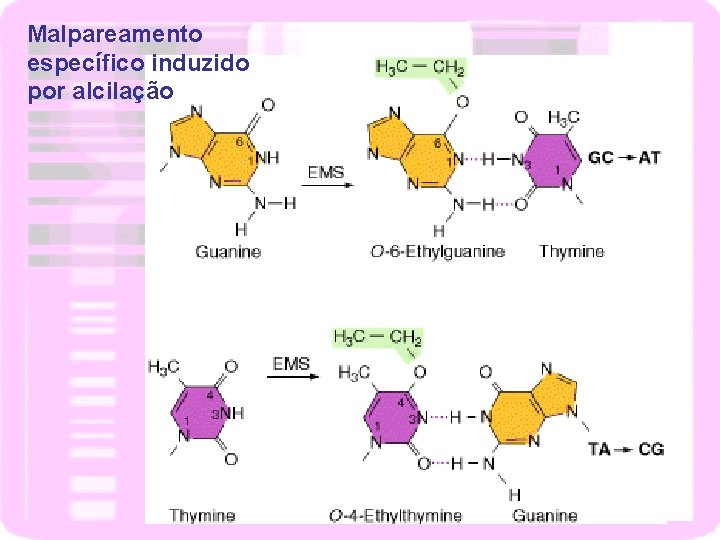
Malpareamento específico induzido por alcilação
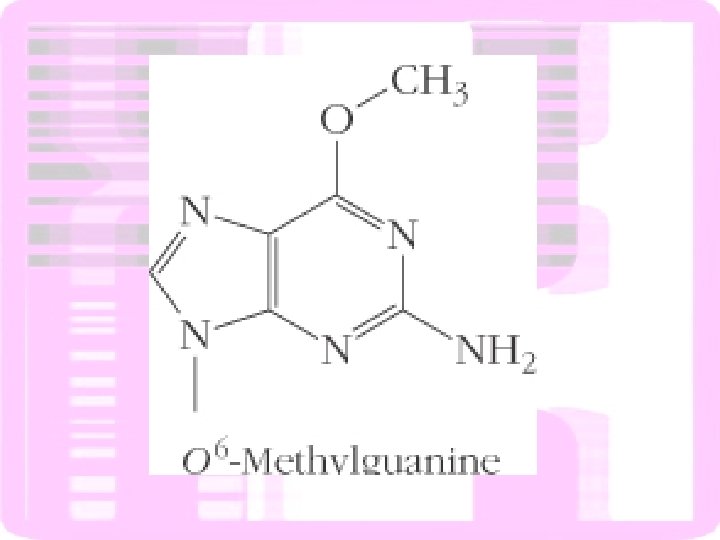
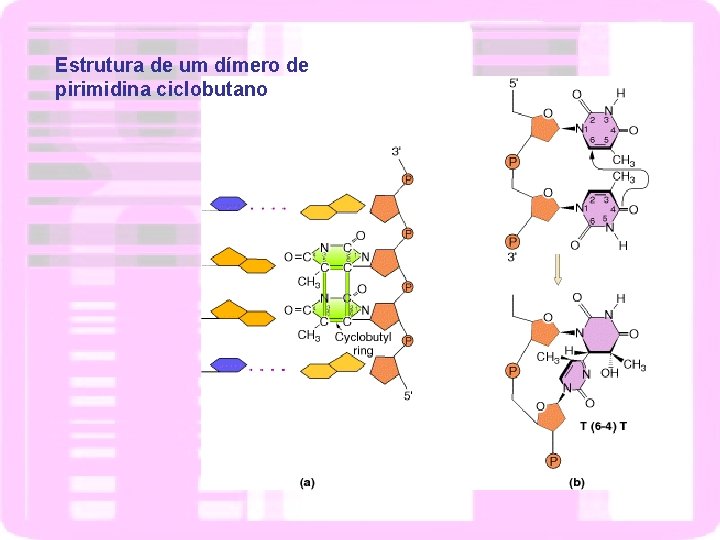
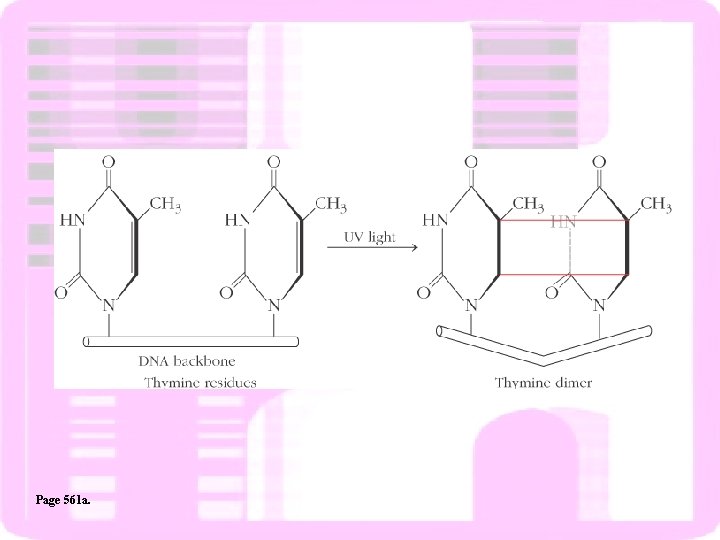
Estrutura de um dímero de pirimidina ciclobutano
Page 561 a.
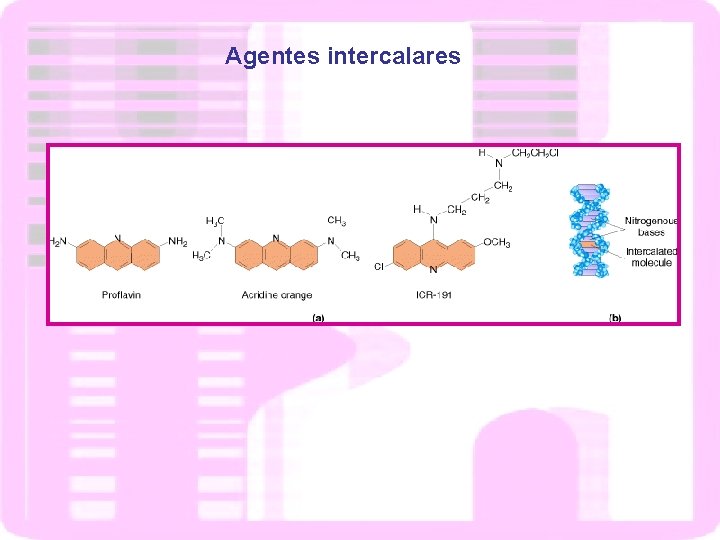
Agentes intercalares
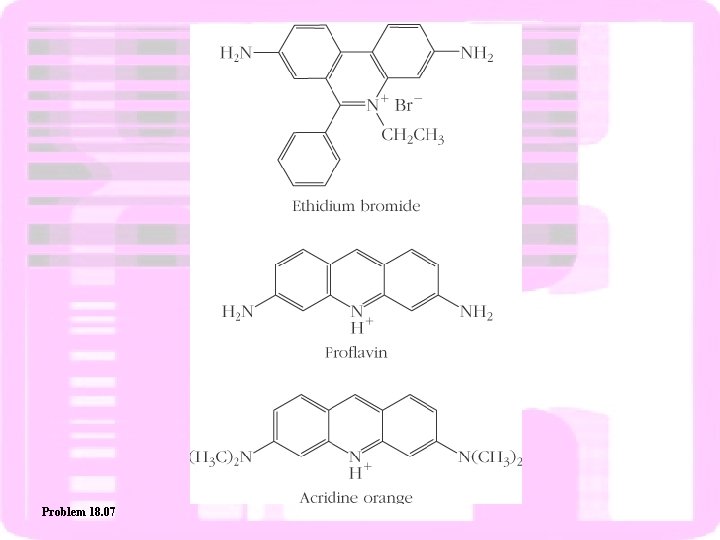
Problem 18. 07

Page 561 b.
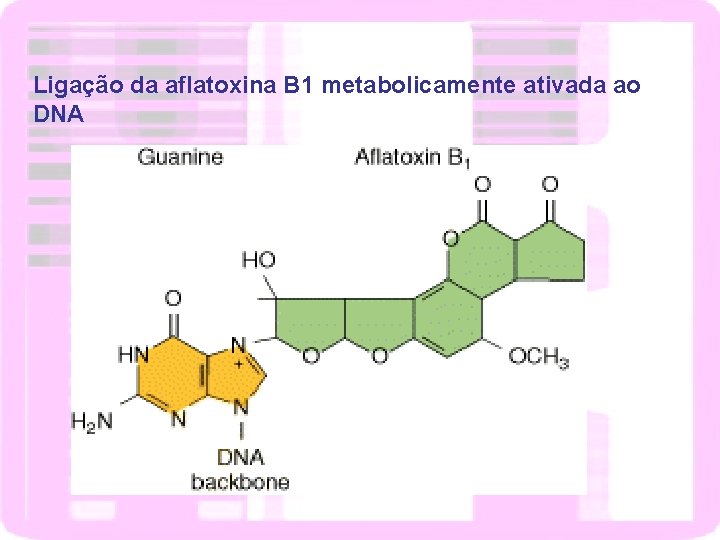
Ligação da aflatoxina B 1 metabolicamente ativada ao DNA
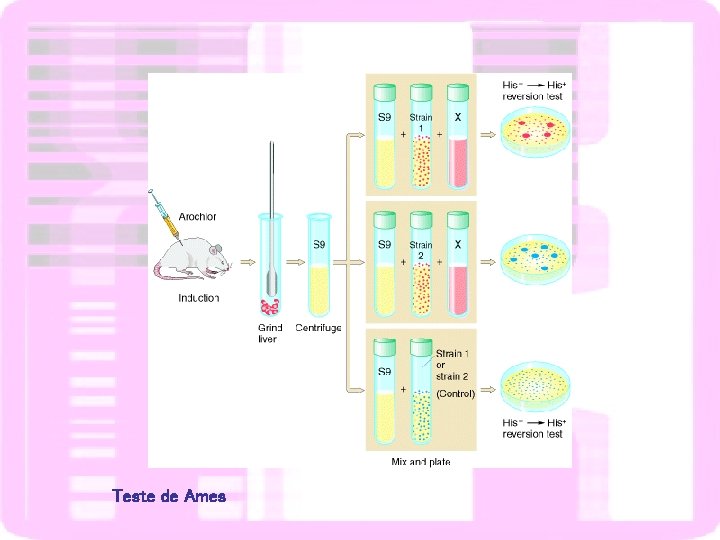
Teste de Ames
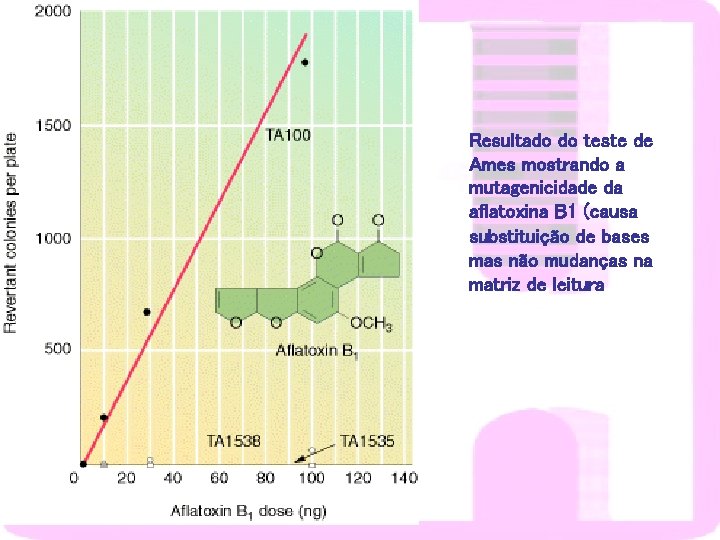
Resultado do teste de Ames mostrando a mutagenicidade da aflatoxina B 1 (causa substituição de bases mas não mudanças na matriz de leitura
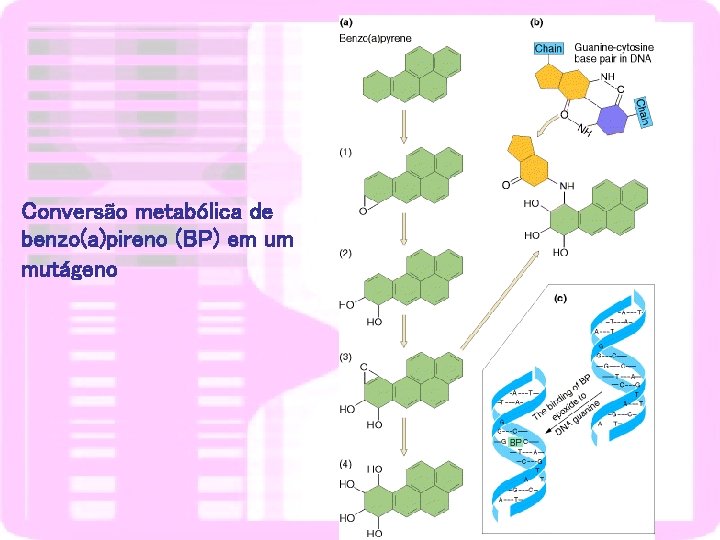
Conversão metabólica de benzo(a)pireno (BP) em um mutágeno
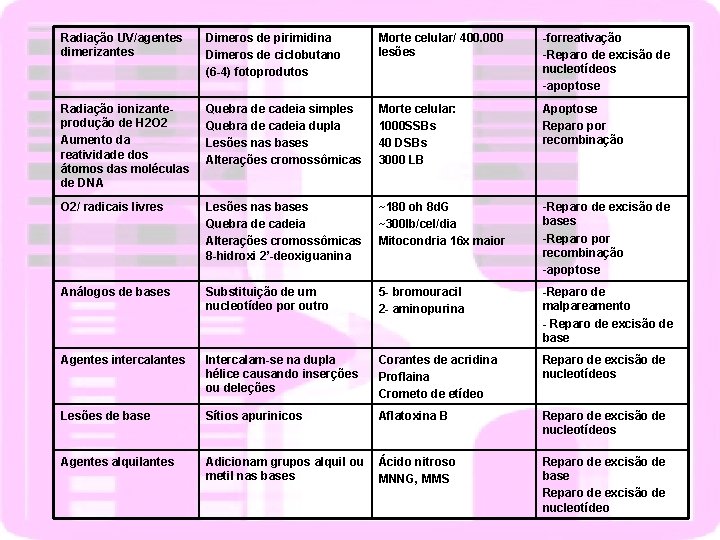
Radiação UV/agentes dimerizantes Dimeros de pirimidina Dimeros de ciclobutano (6 -4) fotoprodutos Morte celular/ 400. 000 lesões -forreativação -Reparo de excisão de nucleotídeos -apoptose Radiação ionizanteprodução de H 2 O 2 Aumento da reatividade dos átomos das moléculas de DNA Quebra de cadeia simples Quebra de cadeia dupla Lesões nas bases Alterações cromossômicas Morte celular: 1000 SSBs 40 DSBs 3000 LB Apoptose Reparo por recombinação O 2/ radicais livres Lesões nas bases Quebra de cadeia Alterações cromossômicas 8 -hidroxi 2’-deoxiguanina ~180 oh 8 d. G ~300 lb/cel/dia Mitocondria 16 x maior -Reparo de excisão de bases -Reparo por recombinação -apoptose Análogos de bases Substituição de um nucleotídeo por outro 5 - bromouracil 2 - aminopurina -Reparo de malpareamento - Reparo de excisão de base Agentes intercalantes Intercalam-se na dupla hélice causando inserções ou deleções Corantes de acridina Proflaina Crometo de etídeo Reparo de excisão de nucleotídeos Lesões de base Sítios apurinicos Aflatoxina B Reparo de excisão de nucleotídeos Agentes alquilantes Adicionam grupos alquil ou metil nas bases Ácido nitroso MNNG, MMS Reparo de excisão de base Reparo de excisão de nucleotídeo

MECANISMOS DE REPARO DO DNA Lesões no DNA: nível de SSBs- interrupção na síntese de DNA Lesões no DNA: bloqueiam DNA e RNA polimerase Relacionadas ao envelhecimento Relacionadas ao aparecimento de câncer
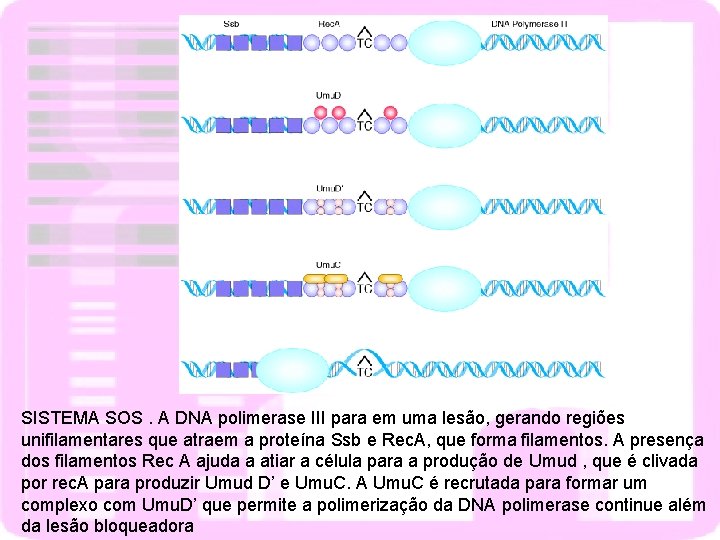
SISTEMA SOS. A DNA polimerase III para em uma lesão, gerando regiões unifilamentares que atraem a proteína Ssb e Rec. A, que forma filamentos. A presença dos filamentos Rec A ajuda a atiar a célula para a produção de Umud , que é clivada por rec. A para produzir Umud D’ e Umu. C. A Umu. C é recrutada para formar um complexo com Umu. D’ que permite a polimerização da DNA polimerase continue além da lesão bloqueadora

FOTORREATIVAÇÃO REVERSÃO DOS DÍMEROS DE PIRIMIDINA DEPENDENTE DA LUZ VISÍVEL ENZIMA FOTOLIASE (enzima não presente em mamíferos placentários) REPARO DE EXCISÃO DE NUCLEOTÍDEOS Reconhecimento da lesão Incisão da cadeia do DNA – exinuclease Excisão do segmento com lesão – DNA helicase Síntese de um novo segmento de DNA – DNA polimerase Ligação do segmento de DNA sintetizado – DNA ligase
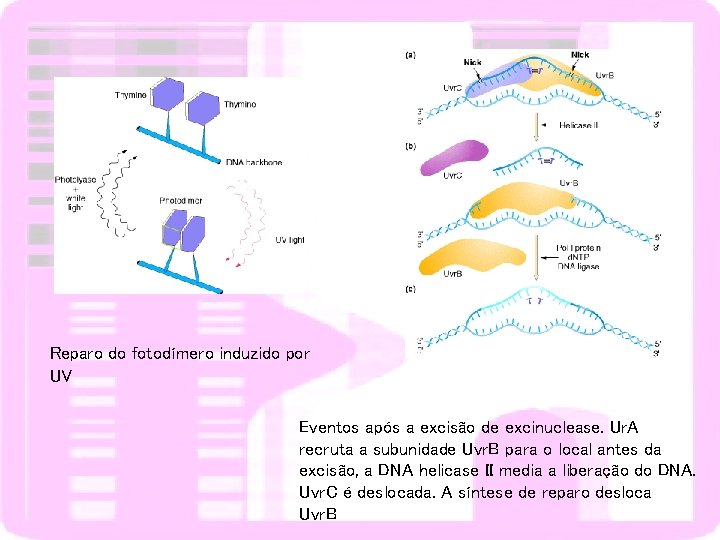
Reparo do fotodímero induzido por UV Eventos após a excisão de excinuclease. Ur. A recruta a subunidade Uvr. B para o local antes da excisão, a DNA helicase II media a liberação do DNA. Uvr. C é deslocada. A síntese de reparo desloca Uvr. B
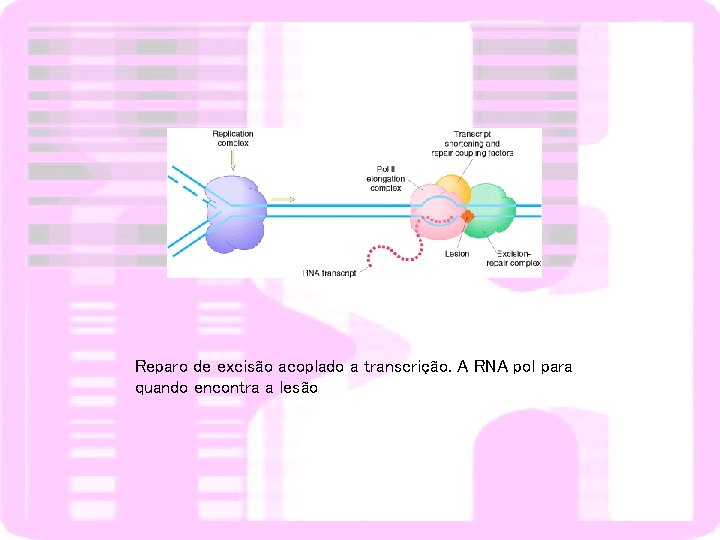
Reparo de excisão acoplado a transcrição. A RNA pol para quando encontra a lesão

REPARO DE EXCISÃO DE BASE Alvo bases modificadas Remoção da base (deaminação) – DNA glicosilase Remoção do nucleotídeo (depurinação)– AP endonucleases Colocação do novo nucleotídeo
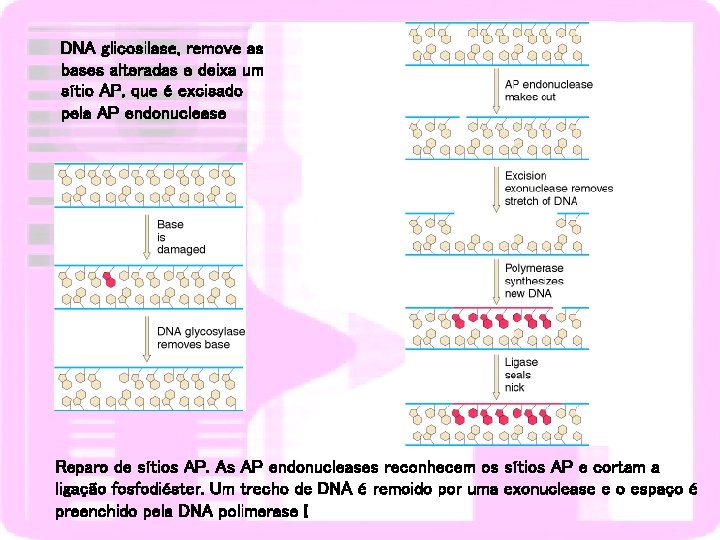
DNA glicosilase, remove as bases alteradas e deixa um sítio AP, que é excisado pela AP endonuclease Reparo de sítios AP. As AP endonucleases reconhecem os sítios AP e cortam a ligação fosfodiéster. Um trecho de DNA é remoido por uma exonuclease e o espaço é preenchido pela DNA polimerase I
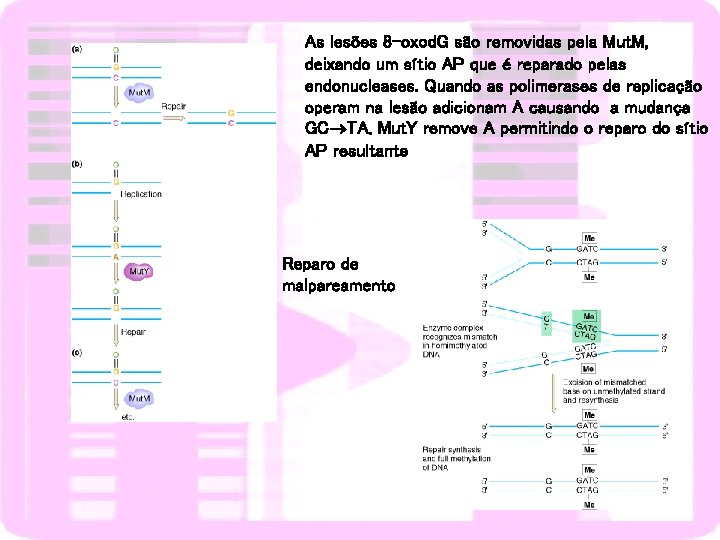
As lesões 8 -oxod. G são removidas pela Mut. M, deixando um sítio AP que é reparado pelas endonucleases. Quando as polimerases de replicação operam na lesão adicionam A causando a mudança GC TA. Mut. Y remove A permitindo o reparo do sítio AP resultante Reparo de malpareamento

REPARO DE MALPAREAMENTO (MISMATCH)/ checagem pós-replicação Erros originados durante a replicação do DNA rastramento do DNA remoção da lesão síntese de DNA polimerase- atividade exonuclease 3’-5’ Diferencia a cadeia certa da cadeia errada
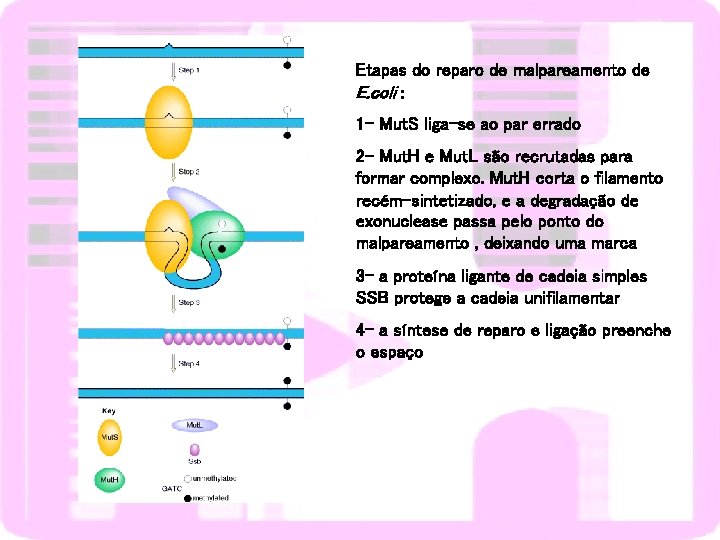
Etapas do reparo de malpareamento de E. coli : 1 - Mut. S liga-se ao par errado 2 - Mut. H e Mut. L são recrutadas para formar complexo. Mut. H corta o filamento recém-sintetizado, e a degradação de exonuclease passa pelo ponto do malpareamento , deixando uma marca 3 - a proteína ligante de cadeia simples SSB protege a cadeia unifilamentar 4 - a síntese de reparo e ligação preenche o espaço
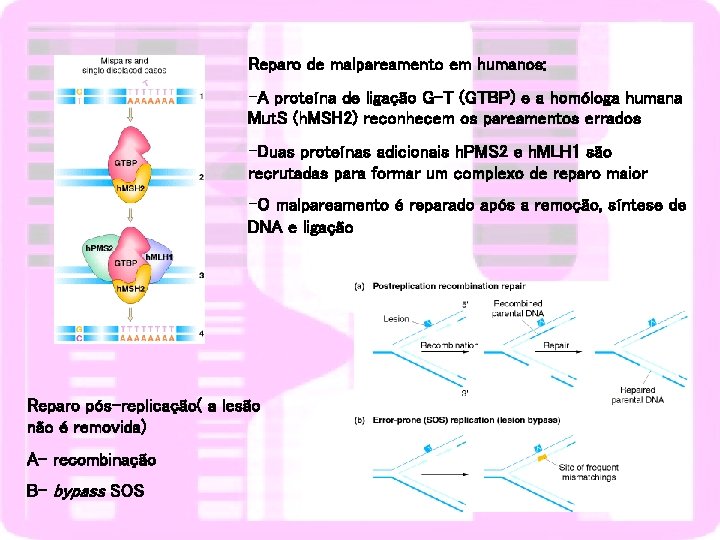
Reparo de malpareamento em humanos: -A proteína de ligação G-T (GTBP) e a homóloga humana Mut. S (h. MSH 2) reconhecem os pareamentos errados -Duas proteínas adicionais h. PMS 2 e h. MLH 1 são recrutadas para formar um complexo de reparo maior -O malpareamento é reparado após a remoção, síntese de DNA e ligação Reparo pós-replicação( a lesão não é removida) A- recombinação B- bypass SOS

REPARO PÓS-REPLICAÇÃO envolve recombinação com o cromossomo homólogo SISTEMA SOS (E. coli) Induzido por agentes que lesam o DNA ou inibem a replicação (UV, agentes alquilantes, cross-link) Aumento da capacidade de reparo do DNA Sinal ativador- presença de região de cadeia simples no local MORTE CELULAR (apoptose) Lesões acima da capacidade dereparo da célula Fragmentação do DNA nos nucleossomos Morte celular programada
- Slides: 65