Vancomicina La base molecolare del suo meccanismo dazione

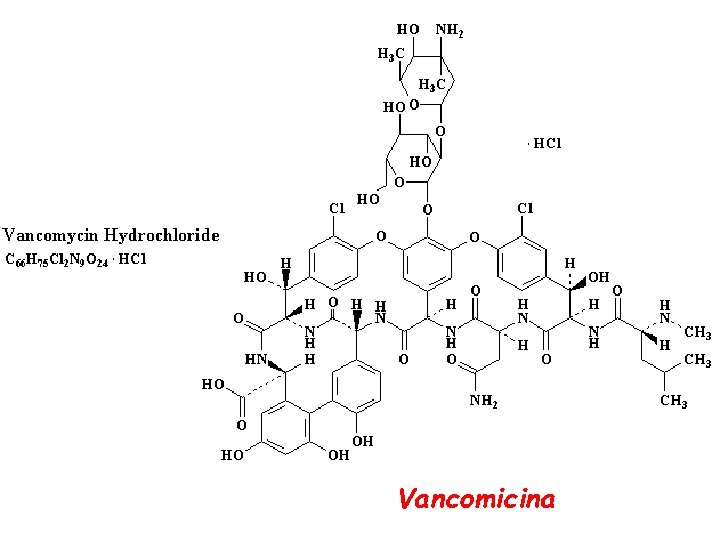
Vancomicina
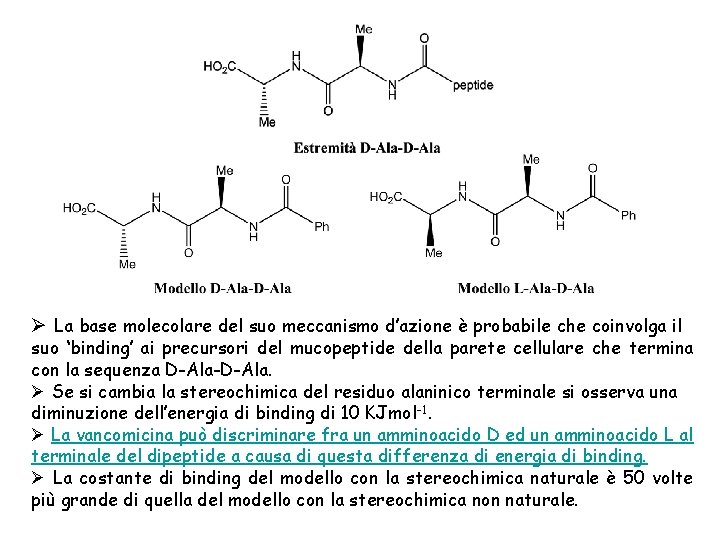
Ø La base molecolare del suo meccanismo d’azione è probabile che coinvolga il suo ‘binding’ ai precursori del mucopeptide della parete cellulare che termina con la sequenza D-Ala-D-Ala. Ø Se si cambia la stereochimica del residuo alaninico terminale si osserva una diminuzione dell’energia di binding di 10 KJmol-1. Ø La vancomicina può discriminare fra un amminoacido D ed un amminoacido L al terminale del dipeptide a causa di questa differenza di energia di binding. Ø La costante di binding del modello con la stereochimica naturale è 50 volte più grande di quella del modello con la stereochimica non naturale.
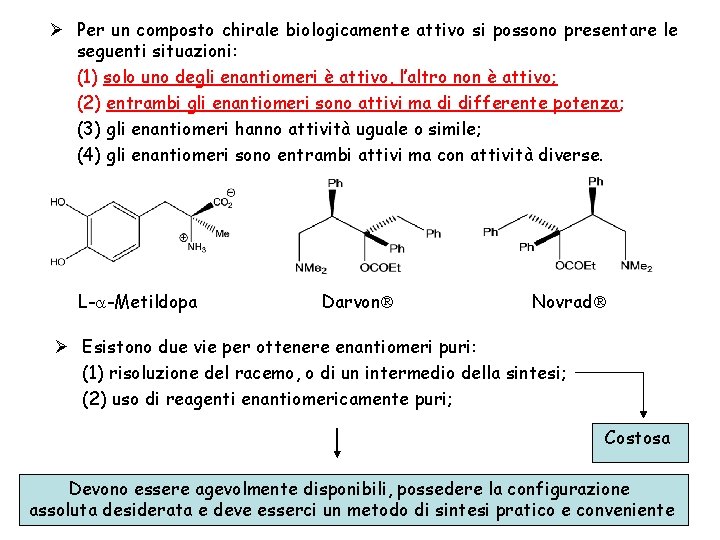
Ø Per un composto chirale biologicamente attivo si possono presentare le seguenti situazioni: (1) solo uno degli enantiomeri è attivo, l’altro non è attivo; (2) entrambi gli enantiomeri sono attivi ma di differente potenza; (3) gli enantiomeri hanno attività uguale o simile; (4) gli enantiomeri sono entrambi attivi ma con attività diverse. L- -Metildopa Darvon Novrad Ø Esistono due vie per ottenere enantiomeri puri: (1) risoluzione del racemo, o di un intermedio della sintesi; (2) uso di reagenti enantiomericamente puri; Costosa Devono essere agevolmente disponibili, possedere la configurazione assoluta desiderata e deve esserci un metodo di sintesi pratico e conveniente
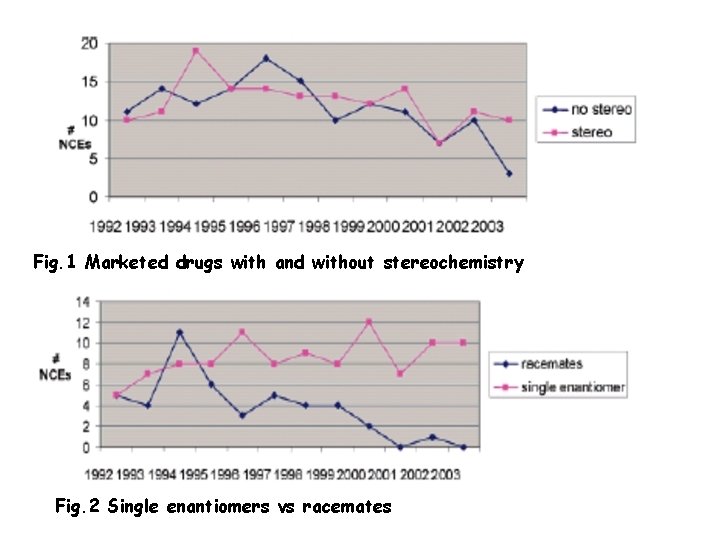
Fig. 1 Marketed drugs with and without stereochemistry Fig. 2 Single enantiomers vs racemates
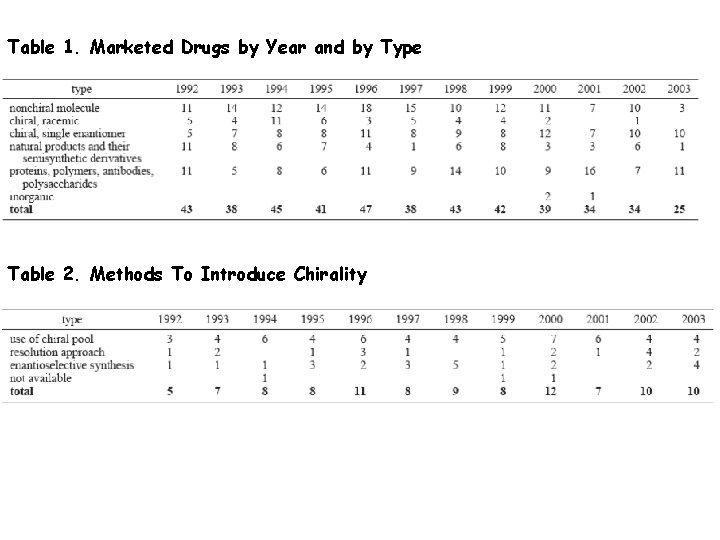
Table 1. Marketed Drugs by Year and by Type Table 2. Methods To Introduce Chirality

Principi della sintesi asimmetrica Ø Per avere una sintesi asimmetrica almeno uno dei componenti della reazione deve essere chirale e non racemico. Ø Se nella reazione non vi è alcun componente asimmetrico, gli stati di transizione che portano agli enantiomeri saranno anch’essi enantiomerici, di uguale energia e si formerà un racemo. Ø Di regola l’uso di un substrato, di un reagente, di un solvente o di un catalizzatore chirale dovrebbe dar luogo ad una sintesi asimmetrica. Ø In generale, una qualsiasi caratteristica del sistema reagente che porta a stati di transizione diastereomerici (laddove normalmente sono enantiomerici) potrebbe portare alla formazione preferenziale di un diastereoisomero o di un enantiomero. Ø Ciò è dovuto al fatto che stati di transizione diastereomerici non necessariamente sono della stessa energia e come conseguenza uno dei possibili prodotti può formarsi più rapidamente.
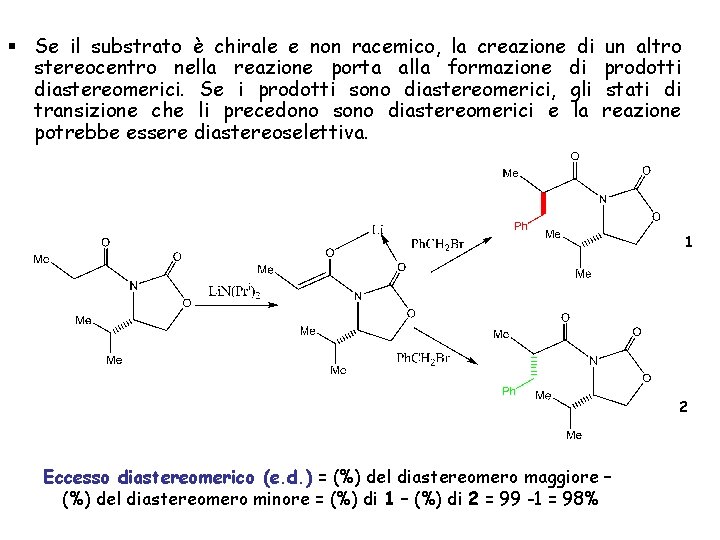
§ Se il substrato è chirale e non racemico, la creazione di stereocentro nella reazione porta alla formazione di diastereomerici. Se i prodotti sono diastereomerici, gli transizione che li precedono sono diastereomerici e la potrebbe essere diastereoselettiva. un altro prodotti stati di reazione 1 2 Eccesso diastereomerico (e. d. ) = (%) del diastereomero maggiore – (%) del diastereomero minore = (%) di 1 – (%) di 2 = 99 -1 = 98%
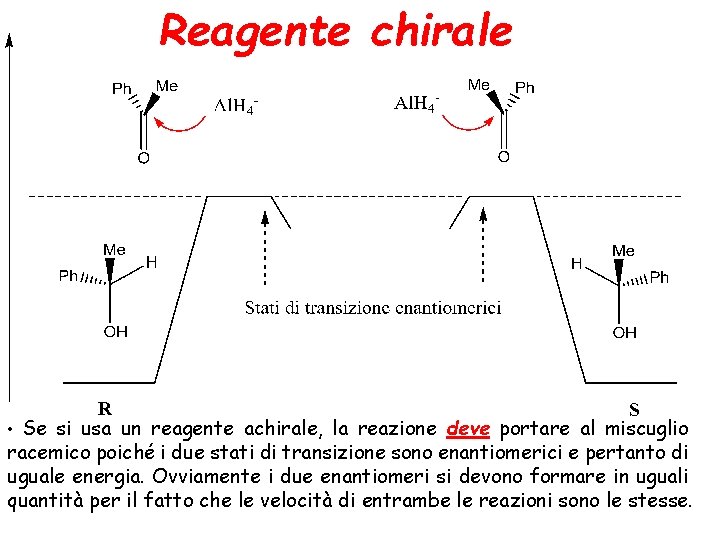
Reagente chirale • Se si usa un reagente achirale, la reazione deve portare al miscuglio racemico poiché i due stati di transizione sono enantiomerici e pertanto di uguale energia. Ovviamente i due enantiomeri si devono formare in uguali quantità per il fatto che le velocità di entrambe le reazioni sono le stesse.
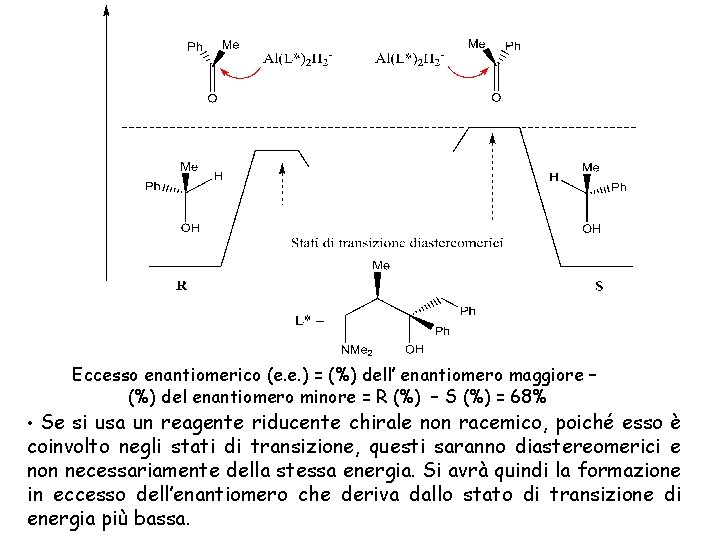
Eccesso enantiomerico (e. e. ) = (%) dell’ enantiomero maggiore – (%) del enantiomero minore = R (%) – S (%) = 68% • Se si usa un reagente riducente chirale non racemico, poiché esso è coinvolto negli stati di transizione, questi saranno diastereomerici e non necessariamente della stessa energia. Si avrà quindi la formazione in eccesso dell’enantiomero che deriva dallo stato di transizione di energia più bassa.

Solvente chirale • In una reazione che avviene in soluzione i componenti sono solvatati. • L’uso di un solvente chirale e non racemico dovrebbe dare luogo ad una sintesi asimmetrica dal momento che è verosimile che il solvente sia coinvolto negli stati di transizione. • Poiché siamo in presenza di un solo enantiomero del solvente gli stati di transizione, che sarebbero enantiomerici in un solvente achirale, diventano diastereomerici e la sintesi può essere asimmetrica. • Approccio di uso poco generale perché il livello di stereoselettività che viene indotto è basso e non prevedibile. Inoltre, ci sono solo pochi composti enantiomericamente puri che sono disponibili in quantità sufficiente ed aventi le proprietà di solvente utile.
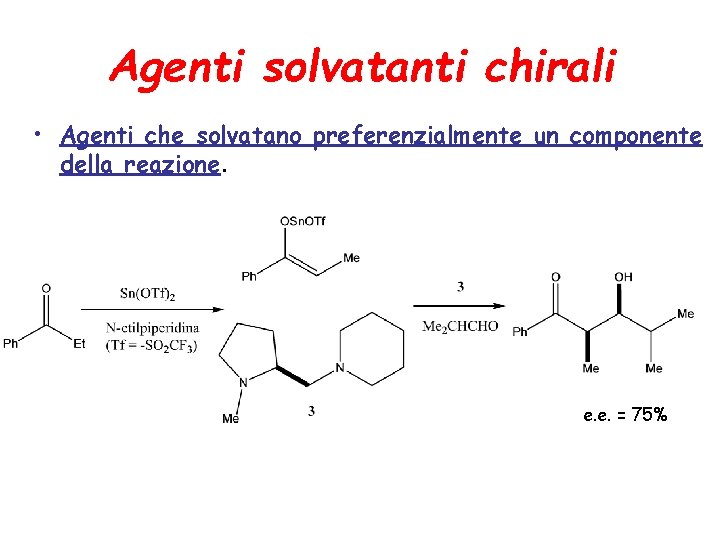
Agenti solvatanti chirali • Agenti che solvatano preferenzialmente un componente della reazione. e. e. = 75%
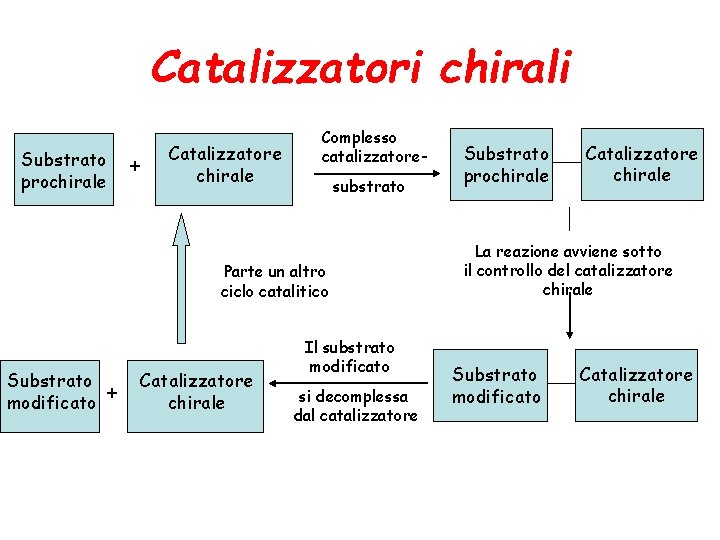
Catalizzatori chirali Substrato prochirale + Catalizzatore chirale Complesso catalizzatoresubstrato Parte un altro ciclo catalitico Substrato + modificato Catalizzatore chirale Il substrato modificato si decomplessa dal catalizzatore Substrato prochirale Catalizzatore chirale La reazione avviene sotto il controllo del catalizzatore chirale Substrato modificato Catalizzatore chirale
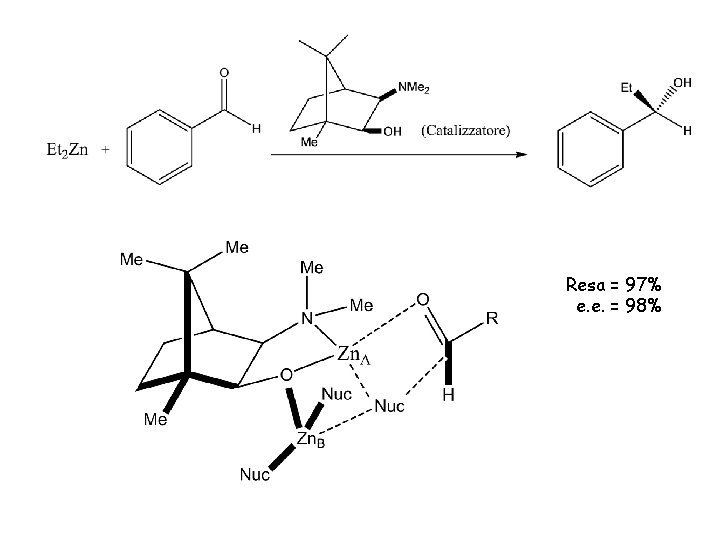
Resa = 97% e. e. = 98%
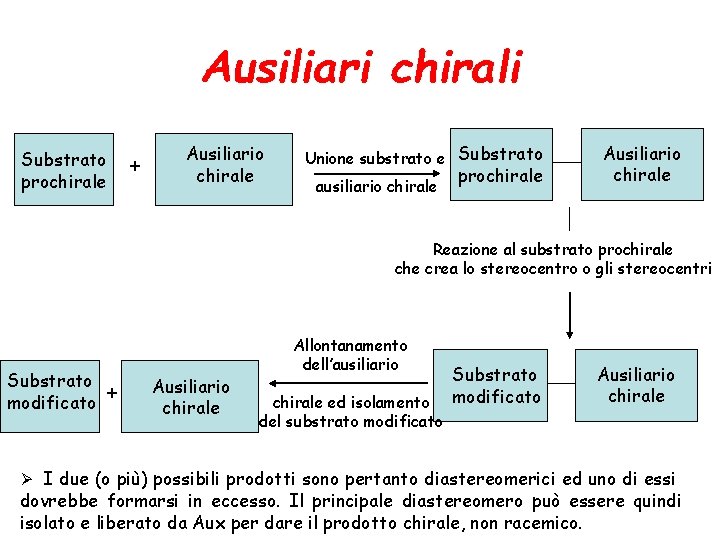
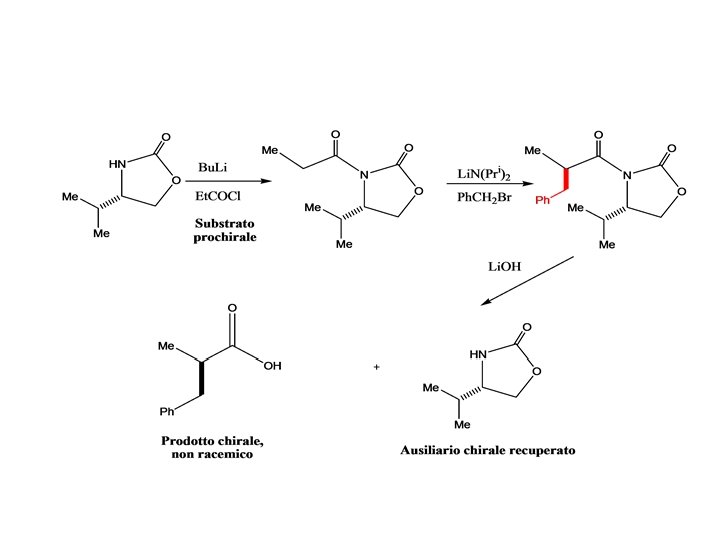
Ausiliari chirali Substrato prochirale + Ausiliario chirale Unione substrato e Substrato ausiliario chirale prochirale Ausiliario chirale Reazione al substrato prochirale che crea lo stereocentro o gli stereocentri Substrato + modificato Ausiliario chirale Allontanamento dell’ausiliario chirale ed isolamento del substrato modificato Substrato modificato Ausiliario chirale Ø I due (o più) possibili prodotti sono pertanto diastereomerici ed uno di essi dovrebbe formarsi in eccesso. Il principale diastereomero può essere quindi isolato e liberato da Aux per dare il prodotto chirale, non racemico.

Requisiti degli ausiliari chirali • • • Enantiomericamente puri Non costosi e disponibili in quantità Facilmente agganciabili al substrato Controllo della stereoselettività alto e prevedibile Facilità di purificazione del principale diastereomero Facilmente rimuovibile senza perdita di purezza enantiomerica e diastereomerica • Facilmente separabile dal prodotto e recuperabile.

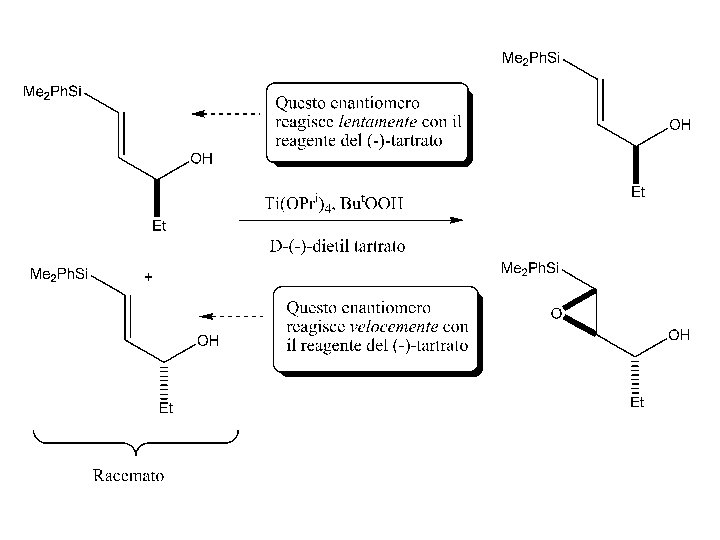
Risoluzione cinetica • Approccio alternativo alla sintesi asimmetrica è quello della risoluzione cinetica in cui una risoluzione del substrato racemico avviene mediante una reazione asimmetrica. • Si basa sulla differenza della velocità di reazione dei singoli enantiomeri del racemo con un reagente enantiomericamente puro o un catalizzatore. • Nel caso ideale questa differenza di velocità è così grande che un enantiomero del racemo è praticamente inerte, mentre l’altro reagisce rapidamente. • Una semplice separazione del prodotto e dell’enantiomero che non ha reagito fornisce entrambi in forme enantiomericamente pure.
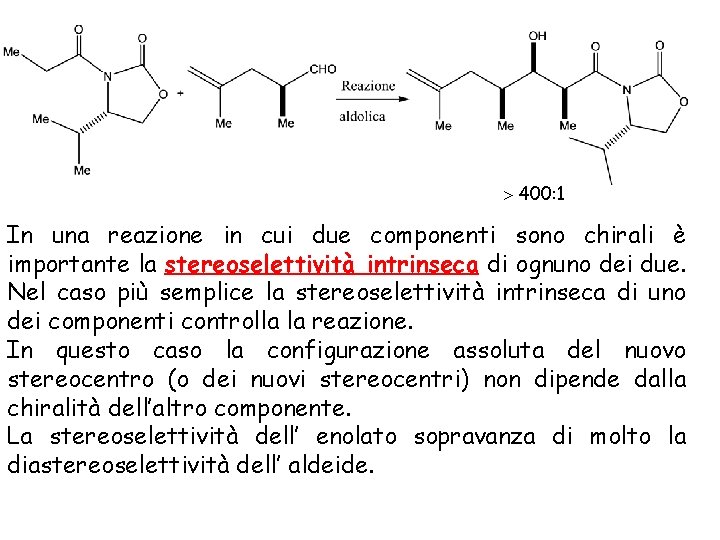
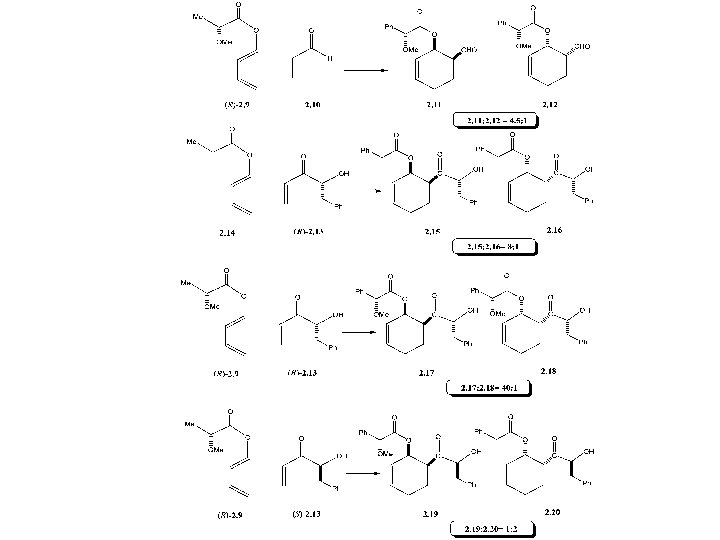
400: 1 In una reazione in cui due componenti sono chirali è importante la stereoselettività intrinseca di ognuno dei due. Nel caso più semplice la stereoselettività intrinseca di uno dei componenti controlla la reazione. In questo caso la configurazione assoluta del nuovo stereocentro (o dei nuovi stereocentri) non dipende dalla chiralità dell’altro componente. La stereoselettività dell’ enolato sopravanza di molto la diastereoselettività dell’ aldeide.
ü Nell’altro caso limite i due componenti chirali hanno diastereoselettività intrinseche simili. In questo caso le diastereoselettività di una coppia di componenti chirali saranno in genere complementari e daranno elevata stereoselettività. MATCHED PAIR (coppia concorde) ü L’altra combinazione stereoselettività. risulterà in MISMATCHED PAIR (coppia discorde) una bassa
- Slides: 22