Vaistini preparat pakuoi apsaugos priemoni taikymo aktualijos Valstybins

Vaistinių preparatų pakuočių apsaugos priemonių taikymo aktualijos Valstybinės vaistų kontrolės tarnybos prie Lietuvos Respublikos sveikatos apsaugos ministerijos Viršininkas Gintautas Barcys 2015 -06 -08 Vilnius 1

Teisės aktai (1) • Direktyva 2011/62/ES (, , Falsifikatų” direktyva). • Nuostatos dėl pakuočių apsaugos priemonių įsigalios po 3 metų nuo Europos Komisijos deleguoto akto paskelbimo. • Europos Komisijos deleguotas aktas – reglamentas dėl apsaugos priemonių (šiuo metu rengiamas projektas). • Farmacijos įstatymas Nr. XII-388, priimtas 2013 m. birželio 18 d. 2

Teisės aktai (2) Registruotų vaistinių preparatų, išskyrus radiofarmacinius preparatus, pakuotės turės būti su apsaugos priemonėmis, kuriomis būtų galima patikrinti vaistinio preparato autentiškumą, identifikuoti atskiras pakuotes ir nustatyti, ar nebuvo pažeista išorinė pakuotė, šiais atvejais: 1) jeigu vaistinis preparatas yra receptinis vaistinis preparatas, išskyrus įrašytus į Europos Komisijos vaistinių preparatų ir jų grupių sąrašą, kuriame nurodyti receptiniai vaistiniai preparatai ar grupės, kuriems netaikomas reikalavimas, kad pakuotės turi būti su apsaugos priemonėmis; 2) jeigu vaistinis preparatas yra nereceptinis vaistinis preparatas, kuris įrašytas į Europos Komisijos vaistinių preparatų ir jų grupių sąrašą, kuriame nurodyti nereceptiniai vaistiniai preparatai ar grupės, kuriems taikomas reikalavimas, kad pakuotės turi būti su apsaugos priemonėmis. Lietuvos Respublikos farmacijos įstatymo 8 straipsnio 81 dalis 3

Apsaugos priemonės • Unikalus identifikatorius (UI) • Prietaisas, parodantis, ar nebuvo bandoma išardyti pakuotę 4

Unikalus identifikatorius (1) UI patikra turės būti atliekama naudojantis duomenų kaupyklų sistema, į kurią turės būti įvesti visų tiekiamų vaistų UI. Išregistravus vaisto UI iš sistemos, vaisto negali būti tiekimo tinkle, išskyrus nustatytus atvejus (pvz. , eksportuojant). 5

Gamintojo pareigos • Patikrinti, ar ant pagamintų vaistų esantis 2 D brūkšninis kodas ir UI atitinka reikalavimus; • Turi įvesti UI į duomenų kaupyklą; • Duomenys, susiję su UI, turės būti saugomi nustatytą laikotarpį po vaisto tinkamumo vartoti laiko pabaigos; • Reikalavimai perpakuotojui (pirma patikrinti UI, po to perpakuoti ir uždėti naują UI). 6

Apsaugos priemonių tikrinimas didmeninio platinimo įmonėse • Nustatomi atvejai, kai vaistų UI privalomai reikia tikrinti, pvz. : - grąžintų iš vaistinės, ligoninių, kitų didmenininkų; - gautų iš didmenininkų, kurie nėra gamintojai ar RTT. • Numatytos išimtys dėl patikrinimų, pvz. : jei vaistas tiekiamas iš vieno į kitą to paties didmenininko sandėlį. • Nustatomi atvejai, kai vaistų UI reikia tikrinti ir išregistruoti iš kaupyklų sistemos, pvz. : kai eksportuojama; kai turi būti sunaikinami; paimami bandiniai kokybės tyrimams. • Suteikiama teisė VN-ei tam tikrais atvejais papildomai įpareigoti didmenininkus tikrinti ir išregistruoti UI (pvz. , kai tiekiama veterinarijos tikslams). 7

Apsaugos priemonių tikrinimas vaistinėse ir sveikatos priežiūros įstaigose • Pagrindinis principas - visi vaistai turi būti patikrinti ir išregistruoti iš kaupyklų sistemos jų išdavimo pacientui metu. • VN-ei suteikiama teisė taikyti išimtis tam tikrais nustatytais atvejais: - ASP įstaigose patikrinti ir išregistruoti vaistus iš sistemos iš karto po jų gavimo; - ASP įstaigose netikrinti ir neišregistruoti vaistus, jei, pvz. : juos gauna iš didmenininko, kuris priklauso tam pačiam juridiniam asmeniui ir patikrina bei išregistruoja tuos vaistus didmenininkas. • Taikant išimtis, pakuotės vientisumas tikrinamas vaistų išdavimo pacientui metu arba prieš išardant pakuotę (jei ardoma). 8

Duomenų kaupyklų sistema (1) • Tai duomenų bazė, į kurią įvesta informacija apie apsaugos priemones. • Gamintojai ir rinkodaros teisės turėtojai turi bendrai kurti ir valdyti kaupyklų sistemas. Išlaidas padengti gamintojai (Direktyvos 2001/83/ES 54 a(2)(e) str. ) • Neapima prietaisų ir priemonių kurias naudos didmeninio platinimo įmonės, vaistinės ir kt. 9
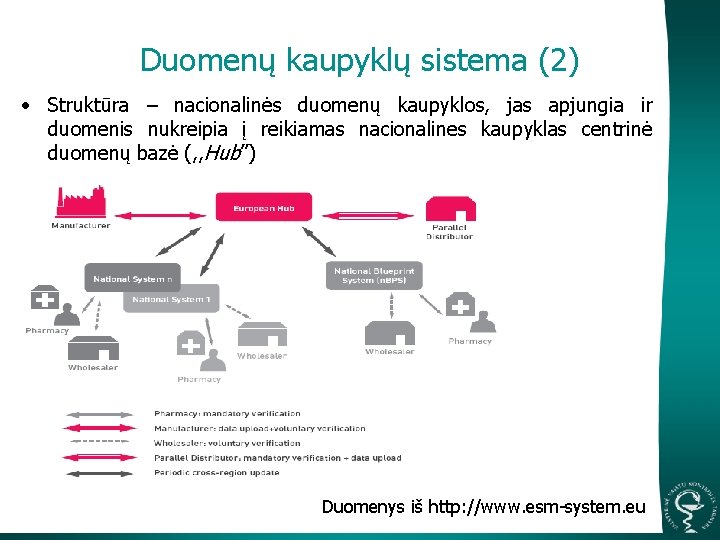
Duomenų kaupyklų sistema (2) • Struktūra – nacionalinės duomenų kaupyklos, jas apjungia ir duomenis nukreipia į reikiamas nacionalines kaupyklas centrinė duomenų bazė (, , Hub”) Duomenys iš http: //www. esm-system. eu

Duomenų kaupyklų sistema (3) • Nustatomi reikalavimai: kokia informacija turės būti įvesta į centrinę duomenų bazę ir nacionalines kaupyklas, kokių operacijų atlikimą turi užtikrinti, galimybės pakeisti UI statusą iš išregistruoto į aktyvų statusą, signalizuoti, kai nustatomas galimas falsifikavimo atvejis ir kt. • Nustatomi reikalavimai juridiniam asmeniui, fiziškai įsteigiančiam nacionalinę kaupyklą. Pvz. , atlikti kaupyklos auditą, užtikrinti jos prieinamumą įgaliotiems asmenims. • Valstybė narė turi prižiūrėti kaupyklų funkcionavimą. 11

VEIKIANČIOS SISTEMOS • secur. Pharm – DE rinkos dalyvių modelis. Tikrinami vaistinių preparatų brūkšniniai kodai, apima 36 gamintojus. • aegate - taikoma kai kurių ES šalių vaistinėse. • ESM&secur. Pharma - Europos rinkos dalyvių modelis (European Stakeholder Model), kurio apimtyje bendradarbiauja vaistų tiekėjai. Prie jo prisijungė secur. Pharm. Tikslas - pademonstruoti, kaip galėtų veikti EMVS (Europos vaistų verifikacijos sistema) • EMVO – (European medicine verification organisation) 2015 m. įsteigta ne pelno siekianti organizacija. Atsako už centrinės duomenų bazės sukūrimą • LIETUVA? 12

Įpareigojimai ir atsakomybė • 2001/83/ES Direktyva įgalioja Komisiją deleguotame akte nustatyti kaupyklų sistemos įsteigimo, valdymo ir prieinamumo reikalavimus, bei nurodo, kad kaupyklų sistemos išlaidas dengia gamybos licencijos turėtojai. • 2011/62/ES Direktyva įpareigoja Valstybes Nares įgyvendinti visas priemones, būtinas užtikrinti atitiktį šios Direktyvos reikalavimams. 13

Dėkoju už dėmesį ! 14
- Slides: 14