Vacina contra a Febre Amarela Naoko Yanagizawa J

Vacina contra a Febre Amarela Naoko Yanagizawa J da Silveira Médica sanitarista – COVISA/SMS Campinas Colaboração : NVE Unicamp

A VACINA n n Descoberta da vacina em 1937 (cepa 17 D) a produção de imunobiológico pelo emprego de cultura de tecido de embrião de galinha – até hoje

INDICAÇÕES DA VACINA RESIDENTES OU VIAJANTES À ÁREAS DE RISCO NO MOMENTO PRIORIZADO PARA ÁREAS CRÍTICAS (MS, 21/01/08)

CONTRA INDICAÇÕES n Menores de 6 meses de idade n Imunodeficiências congênitas n n n 1, 2, 3 Imunodeficiências adquiridas: n Infecção avançada pelo vírus HIV n Transplantados n Portadores de neoplasias n Pacientes em quimioterapia, radioterapia, Corticoterapia História prévia de reação de hipersensibilidade, TIPO ANAFILÁTICA, a ovo de galinha e/ou seus derivados Gestação

CONSIDERAÇÕES: n n n Gestação - contra-indicação relativa. Discutese os riscos e benefícios. A vacina contra febre amarela NÃO tem eficácia e segurança estabelecidas para portadores do vírus HIV. Deve se considerar a contagem, atualizada, de linfócitos T-CD 4 e Carga Viral e a situação epidemiológica. Discussão de casos específicos: COVISA e o Centro de Referência para Imunobiológicos Especiais - Hospital das Clínicas – UNICAMP

EVENTOS ADVERSOS 3, 4, 5 2001 a 2003 - 172 eventos adversos em 22, 8 milhões de doses aplicadas. n Freqüência : 7, 6 eventos adversos/1. 000 doses aplicadas. n Sem evidência de maior reatogenicidade em crianças comparada a adultos

Eventos adversos n Mais freqüentes ( 2 -5% após 5 -10 dias pós-vacinação): n n Hiperemia, dor e edema no sítio de aplicação Cefaléia Febre Mialgia

Eventos adversos n Menos freqüentes: n n n n Linfoadenopatia Artralgia Exantema Astenia Dor abdominal Sintomas gastrointestinais (náusea, vômitos, diarréia) Tontura

Reações de hipersensibilidade n Risco estimado: 1, 9 reações/1. 000 doses aplicadas e 0, 2 choque anafilático/1. 000 doses aplicadas. n População de maior risco: antecedente de alergia a ovo e/ou demais componentes da vacina. n Início do quadro: mais frequente 1 hora após aplicação da vacina. Manifestações clínicas: n Urticária n Sibilos n Edema labial n Laringoespasmo n Hipotensão n Choque

Manifestações Neurológicas n Risco estimado: 4 - 5, 8 eventos/1. 000 doses aplicadas. n População de maior risco: lactentes, imunossuprimidos. n Início do quadro: 7 -21 dias após aplicação da vacina. Eventos neurotrópicos associados à vacina : n Meningite n Meningoencefalite n Encefalite n Síndrome de Guillain Barré

Doença viscerotrópica aguda n n Freqüência: evento raro. No Brasil foram relatados, até o ano de 2007, 7 casos, sendo 5 óbitos. todos os casos descritos associados após à primeira exposição à vacina. Risco estimado: < 1 evento/400. 000 doses aplicadas 3 ou 1 óbito para 450. 000 doses aplicadas. Casos devem ser suspeitados diante dos seguintes sinais/sintomas, nos 15 dias subseqüentes à vacinação: n Icterícia n Hemorragias espontâneas n Hipotensão/choque

CASOS SUSPEITOS DE EVENTOS ADVERSOS RECOMENDAÇÕES PARA O ATENDIMENTO
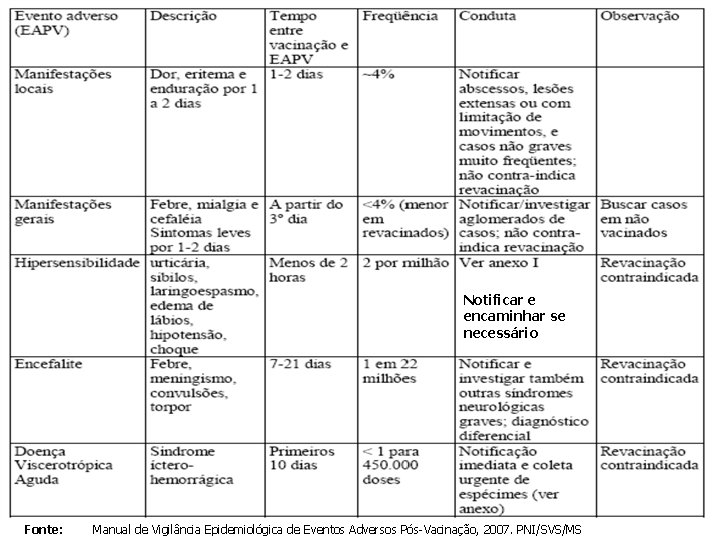
Notificar e encaminhar se necessário Fonte: Manual de Vigilância Epidemiológica de Eventos Adversos Pós-Vacinação, 2007. PNI/SVS/MS

Notificar todos os casos suspeitos de eventos adversos n n Casos graves – meningoencefalite, doença viscerotrópica aguda e reação anafilática – notificar IMEDIATAMENTE à COVISA para que as medidas de investigação – clínica e laboratorial – bem como o possível encaminhamento do para o serviço de referência sejam desencadeados em tempo oportuno. Casos passíveis de internação, para suporte e investigação, serão encaminhados ao Hospital das Clínicas da UNICAMP após contato prévio junto ao Centro de Referência para Imunobiológicos Especiais – CRIE de segunda-feira à sexta-feira das 8: 00 h às 17: 00 h. Nos feriados e fianis de semana - plantão de Moléstias Infecciosas do mesmo Hospital.

Situação em Campinas n n n 22 postos de vacinação 8. 588 doses aplicadas em 15 dias 12. 000 doses recebidas 1 evento adverso notificado Em 2007, mesmo período: cerca de 650 doses aplicadas A restrição de áreas de risco do Ministério da Saúde impõe regras mais rígidas aos municípios, diante de estoque zero nesta semana

VACINAÇAO DE VIAJANTES CONTRA A FEBRE AMARELA NOVA RECOMENDAÇÃO (Secretaria de Vigilância em Saúde/ Ministério da Saúde) 21 de janeiro de 2008

1. Vacinação a partir de 6 meses de vida n n n GOIÁS TOCANTINS DISTRITO FEDERAL MINAS GERAIS os municípios: Arinos, Buriti, Cabeceira Grande, Cascalho Rico, Luislândia, Santo Antônio da Prata. MATO GROSSO DO SUL, os municípios: Anastácio, Aquidauana, Bonito, Dourados.

2. Vacinação a partir de 9 meses de vida (MATAS, RESERVAS e FLORESTAS) n n n n AMAPÁ AMAZONAS ACRE PARÁ RONDÔNIA RORAIMA MARANHÃO MATO GROSSO

QUEM VACINAR? ? TRIAGEM E ACONSELHAMENTO n ONDE VAI? n QUANDO VAI? n TOMOU EM 2000? n LEMBRAR EVENTOS ADVERSOS!!!! MEDIDAS RESTRITIVAS: COMPROVANTE DE VIAGEM OU SIMILAR

Referências 1. 2. 3. 4. 5. Informe Técnico – Febre Amarela. Ação emergencial contra a febre amarela; atualizado em 22/01/2008. Divisão de Zoonoses e de Doenças Transmitidas por Vetores, Centro de Vigilância Epidemiológica “Prof. Alexandre Vranjac”, Secretaria de Estado da Saúde de São Paulo. [http: //www. cve. saude. sp. gov. br/htm/zoo/fa 08_info 2201. htm; acessado em 22/01/2008] Manual dos Centros de Referência para Imunobiológicos Especiais – 3 a Edição. Departamento de Vigilância Epidemiológica, Secretaria de Vigilância em Saúde, Ministério da Saúde, Brasília/DF, 2006. Manual de Vigilância Epidemiológica de Eventos Adversos Pós. Vacinação, 2007. Programa Nacional de Imunizações, Departamento de Vigilância Epidemiológica, Secretaria de Vigilância em Saúde, Ministério da Saúde, Brasília/DF, 2007. Eventos Adversos Sérios Associados com a Vacina 17 D contra a Febre Amarela. FUNASA, Ministério da Saúde. Yellow Fever Vaccine. In Vaccines – Plotkin, Orenstein. 4 th Edition, Chapter 40, p. 1095 -1176. 2004.
- Slides: 20