Vaccination Obligation vaccinale Nouveaut du calendrier vaccinal Grer

Vaccination Obligation vaccinale Nouveauté du calendrier vaccinal Gérer les résistances des patients Dr Valérie Briend-Godet Centre de prévention des maladies infectieuses et transmissibles CHU de Nantes

OBLIGATION VACCINALE

Histoire de l’obligation vaccinale • Variole – En France : vaccination antivariolique obligatoire en 1902 au cours de la 1 re année de la vie, ainsi que la revaccination au cours de la 11 e et de la 21 e année (Art. 6 de la loi du 15/02/1902 relative à la protection de la santé publique) – En France, suspension de l’obligation vaccinale • 1979 : primovaccination (population générale) • 1984 : rappel (population générale) et personnel soignant • Diphtérie (1938) : primovaccination et rappel des 18 mois • Tétanos (1940) : primovaccination et rappel des 18 mois • BCG : à partir de 1950 puis suspension de l’obligation en 2007 • Poliomyélite (1964) : primovaccination et rappels jusqu’à 13 ans Problème de santé publique mise en place de lois pour protéger la population

Et puis après… • Nouveaux vaccins introduit après la fin des 60’s – Uniquement recommandations Volonté de promouvoir la responsabilité individuelle – Sauf : • En milieu professionnel (Article L. 3111 -4 du code de la santé publique) • Fièvre jaune en Guyane (Décret n° 67 -428 du 22 mai 1967 modifié par le décret n° 87 -525 du 9 juillet 1987) • En cas de menace sanitaire grave appelant des mesures d'urgence, notamment en cas de menace d'épidémie (Articles L 3131 -1 et suivants du code de la santé publique)

Obligation vaccinale : Quelles étaient les problématiques ? • Les paradoxes de la vaccination obligatoire – Fardeaux des maladies couvertes par les vaccins : recommandées obligatoires – Obligation ne concerne que les enfants • • • Adultes seuls concernés par les cas résiduels de diphtérie et tétanos Rareté des cas de tétanos liée à la pratique des rappels (non obligatoires) Problèmes soulevés par le régime obligatoire actuel – Discrédit sur les vaccinations recommandées source d’incompréhension – Pas de disponibilité des vaccins obligatoires : combinaison avec des vaccins recommandés Difficulté +++ de n’administrer que les vaccins obligatoires avec les vaccins commercialisés – Modalité d’indemnisation différentes selon que le vaccin est obligatoire ou recommandé Quid de l’indemnisation des vaccins combinant valences obligatoires/recommandées ? • Risques liés à la levée de l’obligation vaccinale (DTP) – Chute des taux de couverture vaccinale ? – Epidémies ? En réflexion depuis plusieurs années : liberté individuelle vs santé publique
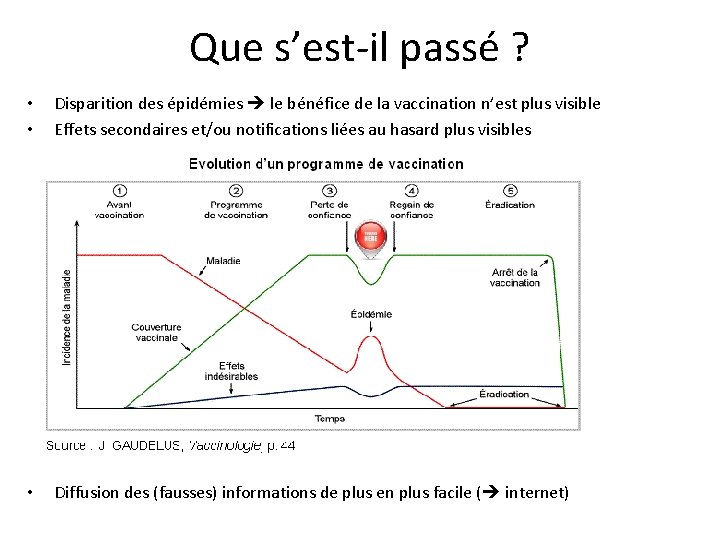
Que s’est-il passé ? • • Disparition des épidémies le bénéfice de la vaccination n’est plus visible Effets secondaires et/ou notifications liées au hasard plus visibles • Diffusion des (fausses) informations de plus en plus facile ( internet)

Obligation vaccinale : Quelle décision finale? • Obligations pour les vaccinations suivantes (Cf. Article L 3111 -2 du CSP, legifrance. gouv. fr) Ø Ø Ø Ø Diphtérie, tétanos, poliomyélitique Coqueluche Haemophilus influenzae de type b Hépatite B Pneumocoque (13 -valent) Rougeole, oreillons, rubéole Méningite C § § • Ne se limitent pas aux enfants entrant en collectivité • Modalités d’applications HAS, recommandation vaccinale, nécessité des rappels vaccinaux chez l'enfant / exigibilité des vaccinations en collectivité, novembre 2017 (has-sante. fr) Décret n° 2018 -42 du 25. 01. 18 relatif à la vaccination obligatoire (legifrance. gouv. fr) – Pas de rétroactivité • • Obligation pour les enfants nés à partir du 1 er janvier 2018 Le DTP reste obligatoire pour les enfants nés avant le 1 er janvier 2018 – Pas d’exemption possible – Contrôle à l’entrée en collectivité • • Preuve fournie pour l'admission ou le maintien dans toutes crèches, garderies, écoles et colonies de vacances ou toute autre collectivité d'enfants y compris les services assurant l'accueil familial non permanent d'enfant au domicile d'assistants maternels A défaut, l'article R. 3111 -17 du code de la santé publique prévoit que les vaccinations obligatoires soient effectuées dans les trois mois suivant l'admission – Pas de sanctions pénales sanctions = refus d’entrée en collectivité (loi applicable au 1/06/18) – Mais cadre juridique

Quels patients vacciner ? Certificats de contreindication ? Comment communiquer ? • Quels patients vacciner ? – Tous ! – Selon le calendrier en vigueur (qui ne change pas) ! • Les contre-indications – Pour l'ensemble des vaccins • Hypersensibilité sévère à l'un des composants (ce qui en pratique est rarissime chez le petit enfant consultation en allergologie) • Épisode infectieux en cours – Pour les vaccins contenant la valence coquelucheuse : encéphalopathie d'étiologie inconnue, survenue dans les 7 jours suivant une vaccination antérieure par un vaccin contenant la valence coquelucheuse – Pour le ROR (VVA) : déficits immunitaires congénitaux ou acquis • Comment communiquer ? – Ne pas se retrancher derrière l’obligation vaccinale – Expliquer aux patients • Les raisons de santé publique • Pas d’ajouts de vaccins on continue à faire ce qu’on faisait avant

Calendrier vaccinal 2018 complet disponible sur : http: //solidarites-sante. gouv. fr/prevention-en-sante/preserver-sa-sante/vaccination/calendrier-vaccinal Rougeole Nouveaux vaccins (AMM) Méningocoques C Papillomavirus Pneumocoque Zona LE « NOUVEAU » CALENDRIER VACCINAL (2016) 2017 -2018

Recrudescence de la rougeole en 2017 -2018 épidémie http: //invs. santepubliquefrance. fr/Dossiers-thematiques/Maladies-infectieuses/Maladies-a-prevention-vaccinale/Rougeole/Points-d-actualites/Bulletinepidemiologique-rougeole. -Donnees-de-surveillance-au-30 -mai-2018 q Recrudescence de la rougeole depuis 11/2017 q Au 27 mai 2018, 2364 cas déclarés (depuis 11/2017) Ø Ø Ø Baisse du nombre de nouveaux cas hebdomadaires depuis la semaine 13 22% des cas déclarés ont été hospitalisés Décès en février d’une jeune femme de 32 ans non vaccinée 21 décès dus à la rougeole depuis 2008 (dont 1 en 2017, jeune fille de 16 ans) Incidence la plus élevée chez les moins de 1 an: 23, 8 cas/100 000 habitants q 83 départements touchés par la rougeole Ø Région Nouvelle-Aquitaine +++ q 88% des cas sont survenus chez des personnes non ou incomplètement vaccinées

Rougeole : recommandations • Vaccins vivants atténués trivalent ROR : CI immunodépression et grossesse – MMRVax. Pro® – Priorix® • Vaccination du nourrisson – ROR n° 1 à 12 mois (quel que soit le mode de garde) – ROR n° 2 à 16 -18 mois • Arrêt de commercialisation du vaccin rougeoleux monovalent Rouvax® (date de préemption des derniers stocks jusqu'au 30/04/2018) – A partir du 1 er mai 2018, les nourrissons entre 6 et 11 mois en contact avec un cas de rougeole devront recevoir un vaccin trivalent ROR (hors AMM pour les 6 -8 mois révolus) dans les 72 h suivant le contact présumé (idem voyageur, VIH et attente de greffe, cf. avis de l’HAS, mars 2018) – A noter que l'injection reste préconisée même si le délai est dépassé – L’enfant recevra par la suite deux doses de vaccin trivalent suivant les recommandations du calendrier vaccinal : 1 re dose à l’âge de 12 mois, 2 e dose entre 16 et 18 mois

ROR : rattrapage • Rattrapage – Les personnes nées après 1980 doivent avoir reçu 2 doses de ROR – Les femmes nées avant 1980 et ayant un projet de grossesse doivent recevoir 1 dose de vaccin ROR si elles ne sont pas vaccinées contre la rubéole – Les professionnels de santé et de la petite enfance nés avant 1980, non vaccinés et sans antécédent de rougeole doivent recevoir 1 dose de vaccin ROR • Dans le cadre des recommandations autour d’un ou plusieurs cas – Rougeole : recommandations autour d’un ou plusieurs cas • Vaccination des sujets réceptifs contacts (cf. recommandations selon les cas) • L’administration d’une dose de vaccin réalisée dans les 72 h qui suivent le contage peut éviter la survenue de la maladie mais reste préconisée même si ce délai est dépassé – Oreillons : situation de cas groupés en collectivité • Mise à jour du statut vaccinal à deux doses de ROR • 3 e dose de vaccin ROR systématique pour les personnes déjà vaccinées avec deux doses et dont la seconde dose a été administrée depuis plus de 10 ans • La vaccination ROR est contre-indiquée pendant la grossesse et toute grossesse doit être évitée dans le mois suivant la vaccination

Rougeole et professionnels de santé • • • Les personnes nées depuis 1980 (soit = ou > à 1980) doivent avoir reçu au total deux doses de vaccin trivalent – Délai minimal d’un mois entre les deux doses, quels que soient les antécédents vis-à-vis des trois maladies – Administrer un ROR à une personne déjà immunisée contre une ou plusieurs des maladies ne présente aucun inconvénient du fait de l’inactivation du virus vaccinal par les anticorps préexistants Les personnes nées avant 1980 (soit < 1980), non vaccinées et sans antécédent connu de rougeole ou de rubéole doivent recevoir une dose de vaccin trivalent – Professions de santé en formation, à l’embauche ou en poste, en particulier les personnes travaillant dans les services accueillant des patients à risque de rougeole grave (immunodéprimés, nouveau-nés, femmes enceintes) – Pour l’ensemble de ces personnels dont les antécédents de vaccination ou de maladie (rougeole, rubéole) sont incertains, la vaccination peut être pratiquée sans qu’un contrôle sérologique préalable soit systématiquement réalisé En cas de contage rougeoleux – Administration d’une dose de vaccin trivalent à tous les personnels susceptibles d’être ou d’avoir été exposés pour lesquels il n’existe pas de preuve de rougeole antérieure ou qui n’ont pas reçu auparavant une vaccination complète à deux doses – Cette vaccination, si elle est réalisée dans les 72 heures qui suivent un contact avec un cas, peut éviter la survenue de la maladie – Elle reste préconisée même si ce délai est dépassé

Nouveaux vaccins sur le marché • Vaccins hexavalents contre diphtérie, tétanos, coqueluche, poliomyélite, Haemophilus influenzae de type b, hépatite B – Un 3 e vaccin est désormais disponible : Vaxelis® – Indications identiques à celles des autres vaccins hexavalents – En l’absence de données d’interchangeabilité pour l’ensemble des vaccins hexavalents, tout schéma vaccinal débuté avec un hexavalent doit être poursuivi avec le même hexavalent (NDLR : Hexyon interchangeable sur le RCP) • Vaccins tétravalents contre la grippe saisonnière – 3 vaccins grippaux tétravalents disposent d’une autorisation de mise sur le marché (AMM) – Influvac Tetra®, Vaxigrip Tetra®, Fluarix Tetra®

Méningocoque C • • NEISVAC ou MENJUGATE Stratégie avant 2017 Levée des recommandations pour les HSH (Avis du HCSP de 2014 puis 2016 caduc) – Une seule dose à un an et rattrapage jusqu’à 24 ans inclus (pour éradication du portage) • Objectifs : protection individuelle pour les 1 -24 ans et collective pour les < 1 an les plus touchés • Inconvénients : pas de protection collective si couverture vaccinale insuffisante – Couverture vaccinale : constat en 2017 Bulletin de Veille Sanitaire Pays de la Loire, n° 43 / janvier 2018 Ajustement des recommandations vaccinales

Recommandations en 2017 • Constats et apports scientifiques récents – Couverture vaccinale insuffisante, notamment des adolescents et des adultes jeunes Absence d’immunité de groupe Nourrissons de moins d’un an non protégée Tranches d’âge 11 -24 très à risque sur le plan individuel – Neisvac : AMM en 2015 une dose à partir de 4 mois suivi d’un rappel à 12 mois • Recommandations 2017 – Rattrapage vaccinal des tranches d’âge les moins bien vaccinées – Pas de rappel systématique à l’adolescence des sujets vaccinés nourrissons (divergence+++) – En attendant immunité de groupe : vaccination des nourrissons à 5 mois (avec le Neisvac) suivi d’un rappel à 12 mois – Un intervalle minimum de 6 mois sera respecté entre l’administration des 2 doses – Vaccination Mn ACWY tous les 5 ans pour les personnes à risque d’IIM Nécessité d’un rappel non encore établi car les données d’immunogénicité doivent être confrontées aux échecs vaccinaux (peu nombreux en France et concernant surtout les moins de 10 ans non concernés par le rappel)

HPV : recommandations et vaccins • Recommandations – AMM : lésions précancéreuses et cancers du col de l’utérus, de la vulve, du vagin et de l’anus, verrues génitales liées aux HPV – Jeunes filles de 11 à 19 ans – Immunodéprimés jusqu’à 19 ans inclus – HSH jusqu’à l’âge de 26 ans : vaccination dans les Cegidd et les centres publics de vaccination afin de permettre un accès gratuit à la vaccination • Gardasil 9 HAS, Commission de la transparence, 13/09/2017 – Couvrira 90% des souches responsables des cancer du col de l’utérus – Efficacité sur les génotypes additionnels/q. HPV chez les femmes naïves : 1 étude randomisée, double aveugle, suivi médian 3, 6 ans • • 97, 4%, IC 95% [85, 0 ; 99, 9] en prévention des lésions de haut grade (critère principal) Plus de 90% en prévention des infections persistantes / frottis anormaux / conisations du col de l’utérus – Immunogénicité sur les génotypes 6, 11, 16 et 18 non inférieurs au q. HPV – Tolérance identique au q. HPV – Pas de donnée sur l’interchangeabilité Cervarix Gardasil 9 16 et 18 6, 11, 16, 18 + 31, 33, 45, 52, 58 De 11 à 14 ans inclus M 0 -M 6 De 15 à 19 ans inclus M 0 -M 1 -M 6 De 11 à 13 ans inclus M 0 -M 6 De 14 à 19 ans inclus M 0 -M 2 -M 6 De 11 à 14 ans inclus M 0 -M 6 De 15 à 19 ans inclus M 0 -M 2 -M 6 JF (11 à 14 ans et rattrapage jusqu’à 19 ans inclus) HSH (jusqu’à 26 ans révolus)

Les vaccins antipneumococciques (+/-) disponibles • 2 vaccins – PREVENAR 13 : vaccin 13 -valent conjugué – PNEUMOVAX : vaccin 23 -valent polyosidique (non conjugué) • Arrêt de commercialisation du PNEUMO 23 en 2017 • Tensions d’approvisionnement : rétrocession à la pharmacie des hôpitaux possible 1 • Populations prioritaires pour le vaccin 23 -valent 2 – Enfants à risque élevé d'infection à pneumocoque qui, après vaccination par le vaccin VPC 13, doivent recevoir une dose de vaccin VPP 23 à l'âge de 2 ans – Populations à risque élevé d'infection à pneumocoque non antérieurement vaccinées et dont la maladie ou la comorbidité justifiant la vaccination a été nouvellement diagnostiquée – Autres populations à risque élevé d'infection à pneumocoque (populations diagnostiquées avant 2017 ou antérieurement vaccinées) : (ré)administration de VPP 23 différée à la fin de la période de pénurie 1 2 ANSM. http: //ansm. sante. fr/Dossiers/Vaccins/Situation-des-approvisionnements-en-vaccins/(offset)/5#paragraph_139303 HAS. Vaccination contre les infections à pneumocoque en contexte de pénurie de vaccin pneumococcique non conjugué 23 -valent. Décembre 2017

Durée de protection Revaccination et hypo-réactivité • Durée de protection – VPP 23 ne semble pas dépasser 5 ans – VPC 13 pas de donnée au-delà de 4 ans mais réponse plus intense et plus durable pour les sérotypes communs • Phénomène d’hypo-réactivité = réponse immune plus faible que lors de la 1 re injection d’un vaccin purement polyosidique (VPP 23 -valent) – Attribuée aux Ag polyosidiques apportés en grande quantité – Inactivation les lymphocytes B • Action directe des polyosaccharides • Et/ou indirecte par l’intermédiaire de cellules dendritiques productrices de cytokines inhibitrices – Transitoire • En pratique – Diminution du titre des Ac – Réponse en Ac d’autant plus faible que le délai entre deux injections de VPP est court – Idem si VPP avant VPC HCSP, Rapport sur les recommandations vaccinales contre les IIP pour les adultes, mars 2017

VPC 13/VPP 23 : raisons des modifications ? • Etude CAPITA, étude randomisée en double aveugle prospective en population générale effectuée entre 2010 et 2014 en Hollande et incluant 84 496 personnes de plus de 65 ans (ID exclus) : « effectiveness » du vaccin VPC 13 vis-à-vis des PP chez les personnes âgées > 65 ans • Plusieurs méta-analyses ou études récentes – Confirment l’efficacité du VPP 23 vis-à-vis des IIP – Sont en faveur d’une efficacité dans la prévention des PP. – L’utilisation conjointe des 2 vaccins = cumul du bénéfice de l’activité intrinsèque supérieure du VPC et celui de la couverture sérotypique plus large du VPP 23 • Diminution de l’incidence des IIP dans toutes les tranches d’âge par immunité de groupe – Baisse de la couverture sérotypique des VPC 13 (< 30% en 2015) – Mais sérotypes non couverts par le vaccin VPC 13 couverts par le vaccin VPP 23 à près de 60% • Modèle médico-économique : stratégie VPC 13/VPP 23 coût-efficace • Meilleure compréhension et acceptabilité par les PS meilleure couverture vaccinale • Immunité protectrice du VPP 23 = 5 ans – – Pas de données épidémiologiques démontrant l’efficacité des revaccinations par ce vaccin Mais, il semble difficile de ne pas en proposer, notamment pour les personnes vaccinées jeunes Revaccination avec un délai < 5 ans ne semble pas acceptable (tolérance) La nécessité de revaccinations ultérieures devra être considérée si des études d’efficacité le justifient HCSP, avis relatif aux recommandations vaccinales contre les infections à pneumocoque pour les adultes (10/03/2017)

Qui vacciner ? = Enfants < 2 ans = Patients présentant une (des) maladie(s) sous-jacente(s) prédisposant à la survenue d’IIP § § § Cardiopathie congénitale cyanogène, insuffisance cardiaque IRC, BPCO, emphysème Asthme sévère sous traitement continu Insuffisance rénale Hépatopathie chronique (d’origine alcoolique ou non) Diabète non équilibré par le simple régime RR = 4 § § § Brèche ostéoméningée Implant cochléaire Immunodépressions RR = 20 à 50 o Asplénies (fonctionnelles ou anatomiques) ou hyposplénie (y compris les drépanocytaires majeurs) o Déficits immunitaires héréditaires o Infection par le VIH o Tumeur solide ou hémopathie maligne o Transplanté d’organe solide (TOS) ou en attente de TOS o Greffé de cellules souches hématopoïétiques o Traitements par immunosuppresseurs, biothérapie ou corticothérapie pour MAI ou inflammatoire chronique o Syndrome néphrotique Ministère de la santé, calendrier vaccinal 2018

Vaccin antipneumococcique : schéma de l’enfant • Recommandations systématiques des enfants < 2 ans : Aux âges de 2, 4 et 11 mois avec le VPC 13 (+ rappel à l’âge de 3 mois pour les enfants à risque d’IIP (prématurés. . . ) • Patient de 2 à 5 ans à risque d’IIP : – Vacciné antérieurement par le VPC 13 : un VPP 23 à 2 ans – Non vacciné antérieurement : 2 VPC 13 à 2 mois d’intervalle puis rappel 2 mois plus tard avec un VPP 23

Vaccin antipneumococcique : schéma à partir de 5 ans • Patients à risque d’IIP quel que soit le risque – Primo-vaccination : une dose de VPC 13, suivie d’une dose de VPP 23 avec un délai minimal de 8 semaines – Un rappel à 5 ans de VPP 23 pour les personnes déjà vaccinées VPC 13 -VPP 23 – Rattrapage • Les personnes qui n’ont reçu antérieurement que le vaccin VPP 23 pourront recevoir une injection du VPC 13, au moins un an après le VPP 23 • L’injection ultérieure de VPP 23 sera réalisée avec un délai d’au moins 5 ans par rapport à la date de l’injection de VPP 23 Délai minimum à respecter avec le VPP 23 antérieur (T 0) réalisé sans VPC 13 préalable 0 VPP 23 1 an VPC 13 2 ans 3 ans Délai minimal de 2 mois entre un VPC 13 et un VPP 23 4 ans 5 ans VPP 23 (Avis HCSP 10 mars 2017)

Zona • Diminution des épisodes de zona et des douleurs post-zostériennes • Recommandation systématique pour les adultes de 65 à 74 ans révolus – Pas de rappel actuellement • Intéractions – Co-administration possible avec le virus contre la grippe saisonnière mais en des sites d’injection différents – Espacer d’au moins 4 semaines avec le Pneumo 23 – Pas de données disponibles avec les autres vaccins • VVA = contre-indications pour les immunodéprimés

Rappel : recommandation coqueluche HCSP 20/02/2014 relatif à la stratégie de cocooning et CV 2017 Qui ? Rappel adulte systématique Cocooning Professionnels 25 ans (rattrapage possible jusqu’à 39 ans) Parents, fratrie, personnes susceptibles d’être en contact étroit et durable avec le nourrisson < 6 mois Personnels soignants, étudiants des filières médicales et paramédicales, professionnels de la petite enfance, assistantes maternelles, babysitting régulier Personnes non antérieurement vaccinées contre la coqueluche 1 d. TPc Modalités Délai minimal entre 2 vaccins d. Tca. P d. TPc systématique > 5 ans Personnes vaccinées Adolescent et jeune adulte < 25 ans Adulte > 25 ans >10 ans Personnes ayant Personnes non vaccinées déjà reçu une dose antérieurement ou à l’âge adulte n’ayant pas reçu de recalage sur le valence coq depuis l’âge calendrier vaccinal de 18 ans 1 fois (selon modalités de rattrapage) + rappels systématiques à 25, 45 et 65 ans > 5 ans - Délai minimal entre un d. TP et un d. Tca. P > 1 mois Et après une coqueluche maladie ? Une injection de rappel est recommandée aux personnes éligibles ayant contracté la maladie plus de 10 ans auparavant
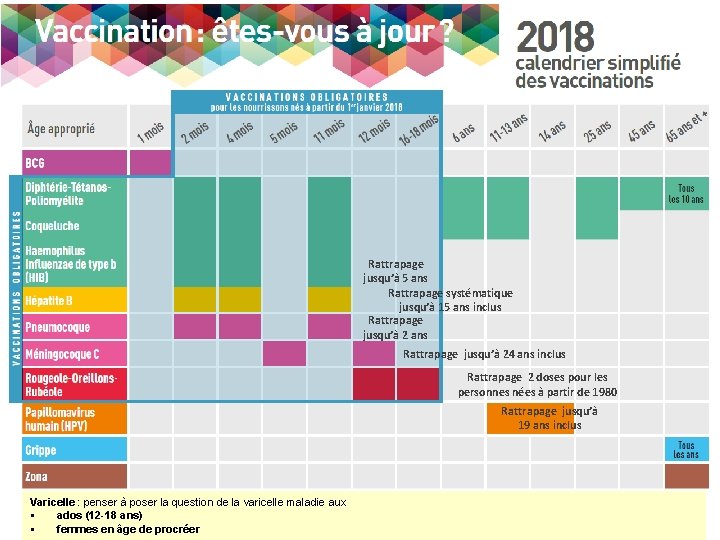
Rattrapage jusqu’à 5 ans Rattrapage systématique jusqu’à 15 ans inclus Rattrapage jusqu’à 2 ans Rattrapage jusqu’à 24 ans inclus Rattrapage 2 doses pour les personnes nées à partir de 1980 Rattrapage jusqu’à 19 ans inclus Varicelle : penser à poser la question de la varicelle maladie aux § ados (12 -18 ans) § femmes en âge de procréer

Effets secondaires Aluminium et MFM Hépatite B Papillomavirus Comment communiquer ? LES CONTROVERSES : LES COMPRENDRE COMMUNIQUER AVEC SON PATIENT

VACCINS ET EFFETS INDÉSIRABLES

Effets indésirables/secondaires et notifications • Selon les vaccins – Vaccins vivants : réactions et complications retardées, de nature infectieuse – Vaccins inertes : réactions et complications immédiates ou précoces, de type hypersensibilité • Type de réactions – Réactions mineures, bénignes +++ et fréquentes – Accidents graves, rares
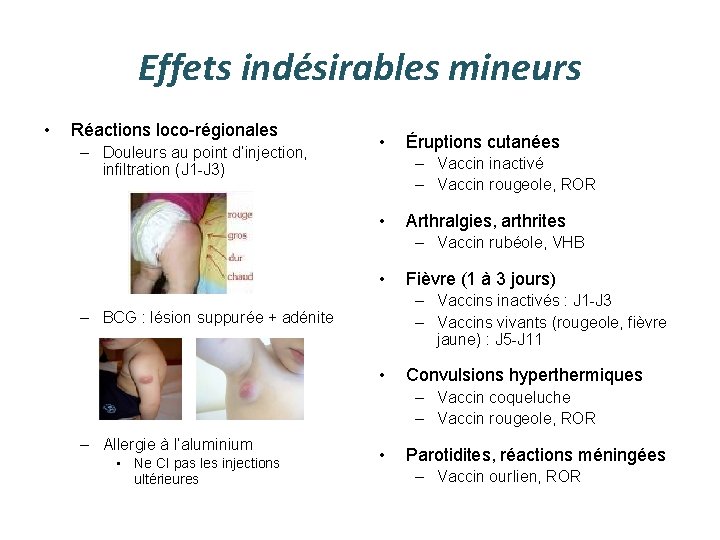
Effets indésirables mineurs • Réactions loco-régionales – Douleurs au point d’injection, infiltration (J 1 -J 3) • Éruptions cutanées – Vaccin inactivé – Vaccin rougeole, ROR • Arthralgies, arthrites – Vaccin rubéole, VHB • Fièvre (1 à 3 jours) – Vaccins inactivés : J 1 -J 3 – Vaccins vivants (rougeole, fièvre jaune) : J 5 -J 11 – BCG : lésion suppurée + adénite • Convulsions hyperthermiques – Vaccin coqueluche – Vaccin rougeole, ROR – Allergie à l’aluminium • Ne CI pas les injections ultérieures • Parotidites, réactions méningées – Vaccin ourlien, ROR

Effets indésirables graves • Réactions anaphylactiques (1/100 000 à 1/1 000) : • – – – – Dans les minutes suivants l’injection d’un vaccin • Vaccin antiamaril (fièvre jaune) – EIG viscérotropes et neurotropes surtout si > 60 ans et immunodépression (thymectomie notamment) (1/200000) • BCGite généralisée : – BCG chez un patient immunodéprimé • Vaccin anti-coquelucheux (entier +++) : – Syndrome de cris persistants, convulsions (1/2 000 à 10 000) • Vaccin anti-poliomyélitique oral : – Paralysies (1/ 3, 2 M. de doses) Restent exceptionnels !!! Liens jamais prouvés entre • SEP et VHB Autisme et ROR Maladies démyélinisantes et HPV Vaccins et allergies Vaccins et eczéma. . . Etc. . . Sur-risque ≠ lien de causalité mis en évidence pour – Narcolepsie et PANDEMRIX® – Langer-Gould A. JAMA Neurol 2014 : étude cas-contrôles de la KPSC • • Sous-groupe < 50 ans, dans les 30 j : sur risque de poussée d’affection démyélinisante du SNC après vaccination (tous vaccins confondus), OR = 2, 32, IC 95% (1, 18 -4, 57) Pas d’association entre vaccin VHB et survenue d’affection démyélinisante du SNC à 3 ans, OR = 1, 12, IC 95% (0, 72 -1, 73) – Guillain-Barré / GARDASIL® ou vaccin grippe • Uniquement dans certaines études

Effets indésirables ou effets nocébo ? Nichol KL. The effectiveness of vaccination against influenza in healthy, working adults. NEJM 1995

Notification des effets secondaires à la pharmacovigilance La Pharmacovigilance repose sur l’OBLIGATION LEGALE pour certains professionnels de santé de notifier à un CRPV tout effet indésirable (Loi n° 2011 -2012 du 29 décembre 2011 ) Surveillance du médicament après sa mise sur le marché • • Le médicament doit faire l’objet d’une surveillance permanente après avoir obtenu une AMM, afin d’optimiser son bon usage La PV dure donc toute la vie du médicament et concerne une large population dans la «vie réelle» Enregistrement (anonyme) informatique des cas (base de données nationale BNPV) Réseau des 31 Centres Régionaux de Pharmacovigilance Recueil et analyse des effets indésirables après commercialisation indispensable pour réajuster si besoin Médecins, chirurgiens-dentistes, sages Structure équivalente au niveau européen (PRAC= femmes et pharmaciens Pharmacovigilance Risk Assessment Committee ) Comptes rendus du PRAC et du Comité Technique de PV sont Autres professionnels de santé publics : sites internet ANSM et EMA Liste publiée et actualisée des médicaments sous surveillance renforcée Patients et associations de patients

ALUMINIUM ET MFM

Adjuvants = optimiser de la réaction immunitaire • Définition et modes d’action – Molécule ou substance qui augmente l’immunogénicité des antigènes (réponse primaire et mémoire) – Amplification de la réaction immunitaire • Intérêt vaccinal – Réduction de la dose d’Ag et/ou du nombre d’injections nécessaires – Augmentation de l’efficacité des vaccins chez les nouveau-nés, les personnes âgées ou les patients immunodéficients • Inutile pour les vaccins vivants atténués qui sont suffisamment immunogènes (adjuvants naturels intrinsèques) – Pas d’adjuvants dans les vaccins antigrippaux saisonniers commercialisés en France

Aluminium • Références – Rapport de l’Académie de médecine 2012 – Rapport du HCSP 2013 – Rapport de l’Académie de pharmacie 2016 • Vaccin ≠ exposition chronique L’hydroxyde d’aluminium est le plus largement utilisé (depuis les années 20) – Aluminium = origine exogène (aliments, eau de consommation, exposition accidentelle ou professionnelle, médicaments (protecteurs gastriques, onguents et vaccins)) – Neurotoxicité connu à dose importante (industrie de l’aluminium, dialysé) • Valeurs toxicologiques de référence (VTR) pour l’aluminium – L’OMS a fixé une dose journalière tolérable (DJT) de 1 mg/kg de poids corporel – Suite à travaux expérimentaux sur le devenir de l’aluminium dans l’organisme ingéré ou inoculé : niveau de sécurité de 0, 85 mg d’aluminium par dose de vaccin • Dans l'organisme : ce que l’on sait – Voie digestive/respiratoire/cutanée : barrière (pas de preuve de lien entre absorption et maladies) – Vaccin : persistance plus ou moins longtemps au site d'injection – Données expérimentales chez l'animal : une dose de 0, 85 mg par voie IM produirait théoriquement une augmentation plasmatique maximale de 0, 04 ng, soit 0, 8% de la concentration de l’aluminium sanguin

Myofaciite à macrophage et aluminium q Myofasciite à macrophage = lésion histologique (décrite dans les années 80) retrouvant des inclusions de cristaux de dérivés de l'aluminium dans les macrophages, sans lésion myocytaire notable ni lésion nécrotique (= « tatouage vaccinal » ) • Syndrome (asthénie, douleur chronique et troubles cognitifs) décrit à la fin des années 90 par l’équipe de Gherardi/Authier hypothèse d’un lien avec l’aluminium contenu dans les vaccins – Lésion histologique souvent retrouvée lors des biopsies, persistance plus longue chez les symptomatiques • • • Description clinique / critères d’inclusion varie selon les études (souvent pas de groupe témoins) Pas ou peu de description chez les enfants qui sont les plus exposés Notification d’un peu plus de 400 cas sur 160 millions de doses administrées – Théorie du « cheval de Troie » /translocation (modèle animaux) – A ce jour, pas de lien mis en évidence entre la survenue des symptômes et l’adjuvant contenu dans les vaccins – Conflits d’intérêts +++ • Quoi de nouveau en 2017 ? – Financement par l’ANSM (2015) à hauteur de 150000€ de travaux de recherche fondamentale (BNAA-AVC) – Etude portant sur la biopersistance et neuromigration des adjuvants aluminiques des vaccins – Approches génétique et expérimentale Les particules plus petites favoriseraient l’internalisation de l’adjuvant par les macrophages et donc la translocation des particules injectées vers les tissus Un défaut du gêne de l’autophagie pourrait diminuer l’autophagie, la prise en charge des nanoparticules et donc augmenter leur toxicité – Communiqué ANSM/conseil scientifique : http: //ansm. sante. fr/S-informer/Presse-Communiques-Pointspresse/Les-vaccins-contenant-de-l-aluminium-sont-surs-Communique Toujours pas de preuve d’un lien

HÉPATITE B ET SÉCURITÉ VACCINALE

Sécurité vaccinale et hépatite B (1) • Bilan de pharmacovigilance et profil de sécurité d’emploi des vaccins contre l’hépatite B (AFSSAPS, février 2012) – Surveillance renforcée depuis 1994 (entre 2007 et 2010, plus de 11 millions de doses distribuées en France) – Trois types d’événements indésirables particulièrement surveillés : • • • Les affections démyélinisantes du système nerveux dont la sclérose en plaques (SEP) Les affections auto-immunes (lupus, polyarthrite rhumatoïde, thyroïdite) Les affections hématologiques (thrombopénie, purpura thrombopénique idiopathique, aplasie médullaire, leucémie) – Nombre de cas déclarés dans la population vaccinée pour chacune de ces pathologies inférieur au nombre de cas attendus dans la population générale • Depuis 1999 : plusieurs études rassurantes (dont Langer-Gould A. JAMA Neurol 2014) – Vaccin et déclenchement de SEP – Vaccin et rechute/poussée de SEP – Toutes négatives sauf une (de méthodologie critiquée, Hernan 2004) • Le 9/03/2016 : ordonnance de non-lieu dans l’instruction menée pendant 17 ans sur le vaccin contre l’hépatite B mis en cause dans l’apparition de maladies neurologiques comme la SEP • Ne pas confondre : lien temporel lien de causalité et liens scientifiques liens juridiques

Sécurité vaccinale et hépatite B (2) • La Cour de justice européenne reconnaît le lien entre le vaccin contre l’hépatite B et la sclérose en plaques ? – Pour les vaccins non obligatoires : « la victime est obligée de prouver le dommage, le défaut et le lien de causalité entre le défaut et le dommage » – Pour la Cour de justice de l’Union européenne (CJUE) (21 juin 2017) • Pas de consensus scientifique • De défaut d’un vaccin et le lien de causalité entre celui-ci et une maladie peuvent être prouvés par un faisceau d’indices graves, précis et concordants • Indices dont la conjonction pourrait conduire le juge national à considérer qu’une victime a satisfait à la charge de la preuve pesant sur elle – la proximité temporelle entre l’administration d’un vaccin et la survenance d’une maladie – l’absence d’antécédents médicaux personnels et familiaux en relation avec cette maladie – l’existence d’un nombre significatif de cas répertoriés de survenance de cette maladie à la suite de telles administrations – Indemnisation possible, si un juge estime qu’ils apportent suffisamment d’éléments à leur dossier, malgré l’absence de preuve du lien de causalité entre le vaccin VHB et la SEP – Appréciation au cas par cas : la justice européenne ayant écarté la possibilité de fixer des critères permettant d’établir automatiquement l’existence d’un lien de causalité – Dans tous les cas, la justice européenne ne s’est ici pas prononcée sur le fond du dossier.

PAPILLOMAVIRUS ET SÉCURITÉ VACCINALE

• La pharmacovigilance Pharmacovilance CRPS/POTS – Vaccin HPV = plan de gestion des risques (PGR) et suivi national renforcé de pharmacovigilance – Pharmacovigilance dans le monde : > 170 millions de doses et pas d’alerte – Depuis la commercialisation en France de Gardasil : > 5, 8 millions de doses (ansm. sante. fr) Effets indésirables majoritairement rapportés : douleur au site d’injection, céphalées, vertiges, nausée ou fièvre présentent un caractère bénin et transitoire. Parmi les cas graves : syncopes vaso-vagales d’évolution favorable prédominent Manifestations auto-immunes rapportées : leur nombre reste faible et inférieur à celui observé dans la population générale de même âge, sur la base des données d’incidence et de prévalence disponibles • Syndrome régional douloureux complexe (CRPS) et le syndrome de tachycardie posturale orthostatique (POTS) (ansm. sante. fr) – 2015 : Evaluation des risques par le PRAC (Comité pour l’Evaluation des Risques en matière de Pharmacovigilance ) de l’Agence européenne des médicaments (EMA) Pas de relation cause à effet et pas de modification des recommandations ni du RCP – Butts BN, Human Papillomavirus Vaccine and Postural Orthostatic Tachycardia Syndrome: A Review of Current Literature. J Child Neurol. 2017 Oct; 32(11): 956 -965 pas de mise en évidence de lien (effectifs trop faibles des “case reports” et “case series”)
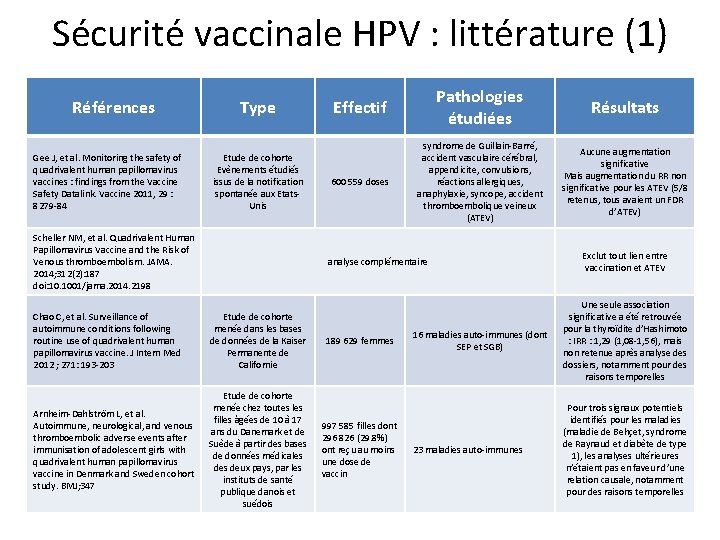
Sécurité vaccinale HPV : littérature (1) Références Gee J, et al. Monitoring the safety of quadrivalent human papillomavirus vaccines : findings from the Vaccine Safety Datalink. Vaccine 2011, 29 : 8279 -84 Type Etude de cohorte Evènements étudiés issus de la notification spontanée aux Etats. Unis Scheller NM, et al. Quadrivalent Human Papillomavirus Vaccine and the Risk of Venous thromboembolism. JAMA. 2014; 312(2): 187 doi: 10. 1001/jama. 2014. 2198 Effectif Pathologies étudiées Résultats 600 559 doses syndrome de Guillain-Barré, accident vasculaire cérébral, appendicite, convulsions, réactions allergiques, anaphylaxie, syncope, accident thromboembolique veineux (ATEV) Aucune augmentation significative Mais augmentation du RR non significative pour les ATEV (5/8 retenus, tous avaient un FDR d’ATEV) analyse complémentaire Chao C, et al. Surveillance of autoimmune conditions following routine use of quadrivalent human papillomavirus vaccine. J Intern Med 2012 ; 271: 193 -203 Etude de cohorte menée dans les bases de données de la Kaiser Permanente de Californie Arnheim-Dahlström L, et al. Autoimmune, neurological, and venous thromboembolic adverse events after immunisation of adolescent girls with quadrivalent human papillomavirus vaccine in Denmark and Sweden cohort study. BMJ; 347 Etude de cohorte menée chez toutes les filles âgées de 10 à 17 ans du Danemark et de Suède à partir des bases de données médicales deux pays, par les instituts de santé publique danois et suédois 189 629 femmes 997 585 filles dont 296 826 (29. 8%) ont reçu au moins une dose de vaccin Exclut tout lien entre vaccination et ATEV 16 maladies auto-immunes (dont SEP et SGB) Une seule association significative a été retrouvée pour la thyroïdite d’Hashimoto : IRR : 1, 29 (1, 08 -1, 56), mais non retenue après analyse des dossiers, notamment pour des raisons temporelles 23 maladies auto-immunes Pour trois signaux potentiels identifiés pour les maladies (maladie de Behçet, syndrome de Raynaud et diabète de type 1), les analyses ultérieures n’étaient pas en faveur d’une relation causale, notamment pour des raisons temporelles

Sécurité vaccinale HPV : littérature (2) Références Type Grimaldi-Bensouda L, et al. Autoimmune disorders and quadrivalent papillomavirus vaccination of young female subjects. J Intern Med 2013; 275(4): 398 -408 Etude menée dans le programme Pharmacoepidemiologic General Research Extension (PGRx), programme recrutant en continu des cas de diverses maladies dans des centres hospitaliers et des témoins en médecine générale Klein NP, et al. Safety of quadrivalent human papillomavirus vaccine administered routinely to females. Arch Pediatr Adolesc Med 2012; 166: 1140 -8 Etudes de cohorte demandée par la Food and Drug Administration : Analyse des consultations aux urgences et des hospitalisations après vaccination Angelo MG, et al. Post-licensure safety surveillance for human papillomavirus 16/18 -ASO 4 -adjuvanted vaccine: more than 4 years of experience. Pharmacoepidemiology and Drug safety 2014; 23(5): 456 -65 Analyse poolée des données issues de 42 études cliniques terminées et en cours, a permis d’évaluer la sécurité d’emploi du Cervarix Effectif 269 cas définis ou possibles (1096 contrôle) Pathologies étudiées Résultats Maladies autoimmunes dont SEP et SGB Pour l’ensemble des maladies auto-immunes étudiées, il n’y avait pas d’association significative avec la vaccination, OR : 0, 9 (0, 5 -1, 5) 189 629 femmes vaccinées Après revue des dossiers médicaux, les auteurs ont retenu une augmentation du risque de syncope le jour de la vaccination, OR : 6, 0 (3, 9 – 9, 2) ainsi qu’une augmentation des infections cutanées pour la période de 1 à 14 jours, OR : 2, 0 (1, 4 – 2, 9) 31 173 adolescentes et jeunes femmes Profil de tolérance observé chez les sujets vaccinés avec Cervarix® semblable à celui observé chez les sujets inclus dans les groupes contrôles

Sécurité vaccinale HPV : littérature (3) Références Type Effectif Pathologies étudiées Résultats MHRA Public Assessment Report : Cervarix HPV vaccine - update on UK safety experience at end of 4 years use in the HPV routine immunisation programme. Bilan sur les données de pharmacovigilance colligées et analysées durant quatre années d’utilisation du Cervarix® au Royaume -Uni (2008 -2011) incluant une surveillance renforcée de deux années en milieu scolaire (2008/2009 - 2009/2010) 6 millions de doses Maladies auto-immunes Pas de risque accru 14 maladies dont les maladies démyélinisantes et le SGB Pas d’augmentation des maladies démyélinisante Sur-risque par 4 pour le SGB Pas de mise en évidence d’un risque Miranda S. Human papillomavirus vaccination and risk of autoimmune diseases: A large cohort study of over 2 million young girls in France. Vaccine. 2017 Aug 24; 35(36): 4761 -4768 Gee J, Risk of Guillain-Barré Syndrome following quadrivalent human papillomavirus vaccine in the Vaccine Safety Datalink. Vaccine. 2017 Oct 13; 35(43): 5756 -5758 Andrews N. No increased risk of Guillain-Barré syndrome after human papilloma virus vaccine: A self-controlled case-series study in England. Vaccine. 2017 Mar 23; 35(13): 1729 -1732 Etude de cohorte observationnelle Base de données ANSM/CPAM Analyse des données du Vaccine Safety Datalink 2006 -2015 2 773 185 doses pour 1 708 075 personnes vaccinées estimées Aussi : point de l’OMS dans le Relevé épidémiologique hebdomadaire, No 19, 2017, 92, 241– 268

Pourquoi la vaccination est importante ? Quelques données • Clairance naturelle du virus mais possibilité de persistance du virus (3 à 10% chez les femmes)1, responsable de lésions – Atteintes bénignes cutanéomuqueuses (condylomes) ou respiratoire (papillomatose) – Lésions précancéreuses et cancers : col de l’utérus mais aussi de la vulve, du vagin, de l’anus, du pénis, ORL • Histoire naturelle de l’infection HPV (évoluant vers le cancer du col)2 § § 1 2 En France, 3000 nouveaux cas chaque année, plus de 1000 décès Diagnostic de néoplasie cervicale de haut grade ou de cancer est posé chaque année chez environ 30 000 femmes 1 = Conisations parfois répétées Problèmes obstétricaux = Hystérectomie Pic de l’incidence : 40 ans Les HPV 16 et 18 représentent 70% des virus responsables des cancers du col Institut Pasteur. https: //www. pasteur. fr/fr/centre-medical/fiches-maladies/cancer-du-col-uterus-papillomavirus Pr Chidiac, infectiologie. com

Pourquoi la vaccination est importante ? Intérêt du vaccin • Objectif de la politique vaccinale en France : lutte contre le cancer du col de l’utérus • Efficacité des vaccins démontrée – Prévention des lésions précancéreuses du col de l’utérus dans les essais cliniques – Dans des études post-AMM, conduites dans plusieurs pays à ce jour, évaluation en conditions réelles : infection HPV, condylomes (pour le vaccin quadrivalent) et lésions précancéreuses du col – Immunité de groupe – Immunité croisée avec certains génotypes oncogènes (HPV 31 notamment) • Dépistage du cancer du col en France – Couverture estimée proche de 60 % – Fortes disparités territoriales en partie par l’existence d’une faible démographie en gynécologues, médecins généralistes ou anatomo-cytopathologistes – Recours au dépistage par frottis cervico-utérin moins fréquent chez les femmes disposant d’un faible revenu, bénéficiant de la CMU complémentaire (CMUc), ou ayant un niveau de diplôme inférieur au baccalauréat – Dépistage organisé dans les départements pilotes, bien que le dépistage organisé du cancer du col de l’utérus augmente significativement, le pourcentage de femmes dépistées dépasse de peu les 70 % pour les plus performants La vaccination est donc bien une stratégie complémentaire nécessaire HCSP, Vaccination contre les infections à papillomavirus humains, 2014

COMMENT COMMUNIQUER ?

Les impasses relationnelles ( T Gordon) • • • Ordonner Alarmer, mettre en garde, menacer Conseiller, faire des suggestions, fournir des solutions Démontrer, argumenter, enseigner Moraliser Juger Étiqueter Interpréter, analyser Sympathiser, consoler Mettre à l’épreuve Plaisanter…

L'entretien motivationnel (infovac DPC 2014) Miller et Rollnick, the guildford press 2002 et 2008 https: //www. afdem. org/ « L’entretien motivationnel (EM) est une méthode de communication participative orientée vers un objectif précis. Elle se focalise tout particulièrement sur le langage du changement. L’objectif est de renforcer les motivations personnelles et l’engagement vers le changement » . (Miller, W. R. et S. Rollnick, 2010). Constat Principes Le médecin convaincu a toujours tendance à apporter d'emblée l'information juste Le patient réticent a toujours tendance à le refuser d'emblée Empathie Absence d'argumentation Exploration de l'ambivalence Respect de l'autonomie (pas de jugement) Se rappeler ces règles Lorsque quelqu'un est ambivalent ou réticent, il est préférable d'explorer ses croyances et ses attitudes que de lui donner d'emblée des conseils Le résultat prévisible d'une argumentation est que chacun consolide sa position
- Slides: 50