Va grupa periodnog sistema ns 2 np 3












































































- Slides: 96

Va grupa periodnog sistema ns 2 np 3 AZOT FOSFOR ARSEN ANTIMON BIZMUT 1 11/22/2020

Opšte osobine grupe N i P nemetali l As i Sb metaloidi l Bi metal l Metalne osobine i reaktivnost u grupi rastu l Ej, afinitet prema elektronu, elektronegativnostopadaju l Oksidaciona stanja od -3 do +5 za N, P +3, +5 za As, Sb, Bi l 2 11/22/2020

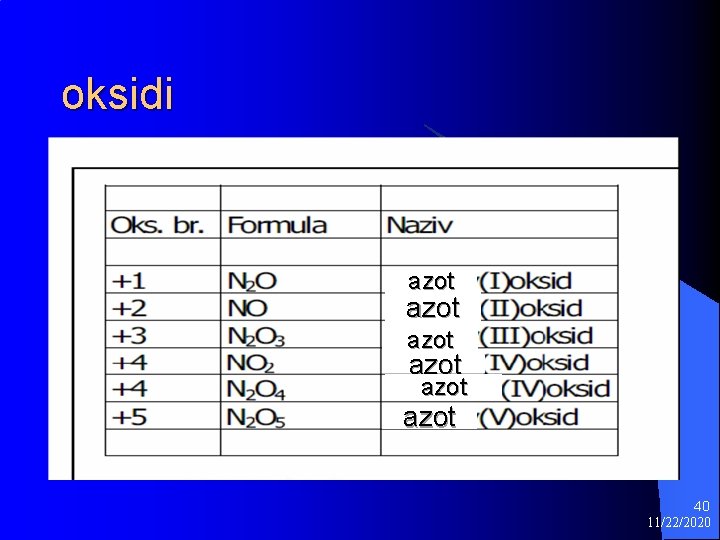
Jedinjenja koja grade Oksidi E 2 O 3 ; E 2 O 5 najzastupljeniji l Azot gradi pet oksida o. b. od+1 do +5 l Kiseline o. b +5 l Baze o. b. +3 (za As, Sb, Bi) amfoternog karaktera l Azot iako nemetal gradi bazu l NH 3 -amonijak , rastvaranjem u vodi NH 3+H 2 O NH 4+ + OHl amonijum jon 3 11/22/2020

AZOT Nalazi se u prirodi kao gas N 2 u vazduhu l 78% l u obliku jedinjenja je veoma rasprostranjen u zemlji l 4 11/22/2020

NO 2 5 11/22/2020

Azot hemijski element l l l l Položaj azota u periodnom sistemu elemenata * Ar(N) = ? *( 7 N +7 ) ? ? Redni broj Elektronska formula atoma azota je: : : : : Oksidaciona stanja : ? valentnost : ? 6 11/22/2020

l AZOT 7 11/22/2020

Značaj azota Аzot – “neživi”. l Аzот – glavni element života na Zemlji. l 1. Struktura molekula l 2. fizičke osobine l 3. hemijske osobine l 4. načini dobijanja l * primena azota i značaj l 8 11/22/2020

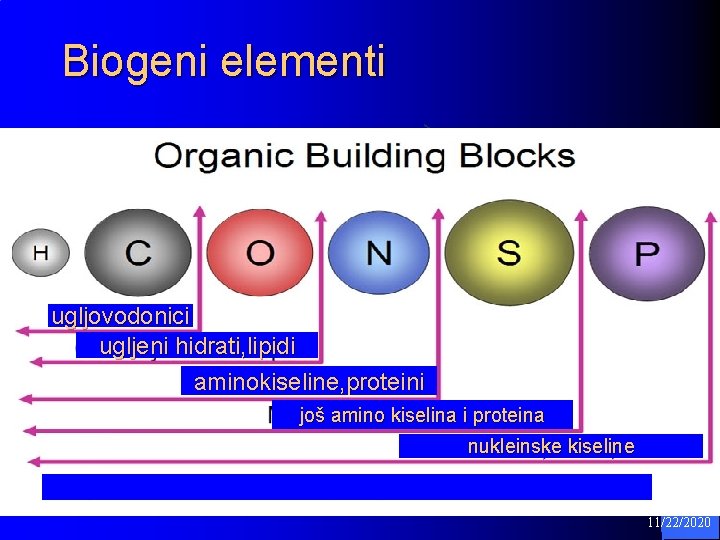
Biogeni elementi ugljovodonici ugljeni hidrati, lipidi aminokiseline, proteini još amino kiselina i proteina nukleinske kiseline 9 11/22/2020

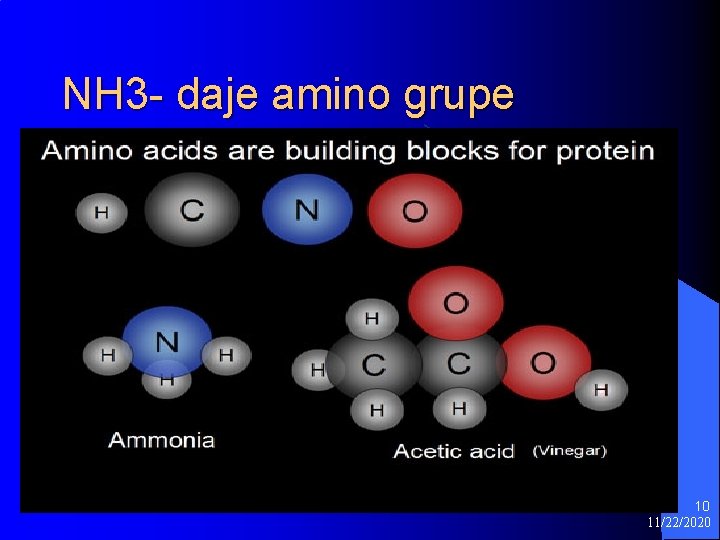
NH 3 - daje amino grupe 10 11/22/2020

Molekul azota : energija disocijacije na atome je 942, 9 к. J/моl, i na temperaturi od 3300° disocija je svega 0, 1%. l Kakve su veze u molekulu azota l 11 11/22/2020

Molekul azota se razlaže na 2 N 12 11/22/2020

Inertan gas N N l Trostruka veza –tri elektronska para l Jedna sigma s i dve pi p veze l Veoma stabilan i slabo reaguje l Visok pritisak i velika količina E omogućuju raskidanje veza l 13 11/22/2020

VISOLAT 14 11/22/2020

NITER 15 11/22/2020

Fizičke osobine azota Malo je lakši od vazduha; gustine 1, 2506 g/cm 3 (prin. u. . ), tt. = - 209, 8 о. С, tk. = 195, 8 о. С. Azot sagoreva teško. Gustina tečnog azota je 800 g/cm 3. U vodi je teško rastvoran-manje od kiseonika na 0 о. С u 1 m 3 Н 2 О rastvara se 23, 3 g azota. l Azot ne pomaže gorenje niti disanje l 16 11/22/2020

Hemijska svojstva azota S metalima AZIDI: l N 2+Li Li 3 N l N 2+Mg Mg 3 N 2 l N 2+Al Al. N l S nemetalima: l N 2+H 2 NH 3 l N 2+O 2 (2000 o) NO l N 2+F 2 NF 3 l 17 11/22/2020

laboratorijski N dobivamo termičkim raspadanjem npr. Amonijum nitrita l NH 4 NO 2(s) N 2(g)+ 2 H 2 O(g) l • koristi se kao najjeftiniji inertni gas l 18 11/22/2020

Dobijanje azota-vulkan (NH 4)2 Cr 2 O 7 N 2 + Cr 2 O 3 + H 2 O 19 11/22/2020

Dobijanje azota NH 4 NO 2 N 2+ 2 H 2 O l Frakcionom destilacijom tečnog vazduha l Primena: -očuvanje inertnih sredina u metalurgiji -sinteza amonijaka i azotne kiseline -proizvodnja mineralnih djubriva -tečni azot u medicini 20 11/22/2020

Tečni azot 21 11/22/2020

Tečni azot u bazenu 22 11/22/2020

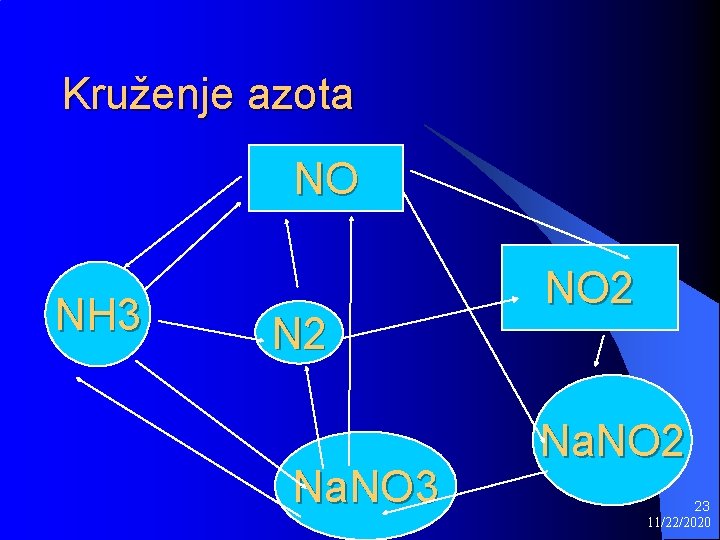
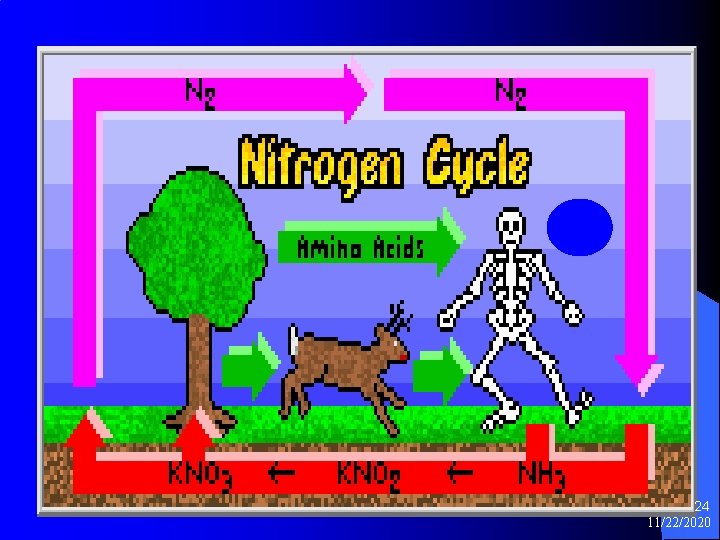
Kruženje azota NO NH 3 N 2 Na. NO 3 NO 2 Na. NO 2 23 11/22/2020

24 11/22/2020

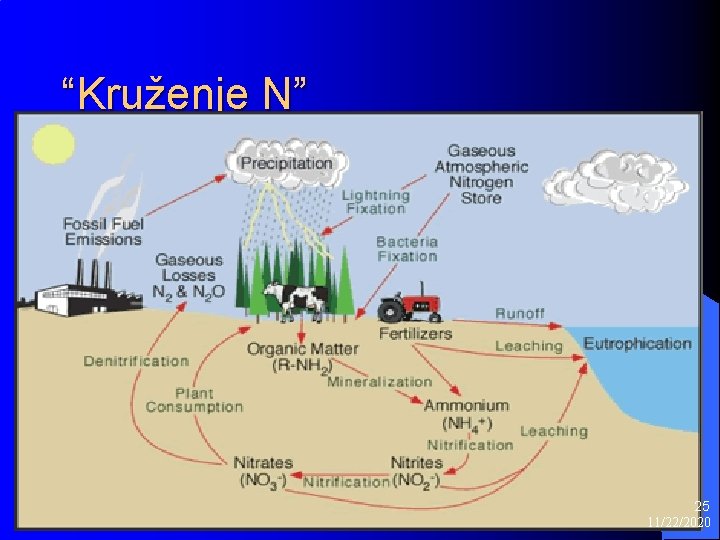
“Kruženje N” 25 11/22/2020

26 11/22/2020

Amonijak NH 3 l l l O. b. -3 Dobija se u industriji HABER-BOŠOVIM postupkom N 2+ 3 H 2 2 NH 3 DH= -92, 5 k. J Povratna reakcija kojoj odgovara promena pritiska da bi ZAŠTO? Zašto ne zagrevamo sistem? 27 11/22/2020

Dobijanje amonijaka Zagrevanjem NH 4 Cl l NH 4 Cl NH 3 +HCl l ili NH 4 Cl u reakciji sa nekom jačom bazom l 2 NH 4 Cl + Ca(OH)2 2 NH 3 +Ca. Cl 2 +2 H 2 O U organizmu nastaje razgradnjom proteina ; kod nižih organizama se direktno izlučuje ; kod viših se vezuje sa CO 2 gradeći karbamid (ureu) NH 2 CONH 2 i izlučuje se u vidu mokraće 28 11/22/2020

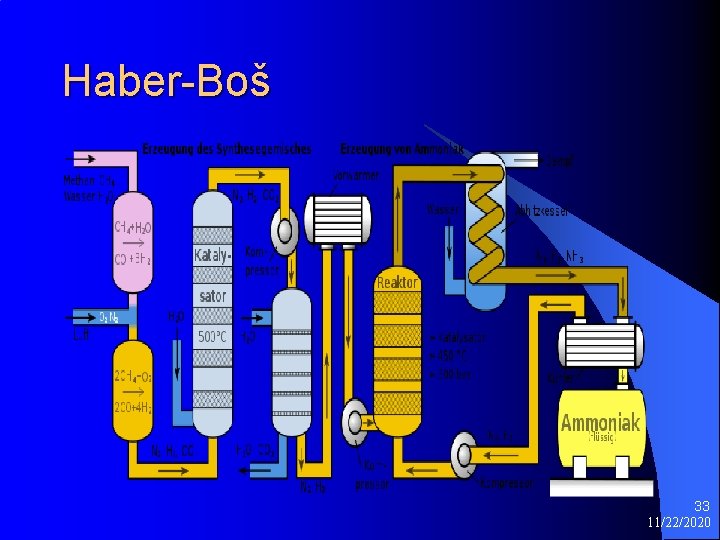
HABER-BOŠOV PROCES l 3 H 2(g) + N 2(g) = 2 NH 3(g) DH=-92 k. Jmol-1 AMONIJAK i NITRATNA KISELINA 450ºC temperatura usporava proces ali 300 ATM visok pritisak ubrzava proces Fe katalizator KOH ubrzava proces 15% 29 11/22/2020

OSTWALD PROCES! l l l AMONIJAK se prevodi u NITRATNU kiselinu 4 NH 3(g) + 5 O 2(g) = 4 NO(g) + 6 H 2 O(g) DH= -900 k. Jmol-1 4 NO(g) + 3 O 2(g) +2 H 2 O(l) 4 HNO 3(aq) 900ºC 10 ATM PLATINUM/RHODIUM KATALIZATOR 65% prinos 30 11/22/2020

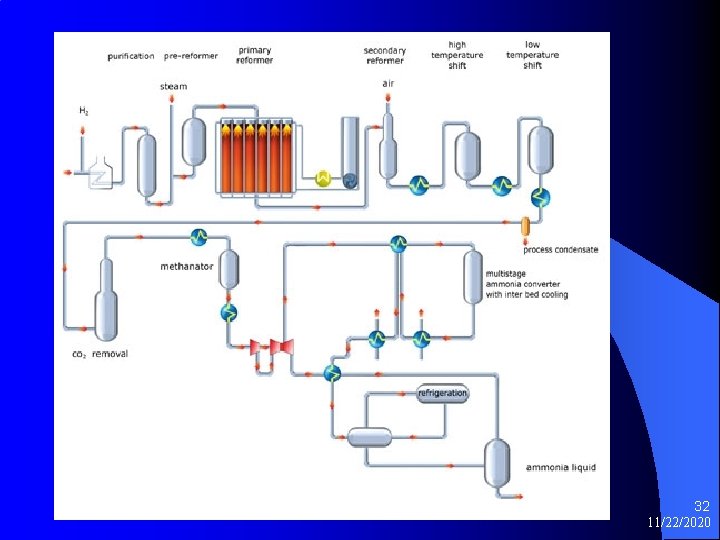
Proizvodnja amonijaka 31 11/22/2020

32 11/22/2020

Haber-Boš 33 11/22/2020

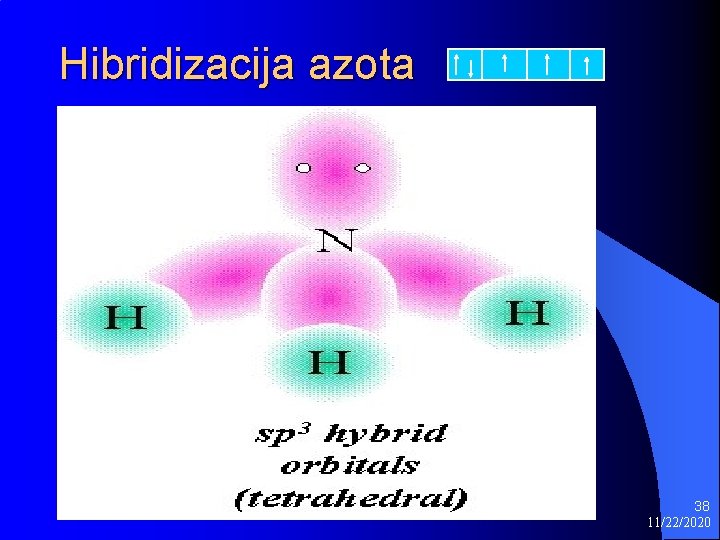
Polarnost amonijaka Hibridizovan azot sp 3 l Ima slobodni elektronski par kojim gradi koordinativnu vezu s polarnim molekulima l Napr voda, kiseline l H- N: H - O: : H H kiseonik ima sp 3 hibridne orbitale i dva slobodna el. para l 34 11/22/2020

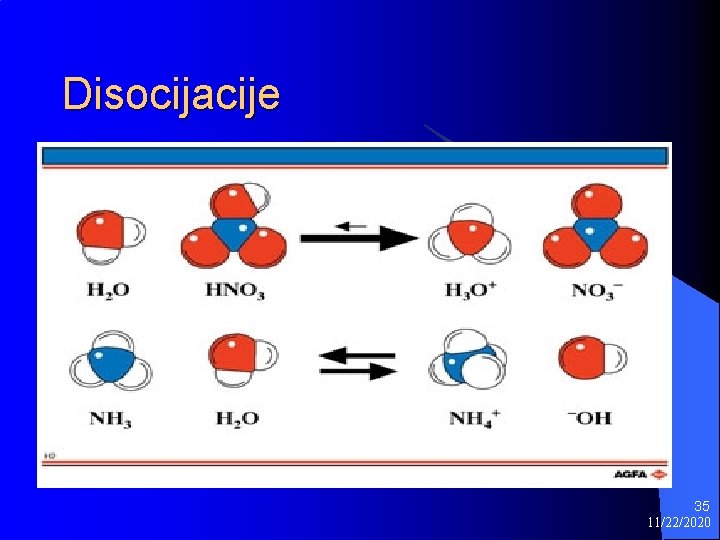
Disocijacije 35 11/22/2020

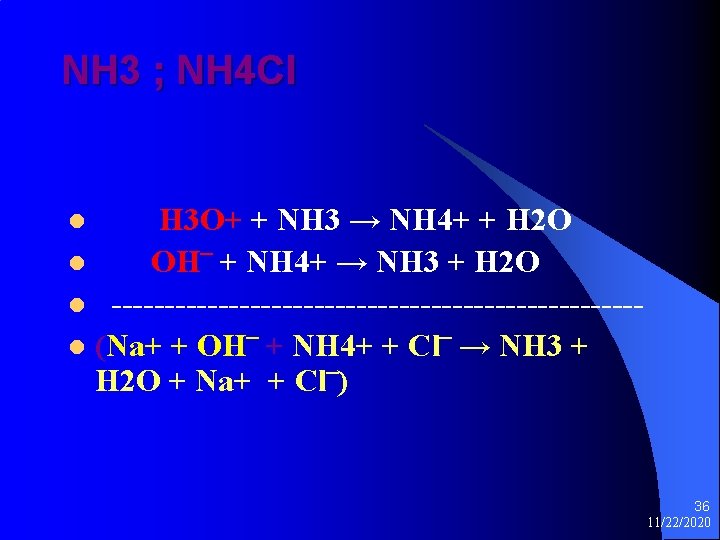
NH 3 ; NH 4 Cl H 3 O+ + NH 3 → NH 4+ + H 2 O l OH‾ + NH 4+ → NH 3 + H 2 O l -------------------------l (Na+ + OH‾ + NH 4+ + Cl‾ → NH 3 + H 2 O + Na+ + Cl‾) l 36 11/22/2020

Osobine amonijaka Gas, karakterističnog neprijatnog mirisa l Udisanjem deluje na sluzokožu i izaziva opekotine l Rastvara se u vodi i dje jak bazni rastvor poznat po nazivu amonijum hidroksid l Veoma reaktivan, l l Sa kiselinama gradi amonijum soli 37 11/22/2020

Hibridizacija azota 38 11/22/2020

Derivati amonijaka ako se atomi vodika zamene metalom nastaju amidi, imidi i nitridi l NH 3 H+ + NH 2 - amidi l NH 2 - H+ + NH 2 - imidi l NH 2 - H+ + N 3 - nitridi l amidi se dobiju delovanjem amonijaka na alkalne i l zemnoalkalne metale, jonskog su karaktera l 2 Na(1) + 2 NH 3(g) 2 Na. NH 2(s) +H 2 l imidi su retki l nitridi: ionski (s I i II grupom) kovalentni (s IIIB i IVB) i metalni (s IIIA, IVA i VA) l 39 11/22/2020

oksidi azot azot 40 11/22/2020

Azot(I) oksid N 2 O, gas bez boje i mirisa, slatkastog ukusa, male količine izazivaju smeh (rajski gas), a veće količine uzrokuju opštu anesteziju l dobija se blagim zagrevanjem amonijum nitrata NH 4 NO 3 N 2 O(g) + 2 H 2 O(g) l l l molekul je linearni rezonantni hibrid, nije dipol pri višim temperaturama je jako oksidaciono sredstvo, zagrevanjem se raspada N 2 O(g) N 2(g) + O 2(g) 41 11/22/2020

Ob. +3 azotasta kiselina (nitritna kiselina) Nastaje rastvaranjem N 2 O 3 u vodi l N 2 O 3 + H 2 O 2 HNO 2. l delovanjem kiseline na nitrite l Na. NO 2+HCl HNO 2 + Na. Cl l nepostojana je i razlaže se na više načina l 3 HNO 2 H+ + NO 3 - + 2 NO(g) + H 2 O l 2 HNO 2_ NO(g) + NO 2(g)+ H 2 O l HNO 2 je slaba kiselina (KA=4. 5× 10 -4) i njene soli u vodi hidrolizuju bazno l NO 2 - + H 2 O HNO 2 + OHl 42 11/22/2020

Ag. NO 2 hidrolizuje kiselo-jedini 43 11/22/2020

• nitriti l se mogu dobiti zagrevanjem nitrata l 2 Na. NO 3(1) 2 Na. NO 2(1) + O 2(g) l ili redukcijom nitrata uz C ili olovo l Na. NO 3(s) + Pb(s) Na. NO 2(s) + Pb. O(s) nitrit ion lako pravi komplekse, postoje dve vrste l nitrito-kompleksi M-O-N=O, npr. l kalijum heksanitrokobaltat(III) koji služi kao analitički dokaz K+, odnosno NO 2 - -iona l nitro-kompleksi M - NO 2, su retki i nestabilni l kiselina u kiselom i nitriti u baznoj sredini mogu biti I l Oksidaciona i redukciona sredstva l 44 11/22/2020

Dobijanje NO 2 i rastvaranje u vodi HNO 3 NO 2 Cu HNO 2 +HNO 3 45 11/22/2020

Ob +5 azot(V) oksid, nitratna kiselina i njene soli l nitrili (odvode od katjona NO 2+) l azot(V) oksid ili azot-pentoksid (N 2 O 5) iznad 0°C raspada se l l N 2 O 5(s) N 2 O 4(g) + 1/2 O 2(g) s vodom burno reaguje dajući nitratnu kiselinu HNO 3 l 46 11/22/2020

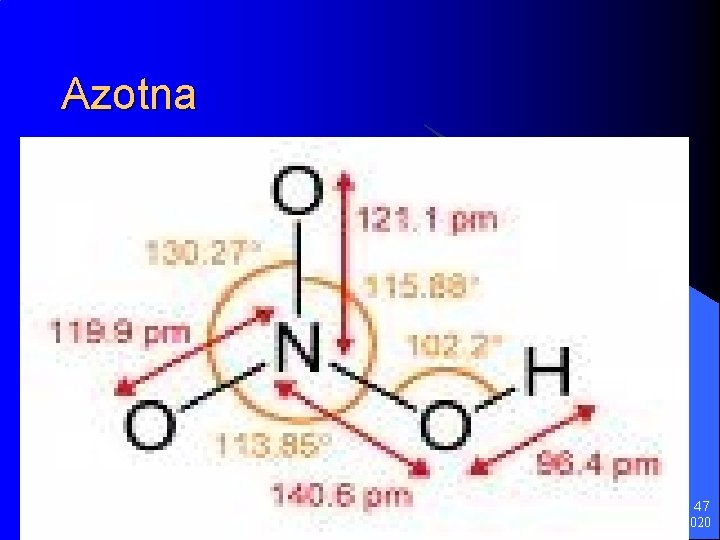
Azotna 47 11/22/2020

HNO 3 l Nestabilna pa se razlaže na: 4 HNO 3 2 H 2 O+ 4 NO 2(g) + O 2(g) (smedja boja od NO 2) Neki metali u azotnoj kiselini daju NO 2 Cu + 4 HNO 3 Cu(NO 3)2+NO 2+ 2 H 2 O u razblaženoj 3 Cu +8 HNO 3 3 Cu(NO 3)2 +2 NO+4 H 2 O 48 11/22/2020

Postupak dobijanja azotne l Iz amonijaka 4 NH 3(g) + 5 O 2(g) 4 NO(g) + 6 H 2 O(g) 2 NO(g) + O 2(g) 2 NO 2(g) 3 NO 2(g) + H 2 O 2 HNO 3 - + NO(g) Jaka kiselina Iz nitrata l Na. NO 3(s) + H 2 SO 4 HNO 3(g) + Na. HSO 4 l l l 49 11/22/2020

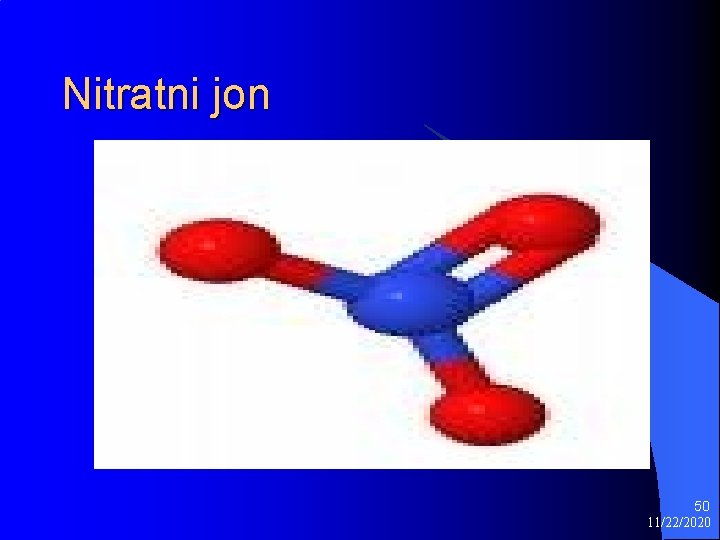
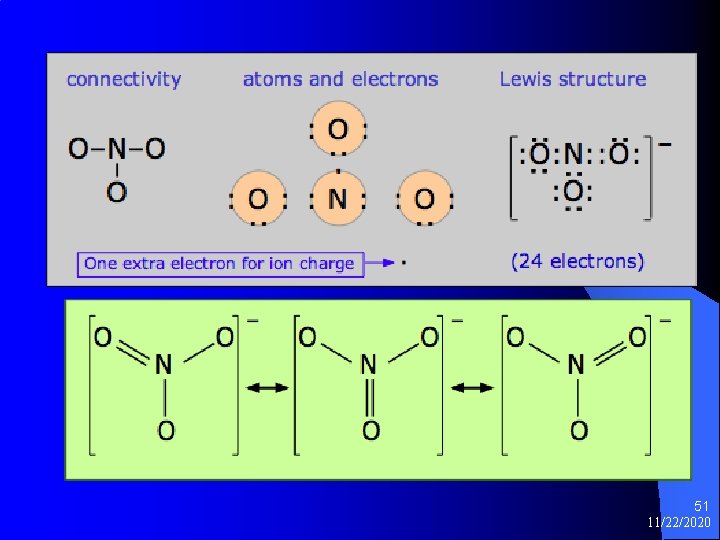
Nitratni jon 50 11/22/2020

51 11/22/2020

NH 4 NO 3 52 11/22/2020

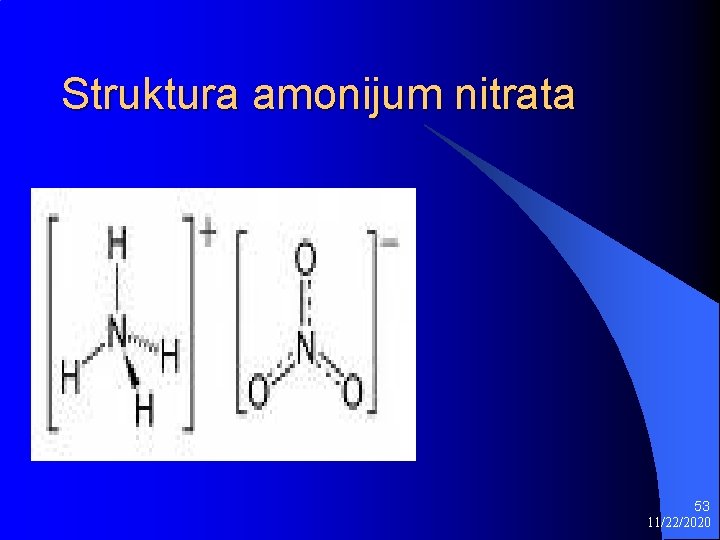
Struktura amonijum nitrata 53 11/22/2020

NH 4 NO 3 NH 4 Cl 54 11/22/2020

Šalitra 55 11/22/2020

Upotreba Na. NO 3 Tehnologija hrane Inhibira razvoj bakterija naročito Clostridium botulinum Stabilizuje sastojke mesa da se ne oksidujuju i da ne dodje do fermentacije zadržava crvenu boju mesu 56 11/22/2020

Upotreba l l l Amonijak I azotna kiselina Za rast biljaka je neophodan azot. Vecina biljaka ne koristi azot direktno iz vazduha vec iz jedinjanja. Amonijak I azotna kiselina sadrze velike kolicine vezanog azota ALI amonijak je suvise bazan , a kiselina suvise KISELA. Zato je najbolje ako se neutralisu u amonijum nitrat NH 3(g) + HNO 3(aq) NH 4 NO 3(aq) amonjiak_- detergenti i sapuni, boje i pigmenti azotna kiselina- najlon, plastika i eksplozivi 57 11/22/2020

Ostala jedinjenja l l l l l cijanidi CN- dicijan (CN)2 cijanat OCN tiocijanat. SCN- tiocijan (SCN)2 selenocijanati Se. CN selenocijan Se(CN) nitridi N 3 ponašaju se slično halogenidima i halogenima, npr. : Cl 2 + 2 OH- C 1 - + C 1 O- + H 2 O (CN)2 + 2 OH- CN- + OCN- + H 2 O 58 11/22/2020

cijanidi cijanovodik (HCN) je vrlo otrovan l mirisa gorkih badema, l krvni otrov (ne sme doći na rane) l cijanidi prave cijano komplekse l npr. [Fe(CN)6]4 -, [Ag(CN)2]-, [Pt(CN)4]2 -. . . l tiocijanati prave komplekse, l SCN- je reagens za dokaz Fe 3+ jona l nastaje [Fe(SCN)6]3 -karakteristične crvene boje. 59 11/22/2020

NF 3 60 11/22/2020

Reaktor 61 11/22/2020

Proizvodnja Azotne kiseline 62 11/22/2020

Azotara 63 11/22/2020

Proizvodnja- Uree(karbamida) 64 11/22/2020

Drvo posle kisele kiše 65 11/22/2020

Kiseli kišobran 66 11/22/2020

Fosfor l l Otkrio ga alhemičar H. Brandt 1669 god. A želeo je da napravi zlato 67 11/22/2020

Javlja se u tri alotropske modifikacije -beli -crveni -crni 68 11/22/2020

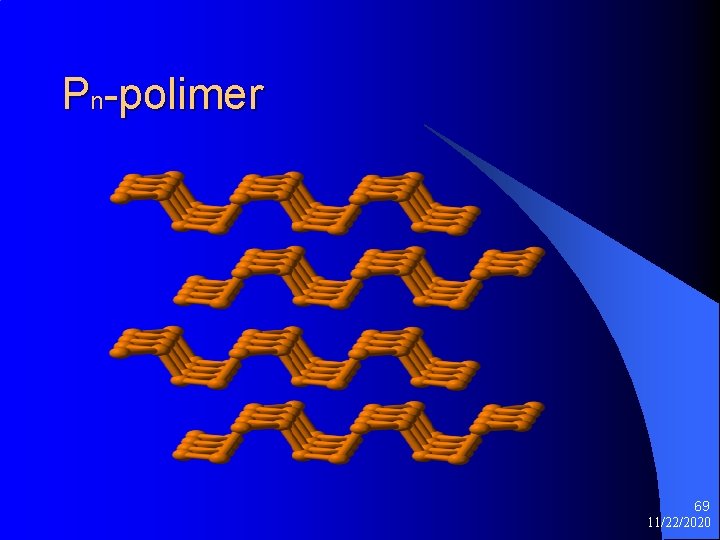
Pn-polimer 69 11/22/2020

Pn 70 11/22/2020

P (phosphorus) FOSFOR (od grč. svetlonoša), postoji samo u jedinjenjima, najčešće u solima fosfatne kiseline, fosfatima. Apatiti (fluoruapatit [Ca 5(PO 4)2] i hidroksiapatit [Ca 5(OH)(PO 4)2] glavni su sastojci fosfornih ruda ili fosforita. Veća nalazišta su u sev. Africi, SAD (Florida i Tenese), u Rusiji. Fosfor je normalni sastojak biljaka pa se stoga iscrpljenoj zemlji mora dodavati u obliku fosfornih djubriva. Sastavni je deo kostiju, mozga, mišića, živaca, a u obliku fosfatida nalazi se u biljnim i životinjskim ćelijama Fosforoproteini su belančevine koje sadrže fosfor. 71 11/22/2020

apatit 72 11/22/2020

Beli fosfor je bela (slabo žućkasta), prozračna, mekana, vosku slična materija gustine 1. 82 koja se na 44, 25°C topi u providnu uljanu tečnost. Iako ključa tek na 280°C, beli fosfor već na običnoj temperaturi znatno ispari. U vodi je nerastvoran, u alkoholu se rastvara neznatno, bolje u etru, vrlo lako u CS 2. Vrlo je reaktivan: spaja se direktno i često vrlo žestoko sa gotovo svim drugim elementima. 73 11/22/2020

beli fosfor na vazduhu se sam zapali i gori svetlim plamenom (upotrebljava se za zapaljive bombe) stoga se uvijek čuva pod vodom. Sporu oksidaciju fosfora na vlažnom vazduhu prati pojava svetlucanja. Beli fosfor je jak otrov; već u malim količinama djeluje smrtonosno stoga se upotrebljava za trovanje štetočina. Beli se fosfor dobija iz fosforita, kvarcnog peska i koksa u električnim pećima. Beli fosfor služi za proizvodnju crvenog fosfora te fosfatne kiseline i drugih jedinjenja fosfora. 74 11/22/2020

Crveni fosfor (zapravo više ljubičaste boje) nastaje iz beloga fosfora kroz na temperaturi 240 -250°C. Po svojim svojstvima vrlo se razlikuje od belog fosfora. Na običnoj temperaturi ne isparava, topi se tek na 590°C, hemijski je u poredjenju s belim fosforom slabo reaktivan, ne svetluca na vazduhu, zapali se tek na 250 -260°C, nije otrovan. Crveni se fosfor upotrebljava u industriji šibica. 75 11/22/2020

Upotreba veštačko đubrivo napalm bombe 76 11/22/2020

77 11/22/2020

Šibice 78 11/22/2020

Elementarni fosfor l l dobiva se isključivo žarenjem kalcijum fosfata sa silicijum(IV) oksidom i koksom u električnim pećima pri temperaturi 1573 K: 2 Ca 3(PO 4)2(s) + 6 Si. O 2(S) + 10 C(s) 6 Ca. Si. O 3(l) + l 0 CO(g) + P 4(g) l stepen oksidacije -3 l fosfin, PH 3 slabija baza od amonijaka, nepolaran , miris trule ribe soli fosfidi l l 79 11/22/2020

stepen oksidacije +3 l l fosfor(III) oksid, P 4 O 6, fosforasta (fosfitna) kiselina, H 2 PHO 3, i njene soli fosfor(III) oksid nastaje gorenjem fgosfora s nedovoljno O 2 H 2 PHO 3 nastaje ako na fosfor(III) oksid delujemo hladnom vodom: l P 4 O 6(s) + 6 H 2 O 4 H 2 PH 03 l čista kiselina se kao i njen vodeni rastvor, zagrevanjem razlaže na fosfin i fosfornu kiselinu: l 4 H 2 PHO 3 PH 3(g) + 3 H 3 PO 4 l H 2 PHO 3 diprotonska kiselina (umereno jaka) koja jonizuje u dva stupnja i daje dva niza soli hidrogenfosfite i fosfite: 80 11/22/2020

hidrogenfosfite i fosfite: l l l l H 2 PHO 3 H+ + HPHO 3 K 1 = 1. 6× 10 -2 mol dm-3 HPHO 3 H+ + PHO 3 2 - K 2 = 7. 0× 10 -7 mol dm-3 PHO 32 - + 3 OH- PO 43 - + 2 H 2 O + 2 e- H 2 PHO 3 + H 2 O H 3 PO 4 + 2 H+ + 2 e- Svi alkalni fosfiti lako su rastvorljivi u vodi, a zemnoalkalni nešto manje. Najvažnije su natrijumove soli: Na. HPHO 3 i Na 2 PHO 3 (antiseptici) 81 11/22/2020

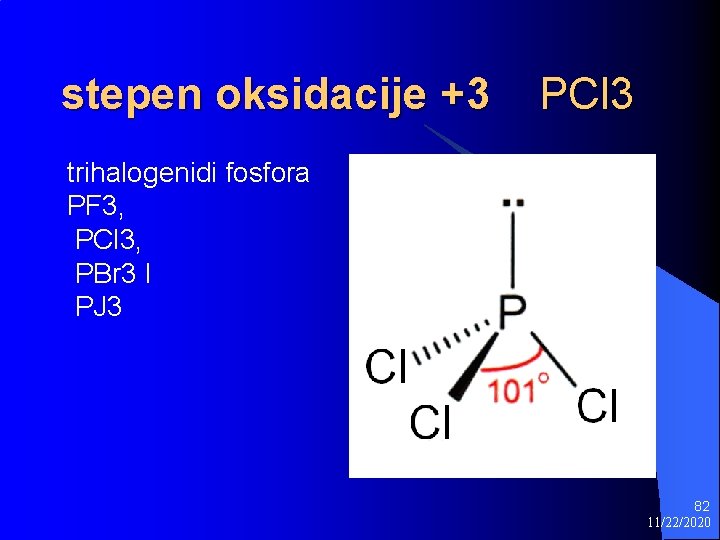
stepen oksidacije +3 PCl 3 trihalogenidi fosfora PF 3, PCl 3, PBr 3 I PJ 3 82 11/22/2020

stepen oksidacije +5 pentahalogenidi , fosfor(V) oksid, P 4 O 10, l fosforna kiselina, H 3 PO 4 i njene soli l fosfor(V) oksid nastaje gorenjem fosfora s dovoljnom količinom O 2: l l P 4(s)+5 O 2(g) P 4 O 10(g) 83 11/22/2020

P 4 + 5 O 2 P 4 O 10 84 11/22/2020

Fosforna kiselina 85 11/22/2020

Dobijanje fosforna kiselina može se dobiti reakcijom izmedju fosfor(V)oksida i dovoljno vode: P 4 O 10(S) + 6 H 2 O 4 H 3 PO 4 l ili 3 H 2 SO 4(aq) + Ca 3(PO 4)2(s) + 6 H 2 O(l) 2 H 3 PO 4(s) + 3 Ca. SO 4 +2 H 2 O(l) 86 11/22/2020

Upotreba : l l l l Za poljoprivredna djubriva, insekticide Za deterdžente-omekšavaju tvrde vode sredstva za čišćenje-rdje ( CILIT BANG) U sapunima kao antibakterijska sredstva Aditivi kod namirnica(coca-cola, pivo, džemovi) Puferi U medicini i farmaciji 87 11/22/2020

Disocija H 3 PO 4(aq) < H+(aq) + H 2 PO 4 -(aq) l Ka 1 = 7. 5 × 10 -3 dihidrogen fosfat l H 2 PO 4 -(aq) < H+(aq) + HPO 42 - (aq) l Ka 2 = 6. 2 × 10 -8 hidrogen fosfat l HPO 42 -(aq) < H+(aq) + PO 4 3 - (aq) l Ka 3 = 1. 7 × 10 -12 fosfat l 88 11/22/2020

Soli fosforne kiseline-FOSFATI 89 11/22/2020

soli H 3 PO 4(aq) + Na. OH(aq) Na. H 2 PO 4(aq) + H 2 O(l) primarni fosfat l H 3 PO 4(aq) + OH-(aq) H 2 PO 4 -(aq) + H 2 O(l) l H 3 PO 4(aq) + 2 OH-(aq) HPO 4 2 -(aq) +H 2 O(l) sekundarni fosfat l 90 11/22/2020

Biološka uloga: l l l Fosfor je još jedan mineral koji spada u grupu makroelemenata, i najveća količina fosfora (oko 80%) nalazi se u zubima i kostima. Mnogo ljudi misli da je kalcijum mineral koji je odgovoran za pravilan razvoj kostiju i njihovo održavanje, on u stvari ovaj zadatak ne obavlja sam. Kalcijum zajedno sa fosforom je odgovoran za zube i kosti, fosfor je prisutan kao kalcijumfosfat. 91 11/22/2020

Osim ovog veoma važog partnerstva sa kalcijumom, fosfor je neophodan za mnoge druge procese u organizmu. . l sledeća važna uloga je u procesu proizvodnje kolagena. l Kosti su 75% kolagen, ali i zglobovi, ligamenti, tkiva, hrskavica, oči i koža su uglavnom sačinjeni od kolagena. l Telo ne bi moglo da napravi vezivno tkivo i organe koji su vitalni bez konstantnog unosa fosfora. l 92 11/22/2020

Fosfolipidi l l l koji su sastavljeni od fosfora(PO 4) ujedinjenog sa masnom kiselinom, nalazi se unutar ćelijskih membrana. Pošto je i rastvorljiv u vodi i u mastima, fosfolipidi su ono što omogućava nutritijentima (i rastvorljivim u mastima i vodi) da prođu kroz ćelijsku membranu. Ćelija će odumreti ako ne postoji način da uđu i izađu nuntritijenti koji su rastvorljivi i u vodi i u mastima. Fosfor je ono što ćelijama daje energiju i glavna je komponenta adenozim trifosfata (ATP) 93 11/22/2020

Dobri izvori fosfora nalaze se u istoj hrani u kojoj se nalazi i kalcijum. l Mleko, tvrdi sir, jogurt, jaja, konzervirana riba, piletina, crveno meso, orasi, badem, žitarice celog zrna, pšenične klice i seme bundeve su veoma dobri izvori fosfora. l Preporučena dnevna doza fosfora je 1000 mg na dan za odrasle l 94 11/22/2020

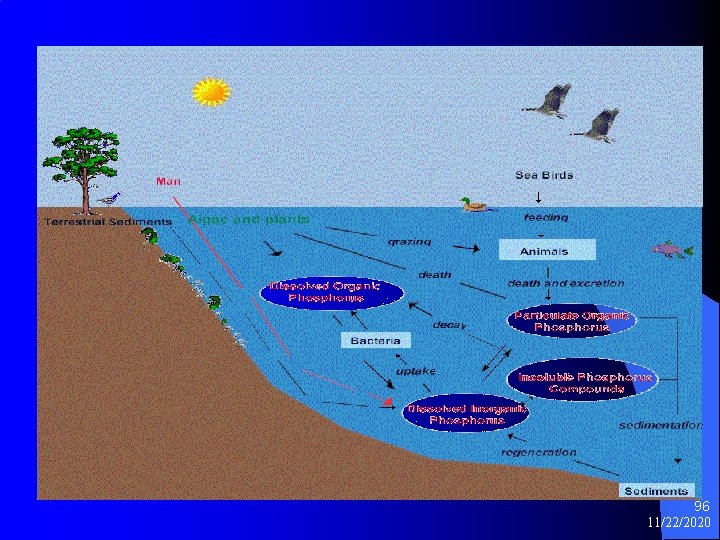
l l l Sastavni je dio DNA, ATP-a i mnogih drugih biohemijskih molekula. Fosfatni ciklus u prirodi je vrlo važan i kao hranjiva supstanca može biti ograničavajući faktor, npr. u okeanima. Toksični unos: (Beli P, oralno, pacov) = 11 mikro-g kg^1 Smrtonosna doza: (Beli P, oralno, čovek) = 100 mg Opasnosti: Beli fosfor je mnogo otrovniji od crvenog fosfora. Hronično trovanje osoba koje nezaštićeno rade sa njim vodi do nekroze vilice. 95 11/22/2020

96 11/22/2020