V CHEMICK VAZBA a mezimolekulrn sly 1 CHEMICK

V. CHEMICKÁ VAZBA a mezimolekulární síly

1) CHEMICKÁ VAZBA A) VZNIK CHEMICKÉ VAZBY: Při vzniku vazby : • • • se uvolní energie se změní uspořádání valenčních elektronů každý atom se snaží o nejstabilnější elektron. konfiguraci (oktet, duet)

Pozn. : v této kapitole je výhodné použít zápis atomů s valenčními elektrony: prvek počet val. el. symbol elektron. konfigurace Na 1 Na [Ne] 3 s 1 Mg 2 Mg či Mg [Ne] 3 s 2 C 4 C či C [Ne] 3 s 2 3 px 1 3 py 1 N 5 N či N [Ne] 3 s 2 3 px 1 3 py 1 3 pz 1 O 6 O či O [Ne] 3 s 2 3 px 2 3 py 1 3 pz 1 Cl 7 Cl či Cl [Ne] 3 s 2 3 px 2 3 py 2 3 pz 1
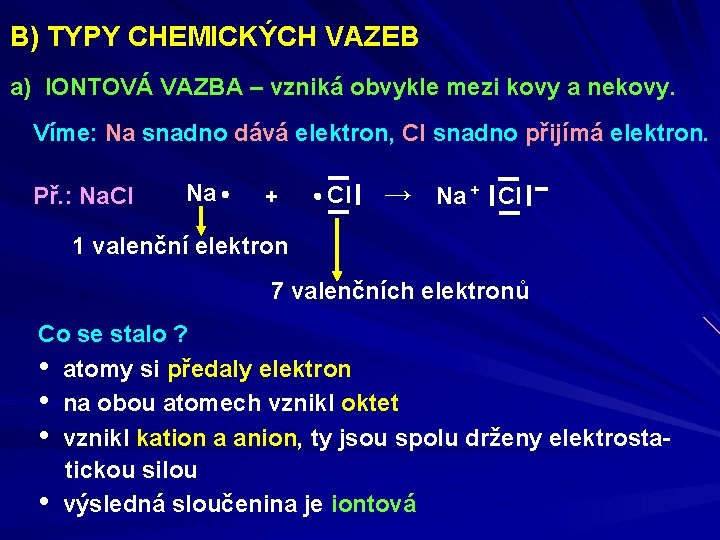
B) TYPY CHEMICKÝCH VAZEB a) IONTOVÁ VAZBA – vzniká obvykle mezi kovy a nekovy. Víme: Na snadno dává elektron, Cl snadno přijímá elektron. Př. : Na. Cl Na + Cl → Na + Cl 1 valenční elektron 7 valenčních elektronů Co se stalo ? • atomy si předaly elektron • na obou atomech vznikl oktet • vznikl kation a anion, ty jsou spolu drženy elektrostatickou silou • výsledná sloučenina je iontová

ALE: Nekovy netvoří iontové sloučeniny, „nechtějí dávat“ elektrony, a přesto jsou miliony sloučenin mezi C, H, O, N, Cl. . . (organické sloučeniny). Jak to? ? V těchto případech vzniká: b) KOVALENTNÍ VAZBA Její vznik: • • • atomy se přiblíží vnější orbitaly se překryjí z valenčních elektronů vzniká 1 či více sdílených (vazebných) elektronových párů Vazebný pár patří oběma atomům a tvoří kovalentní vazbu.
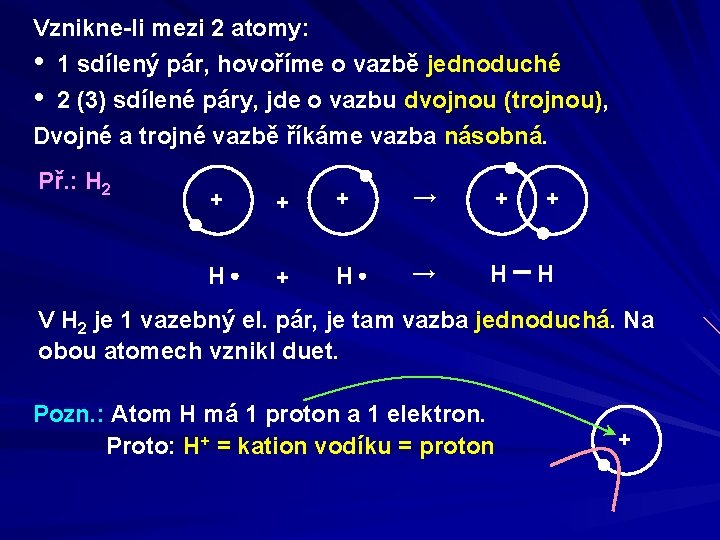
Vznikne-li mezi 2 atomy: • • 1 sdílený pár, hovoříme o vazbě jednoduché 2 (3) sdílené páry, jde o vazbu dvojnou (trojnou), Dvojné a trojné vazbě říkáme vazba násobná. Př. : H 2 + + + → + + H → H H V H 2 je 1 vazebný el. pár, je tam vazba jednoduchá. Na obou atomech vznikl duet. Pozn. : Atom H má 1 proton a 1 elektron. Proto: H+ = kation vodíku = proton +

Př. : Cl 2 Cl Cl + → Cl Cl V Cl 2 je vazba jednoduchá. Na obou atomech vznikl oktet. Na každém atomu chloru v molekule Cl 2 jsou též 3 volné elektronové páry (neúčastní se vazby). Př. : N 2 N + N → N N V N 2 je vazba trojná. Na obou atomech vznikl oktet. Dále rozlišujeme: • vazbu : vazebný pár je na spojnici jader; vzniká např. překrytím orbitalů s + s či px + px; je např. v Cl 2, H 2 • vazbu : vazebný pár je mimo spojnice jader; vzniká např. překrytím py + py či pz + pz; v N 2 je tedy 1 vazba a 2 vazby
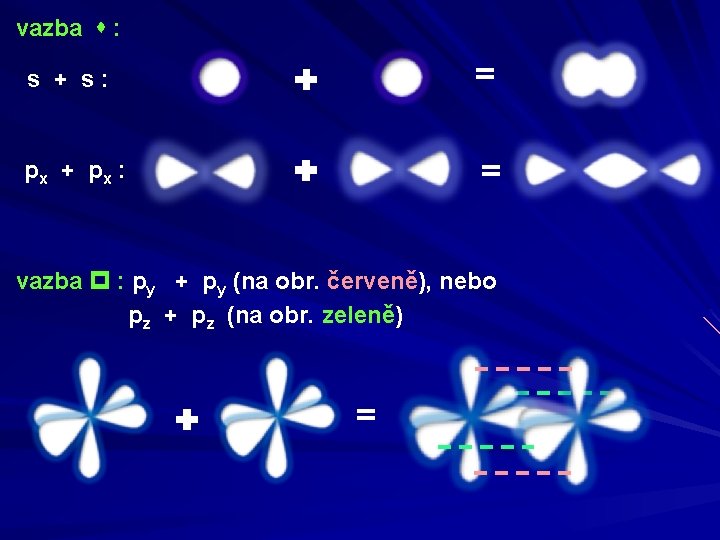
vazba : s + s: = px + p x : = vazba : py + py (na obr. červeně), nebo pz + pz (na obr. zeleně) =

Tvoří-li vazbu 2 RŮZNÉ ATOMY : • • jeden z nich má větší sílu poutat vazebný pár (má větší elektronegativitu), na něm je pak částečný záporný náboj, na 2. atomu částečný kladný náboj a vznikne: c) POLÁRNĚ KOVALENTNÍ VAZBA (zkráceně polární vazba) : Ta je u většiny sloučenin. Elektronegativita atomů : Je v PSP. Přibližně platí, když je: 1. sk. 2. sk. 13. sk. . . . 17. sk. > 1. 7, vazba je iontová < 0. 4, vazba je kovalentní 1. 7 > > 0. 4, vazba je polární kde rozdíl elektronegativit P = min S = max P

Př. : HCl H + Cl → H+ Cl Na H vznikl duet, na Cl oktet. = (Cl) - (H) = 2, 8 – 2, 2 = 0, 6 > 0, 4; vazba je polární; Cl má větší sílu poutat vazebný pár, na Cl vznikl částečný záporný náboj, na H částečný kladný náboj. Vznikla POLÁRNÍ MOLEKULA – DIPÓL. d) VAZBA KOORDINAČNĚ KOVALENTNÍ Vazba mezi atomem s prázdným orbitalem a atomem s volným elektronovým párem. Do vazebného páru přispěje 1 atom 2 elektrony, 2. atom žádným; přesto jsou všechny vazby rovnocenné.
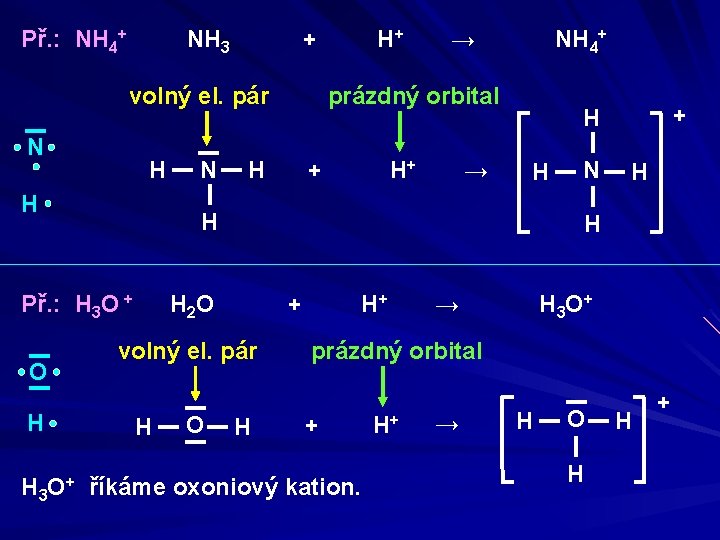
Př. : NH 4+ NH 3 + volný el. pár N H H H → NH 4+ prázdný orbital H + H+ → H + volný el. pár O N H H H 2 O H + H H Př. : H 3 O + O N H+ H H+ → H 3 O + prázdný orbital + H 3 O+ říkáme oxoniový kation. H+ → H O H H +

VÝJIMKY Z OKTETOVÉHO PRAVIDLA: a) RADIKÁLY (jen pro FBI) = uskupení atomů s lichým počtem valenčních elektronů. Jsou vysoce reaktivní. Způsobují řetězové reakce (hoření, exploze). Př. : hoření H 2 , probíhá v krocích: H 2 → H + H vznik 2 radikálů (atom H má 1 el. , je to tedy radikál) H + O 2 → HO + O O + H 2 → HO + H 2 HO + 2 H atom O má 2 „liché“ el. , je radikál opět z 1 radikálu vznikají 2 radikály → 2 H 2 O radikály reagují spolu a tak zanikají Výsledná reakce (součet kroků) : 2 H 2 + O 2 → 2 H 2 O
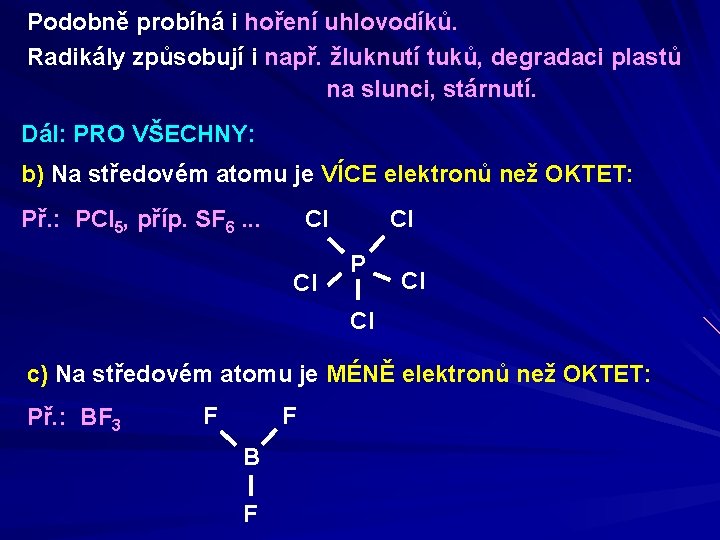
Podobně probíhá i hoření uhlovodíků. Radikály způsobují i např. žluknutí tuků, degradaci plastů na slunci, stárnutí. Dál: PRO VŠECHNY: b) Na středovém atomu je VÍCE elektronů než OKTET: Př. : PCl 5, příp. SF 6. . . Cl Cl Cl P Cl Cl c) Na středovém atomu je MÉNĚ elektronů než OKTET: Př. : BF 3 F F B F

C) CHARAKTERISTIKY CHEMICKÝCH VAZEB • • • délka vazby polarita vazby energie vazby = energie, kterou je nutno dodat k rozbití vazby; čím je menší, tím je sloučenina reaktivnější 2) MEZIMOLEKULÁRNÍ SÍLY Jsou menší než síly mezi atomy v chemické vazbě. Patří k nim: a) Síly mezi okamžitými dipóly - jsou mezi všemi molekulami. Vznik těchto dipólů: elektronový obal molekuly víří, proto těžiště + a – nábojů nejsou stejná a stále se přestavují.

b) Síly mezi trvalými dipóly, tj. mezi polárními molekulami; př. mezi molekulami HCl (viz snímek 9 a 10 této kapitoly) c) Vodíková vazba: Vznik: když atom H leží mezi atomy N, O či F (atomy s velkou elektronegativitou a s volným elektronovým párem). Je z mezimolekulárních sil největší a výrazně ovlivňuje vlastnosti dané látky. Např. : je v H 2 O, NH 3, HF H 2 O O je vodíková vazba O O H H H H O H H H O O H H H H O O O H H H O H O H H H
- Slides: 15