V A skup prvkov PSP Charakteristika veobecne Dusk

V. A skup. prvkov PSP Charakteristika všeobecne Dusík Fosfor
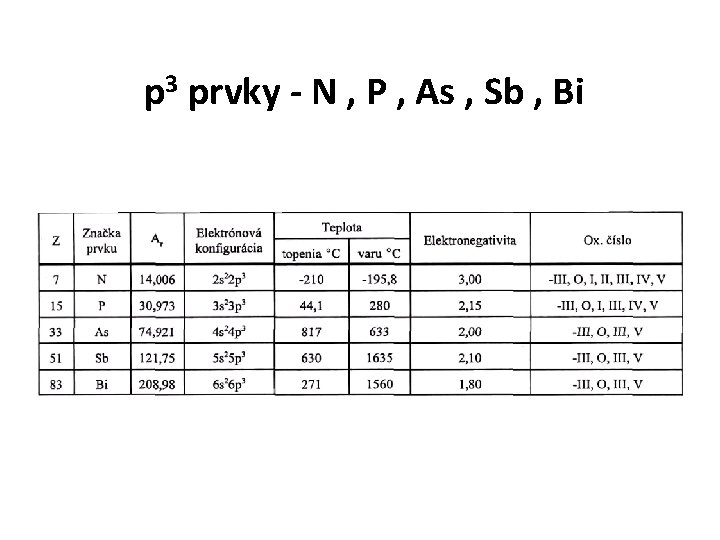
p 3 prvky - N , P , As , Sb , Bi

DOPÍŠTE • Ako stúpa kovový charakter? • Keď prijme N a P 3 elektróny, aké ióny vytvoria? • Prečo voláme tieto prvky, prvkami p 3 ?

DUSÍK - N • Výskyt a) voľný: 78% vo vzduchu b) viazaný: - v dusičnanoch, napr. : Na. NO 3 – čilský liadok, KNO 3 – draselný liadok c) biogénny prvok → v bielkovinách, nukleových kyselinách

Vlastnosti • - za normálnych podmienok bezfarebný plyn bez chuti a zápachu, ľahší ako vzduch, vo vode menej rozpustný ako kyslík • - tvorí dvojatómové molekuly = molekulový dusík – N 2 trojitá väzba → stabilná molekula, N Ξ N , ktorá sa štiepi až pri vysokých teplotách (okolo 4000 °C), preto je molekulový dusík veľmi málo reaktívny • atómový dusík - veľmi reaktívny

Výroba a použitie 1. frakčnou destiláciou skvapalneného vzduchu 2. tepelným rozkladom dusitanu amónneho dopíš chemickú reakciu ! Prepravuje sa stlačený v oceľových nádobách označených zeleným pruhom ! - na výrobu NH 3 , HNO 3, priemyselných hnojív - zmes argónu a dusíku = náplň žiaroviek - vytváranie inertnej atmosféry (napr. pri výrobe výbušnín, v žiarovkách)

Zlúčeniny NH 3 – amoniak, čpavok - v bežných podmienkach bezfarebný, štipľavo páchnuci plyn, leptá sliznicu - prítomný v nepatrnom množstve vo vzduchu a sopečných plynoch - vzniká rozkladom dusíkatých organických látok - je dobre rozpustný vo vode → kvapal. NH 3 - má amfotérny charaktakter- vysvetli!

Soli amoniaku • NH 4 Cl - chlorid amónny (salmiak): používa sa pri spájkovaní, v suchých článkoch • (NH 4)2 SO 4 , NH 4 NO 3 – priemyselné hnojivá • (NH 4) 2 CO 3 – súčasť kypriacich práškov

Kyslíkaté zlúčeniny N • N 2 O , N 2 O 3 , NO 2 , N 2 O 5 – súčasť výfukových plynov a priemyselných exhalátov • N 2 O - "rajský plyn" , oxid dusný – plynná narkotická látka = niekedy bol používaný na narkózy • HNO 2 – kys. Dusitá – slabá kyselina, dôležitá látka pri výrobe farbív • HNO 3 – kys. Dusičná – silná kyselina • uchováva sa v tmavých fľašiach - pôsobením svetla sa rozkladá na vodu, kyslík a NO 2 • oxiduje všetky kovy s výnimkou Au, Pt a niektorých platinových kovov • tie sa rozpúšťajú v lúčavke kráľovskej = HNO 3 a HCl v pomere 1: 3 • bielkoviny pôsobením HNO 3 žltnú (xantoproteínová reakcia) POUŽITIE: výroba dusíkatých hnojív, výbušnín a farbív, pyrotechnika

FOSFOR - P • 3 modifikácie: biely, červený, čierny biely „P 4“- voskovitá biela pevná látka - stabilný až do 800°C, vo vode nerozpustný - veľmi reaktívny (samozápalný) - prudký jed – smrteľ. dávka pre človeka 0, 15 g, reaguje s tukmi!!! Nebrať do rúk!!! - využitie ako jed na krysy červený - nejedovatý bordový prášok - použitie: v zápalkách, pesticídoch čierny - najmenej reaktívny a najstabilnejší

Výskyt a použitie • minerály fluoroapatit a hydroxyapatit • P 4 sa (kvôli samozápalnosti) skladuje pod vodou Použitie • pyrotechnika, dymové bomby, výroba ocele a zliatin • zmes červeného fosforu s pieskom sa nanáša na zápalkové krabičky • Na 3 PO 4 - zmäkčovanie vody (proti tvorbe vodného kameňa v bojleroch a potrubí) • výroba hnojív • dôležitý biogénny prvok (kosti, zuby, bunk. membrány, DNA, RNA)
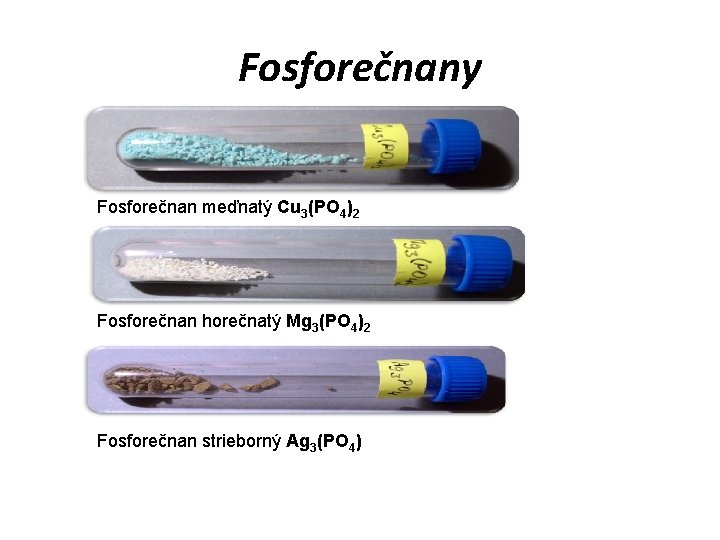
Fosforečnany Fosforečnan meďnatý Cu 3(PO 4)2 Fosforečnan horečnatý Mg 3(PO 4)2 Fosforečnan strieborný Ag 3(PO 4)

Využitie fosforečnanov • • Pri výrobe priemyselných hnojív Využitie v potravinárskom priemysle: napr. Ca(H 2 PO 4)2 pri pečeni chleba, KH 2 PO 4 ako protikoagulant v sušenom mlieku, do kávy Na 2 HPO 4 ako emulzifikátor pri výrobe syra Vápenaté a sodné fosforečnany sa pridávajú do zubných pást Sodné soli kyseliny fosforečnej sa uplatňujú ako súčasť práškov na pranie alebo prostriedkov na umývanie riadu v automatických umývačkách na zmäkčenie vody (Na 3 PO 4),

Kyselina fosforečná – vzorec? • bzf. kryštalická látka (tt = 42, 3 °C) - trojsýtna, stredne silná kyselina, málo reaktívna bez oxidačných vlastností - pripravuje sa reakciou oxidu fosforečného s vodou alebo reakciou fosforečnanov s kyselinou sírovou - je súčasťou viacerých čistiacich prostriedkov - používa sa na konzerváciu potravín a - pri výrobe hnojív (90 % svetovej produkcie)

ZAUJÍMAVOSTI • biely fosfor sa na vzduchu oxiduje a svetielkuje = jedná sa fosforescenciu Svetielkovanie sa dá vyrobiť pomocou chemoluminiscencie: • Reakcia luminolu v zásaditom roztoku, pri reakcii s peroxidom vodíka za prítomnosti vhodného katalyzátoru
- Slides: 15